低温等离子体技术同步去除水中Cr(Ⅵ)和苯酚的研究
刘华瑜,宋泽群,宋 超,王曙光
(山东大学环境科学与工程学院,山东青岛266200)
六价铬是电镀、制革等工业排放废水中的重要污染物,具有易被机体吸收、毒性强、可致癌等特点,严重威胁生态系统甚至人类健康,被我国生态环境部列为重点监测物质〔1〕。目前主流的处理思路是通过化学还原先将高毒性的Cr(Ⅵ)转化成低毒的Cr(Ⅲ),再通过沉淀等方法进行去除。传统处理方法虽然能达到较好的去除效果,但处理过程中往往需要额外添加化学药剂,易造成二次污染。另外,由于含Cr(Ⅵ)废水中还存在大量有机污染物,需进行预处理或增加后续处理工序,导致废水处理的难度和成本增大,因此,亟需开发高效清洁、能同步处理Cr(Ⅵ)和有机污染物的新型废水处理技术。
作为一类新型高级氧化技术,低温等离子体技术具有处理效率高、无二次污染等优点,近年来被广泛应用于废水处理领域〔2〕。该技术能通过放电产生·OH、O3等大量强氧化性物质,实现有机污染物的快速高效处理〔3〕。值得注意的是,放电过程中也会产生许多还原性物质,如·H、H2O2及水合离子(e-)等,尤其是具有极强还原性的·H,可作为污染物的还原剂〔4〕。Lei Wang等〔4〕研究了低温等离子体对含铬废水的去除过程,发现无需添加化学药剂即可实现Cr(Ⅵ)的快速还原,10 min时去除率高达95%。Zhigang Ke等〔5〕用水液界面的辉光放电等离子体高效去除废水中的Cr(Ⅵ)。近年来,利用低温等离子体技术还原去除Cr(Ⅵ)等重金属污染物的研究已有陆续报道,但充分考虑废水中有机污染物的影响,用低温等离子体同步去除Cr(Ⅵ)和有机污染物的研究鲜见报道。
本研究选用苯酚作为典型有机污染物,利用介质阻挡放电(DBD)产生低温等离子体,同步去除水中苯酚和Cr(Ⅵ)。解析了苯酚和Cr(Ⅵ)的去除机制,同时探究苯酚和Cr(Ⅵ)共存条件下的相互作用机理,为低温等离子体技术在废水处理领域的应用提供新思路和一定理论依据。
1 材料与方法
1.1 仪器与试剂
仪器:CTP-2000型等离子体放电电源,南京苏曼有限公司;UV-6100型紫外分光光度计,上海元析仪器有限公司;LC-20AT高效液相色谱仪,日本岛津公司;SP-3520AA型原子吸收分光光度计,上海光谱仪器有限公司;BT100-2J型蠕动泵,兰格恒流泵有限公司;TOC-L CPH型TOC分析仪,日本岛津公司。
试剂:重铬酸钾、氯化铵、氨水、硫酸、磷酸、丙酮,分析纯,国药试剂有限公司;4-氨基安替比林、铁氰化钾、苯酚、二苯碳酰二肼,分析纯,阿拉丁试剂公司;甲醇,色谱纯,国药试剂有限公司;实验用水为去离子水。
1.2 实验装置及参数
实验所用低温等离子体装置如图1所示。

图1 实验装置
该装置由放电电源和等离子体反应容器构成。反应容器由有机玻璃制成,分内外2个中空圆柱体。待处理废水(500 mL)为去离子水配制的含苯酚及含铬废水,初始质量浓度为苯酚50 mg/L,Cr(Ⅵ)5 mg/L,经蠕动泵从内部小圆柱体(直径7 cm)底部的进水孔进入反应器,通过蜂窝陶瓷布水板后溢出到外部大圆柱体(直径15 cm)中,然后经出水孔流回进水容器。放电高压电极固定在反应器架上,电极底部与绝缘介质石英玻璃片紧密贴合,并置于内部小圆柱正上方。内部小圆柱底部装有不锈钢网并通过导线连接到接地电极。
1.3 实验方法
实验装置运行时,等离子体放电电源的输入电压设为40 V,调整电流频率至放电稳定,通过反应器架的调节杆调节石英玻璃片与反应器液面间距至5mm。待处理废水流速由蠕动泵调整为180 mL/min,在不同反应时刻从进水容器取2 mL水样用于后续分析。
1.4 分析方法
Cr(Ⅵ)采用二苯碳酰二肼分光光度法(GB 7466—1987)测定,测定波长为540 nm。苯酚采用4-氨基安替比林直接光度法(GB 7490—1987)测定,测定波长为510 nm。总铬采用火焰原子吸收法进行测定,波长为357.9 nm。总有机碳(TOC)用TOC分析仪进行测定。
用水杨酸捕获法测定反应器中·OH产率。向反应溶液中加入1 mol/L水杨酸,在预定时间取样,用高效液相色谱仪检测水杨酸反应产物2,3-二羟基苯甲酸(2,3-DHBA)和 2,5-二羟基苯甲酸(2,5-DHBA)的含量,二者浓度之和可反映体系中·OH的含量〔6〕。液相色谱仪配备反相色谱柱(ODS-C18)和紫外检测器,流动相为60%的甲醇水溶液,用磷酸调节溶液pH至2.01,流速为0.6 mL/min,检测波长为300 nm。
苯酚和Cr(Ⅵ)浓度采用动力学模型进行拟合分析,见式(1)。

式中:C0——DHBA初始质量浓度,mg/L;
C——t时刻的DHBA质量浓度,mg/L;
k——反应常数,min-1。
2 结果与讨论
2.1 苯酚氧化效果
在等离子体输入电压为40 V、电流调节至稳定(约1.7 A)、石英玻璃片与液面间距为5 mm、废水流速180 mL/min的条件下,考察低温等离子体对苯酚的去除效果,结果见图 2(a)。

图2 不同条件下低温等离子体对苯酚的去除及降解动力学
由图2可见,空白水样中苯酚的浓度没有发生明显变化,说明水解、光解、挥发等作用造成的苯酚损失可以忽略不计。在等离子体处理过程中苯酚浓度不断下降,150min时大部分苯酚被氧化,去除率达到87%,说明低温等离子体对苯酚有较强的去除能力。低温等离子体放电过程中能产生大量强氧化性物质,尤其是·OH,其氧化还原电位可达2.8 eV,在有机物氧化去除过程中可起到重要作用〔7〕。为探究实验中·OH在苯酚氧化过程中的作用,用水杨酸作捕获剂测定等离子体体系中·OH的产率,结果见图3。

图3 ·OH产率变化
由图3可见,放电过程中溶液的·OH浓度不断升高,120 min时其浓度达到0.068 mmol/L,表明低温等离子体在放电过程中持续产生·OH,为苯酚降解提供了强氧化剂。
进一步选用甲醇作为·OH 猝灭剂〔8〕,考察·OH对苯酚降解过程去除率的影响,如图2(b)所示。结果表明,添加体积分数为2%的甲醇(10 mL)后苯酚的去除明显被抑制,150 min时苯酚去除率仅为45%。
不同条件下苯酚和Cr(Ⅵ)降解动力学参数如表1所示。
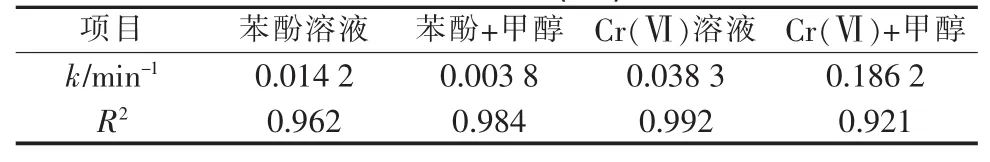
表1 不同条件下苯酚和Cr(Ⅵ)降解动力学参数
由表1可见,添加甲醇后苯酚的降解速率降低,其降解常数仅为不加甲醇时降解常数的1/4。甲醇能与·OH迅速发生反应,使溶液中与苯酚反应的·OH减少,从而降低苯酚的氧化速率。可见·OH含量减少会直接影响苯酚的去除率和降解速率,说明·OH在苯酚氧化过程中起到重要作用。
2.2 Cr(Ⅵ)还原效果
在等离子体输入电压为40 V、电流调节至稳定(约为1.7 A)、石英玻璃片与液面间距为5 mm、废水流速180 mL/min条件下,考察低温等离子体对Cr(Ⅵ)的还原效果,结果见图 4(a)。
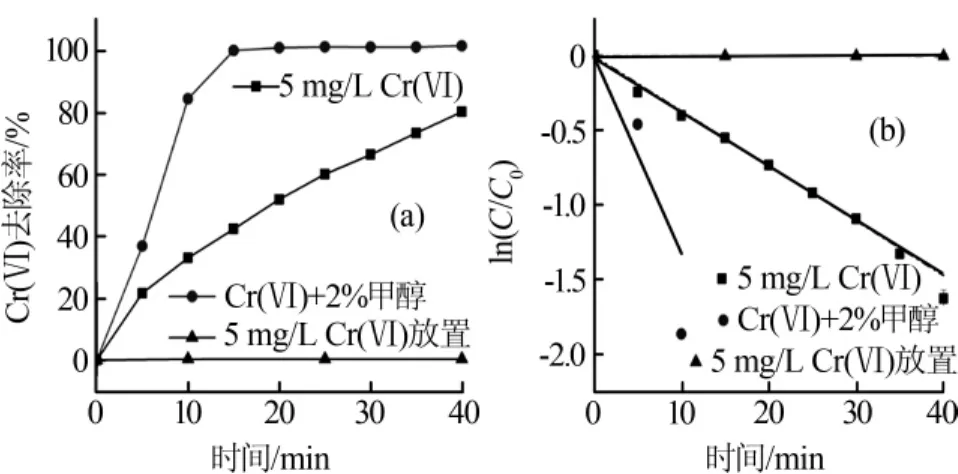
图4 不同条件下低温等离子体对Cr(Ⅵ)还原率的影响及降解动力学
由图 4(a)可见,不加等离子体时,Cr(Ⅵ)还原率可以忽略;用等离子体处理,40 min内Cr(Ⅵ)还原率达到80.3%。这是因为在低温等离子体放电过程中,等离子体-溶液界面处的水分子被解离为水合离子和自由基,见式(1)。
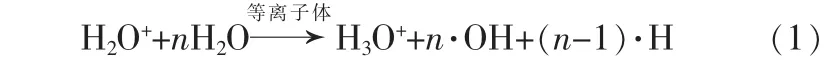
其中n是平均每个H2O+解离的水分子数量,Sengupta预测n值可达12。这一过程中产生的·H可将 Cr(Ⅵ)还原,见式(2)。
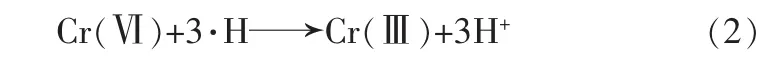
同样,用甲醇作猝灭剂研究了·OH对Cr(Ⅵ)还原的影响。加入10 mL体积分数为2%甲醇后,Cr(Ⅵ)还原率显著升高,15 min 时 Cr(Ⅵ)还原率达到99%以上。此外降解动力学〔图4(b)〕表明,加入甲醇后Cr(Ⅵ)的还原速率变快,降解常数升高至不加甲醇时的5倍(见表1)。原因在于,一方面Cr(Ⅵ)的还原主要依靠溶液中的·H,·OH作为强氧化剂会争夺溶液中的·H,甲醇的加入大大减少了·OH的数量,使溶液中与Cr(Ⅵ)反应的·H增多,促进Cr(Ⅵ)的还原;另一方面,·OH减少抑制了Cr(Ⅲ)重新被氧化为 Cr(Ⅵ),同样有利于 Cr(Ⅵ)的还原〔9〕。
2.3 Cr(Ⅵ)对苯酚氧化的影响
在低温等离子体反应过程中,苯酚去除主要依靠·OH的氧化作用,而·OH的消耗可以促进Cr(Ⅵ)还原。由此可以推断,苯酚和Cr(Ⅵ)的去除可能存在协同作用。为了验证这一假设,考察了苯酚和Cr(Ⅵ)共存条件下低温等离子体对二者的去除效果及其相互影响,结果见图5(a)。
将苯酚和Cr(Ⅵ)混合,不用等离子体处理,结果发现苯酚无明显变化,说明Cr(Ⅵ)不会直接氧化苯酚。随后在初始质量浓度为50 mg/L的苯酚溶液中,分别加入 0.1、1、10 mg/L Cr(Ⅵ),用低温等离子体对该混合溶液进行处理。由图5可见,加入Cr(Ⅵ)后苯酚去除率显著增加,说明Cr(Ⅵ)促进了苯酚的降解,但Cr(Ⅵ)对苯酚氧化的促进程度与Cr(Ⅵ)浓度没有明显的关系。150 min时,不添加Cr(Ⅵ)的苯酚去除率仅为85%;加入0.1 mg/L Cr(Ⅵ)后苯酚去除率达到 95%;Cr(Ⅵ)为 1、10 mg/L 时,苯酚去除率分别为93%、91%,比0.1 mg/L Cr(Ⅵ)时的去除率略有降低。
Cr(Ⅵ)对苯酚去除的促进作用有两方面原因:首先,Cr(Ⅵ)可以与溶液中的·H等还原剂反应,减少·OH 的消耗〔10〕;其次,Cr(Ⅵ)可作为催化剂,催化放电过程中产生的H2O2发生类Fenton反应,产生·OH〔11〕,这 2 个过程都可使氧化苯酚的·OH 增多。同时,Cr(Ⅵ)的还原产物会以较低的反应速率重新被·OH 氧化〔4〕,这一过程只有在 Cr(Ⅵ)的还原产物浓度较高时才比较明显,可能是Cr(Ⅵ)较高时苯酚促进效果降低的主要原因。
同时考察了苯酚氧化过程中添加Cr(Ⅵ)对TOC去除率的影响,见图 5(b)。
如图5(b)所示,在苯酚溶液中添加不同质量浓度的Cr(Ⅵ)时,TOC去除率变化不大,平均为17.1%±1.5%,说明添加Cr(Ⅵ)没有促进苯酚的矿化,且大部分苯酚没有完全氧化为CO2和水,而是转化为其他产物。

图5 不同Cr(Ⅵ)质量浓度下苯酚与TOC的变化情况
2.4 苯酚对Cr(Ⅵ)还原的影响
向初始质量浓度为5 mg/L的Cr(Ⅵ)溶液中分别加入 0.1、1、5、10 mg/L 苯酚,40 min 后计算 Cr(Ⅵ)还原率,考察苯酚对Cr(Ⅵ)还原的影响,结果见图6(a)。
如图6(a)所示,添加苯酚后,初始质量浓度为5 mg/L的Cr(Ⅵ)还原率显著提高。处理40 min时,未添加苯酚的溶液中Cr(Ⅵ)还原率为76%;苯酚为0.1 mg/L时,Cr(Ⅵ)还原率增加到85%;苯酚质量浓度为10 mg/L时,Cr(Ⅵ)还原率升高到93%。这是由于苯酚可与·OH等氧化性物质反应,减少了·H的消耗;另一方面,·OH减少也降低了Cr(Ⅲ)被重新氧化为Cr(Ⅵ)的反应几率,从而提高了Cr(Ⅵ)还原率〔10〕。实验还研究了放电过程中总铬的变化情况,如图6(b)所示。可见无论是否添加苯酚,放电过程中总铬的浓度变化都很小,说明苯酚可促进Cr(Ⅵ)还原为其他可溶性低价态铬。

图6 不同苯酚质量浓度下Cr(Ⅵ)的变化情况
3 结论
采用介质阻挡放电等离子体同步去除苯酚和Cr(Ⅵ)。结果表明,低温等离子体对苯酚和Cr(Ⅵ)均有较强的去除能力。等离子体放电过程中有大量·OH产生,·OH是氧化苯酚的主要物质,·OH消耗会抑制苯酚氧化,促进Cr(Ⅵ)的还原。
等离子体放电过程中苯酚和Cr(Ⅵ)具有协同作用。苯酚能与·OH发生反应,增加还原性·H含量,从而促进溶液中Cr(Ⅵ)还原为可溶性低价态铬;另外,Cr(Ⅵ)能够消耗还原性·H,间接增加了与苯酚反应的·OH含量,促进了苯酚的氧化。低浓度Cr(Ⅵ)对苯酚的促进作用更加明显,但苯酚大部分被氧化为其他产物,并没有完全矿化为CO2和水。

