溶剂和水分活度对OPO结构脂合成中酰基迁移的影响
肖乾煌,徐雨茜,熊 华,胡蒋宁,朱雪梅,张钰岩
(南昌大学 食品学院,南昌 330047)
1,3-二油酸-2-棕榈酸甘油酯(OPO)是一种具有结构和营养成分的sn-USU型油脂,现已被广泛应用于婴幼儿食品中。通常采用酶促合成的方法,通过采用专一性脂酶催化制备OPO结构脂,其相较于化学合成法,具有反应条件温和、反应产物易回收等优点。
过去,人们在利用专一性脂酶合成结构脂时发现,其催化特性并不具有绝对专一性[1],如通过sn-1,3专一性脂酶催化酸解法和转酯换法制备MLM型结构脂中发现有MML异构体,在利用sn-1,3专一性脂酶催化制备sn-1,3-DAG时检测到sn-1,2-DAG和TAG[2],在利用sn-1,3专一性脂酶催化天然植物油脂制备低反式脂肪酸的固态脂肪时发现sn-2位不饱和脂肪酸减少的现象[3]。这些研究结果均表明,专一性脂酶法制备结构脂中存在TAG中sn-2位脂肪酸迁移至sn-1,3位或反之的现象,这就是酰基迁移现象。发生酰基迁移会影响结构脂的得率。影响酰基迁移的因素众多,课题组前期研究发现延长反应时间、升高反应温度、过低的水分活度(aw)都会促进酰基迁移的发生。但是关于反应介质对酰基迁移的研究还较少,特别是在特定反应介质下不同aw对酰基迁移的影响尚未见报道。
本文以三棕榈酸甘油酯(PPP)和油茶籽油游离脂肪酸(FFA)为底物制备OPO结构脂为反应模型,专一性脂肪酶Lipozyme RM IM为催化剂(合成原理及可能的酰基迁移路径如图1所示),研究不同溶剂、不同aw、不同反应时间条件下发生的酰基迁移情况,以期对酰基迁移的发生及调控机制有一定指导意义。
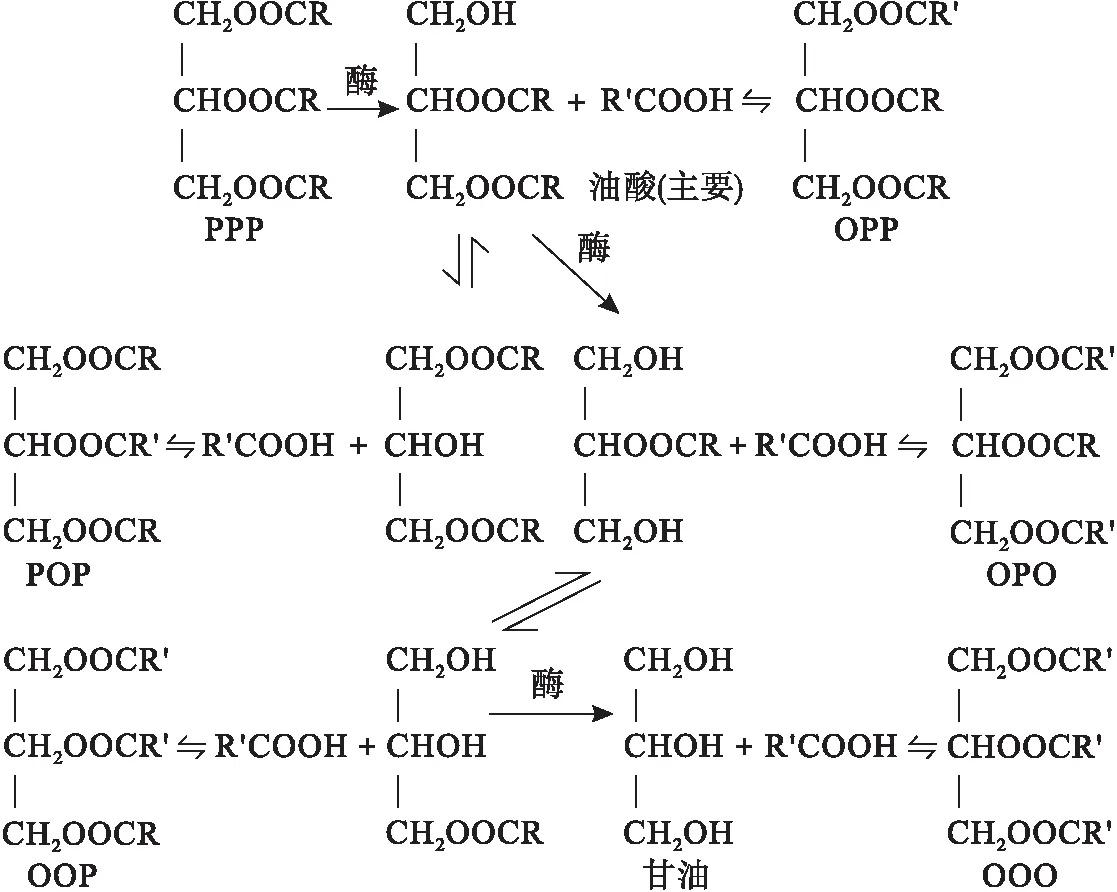
图1 OPO结构脂合成过程及酰基迁移路径图
1 材料与方法
1.1 实验材料
油茶籽油,购于当地超市(油酸含量80%);PPP(CAS为555-44-2,纯度85%),上海百灵威化学技术有限公司;固定化脂肪酶Lipozyme RM IM,诺维信(中国天津)生物技术公司;胰脂肪酶(CAS为9001-62-1),美国Sigma-Aldrich公司;脂肪酸甲酯标准品(#463),美国Nu-Chekprep公司;正己烷、三氯甲烷、异丙醇,色谱纯,美国天地试剂有限公司(上海);胆盐、甲醇钠、乙酸甲酯,分析纯,阿拉丁试剂;95%乙醇、盐酸、氢氧化钾、硝酸镁、氯化锂、硫酸钾、乙酸、无水硫酸钠、无水乙醚、石油醚、正己烷、丙酮、叔丁醇等均为分析纯。
Agilent Technologies 7890B 气相色谱仪、火焰检测器,美国安捷伦公司;RV10旋转蒸发仪,德国IKA集团;BS224S型电子天平,赛多利斯科学仪器(北京)公司;ZH-S全温振荡器;磁力搅拌水浴锅;LXJ-IIB 型台式离心机;UGC-12M型氮吹仪;硅胶板;薄层层析展开缸;碘蒸气层析缸。
1.2 实验方法
1.2.1 油茶籽油FFA的提取
参照Wanasundara等[4]的方法并稍作改动。称取25 g油茶籽油置于平底烧瓶中,依次加入5.75 g KOH、77 mL去离子水-95%乙醇溶液(体积比1∶6),四者混合物置于80℃、200 r/min条件下油浴冷凝回流皂化1 h。皂化结束后,加入150 mL去离子水-正己烷溶液(体积比1∶2),充分振荡后萃取冷却反应物两次,收集含皂化物的无机相后用3 mol/L HCl调节pH至1~2释放FFA。然后加入55 mL正己烷萃取FFA,收集有机相并用无水Na2SO4柱脱水, 40℃旋蒸去除有机溶剂,即得油茶籽油FFA,充N2后于-20℃储存。
1.2.2aw的预平衡
根据Sabbani等[5]采用饱和盐溶液预平衡各反应物aw法,对合成OPO结构脂的原材料进行aw的调控。将油茶籽油FFA和PPP、有机溶剂(正己烷、丙酮、叔丁醇)以及固定化脂肪酶Lipozyme RM IM分别放置于装有饱和盐溶液的密封干燥器中预平衡48 h以上。饱和盐溶液的水分活度分别为:LiCl,aw=0.11;Mg(NO3)2,aw=0.53;K2SO4,aw=0.97。
1.2.3 OPO结构脂的合成[6]
称取摩尔比为1∶5的底物PPP和油茶籽油FFA于具塞三角瓶中,加入3倍底物总质量的溶剂,反应物置于全温振荡器中50℃、200 r/min充分振荡混合20 min。待底物充分溶解后,加入底物总质量10%的固定化脂肪酶Lipozyme RM IM于体系中分别反应0、2、4、6、8 h,反应结束离心除酶后,将产物OPO结构脂置于-20℃储存。
1.2.4 脂肪酸组成分析
根据Zou等[7]方法对反应产物 OPO结构脂进行总脂肪酸分析。准确称量2 mg反应产物于玻璃试管中,依次加入正己烷1.5 mL、乙酸甲酯40 μL、0.5 mol/L甲醇钠100 μL,充分涡旋混匀溶解,室温条件下水浴甲基化反应30 min后转入-20℃冷冻处理10 min,冷冻结束后立即加入饱和草酸溶液60 μL,与过量Na+反应,4 500 r/min离心5 min去除草酸钠等沉淀。取离心管内上层有机相溶液过无水Na2SO4柱,N2吹干。样品经正己烷稀释后,过0.22 μm有机相滤膜,吸取1 mL样品进行GC分析。
GC分析条件参考文献[8]。样品GC数据分别根据标准品的保留时间定性,峰面积归一化法定量分析。
1.2.5 sn-2位脂肪酸组成分析
根据Pacheco等[9]的方法对样品进行脱酸处理。由于合成OPO结构脂底物原料PPP熔点较高(>60℃),所以在脱酸处理过程中需加入适量正己烷使其充分溶解,从而有利于发挥胰脂肪酶对底物的水解作用。
准确称取0.01 g反应产物置于带盖玻璃管中,加入20 μL正己烷溶解,随后依次加入0.05%胆盐溶液2.5 mL、2.2% CaCl2溶液1 mL、1 mol/L Tris-HCl缓冲液10 mL,涡旋后加入0.01 g胰脂肪酶,再次涡旋1 min。室温条件下水浴反应10 min,取出振荡,重复一次。待反应物水解完全,加5 mL正己烷充分摇匀萃取。最后取上层萃取液过无水Na2SO4柱,N2浓缩,样品于-20℃储存待用。
取少量三氯甲烷于上述氮吹样品中复溶,进行薄层色谱分离。待点板在室温下风干后,在展开剂为乙醚-正己烷-乙酸(体积比50∶50∶1)下展开,随后使用碘蒸气染色,刮取MAG硅胶带,置于玻璃试管中,加3 mL正己烷振荡溶解,然后加1 mL 2 mol/L甲醇钠-KOH溶液甲酯化,涡旋混匀,2 500 r/min离心20 min,取上清液过无水Na2SO4柱、0.22 μm有机相滤膜,进行GC分析。
sn-1,3位脂肪酸含量计算公式为:sn-1,3位脂肪酸含量=(3×总脂肪酸含量-sn-2位脂肪酸含量)/2。
1.2.6 数据处理
所有实验结果均以“平均值±标准差”表示,使用Origin Pro 8.5软件进行数据分析,每个样品均重复3次。
2 结果与分析
2.1 溶剂对OPO结构脂合成中酰基迁移的影响
在酶促酸解合成OPO结构脂反应期间,通过使用不同因素影响sn-1,3位特异性脂肪酶的结构构象和催化活性,从而合成理想产物。李人望[10]研究发现,在相同的aw下,有机溶剂可通过立体障碍和传质阻力阻碍脂肪酶接近底物,从而降低其催化活性。同时,由于亲、疏水性溶剂对脂肪酶必需水化层剥夺能力的不同(亲水性>疏水性),所以有机溶剂剥离脂肪酶必需水化层的能力不可忽略。aw为0.53时,不同溶剂对固定化脂肪酶Lipozyme RM IM合成OPO结构脂脂肪酸组成的影响如图2所示。
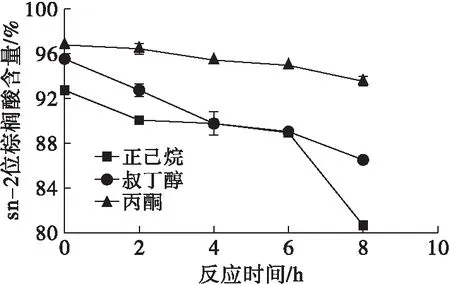
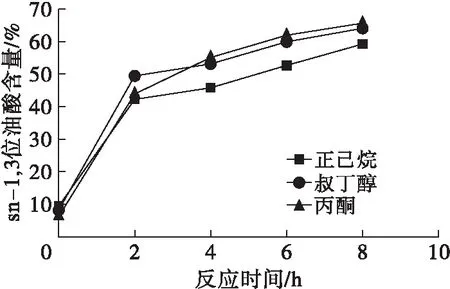
图2 溶剂对Lipozyme RM IM合成OPO结构脂脂肪酸组成的影响
由图2可知,在aw为0.53时,棕榈酸(P)在终产物sn-2位的含量为丙酮>叔丁醇>正己烷,油酸(O)在终产物sn-1,3位的含量与P有相同顺序。在叔丁醇与丙酮反应体系中,sn-1,3位O含量分布大体一致。各溶剂的结构和极性差异是造成3种溶剂对sn-1,3位O和sn-2位P含量高低分布影响的主要因素。此外,酶促酸解反应在3种反应介质体系的反应过程中,sn-2位P含量均随反应时间的延长而降低,其中正己烷反应介质体系的sn-2位P含量的相关曲线在2~8 h阶段呈现先趋于稳定不变而后急剧下降的趋势,而丙酮反应介质体系的相关曲线在整个反应过程中sn-2位P含量变化较其余两组平缓。3种反应介质体系中sn-1,3位O含量均随着反应时间的延长而不断增加。在酶促酸解反应初期, sn-1,3位O含量迅速上升,之后在2~8 h之间,其含量呈缓慢上升趋势。对终产物sn-2位P含量变化的考察结果说明底物在酶促酸解反应过程中确实发生了酰基迁移,与合成OPO结构脂酰基迁移原理理论上一致(见图1)。
研究表明,酰基迁移是自发产生的,且在酶促酸解反应体系中无法制止[11]。对酶促酸解反应影响最小即迁移率最低的为非质子极性溶剂(丙酮)[12-13]。在酶促酸解反应过程中,自发性酰基迁移与溶剂物化性质以及酶的立体特异性有不同程度的线性关系。其中脂肪酶立体特异性与溶剂的极性密切相关,在反应过程中,固定化脂肪酶Lipozyme RM IM专一性水解PPP的sn-1位和sn-3位,其专一性的稳定与结构特性和本身的催化活性呈正相关。不同极性溶剂通过改变酶促酸解反应过渡态中间体-5原子酯环的电荷分散情况来影响反应体系所需的活化能,所以酶促酸解反应过程中电荷越分散,过渡态所需活化能越低,越利于酰基迁移的发生[14-16]。研究显示,固定化脂肪酶Lipozyme RM IM在丙酮体系中对sn-1,3位专一性最好,而在正己烷体系中最弱,与3种溶剂的极性大小呈负相关[17]。
2.2 aw对OPO结构脂合成中酰基迁移的影响
在绝对无水的情况下,固定化脂肪酶Lipozyme RM IM理论上不具有催化活性。水分子在稳定脂肪酶活性中具有重要作用,因为它能通过多种作用力(疏水键、氢键、范德华力、静电吸附等)直接或间接对其产生影响,尤其在非水相-有机介质酶催化反应过程中,与溶剂的亲、疏水性密切相关。根据报道,有机介质中水分子的有效性无法通过其浓度进行量化,因为溶剂的极性强烈影响着水与有机溶剂相互结合的能力[18]。图3、图4和图5分别展现了在正己烷、叔丁醇、丙酮反应介质体系中不同aw(0.11、0.53、0.97)下,对固定化脂肪酶Lipozyme RM IM合成OPO结构脂脂肪酸组成的影响。
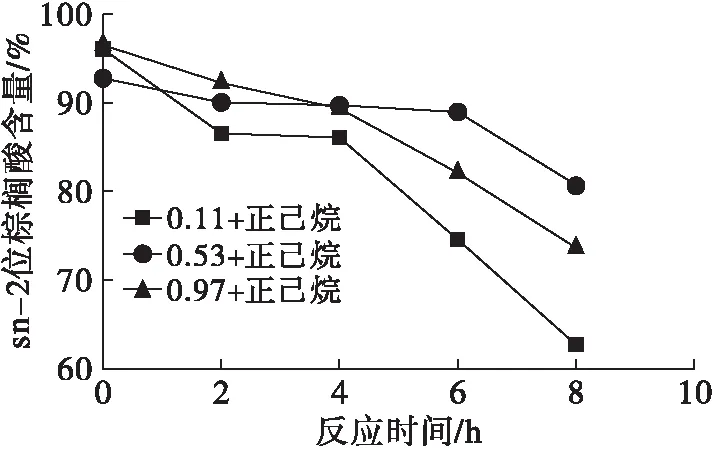
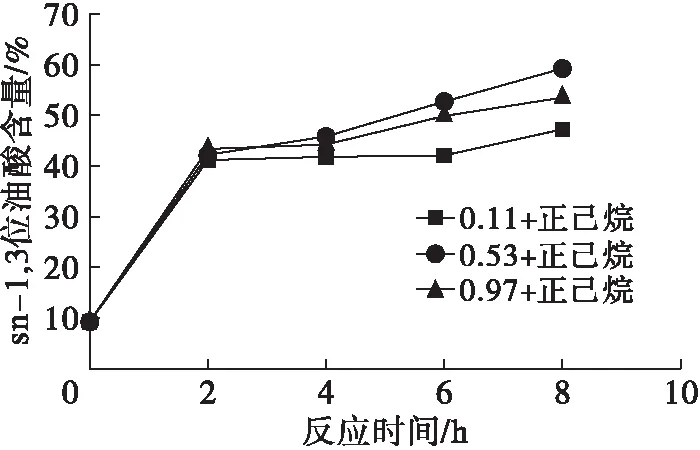
图3 aw对正己烷体系Lipozyme RM IM合成OPO结构脂脂肪酸组成的影响
由图3~图5可知,sn-2位P含量均随反应时间延长存在不同程度的下降,表明PPP在酶促酸解反应过程中确实发生了酰基迁移。而sn-1,3位O含量上升趋势不同,说明不同aw对固定化脂肪酶Lipozyme RM IM在酶促酸解反应过程中的催化活性和TAG sn-1,3位选择性的影响有显著差异。
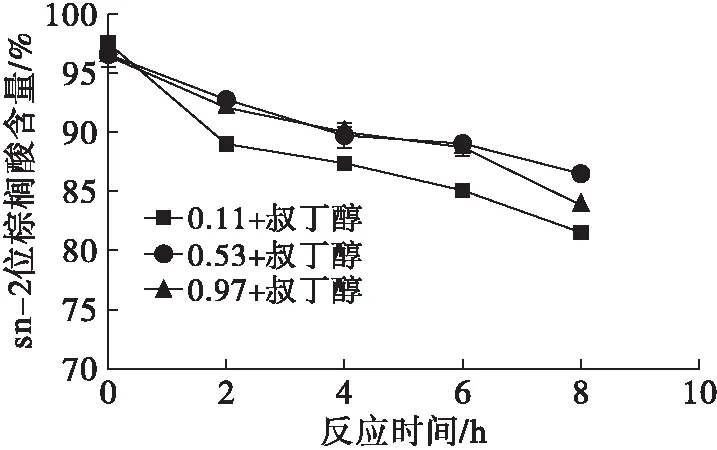
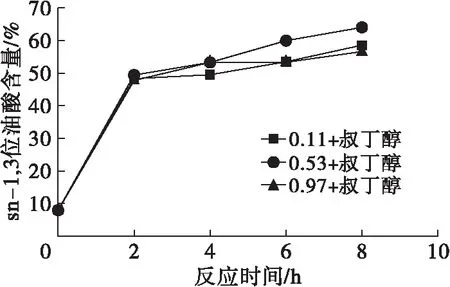
图4 aw对叔丁醇体系Lipozyme RM IM合成OPO结构脂脂肪酸组成的影响
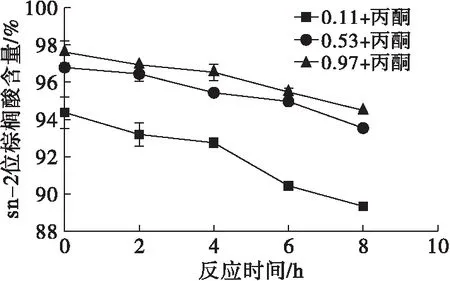
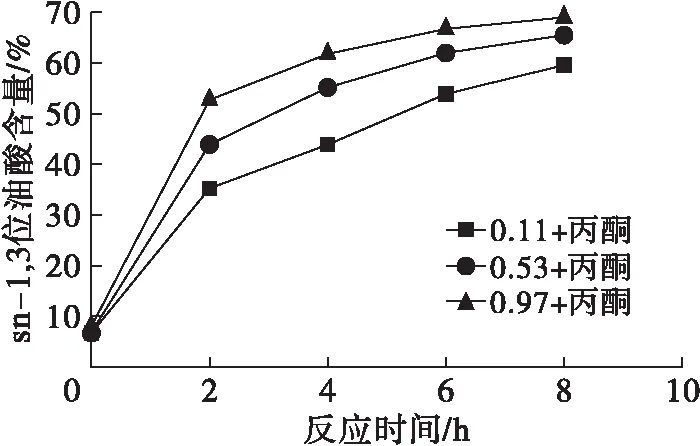
图5 aw对丙酮体系Lipozyme RM IM合成OPO结构脂脂肪酸组成的影响
在正己烷体系中、当酶促酸解反应4 h时,aw为0.53的sn-2位P含量开始较相同情况下aw为0.11、0.97的高。sn-1,3位O含量在反应2 h内,3组aw对应的脂肪酸含量趋于吻合,而随着反应的进行,3组aw下的O含量逐渐上升,其中aw为0.11上升趋势最为缓慢,aw为0.53最快。不过aw为0.97与aw为0.53的O含量曲线上升幅度相当。总体而言,3组aw的大小与相应位置脂肪酸的含量成线性关系,即sn-1,3位O和sn-2位P含量大小:aw为0.53>aw为0.97>aw为0.11。其原因是固定化脂肪酶Lipozyme RM IM在不同aw下,内部柔韧性和氨基酸运动造成的[19-20]。随着体系aw上升,脂肪酶柔性增强,从而在脂肪酶的活性位点周围有更多的水分子与其结合,使脂肪酶活性增加,进攻1,3位置的能力增强。随着aw的进一步提高,可能由于脂肪酶水合作用达到临界值,体系中存在大量水分子从而导致竞争性水解反应增强。此外,也有可能是因为过量的水分子阻塞脂肪酶部分活性位点,抑制底物与脂肪酶的接触造成的[21-24]。综合分析,aw为0.53的正己烷体系,在酶促酸解反应6 h下能够得到较理想的终产物。
在叔丁醇体系中,3组aw对终产物sn-2位P及sn-1,3位O含量的影响无显著性差异。aw为0.11时,sn-2位P含量随反应的进行而缓慢降低,较其余两组下降速度更快,aw为0.53和aw为0.97的含量曲线几乎重合。酶促酸解反应2 h内,3组aw的sn-1,3位O含量曲线基本重合,与正己烷体系中一致。反应2~8 h sn-1,3位O含量缓慢上升,其中aw为0.53时O含量上升最快。这可能与固定化脂肪酶Lipozyme RM IM在叔丁醇体系中的活性有关。
在丙酮体系中,3组aw的sn-2位P和sn-1,3 位O含量曲线差异明显,含量高低顺序:aw为0.97>aw为0.53>aw为0.11,表明aw越高,越不利于酶促酸解反应过程中酰基迁移的发生。aw为0.11时sn-2位P含量最低,与aw为0.53和aw为0.97的P含量相差较大,aw为0.53和aw为0.97的P含量相差较小,这可能是由于在低aw环境下,中间体电荷更为容易分散,反应所需活化能较低,从而导致酰基迁移率更高。3组aw在反应2 h内,sn-1,3位O含量均迅速上升,而后缓慢增加。反应6 h后,O含量变化平缓,可能由于此时反应体系已趋于平衡。与正己烷、叔丁醇体系相比,其sn-2位P和sn-1,3位O含量更高,3组溶剂体系sn-2位P、sn-1,3位O含量范围分别为:62.69%~80.63%、47.18%~59.21%(正己烷体系);81.53%~86.52%、56.66%~64.06%(叔丁醇体系);89.35%~94.51%、59.60%~69.01%(丙酮体系)。
3 结 论
采用酶促酸解法,以油茶籽油FFA为酰基供体、PPP为酰基受体,对比不同溶剂和aw在OPO结构脂合成中酰基迁移的影响。结果表明,当aw为0.53时,不同溶剂下对固定化脂肪酶Lipozyme RM IM合成OPO结构脂酰基迁移的影响结果为:棕榈酸在终产物sn-2位的含量高低顺序为丙酮>叔丁醇>正己烷;油酸在终产物sn-1,3位的含量高低顺序为丙酮>叔丁醇>正己烷。在3种溶剂中,丙酮的反应环境下酰基迁移发生率最低且油酸的键入率最高。相同溶剂、不同aw对酰基迁移的影响结果表明:sn-2位的棕榈酸含量均随反应时间的延长而降低;在3组不同aw条件下,其sn-2位的棕榈酸和sn-1,3位油酸的含量均在aw为0.53时较高,说明即使在不同溶剂环境下,脂肪酶的1,3位置选择性强弱依然决定于aw的高低。鉴于结构脂制备过程中的绿色环保安全角度,可以采用无溶剂体系但是应较好地控制反应体系的aw以抑制酰基迁移。

