扩展stöber法掺氮碳球的制备及其电化学性能
张 焘,徐 丽,高小利,焦玉春,陈香萌
(郑州大学 化工与能源学院,河南 郑州450001)
1 前 言
多孔碳材料因具有较高的比表面积、良好的化学稳定性和热稳定性、无毒无污染、价格低廉等特点而被广泛应用于吸附分离[1-3]、超级电容器[4-6]、催化[7-8]、储能、药物传输等多个领域[9]。但单纯的碳材料表面高度疏水、缺乏足够的活跃吸附位,在一定程度上限制了其应用。而在其表面或骨架中掺杂氮原子不仅保持了原有碳材料的优点,还使其呈现了良好的亲水性、生物兼容性和强电负性,使得碳材料具有更加优良的性能[10]。
制备碳材料常用的方法有软模板法和硬模板法。其中软模板法制备工艺简单,成本相对低廉,但其制备条件较为严格,制备出的介孔碳有序度较差,使其大规模生产受到限制。硬模板法工艺较为成熟,常采用介孔二氧化硅、SBA-15等作为硬模板,但该方法较为繁琐,碳化后需要通过刻蚀除去硬模板。
本文以间苯二酚和甲醛作为碳源,盐酸胍为氮源,聚氧乙烯-聚氧丙烯-聚氧乙烯(F127,PluronicF127)为软模板剂,采用扩展的 stöber法制备出间苯二酚-甲醛-盐酸胍胶体球(nitrogen-doped polymer microporous spheres,NPS),然后对其碳化制得掺氮碳球(nitrogen-doped carbon spheres,NCS)。其中,F127凭借聚氧乙烯(plasma electrolytic oxidation,PEO)段可以通过氢键作用力与间苯二酚-甲醛-盐酸胍树脂的羟基结合在一起自组装成胶体球,随后在碳化过程中分解除去。该方法制备工艺简单,操作成本低,以盐酸胍作为氮源,相对于其他氮源来说,价格低廉且毒性极小,适宜于工业化生产,制备出的掺氮碳球具有较优异的电化学性能。
2 实验材料与方法
2.1 实验材料
氨水(天津市科密欧化学试剂有限公司)、无水乙醇(国药集团化学试剂有限公司)、间苯二酚(上海阿拉丁试剂有限公司)、F127(上海阿拉丁试剂有限公司)、盐酸胍(天津市凯通化学试剂有限公司)、甲醛溶液(西陇化工股份有限公司);硫酸(洛阳昊华化学试剂有限公司)、5% Nafion溶液(上海阿拉丁试剂有限公司)、导电剂乙炔黑(山西力之源电池材料有限公司)均为分析纯,直接使用,去离子水则为实验室自制。
2.2 实验方案
掺氮碳球的制备分为两步。首先利用扩展的stöber法制备出NPS,然后碳化制得掺氮碳球NCS。
(1) NPS的制备:80 mL无水乙醇与200 mL 去离子水在30 ℃下磁力搅拌完全混合,加入1 mL质量分数wB为25%的氨水搅拌1 h,加入2 g间苯二酚搅拌30 min,加入0.28 g F127搅拌30 min,加入一定比例的盐酸胍搅拌30 min(间苯二酚与盐酸胍摩尔比rB为1:1、1:4、1:8、1:16),再加入2.8 mL甲醛溶液搅拌24 h,在100 ℃水热反应釜中反应24 h,水洗、醇洗若干次,置于70 ℃恒温干燥箱中干燥,得到NPS。
(2) 碳化:在N2氛围下以1 ℃⋅min-1的升温速率升至350 ℃并维持2 h,然后以1 ℃⋅min-1的升温速率升至700 ℃并维持4 h,之后再以1 ℃⋅min-1的降温速率降至40 ℃得到NCS,按盐酸胍添加量分别命名为NCS-G-1,NCS-G-4,NCS-G-8和NCS-G-16。
2.3 样品表征及测试
红外光谱测试采用美国 Thermo Nicolet公司的 FT-IR2000型傅里叶变换红外光谱仪(spectrometer,fourier transform infrared spectrometer,FT-IR),样品的孔隙结构分析采用美国康塔仪器公司Autosorb-iQ全自动比表面和孔径分布分析仪,形貌观测采用日本电子株式会社的 JSM-7500F型冷场发射扫描电镜(scanning electron microscope,SEM),晶相分析采用德国BrukerAXS公司的D8 Advance型X射线衍射仪,样品的氮元素含量测定采用德国Elementar公司的Vario EL III型元素分析仪。
2.4 电化学特性分析
采用CHI电化学工作站(上海辰华仪器有限公司)进行测试,测试体系为三电极系统,测试环境为室温大气条件下。工作电极为涂有活性物质的玻碳电极,参比电极为甘汞电极,辅助电极为铂片电极(1 cm×1 cm)。其中,将5 mg样品和1.5 mg乙炔黑超声分散在500 μL Nafion的乙醇溶液中,量取10 μL混合物均匀滴涂在玻碳电极上,常温下静置晾干即得工作电极。配制0.5 mol⋅L-1的H2SO4溶液作为电解液,电化学特性的测试包括循环伏安测试(cyclic voltammetry,CV)和恒电流充放电测试(galvanostatic charge/discharge ,GCD)。其中循环伏安测试以 5 、10、 20、 30、40、50、100 mV⋅s-1的扫描速度,在-0.2~0.8 V 的电压区间进行测量;恒电流充放电测试得到的数据可由式 (1)计算得出活性物质的比电容,

式中:I,Δt,ΔV和m分别为恒定电流(A),放电时间(s),放电电压窗口(V) 和活性物质质量(g)。
3 实验结果与讨论
3.1 化学结构分析
如图1所示为碳球NCS-G-1的FT-IR曲线。由图可知,位于3 450 cm-1处的吸收峰可能归属于样品表面的N─H或者O─H的伸缩振动峰;位于1 630 cm-1的峰可归属为N─H的面内变形振动峰,位于1 390和1 120 cm-1的峰可以归属为C─N的伸缩振动峰,位于650 cm-1的峰对应N─H的面外变形振动峰[11]。从这些峰的归属中可以发现,所得的碳材料中存在含氮官能团。

图1 碳球NCS-G-1的FT-IR谱图Fig.1 FT-IR spectra of NCS-G-1

图2 样品的XRD图Fig.2 Wide-angle XRD patterns of samples
为了确定碳材料的相组成,对制备的样品进行了广角XRD表征,表征结果如图2所示,所得样品均在2θ= 25°和44°处存在2个较弱的衍射峰,分别对应碳材料的(002)和(100)晶面衍射特征峰,说明材料已经石墨化,为典型的无定形碳。通过对XRD图谱的拟合,可以得到平均微晶层间距d002,基面直径La和微晶厚度Lc等表征多孔碳样品的微晶结构有序度的参数,其中,d002的值通过布拉格公式计算,La和Lc通过谢乐公式计算:

式中:λ为Kα射线波长,B为衍射峰半峰宽,θ为衍射角,石墨微晶的有效维度L可根据La和Lc求得

计算结果见表 1。由表 1可以看出,NCS-G-8的有效维度L最大,NCS-G-16的有效维度L最小,说明过量盐酸胍的加入会损害样品的有序性。
采用元素分析对NCS-G-1,NCS-G-4,NCS-G-8和NCS-G-16的表面元素组成进行分析,结果列于表2,由表2可知,样品的表面由C、H、O和N 这4种元素组成,并且N元素的含量随着盐酸胍的增加而有所提高。N元素的掺杂可为材料提供更多的活性位点,提高材料的电负性,同时提高材料对电解质溶液的润湿性,从而提高电化学活性。

表1 样品的晶格特性参数Table 1 Lattice properties from XRD measurements

表2 样品的表面元素组成Table 2 Surface composition of different samples
3.2 微观形貌分析
4种不同的材料的SEM图如图3所示。由 SEM 图可知 NCS-G-1,NCS-G-4都是分布均匀的碳纳米微球,球形颗粒规则且球面光滑,分散性较好,几乎没有出现聚集现象,且粒径大小均一,其球体直径随着盐酸胍加入量的增加而有所增大。这是由于盐酸胍较不稳定,在水溶液中可水解成氨和尿素,随着盐酸胍的增多,氨水浓度增大,导致球径变大。但当盐酸胍的加入量达到一定量时,碳纳米球出现粒径大小不均一的现象,分析认为,盐酸胍的过量加入,使得F127的相对含量减少,不能约束胶体球的规则生成,所以最终获得了尺寸大小不一的碳球。

图3 SEM图Fig.3 SEM micrographs of different samples
3.3 比表面积及孔道结构分析
图4为NCS-G的N2吸附/脱附等温线,由图可知,NCS-G的 N2吸附/脱附等温线在P/P0非常低时,吸附量急剧上升,这是在极低相对压力下的微孔填充;而在 0.1<P/P0<0.9时,曲线出现回滞环,说明有介孔存在;当P/P0>0.9时,曲线出现迅速上升的现象,表明材料中存在少量由于颗粒堆积所造成的大孔,说明该材料为多孔材料。
NCS-G-1,NCS-G-4,NCS-G-8和NCS-G-16孔结构参数如表 3所示。由表 3可知,随着盐酸胍加入量的增加,NCS-G-1,NCS-G-4,NCS-G-8和NCS-G-16的孔结构参数均先减小后增大。分析认为,孔结构参数开始时减小是因为高温引起材料孔道坍塌,孔道出现堵塞,导致比表面积减小;但随着盐酸胍加入量的增大,未参与反应的盐酸胍会在高温下分解,对碳材料有一定的活化扩孔作用,使其微孔数量增多,比表面积增大。
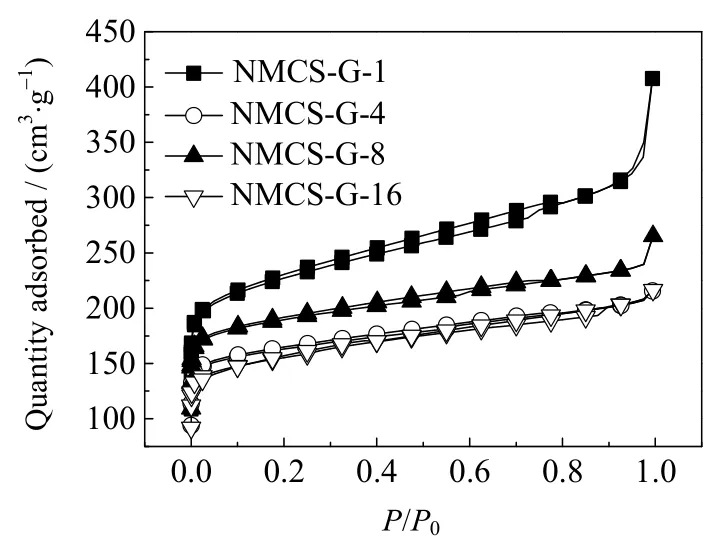
图4 样品的的N2吸附/脱附等温线Fig.4 Nitrogen adsorption-desorption isotherms of the samples

表3 样品的孔结构参数Table 3 Porous texture parameters of the samples
NCS-G-1,NCS-G-4,NCS-G-8和NCS-G-16的孔径分布曲线如图5所示。由图5可知,NCS-G-1,NCS-G-4和NCS-G-8的孔径分布呈现出相似的趋势。在0.6~1.0 nm范围内,随着盐酸胍的加入,相比于不含氮的碳球(nitrogen-free carbon sphere,NCS),NCS-G-1,NCS-G-4,NCS-G-8均出现了新的微孔,说明加入盐酸胍后,反应生成了不同于NCS的新型结构的物质,但NCS-G-16在0.6~1.0 nm范围内,微孔含量较少,说明盐酸胍的加入量并不是越多越好。
3.4 电化学性能测试
3.4.1 循环伏安测试
图6 (a,b)分别为不同样品在5和100 mV⋅s-1的扫描速度下测试得到的CV曲线。从图6 (a)中可以明显看出,在5 mV⋅s-1的扫描速度下,所有样品的 CV曲线均呈现类矩形形状,这种类矩形的曲线表明电荷存储的主要方式为双电层,同时,所有样品均显现出氧化还原峰,这表明赝电容的存在,说明在低的扫描速率下,所制备的样品既表现出双电层电容又表现出法拉第赝电容。另外,CV曲线所覆盖的面积变化大小为NCS-G-8>NCS-G-1>NCS-G-4>NCS-G-16,这说明合适的比表面积大小和合适的氮掺杂浓度共同影响着样品的电容特性。从图6 (b)中可以看出,当扫描速率增加到100 mV⋅s-1时,所制备样品CV曲线的氧化还原峰均消失,但依然保持类矩形形状,说明在高的扫描速度下,样品的电荷存储方式以双电层为主。

图5 样品的孔径分布曲线Fig 5 Profiles of pore size distribution of the samples

图6 样品的循环伏安曲线及比容量Fig.6 CV curves and specific capacitances of the samples
图6 (c)表示系列样品在不同扫描速率下的比容量大小,由图可知,随着扫描速率的降低,样品的比电容都有所增加,当扫描速率降低时,电容会有显著的增大,表明碳球的微孔部分对扩散起到了限制作用。如图所示,样品NCS-G-8展现出最好的电容特性,在5 mV⋅s-1的扫描速率下,可以计算出其比电容为 257 F⋅g-1。
3.4.2 恒流充放电测试
样品NCS-G-1,NCS-G-4,NCS-G-8和NCS-G-16在0.5和10 A⋅g-1电流密度下的GCD曲线如图7(a)、(b)所示,可以观察到所有的GCD曲线都呈现出准三角形对称分布,这是典型理想超级电容器 GCD曲线。图7(c)是随着电流密度为0.5,1,2,5,10 A⋅g-1的增大,电极材料相应比电容的变化趋势,这个趋势可以很好反映电极材料的倍率特性。从图7 (c)中可以得出,样品NCS-G-1,NCS-G-4,NCS-G-8和NCS-G-16在0.5 A⋅g-1电流密度下的比电容分别为417 、278、391和308 F⋅g-1,其中样品NCS-G-1及NCS-G-8的比电容较高;在10 A⋅g-1电流密度下的比电容分别为150、187、252和149 F⋅g-1,其中样品NCS-G-8的比电容较高;样品的电容保留率分别为 35.97%,67.27%,64.45%和 48.37%,其中样品NCS-G-4及NCS-G-8的电容保留率较高。综合样品的比电容及电容保留率,可以看出NCS-G-8具有更加优良的电化学性能。

图7 样品的恒流充放电曲线及倍率特性Fig.7 The charge/discharge profiles and rate performance of the samples
循环稳定性是超级电容器电极材料实用性的一个非常重要的参数,对样品NCS-G-8以10 A⋅g-1的电流密度进行恒流充放电1 000次,图8为每50次循环测试后得到的电极材料比电容变化的结果。从图中可以看出,NCS-G-8的初始比电容为252 F⋅g-1,经过1 000次循环后,比电容变化为245 F⋅g-1,电容保持率为97.2%,说明样品NCS-G-8具有优异的循环寿命。

图8 10 A⋅g-1电流密度下NCS-G-8的循环性能图Fig.8 Specific capacitance of NCS-G-8 as a function of cycle number measured at 10 A⋅g-1
4 结 论
(1) 以盐酸胍为氮源,采用扩展的stöber法成功制备了掺氮多孔碳球,球体表面光滑,粒径均一,分散性好,比表面积较高,含氮量较高,具有较好的双电层电容器特性,说明盐酸胍在制备电容器炭极材料方面具有一定潜力。
(2) 当盐酸胍的加入量为n(盐酸胍):n(间苯二酚) = 8:1时,掺氮碳球NCS-G-8的电容性质最优异:比电容在电流密度为10 A⋅g-1时达到252 F⋅g-1,经历1 000次循环后,电容保持率为97.2%。

