改善心血管和肾脏结局的新型抗高血糖药物临床应用中国专家建议
《改善心血管和肾脏结局的新型抗高血糖药物临床应用中国专家建议》工作组
1 背景
我国成人糖尿病的患病率已高达10.9%[1],据此估算中国至少已有超过1.1 亿的糖尿病患者人群。而2 型糖尿病(T2DM)常常合并动脉粥样硬化性心血管疾病(ASCVD )和(或)慢性肾脏疾病(CKD)。中国心脏调查[2]结果显示,冠心病住院患者中糖尿病患病率为52.9%;2018 年发表的CCC-ACS 研究[3]显示,中国急性冠状动脉综合征(ACS)住院患者中,确诊糖尿病者占36.8%,糖代谢异常者占39.0%。中国肾脏疾病年度报告[4]显示CKD 患病率10.8%,2015 年CKD 住院患者中,首位病因为糖尿病肾病占26.9%。中国3B 研究[5]显示,门诊就诊的T2DM患者中,14.6%合并心血管疾病、10.1%合并脑血管疾病、1.5%合并外周血管疾病、14.4%合并肾脏疾病;1991~2000 年我国住院糖尿病患者中,31.9%合并高血压、15.9%合并心血管疾病、12.2%合并脑血管疾病、5.0%合并下肢血管疾病、33.6%合并肾脏疾病[6]。心血管和肾脏终点事件是糖尿病大血管和微血管病变的结果,是糖尿病患者最主要的致死原因。大规模流行病学死因研究[7]发现,43.2%的中国糖尿病患者死于心脑血管疾病(18.7%死于缺血性心脏病、17.1%死于卒中、7.3%死于其他心血管疾病),5.2%死于CKD,其他常见死因是糖尿病酮症酸中毒或昏迷(10.2%)以及癌症(23.3%)。
近年一系列临床研究证据促使T2DM 的治疗模式从单纯控制血糖转移到改善心血管和肾脏临床结局。UKPDS 35 研究[8]结果提示长期降糖可能改善新诊断且无血管病变的T2DM 患者的心血管结局,但是,进一步大规模随机对照临床研究结果则未发现强化降糖带来的心血管结局获益[9-10],甚至可能使合并心血管疾病或心血管疾病高风险的T2DM 患者增加不良心血管事件和死亡风险[11]。某些降糖药物还可能增加心血管风险[12]。因此,新型抗高血糖药物如二肽基肽酶-4 抑制剂(DPP-4i)、钠-葡萄糖共转运蛋白2 抑制剂(SGLT2i)、胰高糖素样肽-1 受体激动剂(GLP-1 RA)均进行了心血管结局研究(CVOT)和(或)肾脏结局研究(ROT)以验证其心血管及肾脏安全性和临床获益,结果显示,DPP-4i 安全但无心血管或肾脏保护作用[13-16];然而,与人GLP-1 高度同源的GLP-1 RA 及SGLT2i 二类药物具有明显优越性:单用无低血糖反应且耐受性和安全性良好的同时,还能显著改善糖尿病患者的心血管、肾脏临床预后。基于循证医学研究的证据,我国内分泌专家对GLP-1 RA 和SGLT2i 进行了总结,分别发布了临床应用的专家建议[17-18]。美国糖尿病协会(ADA)、美国临床内分泌医师协会(AACE)联合美国内分泌学会(ACE),ADA 联合欧洲糖尿病研究协会(EASD)以及美国心脏病学会(ACC)等分别发布的关于T2DM 管理指南和共识[19-22]虽然推荐首选二甲双胍,但对T2DM 合并ASCVD 或心血管高危风险的患者均明确建议加用GLP-1 RA 或SGLT2i。欧洲心脏病学会(ESC)和EASD 联合发布的《糖尿病,糖尿病前期和心血管疾病指南》[23],则提出T2DM 合并ASCVD 或心血管高危、极高危的患者应首先应用GLP-1 RA 或SGLT2i 治疗,如果已经使用二甲双胍应加用GLP-1 RA 或SGLT2i 类药物。
鉴于中国糖尿病患病率及心血管疾病发病率和死亡率仍呈显著攀升的态势,为进一步提高临床医师对糖尿病的处理能力,改善糖尿病患者的心血管和肾脏结局,中国心血管病学、内分泌学、肾脏病学和神经病学专家,经过多次会议反复研讨,并经广泛征求意见,提出了本建议。本建议旨在简要梳理GLP-1 RA 或SGLT2i 的心血管保护的临床证据及其可能机制,明确这两类药物在临床实践中的合理定位和使用注意事项,强化全体临床医师在临床实践中对T2DM 患者的心血管和肾脏保护理念,及早启动并长期维持能够改善心血管和肾脏结局的新型抗高血糖药物治疗,以期遏止或逆转我国心脑血管和肾脏疾病发病和死亡的上升势头。
2 GLP-1 RA 和SGLT2i 的药理学特征(附表1)
人体进食后,刺激远端回结肠释放GLP-1。GLP-1 与胰岛β 细胞特异性受体结合后,促进胰岛素的分泌,从而降低血糖水平。体内天然GLP-1的半衰期仅数分钟。GLP-1 RA 根据分子结构特点可分为两大类:第一类是基于美洲毒蜥唾液多肽Exendin-4 结构人工合成,其氨基酸序列与人GLP-1 同源性较低,如艾塞那肽和利司那肽;第二类是对人GLP-1 进行结构修饰,保留其生物学效应,但不易被快速降解、延长半衰期,与人GLP-1 氨基酸序列同源性较高,如利拉鲁肽[18]。GLP-1 RA能以葡萄糖浓度依赖性方式,参与机体血糖稳态调节。因此,GLP-1 RA 单用不会导致低血糖。近年发表的CVOT 结果显示,与人GLP-1 高度同源性的GLP-1 RA 具有确凿的心血管保护作用。
SGLT2 是分布在肾脏近曲小管的钠-葡萄糖共转运蛋白,负责90%的尿糖重吸收。SGLT2i 能够抑制SGLT 2 减少原尿中葡萄糖的重吸收(降低肾糖阈),增加尿糖排出,从而在一定程度上降低血糖。SGLT2i 的降糖作用呈现血糖水平依赖性。血糖水平较高时大量葡萄糖被过滤到尿液,此时抑制SGLT2 的作用更为显著;相反,血糖水平正常时抑制SGLT2 所致的降低血糖作用轻微。因此,除非同时合用胰岛素或胰岛素促泌剂(如磺脲类和格列脲类药),临床应用中SGLT2i 极少导致低血糖。
GLP-1 RA 和SGLT2i 均具有利尿、排钠、减轻体重、降低血压和减轻血管炎症的作用。此外,GLP-1 RA 能抑制食物摄入量和胃排空,SGLT2i 亦能增加尿糖和尿酸排泄,降低血容量,提高射血分数,增加心脏能量底物(酮体,游离脂肪酸)[21]。
部分GLP-1 RA 和SGLT2i 药物能降低主要不良心血管事件(MACE)风险,减少蛋白尿,延缓糖尿病肾病的进展,这种有益作用主要体现在T2DM合并ASCVD 患者身上,且不一定与糖化血红蛋白(HbA1c)降低有关,但对此二类药物中的各种药物而言,这种抗动脉粥样硬化的保护作用并非类作用,而更多表现为不同药物各自的效应。然而,SGLT2i对心脏泵功能的影响则呈现明显的类作用[24]。能显著降低心力衰竭住院风险,无论患者有无糖尿病/心力衰竭/ASCVD,SGLT2i 这种对心脏泵功能的保护与HbA1c基线水平或降低幅度无关。
3 GLP-1 RA 和SGLT2i 改善心血管和肾脏结局的临床证据
3.1 GLP-1 RA
LEADER 研究(利拉鲁肽)[25-26]、SUSTAIN-6 研究(司美鲁肽)[27]、REWIND 研究(度拉糖肽)[28-29]、PIONEER 6 研究(口服司美鲁肽)[30]是GLP-1 RA具有代表性的CVOT 研究(表1),主要终点均为首次出现心血管死亡率、非致死性心肌梗死、非致死性卒中事件(3P-MACE)的时间。LEADER 研究和REWIND 研究还对肾脏结局进行了分析[26,29]。利拉鲁肽、司美鲁肽、度拉糖肽均与人GLP-1 具有高度同源性,研究证明它们均有改善心血管预后的作用;而与人同源性低的利司那肽、艾塞那肽没有观察到有统计学意义的心血管保护作用[31-32]。
对T2DM 合并ASCVD 患者,LEADER 研究显示,利拉鲁肽治疗能显著降低MACE 风险(-13%),降低心血管死亡风险(-22%),同时降低全因死亡风险(-15%)。SUSTAIN-6 研究[27]显示每周一次皮下注射司美鲁肽,能显著降低MACE 风险(-26%),其中包括非致死性脑卒中风险的降低(-39%)。PIONEER 6 研究[30]表明口服司美鲁肽亦能降低心血管死亡风险(-51%)。新近发表的REWIND 研究[28-29]显示,在近70%的患者为T2DM 合并ASCVD高危因素的受试患者中,度拉糖肽治疗能显著降低MACE 风险(-12%),其中非致死性卒中风险显著降低(-24%)。
在肾脏保护方面,LEADER 研究[26]显示利拉鲁肽可降低(-22%)肾脏复合终点结局风险,包括持续大量白蛋白尿、血清肌酐倍增、终末期肾脏病(ESKD)或因ESKD 死亡;SUSTAIN-6 研究[27]亦提示司美鲁肽可减少新发肾病或肾病恶化的风险;REWIND 研究[29]专门对肾脏结局进行了分析,在T2DM 合并ASCVD 或高危因素患者中,与安慰剂相比,度拉糖肽治疗能使复合肾脏终点风险降低(-15%),其中新发大量白蛋白尿、估算肾小球滤过率(eGFR)持续下降≥30%的发生率均显著下降。
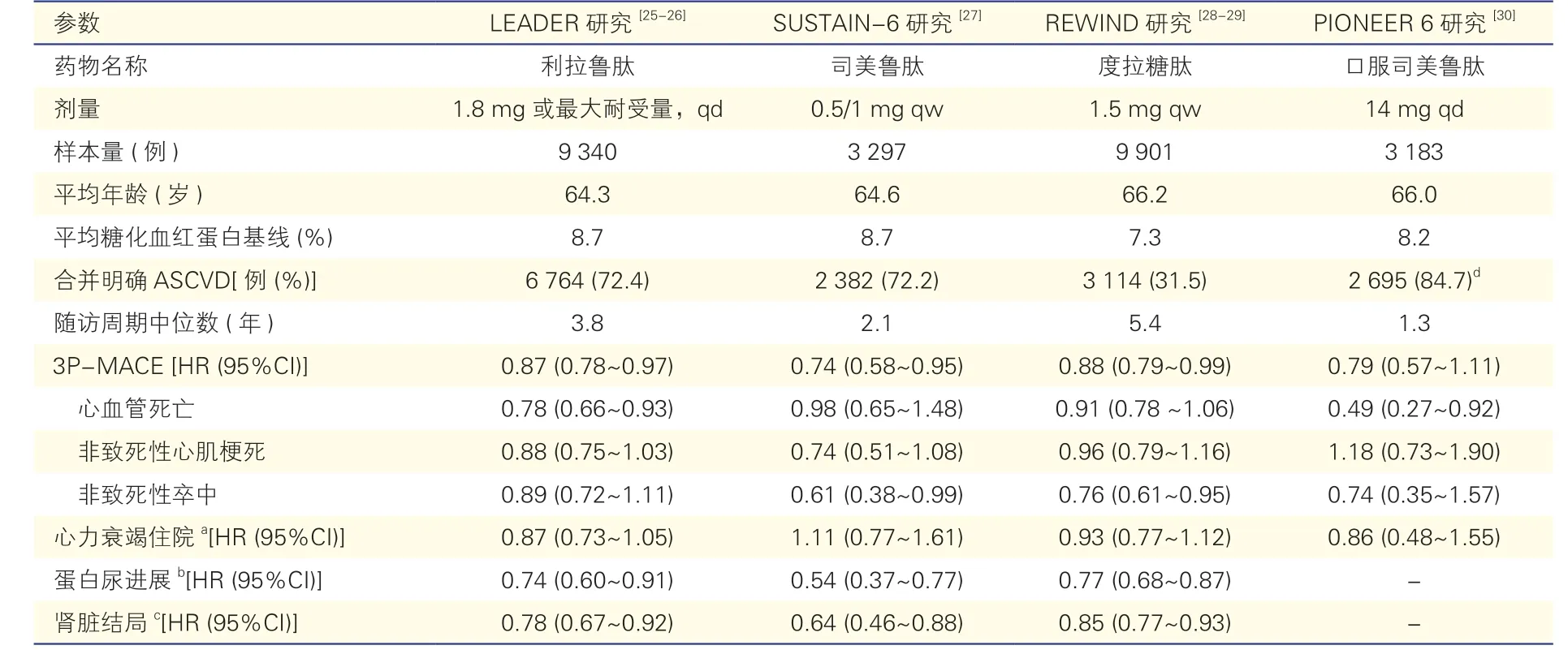
表1 GLP-1 RA 改善心血管和肾脏结局的研究
因此,与人GLP-1 高度同源的GLP-1 RA 治疗T2DM 合并ASCVD 确诊或高危患者,能显著降低心血管和肾脏临床转归终点风险,减少卒中和心肌梗死的发生,改善生存质量。利拉鲁肽还能显著降低全因死亡,延长T2DM 患者的寿命。及早使用度拉糖肽,或者利拉鲁肽、司美鲁肽对T2DM 合并ASCVD 或危险因素的患者,能够延缓心血管疾病和肾脏疾病的进展,保护心脑血管及肾脏。
3.2 SGLT2i
EMPA-REG Outcomes 研究(恩格列净)[33-34]、CANVAS Program 研究(卡格列净)[35]和DECLARETIMI 58 研究(达格列净)[36]是SGLT2i 具有代表性的CVOT 研究,预设主要终点均为3P-MACE;CREDENCE(卡格列净)是ROT 研究[37],主要终点为ESKD、血清肌酐翻倍、肾脏或心血管原因死亡的复合终点;DAPA-HF(达格列净)是针对T2DM 或非糖尿病的心力衰竭患者预后影响的研究[38],主要终点为心力衰竭恶化或心血管死亡复合终点(表2)。
对 确 诊ASCVD 的T2DM 患 者,EMPA-REG Outcomes 研究[33-34]表明,在完善的降糖药物和抗动脉粥样硬化及抗栓治疗基础上,恩格列净进一步显著降低3P-MACE 风险(-14%)和因心力衰竭恶化住院风险(-35%),同时显著降低心血管原因死亡风险(-38%)及全因死亡风险(-32%)。
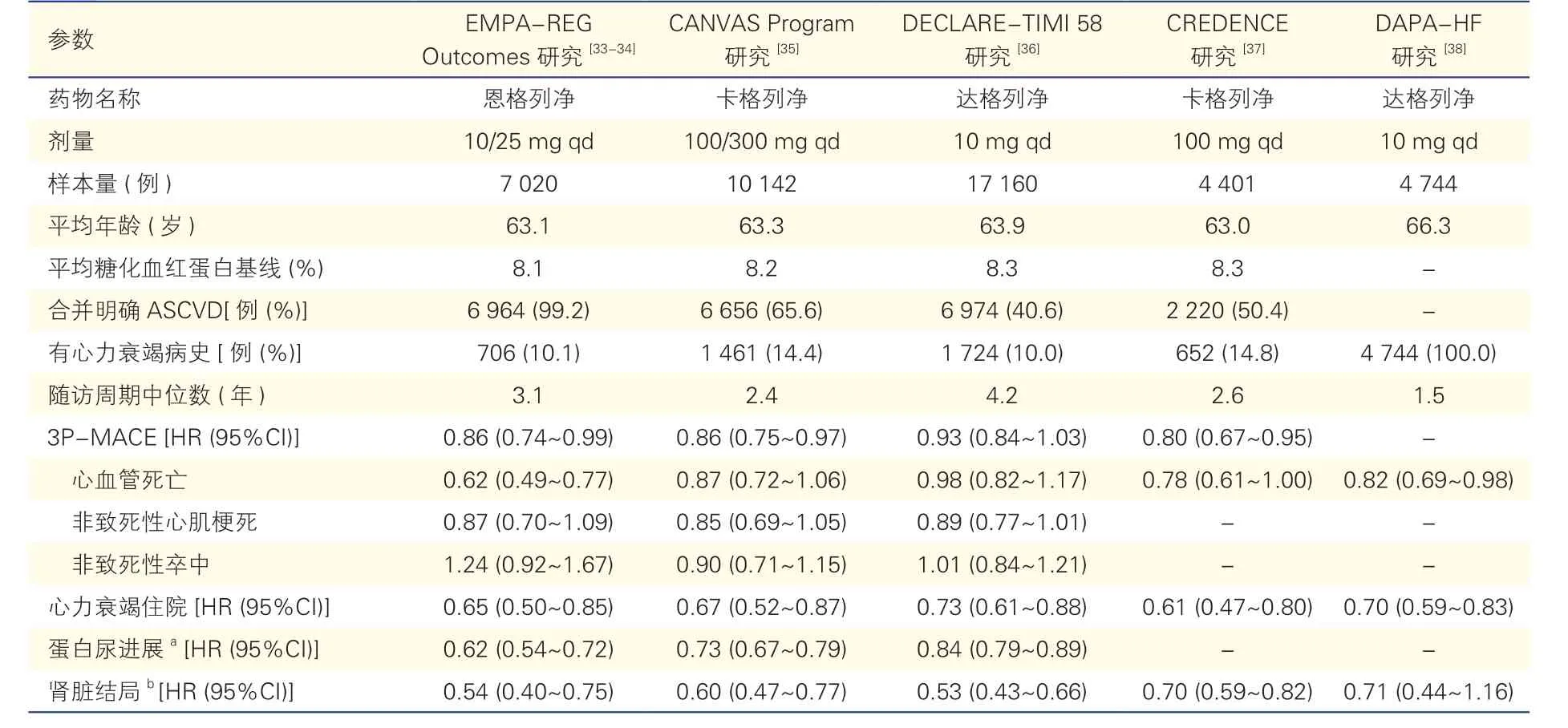
表2 SGLT2i 改善心血管和肾脏结局的研究
CANVAS Program 研究和DECLARE-TIMI 58 研究,纳入确诊ASCVD 或具有ASCVD 高危因素的T2DM 患者,前者显示卡格列净降低3P-MACE 风险(-14%)、以及心血管死亡和心力衰竭的复合终点风险(-22%);后者可能由于纳入更多未确诊ASCVD患者,显示达格列净与安慰剂比3P-MACE 风险差异无统计学意义,但达格列净显著降低心血管原因死亡和心力衰竭住院的风险(-17%)。
新近公布的DAPA-HF 研究[38]显示,无论既往有无T2DM 病史,在完善的抗心力衰竭治疗基础上,达格列净能显著降低心力衰竭恶化复合终点风险(-26%),心血管原因死亡风险(-18%)以及全因死亡风险(-17%)。这一结果直接确认了达格列净对于心力衰竭患者的治疗获益,且这种治疗获益与心力衰竭患者是否合并T2DM 以及基线HbA1c水平无关。
肾脏保护方面,EMPA-REG Outcomes 研究[33-34]、CANVAS Program 研 究[35]、DECLARE-TIMI 58 研 究[36]均显示,即使在充分的肾素—血管紧张素系统抑制剂基础上,SGLT2i 均对T2DM 患者具有极其显著的肾脏保护作用。CREDENCE 研究[37]进一步证实,对T2DM 合并具有蛋白尿的CKD[eGFR 30~90 ml/(min·1.73 m2)]患者,卡格列净能够显著降低ESKD、血肌酐翻倍、肾脏/心血管死亡的复合终点风险(-30 %),同时显著降低3P-MACE 风险(-20%)和心力衰竭住院风险(-39%)。CREDENCE 研究为SGLT2i 治疗T2DM 合并CKD 患者,为同时改善肾脏及心血管预后提供了直接证据。
因此,无论对于合并ASCVD 或心血管高风险因素的T2DM 患者,SGLT2i 具有非常明确的改善心血管结局的作用,其中对于心力衰竭的改善尤为突出,同时一致地显示出对肾脏的保护作用。
4 GLP-1 RA 和SGLT2i 的临床应用建议
对于T2DM 患者的药物治疗,应该采取综合性的策略,包括降糖、降压、调脂(主要是降低低密度脂蛋白胆固醇)及应用阿司匹林治疗,以预防心血管疾病和糖尿病微血管病变的发生。其中,血糖调控目标的首要原则是个体化,应根据患者的年龄、病程、预期寿命、并发症或合并症病情严重程度等进行综合考虑。对T2DM 患者已经接受降糖药物治疗而血糖控制不佳或血糖水平过高的初诊T2DM 患者,须在内分泌专科医师指导下制定安全有效的血糖控制药物治疗方案。
根据已有的大规模随机对照心血管及肾脏结局研究结果,与其它各类降糖药物相比,GLP-1RA 和SGLT2i 不仅能安全有效调控血糖,无低血糖反应(除非与胰岛素或胰岛素促泌剂合用),耐受性好,而且在改善T2DM 患者的心血管及肾脏结局方面具有出色优势。因此,GLP-1 RA 和SGLT2i 均可作为T2DM 患者的首选药物之一。
4.1 适用人群
4.1.1 合并ASCVD 的T2DM:降糖药物首选GLP-1 RA(利拉鲁肽、司美鲁肽、度拉糖肽)或SGLT2i(恩格列净、卡格列净、达格列净)。
4.1.2 伴有ASCVD 高危因素的T2DM:降糖药物首选GLP-1 RA(度拉糖肽、利拉鲁肽、司美鲁肽)或SGLT2i(达格列净、卡格列净、恩格列净)。
4.1.3 心力衰竭[左心室射血分数(LVEF)<40%]合并T2DM:降糖药物首选SGLT2i(达格列净、恩格列净、卡格列净)。
4.1.4 心力衰竭(LVEF <40%)不合并T2DM:推荐SGLT2i(达格列净)为心力衰竭基础治疗药物之一。
4.1.5 CKD 合并T2DM:降糖药物首选GLP-1 RA[度拉糖肽、司美鲁肽、利拉鲁肽,适用于eGFR ≥15 ml/(min·1.73 m2)者];或SGLT2i[卡格列净、恩格列净、达格列净,适用于eGFR ≥45 ml/(min·1.73 m2)者;密切随访下可用于eGFR ≥30 ml/(min·1.73 m2)者]。
4.1.6 肥胖或超重合并T2DM:降糖药物优先考虑GLP-1 RA(利拉鲁肽、司美鲁肽、度拉糖肽),或SGLT2i(恩格列净、卡格列净、达格列净)治疗。
4.2 使用方法(表3)
GLP-1 RA 主要为皮下注射针剂,口服司美鲁肽美国FDA 刚刚批准上市。
SGLT2i 均为口服药物,均为固定剂量治疗。

表3 GLP-1 RA 和SGLT2i 药物使用方法一览表
4.3 临床安全性
4.3.1 禁忌证:(1)GLP-1 RA 禁用于:甲状腺髓样癌(MTC)病史或家族史患者;2 型多发性内分泌肿瘤综合征(MEN2)患者。(2)SGLT2i 禁用于:严重肾损害[eGFR <30 ml/(min·1.73 m2)]或透析患者。
4.3.2 GLP-1 RA 常见不良反应及处理原则:(1)胃肠道反应:较常见。呈剂量依赖性,可随治疗时间延长而减轻。临床使用可从小剂量起始,逐渐加量。(2)GLP-1 RA 有延缓胃排空的作用,可能加重严重胃肠道疾病,如炎症性肠病或胃轻瘫患者的胃肠道不适,因而在此类患者中应慎用。(3)临床应用中有报告急性胰腺炎的发生。故出于安全性考虑,如果怀疑发生了胰腺炎,应立即停用该类药物。
4.3.3 SGLT2i 常见不良反应及处理原则:(1)泌尿生殖道感染:多为轻到中度细菌或真菌感染,常规抗感染治疗有效。建议患者注意个人外阴部卫生,适量饮水,保持排尿通畅,可减少感染的发生。(2)糖尿病酮症酸中毒:少见。如出现腹痛、恶心、呕吐、乏力、呼吸困难时,需立即检测血酮体和动脉血酸碱度以明确诊断。确诊后应立即停用SGLT2i,并遵循糖尿病酮症酸中毒治疗程序进行治疗。
4.3.4 肾功能(附表2):轻度肾功能不全患者无需调整GLP-1 RA 和SGLT2i 的药物剂量。eGFR <45 ml/(min·1.73 m2)患者不建议使用SGLT2i,eGFR<30 ml/(min·1.73 m2)患者禁用SGLT2i。eGFR<15 ml/(min·1.73 m2)患者不建议使用GLP-1 RA;司美鲁肽不受肾功能影响,且无需调整剂量。
4.3.5 肝功能(附表2):轻中度肝功能异常:GLP-1 RA 或SGLT2i 均可使用,无需调整剂量。
4.3.6 妊娠期、哺乳期女性及未成年人,由于缺乏安全性数据,GLP-1 RA 和SGLT2i 均不适用。
5 总结
T2DM 常常合并ASCVD、CKD,因此建议对于已诊断为其中之一的患者,应对是否存在另外两种疾病状态进行筛查和评估,全面考虑药物选择和达标控制,并按照相应的疾病指南进行规范治疗。在糖代谢调整药物的选择上,应该优先选择对心血管和肾脏具有明确临床获益证据的药物。
基于循证医学的原则,本专家组建议推荐对于T2DM 合并ASCVD 或高危因素、CKD 的患者,应该首先考虑选用已被证实改善心血管和肾脏结局的GLP-1 RA 或SGLT2i,并及早启动治疗,以降低ASCVD 和心力衰竭风险,延缓肾脏病变的进程,改善患者生存质量和延长患者寿命。对已经在接受二甲双胍治疗的T2DM 患者,亦须加用有获益证据的GLP-1 RA 或SGLT2i。对心力衰竭的患者,无论是否合并T2DM,建议新增SGLT2i 作为基础治疗药物之一。GLP-1 RA 和SGLT2i 安全性和耐受性好,但在使用过程中仍应注意掌握好注意事项和用药原则。

附表1 GLP-1 RA 和SGLT2i 的药理学特征

附表2 GLP-1 RA 和SGLT2i 药物在肝肾功能异常患者中的使用建议

