Paternò-Büchi(PB)反应与串联质谱结合实现不饱和脂质精确结构解析
马潇潇,胡清源,瑕 瑜
(1.清华大学 精密仪器系 精密测试技术及仪器国家重点实验室,北京 100084;2.清华大学 化学系,北京 100084)



本文主要介绍基于PB反应的脂质分析的基本原理,以及适用于脂质衍生化的电喷雾质谱(ESI-MS)实验设置。以不同类型脂质(如甘油磷脂、脂肪酸和胆固醇酯)为例,介绍了脂质结构解析和定量分析的基本方法。该方法既可直接用于鸟枪脂质组学分析,也可与液相色谱联用。本衍生方法无需对质谱仪器做改造,通过紫外光源即可在离子源处实现脂质快速衍生化,装置简单,谱图易解,有望在各类脂质分析中获得广泛应用。
1 Paternò-Büchi反应


图1 油酸和丙酮间的PB及逆反应
2 PB反应与ESI-MS联用
2.1 光化学反应器
常规用于有机合成的PB反应体系通常体积较大[28-32],量子产率也较低(0.01~0.1),因此需要高浓度的反应试剂(mmol/L到mol/L)、较长的反应时间(3~24 h)和非极性溶剂条件[33]。然而,这些反应条件与电喷雾离子化不兼容。为将PB反应与ESI-MS联用,本课题组发展了流式微反应器和nanoESI在线反应两种分析模式。
2.1.1 流式微反应器发展流式微反应器(Flow microreactor)主要目的是使光衍生反应时间可调,使其能与常规ESI分析联用。流式微反应器采用内径 <1 mm的毛细管作为流道,可实现对UV照射时间的准确控制以及较高的光子效率,并可减少由过度或不均匀UV照射导致的副产物的生成。经过不断优化,目前一般采用可透过UV辐射的熔融石英毛细管作为反应流道(外径363 μm,内径100 μm)。该装置的流速可调范围较大:从亚μL/min到亚mL/min[34-35]。将毛细管以0.5 cm间距绕在UV灯上(反应时间>10 s),或与UV灯距离0.5 cm保持平行(图2A)。UV照射5 s后,PC 16∶0/18∶1(9Z)(5 μmol/L,在70∶30丙酮/水溶液中,1%乙酸)衍生化产物的离子强度基本与底物相当,转化率约为50%。这种反应装置可以提供比体相反应更高的产率,并显著减少副反应。在该类型的反应器中,UV照射5 s后,反应即基本达到平衡。反应器的流速范围(100 nL/min~50 μL/min)恰好与常规ESI-MS进样的流速相当,因而两者可以很好地联用。
2.1.2 nanoESI在线反应在nanoESI在线模式下,衍生化反应在nanoESI喷针中进行。反应前,将5~10 μL不饱和脂质溶液(溶剂:50∶50丙酮/水,体积比)加入喷针中。采用发射波长254 nm的低压汞灯作为激发光源。反应装置示意图如图2B所示。尽管硼硅酸盐玻璃对254 nm的UV光不透明,但喷针的尖端玻璃壁厚已降至μm水平,透光率大大增加,因而使得反应可在此处发生。丙酮既作为PB试剂,也作为nanoESI溶剂。以PC 16∶0/18∶1(9Z)(10 μmol/L,溶于50∶50 丙酮/水中,1%乙酸)为例,UV照射1~2 min后,在 +58 Da的位置清晰检测到光衍生化产物(m/z818.6)。从提取离子流图(XIC)可见,反应在1 min内即达到稳态。除PB产物外,一般还会检测到少量由丙酮的诺里斯类型1断裂和后续氧化所产生的副产物。nanoESI硼硅酸盐玻璃喷针的使用大大简化了实验装置的设计,实现了反应装置和离子源一体化。但由于nanoESI喷针中的脂质溶液受电渗流驱动,因此该装置仅对较小的流速范围(20 ~100 nL/min)适用[36]。
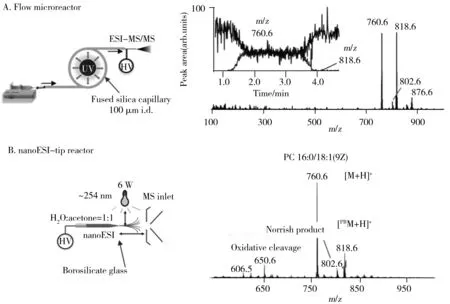
图2 两种反应器的脂质衍生化产率及反应动力学效果比较
在常规有机反应中PB反应通常需在mL级的有机溶剂中反应数小时,无法直接与ESI-MS联用。使用nanoESI-喷针反应器或者流式微反应器极大地提高了PB 反应和分析的速度。PB反应和在线MS分析在20~30 s即可完成,仅需数μL脂质溶液。丙酮作为PB反应试剂具有与大部分溶剂混溶、廉价易得、可直接作为电喷雾溶剂等优点。而与nanoESI-喷针反应器相比,流式微反应器的优点是反应动力学可精确控制、产率高、副反应少。更重要的是,后者能在较宽的流速范围内与ESI-MS及LC-MS联用[37]。
2.2 溶 剂
选择合适的溶剂对脂质的高效PB衍生化非常关键。合适的溶剂应该至少具备溶解性好和对紫外光呈惰性两个特点。例如,对脂肪酸和极性脂质(甘油磷脂(GPs)和鞘磷脂(SMs)等)而言,丙酮/水是最佳的溶剂体系。在丙酮/水中,PB反应的产率较高,同时丙酮/水也是良好的电喷雾溶剂。在溶解性方面,浓度在~100 μmol/L的脂质均可溶于丙酮/水。而对非极性脂质(如糖脂和固醇酯)而言,丙酮/水并非最佳的溶剂体系。例如,用于胆固醇酯(CE)在线衍生化的最佳溶剂体系是含有100 μmol/L LiOH的丙酮/甲醇/二氯甲烷/水(40∶30∶20∶10,体积比)体系[38]。
2.3 副反应
254 nm UV辐射会导致丙酮发生诺里斯类型1断裂[39-40],产生乙酰基(·C(O)CH3)和甲基(·CH3)。这些自由基会从脂肪酰/烷链中捕获丙基氢,产生脂质自由基。脂质自由基会继续与甲基或乙酰基结合,产生稳定取代产物。为了有效减少诺里斯类型1副反应对脂质分析的不利影响,可适当减少紫外光照射时间。尽管反应产率会有所下降,却可以大大降低副反应的干扰。此外实验发现,如果在溶剂体系中加入乙醇等醇类物质,也会在降低PB反应产率的同时,提高反应的选择性,这对于多不饱和脂质的分析往往是有利的。但要注意醇类物质也会被自由基夺氢,并继续与不饱和脂质反应。导致副产物生成的另一个因素是氧气。一般而言,PB反应需在无氧条件下进行。如果存在氧气,反应过程中所产生的脂质自由基会迅速与氧气反应,生成过氧化产物[41],其在抑制PB反应的同时会降低分析灵敏度。
2.4 典型PB反应规律


图3 几种典型脂质的衍生质谱图
3 利用PB-MS/MS分析不同类型脂质的结构

3.1 脂肪酸的分析


图4 油酸(FA 18∶1(9Z))PB产物的碎裂规律及特征离子结构
3.2 不饱和甘油磷脂的分析



图5 脂质结构解析的一般流程:PS 16∶1/18∶1在负离子模式下的PB-MS/MS谱图(A),A中m/z 339.3处对应离子的MS3谱图(B),A中m/z 311.2处对应离子的MS3谱图(C),PE 16∶1/18∶1的MS/MS谱图(D),在m/z 714.6处的去质子PE 16∶1/18∶1的MS/MS谱图(E),PE 16∶1/18∶1在正离子模式下的PB-MS/MS谱图(F)
3.3 胆固醇酯的分析
3.4 脂质位置异构体的定量分析
4 鸟枪脂质分析法
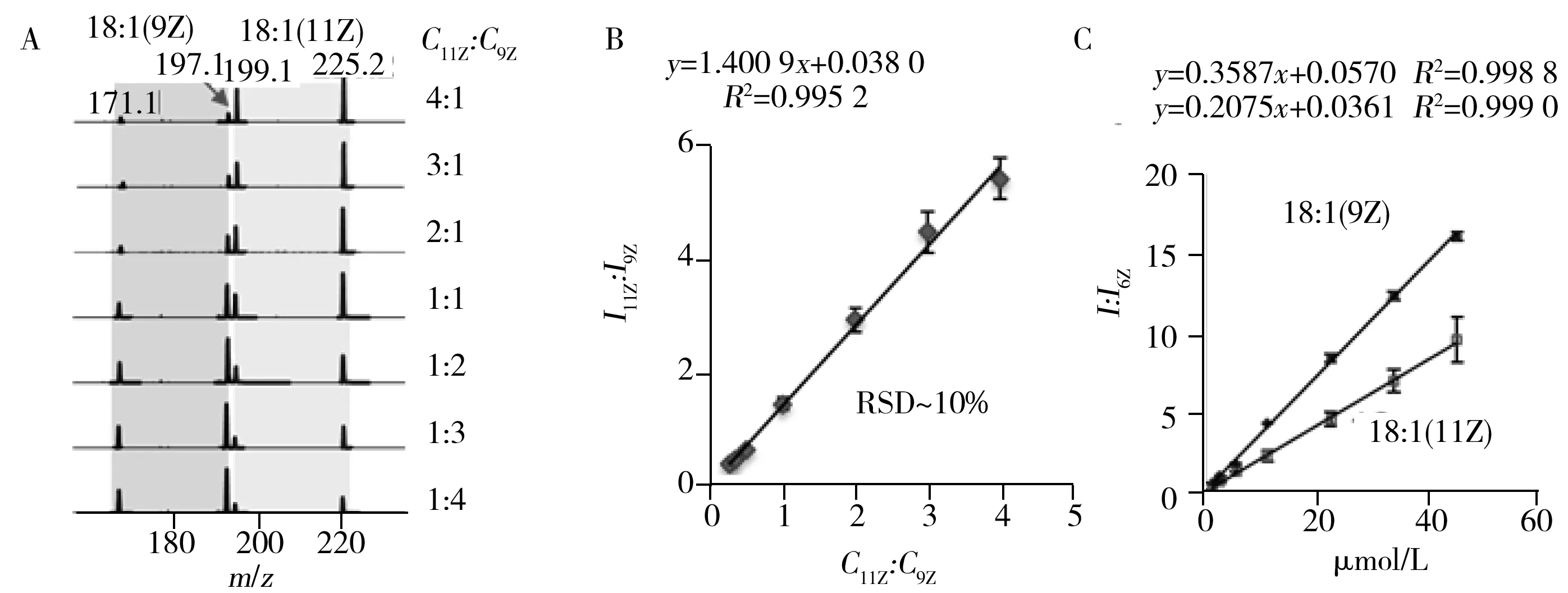
图6 通过PB-MS/MS对脂质异构体进行定性和定量分析:不同摩尔比例(在右边指出)的FA 18∶1的Δ9和Δ11混合物的PB-MS/MS分析(A);建立在FA 18∶1的Δ9和Δ11异构体的诊断离子比例(I11Z/I9Z)和摩尔比例(C11Z/C9Z)间的线性关系(B);以FA 18∶1(6Z)作为内标定量FA 18∶1的Δ9和Δ11异构体的标定曲线(C)
5 PB反应与质谱成像



6 结论与展望




