两种多重核酸血液筛查系统在血液筛查应用中的比较
刘彦哲,李 萍,吉尚志,晏 虹,金桂月,刘天尧,姜雨杉,王慧媛,郑 璐
1.黑龙江省哈尔滨市血液中心,黑龙江哈尔滨 150056;2.新疆维吾尔自治区阿勒泰地区中心血站,新疆阿勒泰 836500;3.北京万泰生物药业股份有限公司,北京 102206
近年来,随着检测技术日益革新和国家对血液安全筛查的日益重视[1],核酸扩增技术(NAT) 以其高灵敏度,能显著缩短病毒感染检测窗口期,降低输血传播病毒风险[2]的优势,成为目前血液筛查的主要手段之一[3-4]。多重核酸[5]血液筛查试剂能在一支反应管中,同时检测并区分乙型肝炎病毒(HBV)、丙型肝炎病毒(HCV)和人类免疫缺陷病毒(HIV),凭借灵敏度高、特异性好、节约检测成本、方便快捷等优势[6],成为市场应用的主流类型试剂。
哈尔滨市血液中心有两套多重核酸血液筛查检测系统,一套为北京万泰生物药业股份有限公司的Wantag2.0系统,一套为罗氏诊断公司的Cobas S201全自动血液核酸筛查系统,通过比较这两套系统在2018年1-10月的标本检测数据,分析二者的差异及原因,现报道如下。
1 资料和方法
1.1一般资料 选择2018 年1-10月哈尔滨市血液中心经ELISA 检测结果HBV表面抗原(HBsAg)、HCV抗体(抗-HCV)和HIV抗原/抗体(HIV Ag /Ab)均为阴性的无偿献血者的血浆标本,共计123 116份。
1.2主要试剂与仪器 罗氏诊断Cobas S201 全自动血液核酸筛查平台:Hamilton Microlab Star全自动混样仪(瑞士Hamilton),Cobas S201 AmpliPrep 核酸提取仪,Cobas S201 TaqMan核酸扩增检测仪,Cobas TaqScreen MPX Test,version2.0 核酸检测试剂盒(批号:215559、232401、257278、283813)。北京万泰生物药业股份有限公司血液核酸筛查平台:核酸混样系统(Tecan自动混样平台),核酸提取仪器(Thermo kingfisher96)伯乐CFX-96 扩增系统(美国伯乐公司),北京万泰HBV、HCV、HIV 1型核酸检测试剂盒(PCR-荧光法)(批号:BCI 20170902、BCI 20171203、BCI 20180301、BCI 20180903),久保田低温离心机(型号:8730);BIOBASE生物安全柜(型号:11240 BBC 86;11230 BBC 86);阳普真空采血管脱盖机(型号:DC-1);ELISA所用试剂:检测HBV使用的是上海科华公司的HBsAg诊断试剂盒(批号:201706221、201709311、201712461、201802061)和法国伯乐公司的HBsAg诊断试剂盒(批号:7A0226、7G0232、7M0239、8C0244);检测HCV使用的是北京万泰公司的抗-HCV诊断试剂盒(批号:CS20170706、CS20171009、CS20180202、CS20180405)和上海科华公司的抗-HCV诊断试剂盒(批号:201707181、201709251、201803061);检测HIV使用的是法国伯乐公司的HIV Ag/Ab诊断试剂盒(批号:7C0393、7J0409、8A0420、8C0428、8F0436)和珠海丽珠公司生产的HIV诊断试剂盒(批号:2017062008、2017093008、2018010208)。
1.3方法 标本采集后送检验科,当日分别采用两种不同厂家的ELISA试剂进行检测,次日从核酸标本管中挑除ELISA检测结果中HBsAg、抗-HCV和HIV Ag/Ab阳性的标本,剩余阴性标本采用两种核酸筛查系统进行核酸检测。罗氏系统是将6份标本汇集到一个标本池(Pool)后,再检测该Pool,每批次试验带有1 个阴性对照NC(-)和3个阳性对照(MPC、HIV-1 O组、HIV-2)和一个康彻斯坦外质控品;万泰系统与罗氏系统相同,也是将6 份标本汇集到一个Pool后,再检测该Pool,每批次试验带有1个阴性对照、1个阳性对照和一个康彻斯坦外质控品,每天两个系统各做一部分标本。罗氏系统通过软件自动判读结果,万泰系统根据其说明书标准判读结果。如果Pool检测为阴性,则该Pool内6份标本均直接出具阴性合格报告;如果Pool检测为阳性,对该Pool所有标本进行单检,并以单检结果为最终结果,单检阳性标本的血液制品淘汰,屏蔽该献血者。并对部分NAT 拆分反应为阳性的献血者做3个月的跟踪随访,采集其血样做常规ELISA检测及2 种系统的NAT 检测。
1.4结果分析 采用统计学软件SPSS 17.0对两种系统的阳性率、假阳性率和无效率进行统计分析。
2 结 果
万泰和罗氏系统分别检测86 475份和36 641份标本。两个检测系统的检测结果见表1。
对其中23份HBV 和1份HCV的核酸检测阳性的献血者进行跟踪检测,汇总其跟踪检测的HBsAg、抗-HCV和NAT结果,见表2。
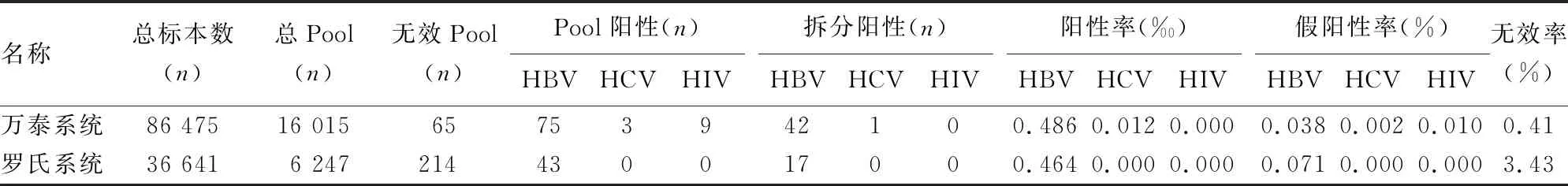
表1 两个核酸检测系统检测结果统计
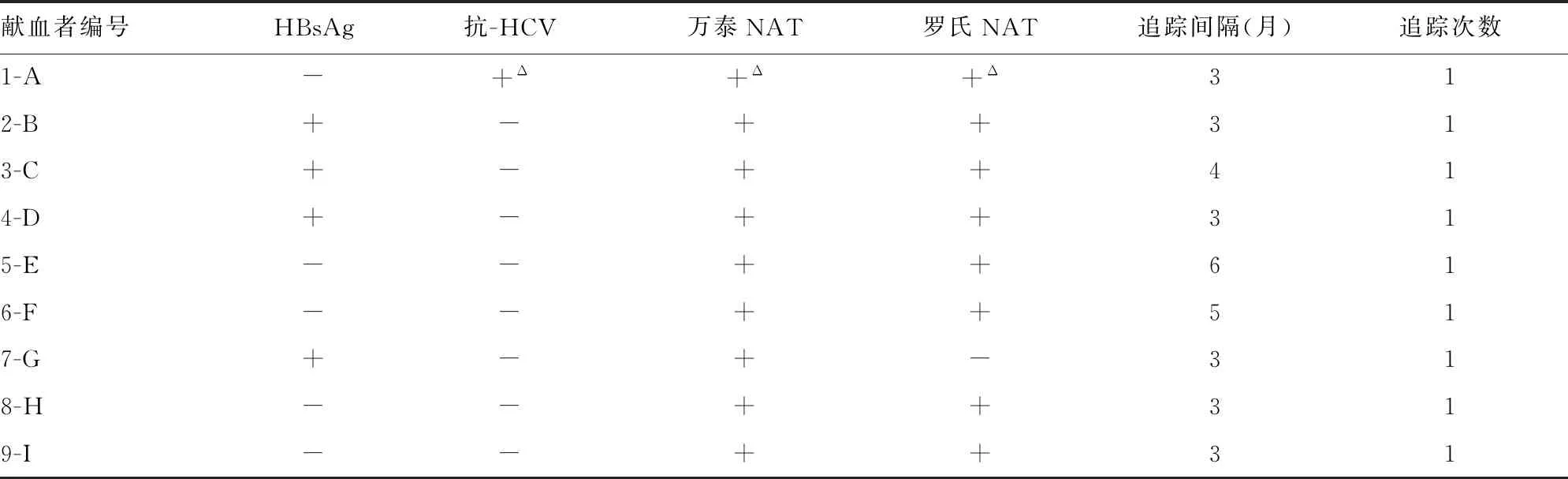
表2 两种NAT 平台检出有反应性献血者的追踪信息

续表2 两种NAT 平台检出有反应性献血者的追踪信息
注:1~24为献血者编号;其中A~Q标识为万泰系统初检阳性标本,a~g标识为罗氏系统初检阳性标本。-表示无反应性,+表示有HBV反应性;+Δ表示有HCV反应性。
3 讨 论
本研究通过用哈尔滨市血液中心的两套多重核酸检测系统检测2018年1-10月ELISA结果阴性的献血人群标本,并对两个检测系统部分核酸阳性标本追踪检测,最后汇总分析数据,分别从阳性率、假阳性率及无效率等方面对两个系统的性能差异进行比较及分析。
两种多重核酸检测试剂均能从ELISA阴性标本中检测出一定比例的HBV核酸阳性标本,其中万泰系统检测HBV核酸阳性率和假阳性率分别为0.486‰、0.038%,罗氏系统检测HBV核酸阳性率和假阳性率分别为0.464‰、0.071%,这与哈尔滨地区2016年报道罗氏系统的HBV阳性率0.469‰相符合[7]。在本研究中,万泰系统的HBV阳性率略高于罗氏系统的阳性率,趋于一致,但万泰系统HBV的假阳性率要明显低于罗氏。对两个系统的部分核酸阳性标本回访追踪发现,23份HBV核酸阳性标本(万泰16份,罗氏7份)中有14份ELISA复检为HBsAg阳性,初步判定这些标本为窗口期标本,表明这两种核酸检测试剂对于防止ELISA试剂窗口期标本[8-11]的漏检具有重要意义。这14份ELISA阳性标本中共有2份为两个核酸检测系统各有一阴一阳的情况,这种差异可能与这两个系统HBV引物探针设计的位点差异不同有关[12],也表明这两种系统具有一定的互补性。同时,值得注意的是,这14份追踪ELISA阳性标本中有1份标本在两个核酸检测系统检测均为阴性,该情况可能与病毒感染阶段、患者用药或者病毒区段缺失或变异有关[13],也进一步表明核酸方法也存在一定程度的漏检风险,故ELISA和核酸两种检测方法具有一定的互补性;另外,有9份追踪标本ELISA复检仍为HBsAg阴性,但核酸阳性,初步分析这9份标本可能与隐匿性HBV感染(OBI)有关[14-16]。
万泰系统检测出1例HCV核酸阳性(罗氏未检测该份标本),罗氏系统未检到HCV核酸阳性,后续两个核酸系统跟踪检测该标本均为HCV阳性,该份标本为HCV窗口期标本,这种差异和两种系统的检测标本量不同(万泰系统检测86 475份,罗氏系统检测36 641份)及HCV经ELISA筛选过的标本核酸阳性率较低有关。但罗氏系统的HCV和HIV假阳性率要低于万泰系统,这可能与两个系统的自动化封闭水平有关。罗氏系统是集核酸提取、扩增和检测于一体的全自动检测系统,干扰因素少;万泰系统的提取与扩增检测是2个独立的系统,人工操作环节相对偏多,会增加污染的概率,但随着人员操作的日益熟练及实验室的逐步规范,假阳性率会有进一步提高。
由于两种系统检测的并非相同标本,且万泰系统检测的标本量要明显多于罗氏系统,所以数据可能存在一定的偏差,但由于所检测的标本是分布于同一地区同一时间段的人群中,从采血到检测均严格按照标准操作规程进行,故其影响较小,因此,该数据具有一定的现实意义和参考价值[17]。
两个系统在无效率方面,罗氏系统的无效率较高,达到3.43%,多与仪器故障有关,而万泰系统的无效率较低,为0.41%,多与试剂检测异常有关。
两个多重核酸检测系统相对于各自的三联检测系统都具有明显的优势,在成本上,万泰检测系统在扩增检测环节可节省近2/3的仪器和耗材,罗氏系统的多重和原三联检测的成本变化不大,因为原罗氏三联系统也是一管多检,只是不能区分具体检测项。在检测时间上,多重检测系统或节省30~60 min的检测时间或去除了鉴定环节时间,且能减少更多的人为操作,方便快捷。
综上所述,从比较两种多重核酸血液筛查系统的综合性看,两个系统均能降低“窗口期”标本漏检的风险;万泰系统的HBV阳性率、假阳性率及整体无效率优于罗氏系统;在HCV和HIV核酸的检测能力上两种系统基本一致,但罗氏系统假阳性率低于万泰系统。由于ELISA阴性标本的HCV和HIV核酸阳性率较低,后续研究需继续统计、比较;罗氏系统检测自动化水平优于万泰系统,但无效率偏高,万泰试剂的检测设备尽管无效率较低,但在自动化水平方面需要进一步整合、提高。

