共掺杂态聚苯胺/环氧树脂复合涂层的耐蚀性分析
宋 航 李 栋 王金福 陈志强
(青岛双瑞海洋环境工程股份有限公司,山东 青岛 266101)
0 引言
金属腐蚀带来的经济损失、安全事故、能源浪费、环境污染等问题阻碍了生产发展和科技进步,在金属表面覆盖一层涂层是防腐蚀最有效的办法之一。自MacDiarmid等[1]发现聚苯胺(PANI)掺杂可形成优良导体后,国内外的学者开始对其进行深入研究。掺杂态聚苯胺及聚苯胺衍生物作为导电高分子聚合物,能有效降低不锈钢[2,3]、低碳钢[4,5]、 铜[6,7]、铝[8,9]等金属的腐蚀速率。Deberry等[10]还发现导电聚苯胺可以促进不锈钢钝化。多种防腐蚀机理促使聚苯胺被广泛地应用在防腐涂料中。聚苯胺的合成[11,12]有化学聚合法和电化学聚合法。化学聚合法中的乳液聚合法具有聚合速率快,产物形貌均一、分子量大等特点,应用广泛。在化学聚合过程中反应物以及氧化剂的浓度、体系的pH、反应温度及时间都直接影响着聚苯胺合成的形貌及性质。将盐酸、磷酸[13,14]等质子酸作为掺杂剂嵌入聚苯胺骨架中,可使合成的聚苯胺具有良好的导电性。大多数文献用十二烷基苯磺酸(DBSA)做乳化剂合成具有良好结构和稳定性的聚苯胺。而十二烷基苯磺酸钠(SDBS)不仅可以做乳化剂,而且在酸性条件下可以作为共掺杂剂参与合成聚苯胺。正丁醇作为助乳化剂的一种,可以参与乳化剂在油水界面的分子排列,减小乳液的粒径,加强乳化效果[15];同时其还可作为多元醇类环氧稀释剂,降低环氧体系黏度,增大流动性。
本文分别选用盐酸和磷酸做质子酸掺杂剂,以十二烷基苯磺酸钠作乳化剂和共掺杂剂,正丁醇为助乳化剂,采用低温慢速搅拌乳液聚合法制备了具有一定电导率的束状聚苯胺,并加入环氧树脂涂料中,涂覆在Q235低碳钢上。通过电化学阻抗谱和浸泡试验,考察了聚苯胺/环氧树脂复合涂层的耐 蚀性。
1 实验
1.1 原料、基材及其预处理
苯胺(ANI,含量>99.8%,经二次减压蒸馏后使用)、过硫酸铵(APS)、十二烷基苯磺酸钠(SDBS)、浓磷酸、浓盐酸、正丁醇,上述试剂均为分析纯,由国药集团化学试剂有限公司提供。苯基缩水甘油醚,上海麦克林生化科技有限公司;凤凰牌环氧树脂E44,蓝星新材料无锡树脂厂;南亚牌固化剂593,昆山南亚环氧树脂公司;环氧助剂,美国道康宁公司等。
基材为Q235低碳钢,用500目和800目的金相砂纸反复打磨至表面光亮,再进行除油,依次用丙酮、无水乙醇、去离子水冲洗,再超声洗净,氮气吹干。
1.2 聚苯胺乳液及其粉末的制备
配制质子酸(HCl或H3PO4)水溶液,分成等量两份,称为A、B液。先在A液中加入SDBS,充分搅拌至溶解,再缓慢滴入ANI至形成乳白色乳液,然后滴入2~5滴正丁醇,泡沫消除后静置。在B液中加入APS,充分搅拌至溶解。质子酸、APS、SDBS与ANI的摩尔比为1∶1∶1∶1,总摩尔浓度1mol/L。将A、B液预冷至反应温度0~5°C,随后在搅拌(150r/min)下将B液缓慢滴入A液,0.5h内滴完,反应6h后保持反应温度静置12h,使乳浊液静置破乳,得到共掺杂态的PANI溶液。
抽滤PANI溶液,再洗涤过滤物数遍至滤液无色,得到PANI滤饼,在60°C下真空干燥24h,最后研磨,即得共掺杂态的PANI粉末。分别用(HCl+DBSA)-PANI和(H3PO4+DBSA)-PANI代表盐酸和磷酸与十二烷基苯磺酸共掺杂的聚苯胺。
1.3 共掺杂态聚苯胺/环氧树脂复合涂层的制备
将环氧树脂与苯基缩水甘油醚按质量比2∶1混合均匀,分别依次加入占总体系0.02wt.%的环氧助剂(消泡剂、流平剂、分散剂、树脂粘结促进剂),充分搅拌1h后加入占体系质量分数1%的共掺杂态PANI粉末,再搅拌1h、超声10min,再按m(环氧树脂)∶m(固化剂)=4∶1加入固化剂,充分搅拌15min,超声3min,静止至气泡消散,得到PANI均匀分散的环氧树脂涂料。
用移液枪移取等量的涂料于碳钢试样上,用软毛刷单面涂覆均匀,膜厚控制在50 μ m左右。电化学实验中的涂覆面积为10×10mm,化学浸泡试验中的涂覆面积为40×30mm,在30°C下恒温干燥48h。不加入共掺杂态PANI粉末即得纯环氧(EP)涂层。
1.4 表征与性能测试
1.4.1 聚苯胺的表征
采用德国布鲁克的EQUINOX55型傅里叶变换红外光谱仪(T-IR),用KBr压片法制样,通过分析比对峰值来判断官能团类型以确定共掺杂态PANI的结构组成。用美国FEI公司的Quanta 450型扫描电镜(SEM)观察PANI的表面形貌,放大5000倍,进一步确定PANI的微观形貌。用日本岛津的6000型X射线衍射仪(XRD)分析共掺杂态PANI的结晶度,扫描速率为0.02°/s,扫描范围5°~ 40°。用北京菁美瑞科技公司的RTS-8型数显式四探针测试仪测试PANI片的电导率,压片直径10mm。
1.4.2 复合涂层的表征
(1)厚度与结合力
用TT260覆层测厚仪测得涂层的厚度平均为 50μ m。参考GB/T 9286—1998《色漆和清漆 漆膜的划格试验》在涂层上纵横垂直交叉划格,间距1mm,用胶带测得涂层的附着力为0级;
(2)电化学性能
用上海辰华CHI750E型电化学工作站测量复合涂层的电化学阻抗谱(EIS)。采用三电极体系:工作电极为涂层试样,辅助电极为铂电极,参比电极为饱和甘汞电极(SCE)。腐蚀介质为3.5%NaCl溶液,在开路电位下测量,先稳定30min再测,正弦波扰动电位幅值为5mV,扫描频率0.01~100000 Hz。用ZSimpWin软件拟合数据。共浸泡150d;
(3)耐蚀性
用刀片划透复合涂层,呈“×”形,浸泡在37°C(水浴加热)的3.5% NaCl溶液中,10d后观察涂层表面的变化,以判断腐蚀情况。
2 结果与讨论
2.1 红外光谱分析
由图1对照表1可知,3445cm-1处为N-H伸缩振动峰,1127cm-1和799cm-1两处分别为苯环上=C-H面内和面外弯曲峰。1570cm-1和1489cm-1两处分别存在醌式结构和苯式结构中的C-C伸缩振动峰,1298cm-1处的峰则对应于C-N伸缩振动。而在1031、665和578cm-1处出现较强吸收峰,分别对应于S-O、C-S和S-O的伸缩振动,说明存在磺酸基团-SO3H;2913 cm-1处有DBSA中烷烃的C-H伸缩振动峰,表明引入了十二烷基苯磺酸大分子。
2.2 扫描电镜分析

图1 (HCl+DBSA)-PANI和(H3PO4+DBSA)-PANI的FT-IR谱图
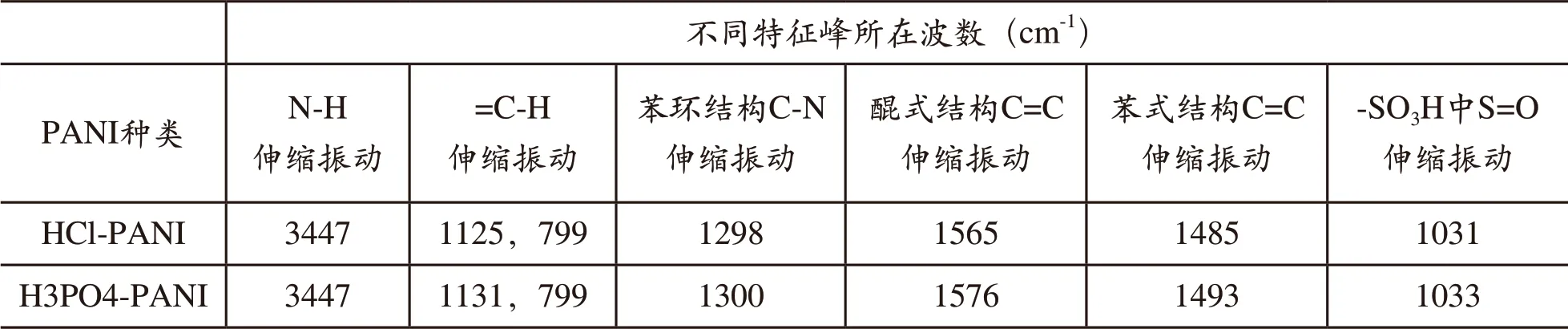
表1 聚苯胺的部分特征吸收峰及其在红外谱图中的位置
如图2所示,两种掺杂态PANI皆呈束状结构,直径0.5~1.0 μm,长度10.0~20.0μm。这是因为在乳液聚合时,大分子磺酸基团与ANI分子相互作用,使ANI不再是直接聚合成单一的PANI单元,而变为沿着PANI分子链方向的纵向生长并延长。其中(H3PO4+DBSA)-PANI虽呈束状,但结构疏松凌乱,表面还有未参与纵向生长的PANI颗粒,而(HCl+DBSA)-PANI的束状结构均一、规整,层层叠加可使覆层变得严实致密,添加至涂料中能增大涂层的屏蔽效应。
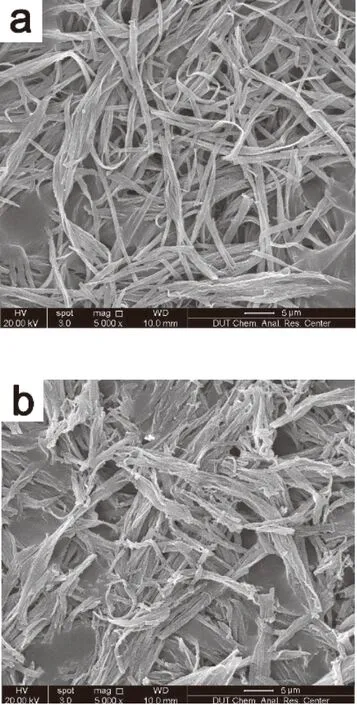
图2 不同质子酸与十二烷基苯磺酸钠共掺杂制备的聚苯胺的SEM照片(a,盐酸;b,磷酸)
2.3 X射线衍射分析
观察图3可知,两种掺杂态PANI在2θ = 20.5°和25.5°处均出现了较宽的衍射峰,说明它们具有一定的结晶度。这是因为HCl与H3PO4在苯胺的聚合过程中,因质子化产生的阳离子与溶液中的阴离子共同作用,使PANI分子链中的部分N原子形成了类似有机“季铵盐”的结构,加强了分子链间作用力,结晶取向增大[16]。且大分子酸DBSA的掺杂使更多的阳离子自由基电荷离域至苯环中的胺基(R-N-R)上,DBSA的支链阻断了致密的PANI链结构,使PANI分子链排列变得规整[17]。
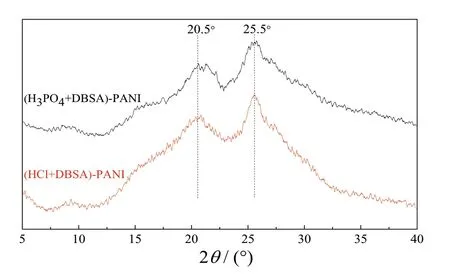
图3 (HCl+DBSA)-PANI和(H3PO4+DBSA)-PANI的XRD谱图
2.4 电导率分析
电子型导电高分子的载流子主要是电子,前文证实了HCl、H3PO4与DBSA共掺杂PANI均具有一定的结晶取向,分子紧密整齐地堆砌排列,分子间键桥为电子提供了有利于传递的通道,电导率随晶体部分的有序排列程度而变化。(HCl+DBSA)-PANI和(H3PO4+DBSA)-PANI的结晶度相差不大,因此它们的电导率较为相近,前者为0.23S/cm,后者为1.67S/cm,处于同一数量级。但(HCl+DBSA)-PANI的分子链间距大于(H3PO4+DBSA)-PANI分子链间距,减弱了分子链间作用力,降低了链间的电荷转移,故其电导率略小[18]。
2.5 电化学阻抗谱分析
2.5.1 不同掺杂酸对聚苯胺/环氧树脂(PANI/EP)复合涂层耐蚀性的影响
从图4可见,(HCl+DBSA)-PANI/EP复合涂层测得的Bode图中低频处模值和Nyquist曲线上半圆弧的直径远大于(H3PO4+DBSA)-PANI/EP复合涂层测得的结果。

图4 不同共掺杂聚苯胺/环氧树脂复合涂层的电化学阻抗谱和等效电路
在等效电路图中,Rs是溶液电阻,Qc是涂层电容,Rc是涂层孔隙电阻。由于电极表面存在弥散效应,引入常相位角元件Q来代替理想电容C,以弥补真实电容和理想电容之间的偏差[19]。鉴于膜层的特殊结构,用n和Q共同表示不稳定电流引起的阻抗变化,n称为弥散指数(0<n<1),其值越趋于1越接近理想电容,越趋于0则越接近理想电阻[20]。Rc显示了离子在金属基体和涂层间传导的途径,它的值越大,离子越不容易渗透进涂层。复合涂层在浸泡前期显示了1个时间常数,表明涂层的耐蚀性主要以屏蔽作用为主。如表2所示,(HCl+DBSA)-PANI/EP涂层比(H3PO4+DBSA)-PANI/EP涂层的Rc大了约1个数量级,表明前者涂层的屏蔽作用更强。这是因为(HCl+DBSA)-PANI粉末的束状结构更均一,加入环氧涂层后交叉层叠,迷宫效应优于(H3PO4+DBSA)-PANI,可减缓离子渗入的速率,所以屏蔽作用更好。
综上所述,(HCl+DBSA)-PANI/EP涂层的耐蚀性优于(H3PO4+DBSA)-PANI/EP涂层,对碳钢基底的保护作用更为优异。
2.5.2 (HCl+DBSA)-PANI/EP复合涂层与纯环氧树脂涂层耐蚀性的对比
选用防腐蚀效果较优的(H C l+D B S A)-PANI/EP涂层与纯EP涂层进行对比。电化学阻抗谱如图5所示,等效电路拟合图如图6所示,拟合结果如表3所示。由两种涂层的Nquist图可知,(HCl+DBSA)-PANI/EP涂层的初始阻抗半弧比EP涂层大了接近3个数量级;Bode图显示,(HCl+DBSA)-PANI/EP涂层浸泡至第150d时仍只有1个时间常数,处于腐蚀浸泡初期,而纯EP涂层只有10d。

表2 等效电路的拟合结果

图5 不同涂层在3.5 wt.%氯化钠溶液中的电化学阻抗谱
从表3可知,在腐蚀浸泡的初期,(HCl+DBSA)-PANI/EP涂层电阻Rc高达3.5×1010Ω·cm2,这在厚度小于100μm的涂层中是极为罕见的。随着腐蚀浸泡的延长,在第150d减小至1.1×108Ω·cm2,且在109Ω·cm2的高阻值下维持了至少60d。在整个腐蚀浸泡期间,其EIS拟合结果显示只有1个时间常数,表明了涂层长期处于腐蚀浸泡初期,等效电路中分别对应了涂层电容Qc和涂层电阻Rc。此时涂层的屏蔽性能优异,没有腐蚀介质到达涂层内部,这也印证了SEM分析的结果,(HCl+DBSA)-PANI具有束装的分子结构,将其添加在EP涂层中可以提供特殊的迷宫效应,极大增强了涂层本身的屏蔽作用。
而纯EP涂层的屏蔽效应明显很差,仅浸泡了15d,涂层电阻Rc就从1.5×108Ω·cm2降至1.0×106Ω·cm2,这与(HCl+DBSA)-PANI/EP涂层的耐蚀效果相差甚远。浸泡到第30d时,涂层电阻Rc仅为2.2×103Ω·cm2,电荷转移电阻Rc为2.0×105Ω·cm2,基本失去了涂层的防腐蚀作用。在第10d之后进入腐蚀浸泡的中后期,其EIS拟合结果显示了2个时间常数,EIS高频区的时间常数对应涂层电容Qc和涂层电阻Rc,在中低频区的时间常数则对应涂层与基体界面的双电层电容Qdl和电荷转移电阻Rct。
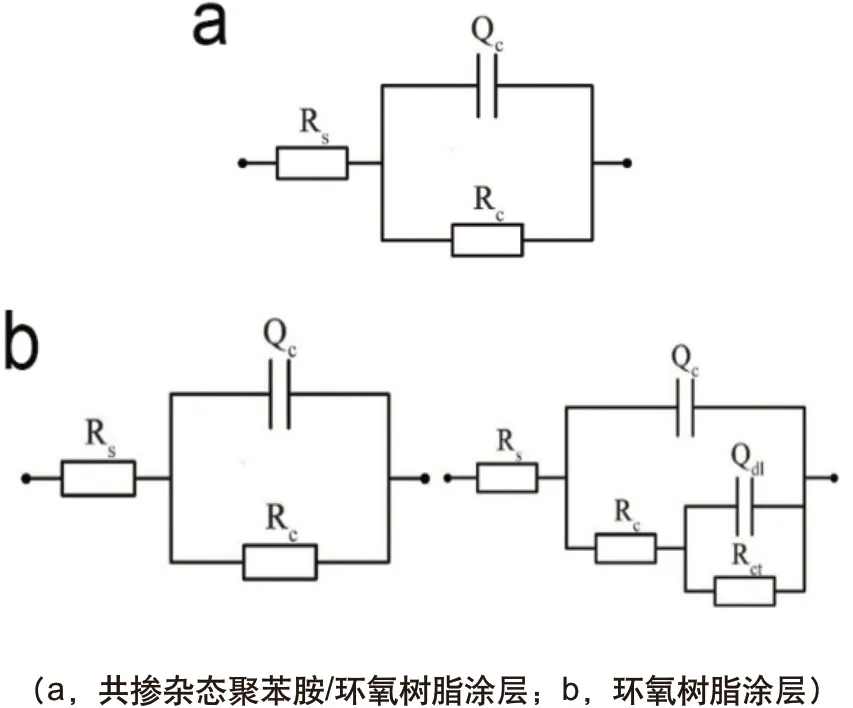
图6 不同涂层拟合的等效电路图

表3 等效电路的拟合结果
与优化前相比,优化后的(HCl+DBSA)-PANI/EP复合涂层具有更为优秀的耐蚀性能,其Bode图0.01Hz处模值|Z|较优化前提高了105数量级,耐蚀周期至少提高了5个月。
2.6 极化曲线分析
图7为(HCl+DBSA)-PANI/EP复合涂层在3.5wt.% NaCl腐蚀溶液下浸泡150d后测得的动电位极化曲线谱图,并以浸泡10d的纯EP涂层和浸泡初期(第1d)的裸钢试样作为参照,拟合了极化曲线如表4所示,其中Icorr为自腐蚀电流密度,Ecorr为自腐蚀电位,Rp为极化电阻,CR为腐蚀速率,PE(Protection Efficiency)为保护效率,采用公式(1)计算[21]:

在这里,I0corr代表裸钢的自腐蚀电流密度,代表复合涂层的自腐蚀电流密度。从表中数据可以看出,涂覆(HCl+DBSA)-PANI/EP复合涂层后,尽管已经在腐蚀溶液中浸泡150d,但仍对碳钢基体具有优秀的保护作用。自腐蚀电流密度Icorr较裸钢明显减小,由4.95×10-5A·cm-2降低至3.82×10-9A·cm-2,甚至比浸泡10d的纯EP涂层的自腐蚀电流密度Icorr还要低;腐蚀速率CR也由5.82×10-1mm·year-1降低至4.49×10-5mm·year-1;保护效率PE高达99.99%。涂覆共掺杂态的PANI后,自腐蚀电位Ecorr由裸钢的-0.687V正移至-0.407V,且较纯EP涂层的-0.592V也有正移,这也进一步表明了其对碳钢基体优良的防腐蚀性能。

表4 共掺杂态聚苯胺/环氧树脂复合涂层的极化曲线拟合结果
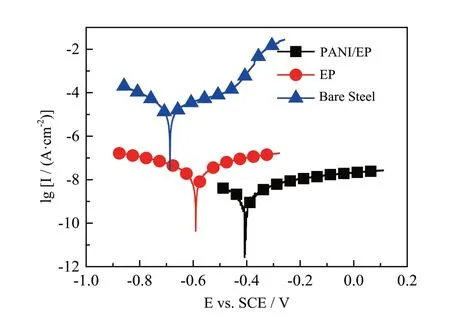
图7 共掺杂态聚苯胺/环氧树脂涂层的极化曲线
2.7 浸泡试验
如图8 所示,为涂覆1.0 w t.%的共掺杂态 (HCl+DBSA)-PANI /EP涂层和纯EP涂层在37°C条件下浸泡10d的前后对比图。
浸泡试验前,涂层均光滑平整,无腐蚀存在。浸泡10d后,与纯EP涂层对比发现(HCl+DBSA)—-PANI/EP涂层表面的锈蚀只分布在划痕部位,观察涂层没有发生起泡现象,划痕也没有明显的扩大迹象。去掉涂层后,(HCl+DBSA)-PANI /EP涂层碳钢基体上的腐蚀产物只堆积在划痕处,说明在划痕处有腐蚀发生,但基体四周及被涂层覆盖的其他部位均没有被腐蚀,而纯EP涂层的基体四周却发现轻微的腐蚀现象。表明(HCl+DBSA)-PANI/EP涂层与基体的结合力更加良好,在加速腐蚀浸泡试验期间也没有发生鼓泡现象,对碳钢基体起到了保护作用。这印证了电化学试验的结果。

图8 涂覆不同涂层的碳钢试样在37 ℃的3.5%氯化钠溶液中浸泡10d后的情况
3 结语
(1)以HCl或H3PO4做质子酸,SDBS做乳化剂和共掺杂剂,用低温慢速搅拌乳液聚合法制得了共掺杂态的PANI,在PANI链中引入了十二烷基苯磺酸大分子,呈现出大小均一的大分子束状结构,具有一定的结晶度和电导率;
(2)将共掺杂的P A N I 添加至环氧树脂涂料中,涂覆于Q235低碳钢表面,得到了致密度高,结合力好的复合涂层。极大地增强了涂层的屏蔽作用,提高了环氧涂层的耐蚀性能。其中(HCl+DBSA)-PANI/EP涂层比(H3PO4+DBSA)-PANI/EP涂层具有更有效的保护作用;
(3)该涂料具有良好的流动性,有效增大了涂层的耐蚀性,很好地解决了聚苯胺的分散问题,可广泛用于工业涂料中。

