Bacillus paralicheniformis左聚糖蔗糖酶基因克隆表达及酶学性质研究
丛豪 罗宁 黄飞 梁月昭 陈硕昌 张声峰 朱萍 杨辉

摘要:【目的】從耐热菌株中克隆表达左聚糖蔗糖酶基因,以获得热稳定性较好、底物耐受性高的重组酶,为左聚糖蔗糖酶催化机理及生产应用研究提供技术基础。【方法】从市售菌肥中筛选耐热菌株并克隆其左聚糖蔗糖酶基因,以pSE380为载体构建重组质粒并转化至大肠杆菌诱导表达,随后通过镍亲和层析获得电泳纯的重组左聚糖蔗糖酶并研究其酶学性质。【结果】分离到耐热菌株LN-05,经16S rDNA序列分析鉴定为Bacillus paralicheniformis。克隆表达的B. paralicheniformis左聚糖蔗糖酶与已公布地衣芽孢杆菌(B. licheniformis)RN-01的左聚糖蔗糖酶存在19个氨基酸残基差异。重组酶催化水解反应最适pH为6.0,最适温度为45 ℃,于40和45 ℃保温3 h后残余酶活力分别为89%和78%。Mn2+、Ag3+和Cr2+对重组左聚糖蔗糖酶的水解活力有明显抑制作用,Co2+和Al3+对水解活力具有一定促进效果;Ba2+、Mg2+和Mn2+对聚合活力有明显抑制作用,Ag3+、Cu2+和K+对聚合活力具有促进作用。EDTA对重组酶水解活力和聚合活力均具有抑制作用。在最适条件下,重组左聚糖蔗糖酶的最大反应速率(Vmax)=74 μmol/(min·mg),米氏常数(Km)为7.57 mmol/L。催化聚合反应的最适温度随着底物蔗糖浓度而变化,当蔗糖浓度为50%时,最适温度为40 ℃;最适聚合反应pH为5.0;当酶浓度为0.9 U/mL,在最适条件下反应24 h,左聚糖产糖量达183.00±1.73 g/L,蔗糖转化率为(36.76±1.84)%。【结论】B. paralicheniformis左聚糖蔗糖酶的热稳定性较好,左聚糖产量高,具有转化蔗糖生产高附加值左聚糖的应用潜力。
关键词: Bacillus paralicheniformis;左聚糖蔗糖酶;克隆表达;酶学性质;热稳定性
中图分类号: S188.3 文献标志码: A 文章编号:2095-1191(2020)11-2808-09
Cloning,expression and enzymatic properties of the levansucrase gene from Bacillus paralicheniformis
CONG Hao1,2, LUO Ning1, HUANG Fei1, LIANG Yue-zhao1, CHEN Shuo-chang1,
ZHANG Sheng-feng1, ZHU Ping1, YANG Hui1,2,3*
(1College of Life Sciences and Technology, Guangxi University, Nanning 530004, China; 2Guangxi Research Center for Microbial and Enzyme Engineering Technology, Nanning 530004, China; 3State Key Laboratory for
Conservation and Utilization of Subtropical Agro-bioresources, Nanning 530004, China)
Abstract:【Objective】Cloning and expressing of a levansucrase gene from heat-resistant strains in order to obtain a recombinant enzyme with good thermal stability and high substrate tolerance,which would provide basis for the study on catalytic mechanism and levansucrase production. 【Method】Heat-resisting strain was screened from commercial fertilizer. Then the gene of levansucrase was cloned. With pSE380 as vector, recombinant plasmid was constructed and transformed into Escherichia coli induced expression. Then electrophoresis pure recombinant levosucrase was obtained by nickel affinity chromatography and its enzymatic properties were studied. 【Result】A heat-resistant strain LN-05 was isola-ted and identified as Bacillus paralicheniformis by 16S rDNA sequencing analysis. B. paralicheniformis levansucrase was then cloned and expressed, which had nineteen amino acid residues difference from the B. licheniformis RN-01 levansucrase previously reported. The enzymatic properties showed that the optimum pH of hydrolysis reaction was 6.0,the optimum temperature was 45 ℃. The residual activity were 89% and 78% of the enzyme incubated for 3 h at 40 and 45 ℃,respectively. The presence of Mn2+,Ag3+ and Cr2+ inhibited hydrolytic activities while Co2+ and Al3+showed positive effects. Ba2+,Mg2+ and Mn2+ had inhibitory effect on the polymerization activities, while Ag3+,Cu2+ and K+had positive effects. EDTA had an inhibitory effect on both recombinant enzyme hydrolysis activity and recombinant enzyme polymerization activity. Under the optimal conditions,the maximum reaction rate(Vmax) of the recombinant levansucrase was Vmax=74 μmol/(min·mg),Michaelis constant(Km)=7.57 mmol/L. The optimum temperature of polymerization reaction varied with the sucrose substrate concentration. The optimum temperature was 40 ℃ at the sucrose concentration of 50%, and its optimum polymerization pH was 5.0. Reacted with 0.9 U/mL enzyme under this optimum condition for 24 h, the amount of the produced levan reached about 183.00±1.73 g/L and the conversion yieldwas(37.76±0.80)%. 【Conclusion】The obtained B. paralicheniformis levansucrase has fine thermal stability and high levan yield, and has the potential to transform sucrose to high value-added levan.
Key words: Bacillus paralicheniformis; levansucrase; cloning and expression; enzymatic properties; thermal stability
Foundation item: Guangxi Natural Science Foundation(2017GXNSFAA198128); Science Research and Techno-logy Development Project of Nanning(20141015)
0 引言
【研究意义】左聚糖是一种由果糖基组成的多糖,其纯品为白色粉末,无味、能溶于水或水的混合溶剂,不溶胀、不形成凝胶,具有假塑性(Bae et al.,2008);此外,其化学结构较稳定,有一定的温度稳定性(Barone and Medynets,2007)。左聚糖具有广泛的应用范围和良好的市场前景(Li et al.,2015),在医学领域具有抗肿瘤活性(Yoo et al.,2004),在食品行业具有益生作用(Korakli et al.,2003),且广泛应用于其他商业非酒精饮料(Bello et al.,2001)。左聚糖蔗糖酶属于GH68糖苷水解酶家族,可催化蔗糖发生水解和聚合2种主要反应,其中聚合反应可将蔗糖转化为高附加值的左聚糖。广西甘蔗资源丰富,但行业产品种类较少,缺乏高附加值的蔗糖深加工产品,易受国外糖制品和甜味剂冲击,限制了蔗糖工业的发展(侯佳,2014)。左聚糖蔗糖酶是利用蔗糖生产左聚糖的关键酶,具有重要的开发价值。因此,通过克隆表达新的高性能左聚糖蔗糖酶,并优化聚合反应条件,提高蔗糖的转化率,对将来规模生产左聚糖具有重要意义。【前人研究进展】目前制备左聚糖的方法主要有4种,分别为从植物中提取、化学合成、微生物发酵和酶法合成(王涵等,2009)。相对而言,酶法合成左聚糖具有制备方法简单、纯化方便、产量较高等优势。近年来,左聚糖的研究热点主要集中在细菌产左聚糖的生物合成及其应用的多样性(Ortiz-Soto et al.,2019)。已有研究表明,不同微生物来源左聚糖蔗糖酶的酶学性质和产物性质有所不同(Srikanth et al.,2015;González-Garcinu et al.,2017)。多数已报道的左聚糖蔗糖酶催化聚合反应的热稳定性欠佳(Han et al.,2009;Xu et al.,2018)。Méndez-Lorenzo等(2015)研究证实枯草芽孢杆菌(Bacillus subtilis 168)的左聚糖蔗糖酶产左聚糖温度为25 ℃。已有报道中,蔗糖转化率较高的是来自地衣芽孢杆菌(B. licheniformis)的左聚糖蔗糖酶,其在10%底物浓度时转化率可达40%以上(陆娟等,2013);但也有研究表明左聚糖蔗糖酶在高底物浓度下左聚糖合成减弱,而制约其生产应用(Lorenzetti et al.,2015;?ner et al.,2016)。例如一种纳豆芽孢杆菌(B. subtilis natto)左聚糖蔗糖酶在蔗糖浓度超过25%以上时则不利于聚合反应(Bersaneti et al.,2018)。【本研究切入点】从耐热微生物中克隆获得热稳定性好、耐高底物浓度且转化率高的左聚糖蔗糖酶是提高左聚糖产量的关键,但目前同时具备这3种性质的左聚糖蔗糖酶较少。【拟解决的关键问题】通过基因工程和酶工程的方法,获得热稳定性好、且在50%高底物浓度下蔗糖转化率达35%以上的左聚糖蔗糖酶,从而为提高左聚糖生产效率和降低生产成本提供技术基础。
1 材料与方法
1. 1 试验材料
Bacillus paralicheniformis LN-05由广西微生物与酶工程技术研究中心实验室从市售菌肥中筛选获得并保存,大肠杆菌(Escherichia coli)XL-10感受态细胞购自北京百奥莱博科技有限公司,质粒pSE380购自Invitrogen公司。Eazy Taq DNA聚合酶购自北京聚合美生物科技有限公司,T4 DNA连接酶、限制性内切酶(PstⅠ、NcoⅠ)、λDNA/Hind Ⅲ DNA Marker、DL2000 DNA Marker、蛋白标准分子量、DNA标准分子量和dNTPs均购自宝日医生物技术(北京)有限公司;柱式质粒DNA小量抽提试剂盒、柱式胶回收试剂盒和柱式PCR产物纯化试剂盒均购自生工生物工程(上海)股份有限公司;酵母粉和胰蛋白胨购自英国Oxoid公司;其他试剂均为国产分析纯。
LB培养基:蛋白胨10.0 g/L,酵母提取物5.0 g/L,NaCl 10.0 g/L。LB瓊脂平板:蛋白胨10.0 g/L,酵母提取物5.0 g/L,NaCl 10.0 g/L,琼脂15 g/L。
1. 2 试验方法
1. 2. 1 菌株16S rDNA序列分析 鉴定提取待测菌基因组,通过通用引物扩增其16S rDNA序列(Erden-Karao?lan et al.,2019),送至广州华大基因科技有限公司测序,将测序结果在NCBI数据库进行BLAST比对分析,并构建系统发育进化树。
1. 2. 2 左聚糖蔗糖酶克隆 根据已公开的地衣芽孢杆菌左聚糖蔗糖酶基因序列(Nakapong et al.,2013)设计引物(F-primer:5'-GATCCATGGTGAAC ATCAAAAACATTGCTAAAAAAGCGTCAGCCTT AACCGCG-3',R-primer:5'-CGCGCTGCAGTTAAT GATGATGATGATGATGTTTGTTTACCGTTAGTT TCCCTG-3'),其中下游引物加入6个组氨酸标签。以目的菌全基因组为模板进行PCR扩增。PCR反应体系如下:DNA 1.0 ng,上、下游引物(10 mmol/L)各1.0 μL,2.5 mmol/L dNTPs 4.0 μL,Easy Taq DNA聚合酶0.8 μL,10×Easy Taq Buffer 5.0 μL,ddH2O补足至50.0 μL。扩增程序:95 ℃预变性3 min;95 ℃ 1 min,55 ℃ 30 s,72 ℃ 4 min,进行24个循环; 72 ℃延伸10 min。
1. 2. 3 重组质粒构建 扩增获得的左聚糖蔗糖酶基因产物经柱式PCR产物纯化试剂盒纯化,再以NcoⅠ和PstⅠ双酶切处理后,连接到经相同双酶切的原核表达载体pSE380上,得到含目的基因的重组质粒,转化XL-10感受态细胞,挑取阳性重组菌送至广州华大基因科技有限公司进行测序,测序结果在NCBI数据库上进行核苷酸序列及推导氨基酸序列比对分析。
1. 2. 4 重组左聚糖蔗糖酶表达 将含有pSE380-Lev重组质粒的XL-10重组菌株接种到含有100 μg/mL氨苄青霉素的LB液体培养基中,37 ℃、220 r/min过夜活化,次日以1%~2%的接种量转接到含有相同抗生素的LB液体培养基中,37 ℃下220 r/min培养3~4 h;当OD600达0.6~0.8时加入终浓度0.8 mmol/L的异丙基硫代半乳糖苷(IPTG),置于24 ℃下220 r/min诱导产酶18 h。
1. 2. 5 重组左聚糖蔗糖酶纯化 取1 L重组左聚糖蔗糖酶的诱导表达培养液,8000 r/min离心15 min,收集菌体,用ddH2O重悬清洗,再用相同条件离心,用5 mmol/L磷酸盐缓冲液(pH 8.0)重悬细胞置于冰水浴,超声波39 W 1 h,间或5 s工作破胞,破胞液经12000 r/min离心15 min,取上清液。用镍柱纯化方式进行提纯操作(Hernandez et al.,1995),洗脱液样品采用SDS-PAGE电泳检测。
1. 2. 6 重组左聚糖蔗糖酶酶学性质研究
1. 2. 6. 1 水解活力测定 用DNS法(杨辉,2012)测定左聚糖蔗糖酶水解活力。1个酶活力单位(U)定义为:在最适温度和pH条件下,1 min催化蔗糖转化为1 μmol葡萄糖所需左聚糖蔗糖酶的量(Belghith et al.,2012),以各反应条件下最大活力值为100%计算相对活力。
1. 2. 6. 2 聚合活力测定 取490 μL含适当浓度蔗糖的50 mmol/L磷酸氢二钠—柠檬酸缓冲液(pH 5.0),加入稀释适当倍数的酶液10 μL,在所需温度下温浴反应24 h后取出;在反应体系中加入3倍体积无水乙醇终止反应,4 ℃静置24 h后,12000 r/min离心25 min;用蒸馏水重悬沉淀,再次离心,直至用DNS显色法检测上清液无还原糖残留。所得左聚糖沉淀烘干至恒重称量,计算蔗糖转化率和左聚糖产量,以各反应条件下最高产量值为100%计算相对活力。
1. 2. 6. 3 水解反应最适温度和最适pH测定 将纯化的酶液稀释适当倍数(稀释至适合检测的浓度范围),分别在25~55 ℃下反应测定最适温度;同时在pH 3.5~7.0的缓冲液中反应测定最适pH。
1. 2. 6. 4 水解活力的热稳定性和pH稳定性测定
将重组左聚糖蔗糖酶保温在不同温度(40~55 ℃)下,每隔30 min取样在最适温度下测定酶活力,考察热稳定性。在pH 3.5~7.0的一系列梯度缓冲液中水浴30 min,以最适pH和温度下的酶活力为参照,确定其pH稳定性。
1. 2. 6. 5 金属离子和EDTA对水解活力的影响 以pH 6.0的磷酸氢二钠—柠檬酸缓冲液为对照,分别用含终浓度为2.5mmol/L的Cr3+、Co2+、Ag3+、Cu2+、Ba2+、Mg2+、Al3+、K+、Mn2+和Fe2+缓冲液及含有0~120 mmol/L不同梯度的EDTA缓冲液稀释重组左聚糖蔗糖酶,于4 ℃下放置12 h后按标准酶活力测定方法测定残余酶活力。
1. 2. 6. 6 水解活力的动力学参数测定 采用双倒数作图法制作Linewaver-Burk曲线,求出水解反应的米氏常数(Km)和最大反应速率(Vmax)。
1. 2. 6. 7 聚合反应的最适温度和最适pH测定 将磷酸氢二钠—柠檬酸缓冲液分别在25~55 ℃的水浴锅内保温5 min后,在对应温度下反应24 h后按照乙醇提取法获得左聚糖(Santos-Moriano et al.,2015),测定最适温度。在pH 3.5~7.5的缓冲液保温30 min,测定最适pH。
1. 2. 6. 8 聚合活力的热稳定性和pH稳定性 将重组左聚糖蔗糖酶保温在不同温度(35~50 ℃)下,每隔30 min取样并反应24 h,在最适pH和温度下考察其熱稳定性。将重组左聚糖蔗糖酶在pH 3.5~7.5的缓冲液中保温30 min,在最适pH和温度下确定其pH稳定性。
1. 2. 6. 9 不同金属离子和化学试剂对聚合活力的影响 以pH 5.0的磷酸氢二钠—柠檬酸缓冲液为对照,分别用含终浓度为2.5 mmol/L的Cr3+、Co2+、Ag3+、Cu2+、Ba2+、Mg2+、Al3+、K+、Mn2+和Fe2+缓冲液及含0~120 mmol/L不同梯度的EDTA缓冲液稀释重组左聚糖蔗糖酶,4 ℃放置12 h后,在最适pH和温度下考察金属离子和化学试剂对其聚合活力的影响。
1. 2. 6. 10 蔗糖浓度、酶浓度和反应时间对聚合活力的影响 用50 mmol/L磷酸氢二钠—柠檬酸缓冲液(pH 5.0)配制10%~50%的蔗糖溶液,重组左聚糖蔗糖酶浓度0.8 U/mL,35 ℃下保温5 min后反应24 h,测定底物浓度对重组左聚糖蔗糖酶聚合活力的影响;在最适底物浓度和酶浓度条件下,将反应液35 ℃保温5 min,反应4~40 h后提取左聚糖,测定反应时间对其聚合活力的影响;在最适底物浓度和35 ℃条件下保温5 min,分别加入0.3~1.5 U/mL的重组左聚糖蔗糖酶反应24 h后,测定酶浓度对其聚合活力的影响。
1. 2. 6. 11 不同温度和底物蔗糖浓度对左聚糖蔗糖酶的影响 取蔗糖浓度20%~50%的缓冲液在35~50 ℃下反应24 h,测定重组左聚糖蔗糖酶的聚合活力。
1. 3 统计分析
采用Excel 2013对试验数据进行统计分析,以Origin 8.5制图。
2 结果与分析
2. 1 菌株 LN-05的16S rDNA序列分析结果
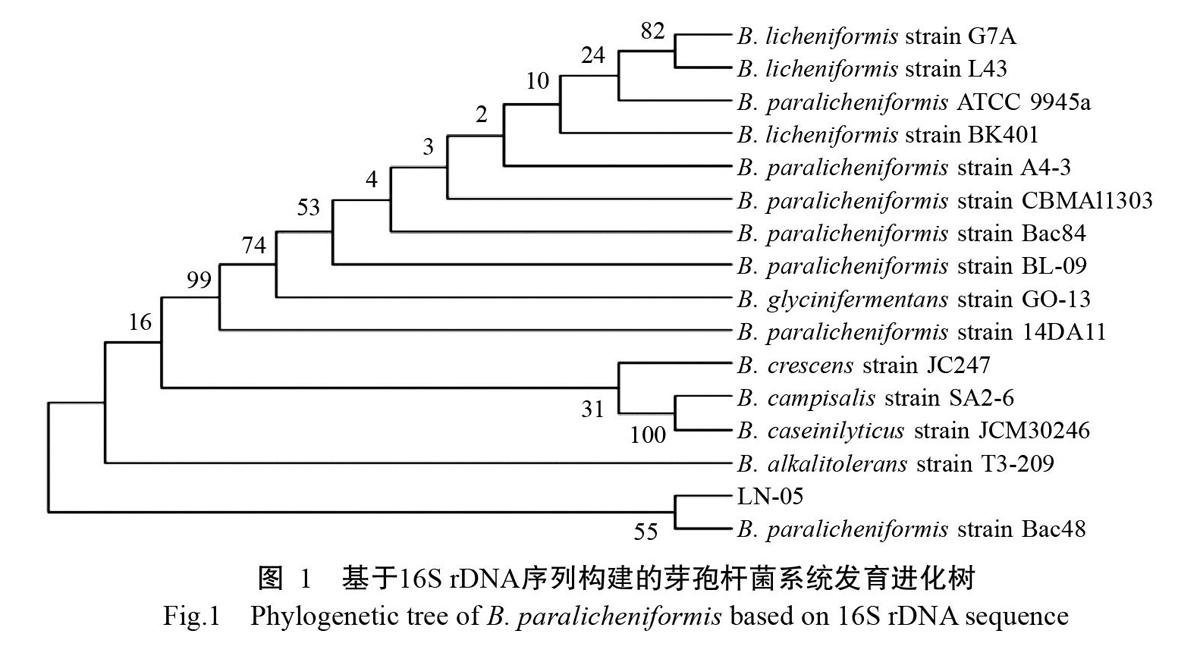
从菌肥中分离出的菌株LN-05经16S rDNA序列分析及构建系统发育进化树(图1),结果表明,菌株LN-05的16S rDNA序列与目前已公布B. paralicheniformi Bac48(Dunlap et al.,2015)的16S rDNA序列相似性达99.7%,可初步鉴定该菌株为B. paralicheniformis。
2. 2 重组左聚糖蔗糖酶基因克隆、表达及纯化结果
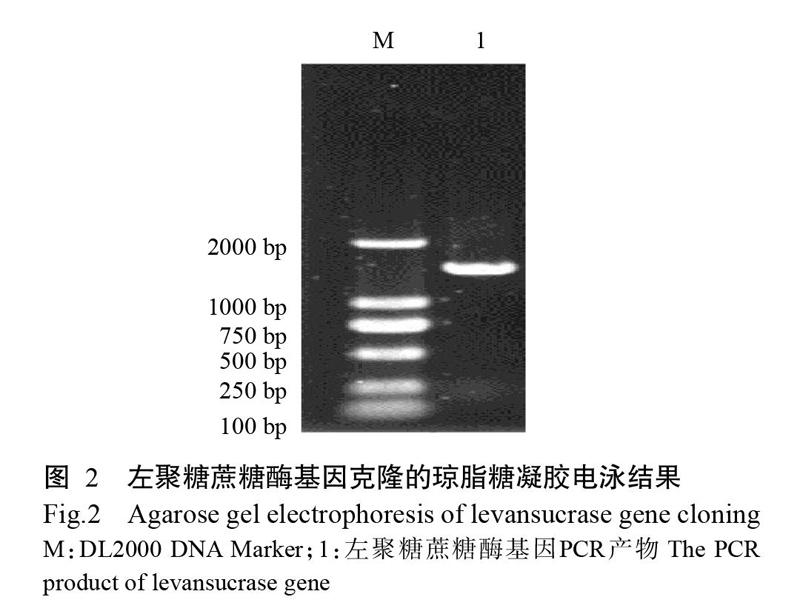
從菌株LN-05基因组中扩增左聚糖蔗糖酶基因,得到大小约1400 bp的扩增产物(图2)。经广州华大基因科技有限公司测序,发现其氨基酸序列与已公布地衣芽孢杆菌RN-01的左聚糖蔗糖酶存在19个氨基酸残基差异(图3)。重组酶诱导表达后,经镍亲和层析纯化再进行SDS-PAGE电泳,结果如图4所示,重组蛋白分子量约53 kD,与理论值53.8 kD较符合。
2. 3 重组左聚糖蔗糖酶酶学性质分析结果
2. 3. 1 温度对重组左聚糖蔗糖酶的影响 由图5可知,重组左聚糖蔗糖酶以蔗糖为底物的水解反应最适温度为45 ℃,温度超过50 ℃后水解活力快速下降。而底物浓度为20%时的聚合反应最适温度为35 ℃,当温度超过35 ℃后,聚合活力逐步下降。由于该重组酶的水解与聚合反应机制有差异,故其最适反应温度并不一致,高温下聚合反应减弱,更倾向水解反应。
2. 3. 2 pH对重组左聚糖蔗糖酶的影响 由图6可知,重组左聚糖蔗糖酶水解反应的最适pH为6.0,当pH大于6.0时其水解活力快速下降;聚合反应的最适pH为5.0,当pH大于5.0时随着pH的升高,重组左聚糖蔗糖酶的聚合活力不断下降,当pH达7.5时,左聚糖产量仅为18.73±0.73 g/L。
2. 3. 3 重组左聚糖蔗糖酶的热稳定性 由图7-A可知,重组左聚糖蔗糖酶的水解活力在40和45 ℃时具有较好的热稳定性,保温3 h的残余酶活力分别仍有89%和78%;当温度超过45 ℃时,该酶的热稳定性较差。由图7-B可知,重组左聚糖蔗糖酶的聚合活力在35 ℃时具有良好的热稳定性,保温3 h后残余酶活力为74%,40 ℃时聚合活力半衰期仍保持在45 min左右。
2. 3. 4 重组左聚糖蔗糖酶的pH稳定性 由图8可知,重组左聚糖蔗糖酶水解活力在pH 4.5~6.0范围内具有较好的pH稳定性,当pH大于6.0时pH稳定性较差,且随着pH不断升高,水解活力的pH稳定性快速下降;当pH为5.0时,重组左聚糖蔗糖酶的聚合活力具备较好的pH稳定性,当pH大于5.0时随着pH的升高其稳定性逐渐变差,当pH达7.5时左聚糖产量仅为8.78±0.70 g/L。
2. 3. 5 金属离子对重组左聚糖蔗糖酶的影响 由图9可知,Mn2+、Ag3+和Cr3+对重组左聚糖蔗糖酶的水解活力有明显抑制作用,而Co2+和Al3+具有促进作用,水解活力较对照分别提高14%和11%;Ag3+、Cu2+和K+对重组左聚糖蔗糖酶聚合活力具有一定的促进作用,Ba2+、Mg2+和Mn2+则具有明显的抑制作用,分别抑制聚合活力32%、28%和34%。
2. 3. 6 EDTA对重组左聚糖蔗糖酶的影响 由图10可知,随着EDTA浓度的增加,重组左聚糖蔗糖酶的水解活力和聚合活力均不断下降,EDTA浓度达120 mmol/L时的水解活力为58.09±0.03 U/mL,下降了66%;左聚糖产量为73.69±0.31 g/L,下降了66.2%。说明重组左聚糖蔗糖酶需要金属离子激活。
2. 3. 7 重组左聚糖蔗糖酶的Linewaver-Burk图 通过Linewaver-Burk双倒数作图(图11),得到米氏拟合方程为y=0.14565x+0.01351(R?=0.9927),Vmax=74 μmol/(min·mg),Km为7.57 mmol/L,表明该重组左聚糖蔗糖酶具有较快的反应速度和较好的底物亲和性。
2. 3. 8 底物浓度、反应时间和酶浓度对重组左聚糖蔗糖酶聚合活力的影响 底物蔗糖浓度明显影响左聚糖的合成,本研究的重组左聚糖蔗糖酶对底物浓度耐受性较高,由图12-A可知,当蔗糖浓度为50%时,重组左聚糖蔗糖酶聚合活力最高,左聚糖产量达176.00±0.80 g/L;当底物浓度为50%,最适pH条件下的最适反应时间为24 h(图12-B),最适聚合反应的酶浓度为0.9 U/mL(图12-C)。在最适聚合反应条件(50%蔗糖溶液、酶浓度0.9 U/mL、35 ℃、pH 5.0、反应24 h)下其蔗糖转化率为(36.60±0.80)%,左聚糖产量为183.20±4.10 g/L。
2. 3. 9 不同温度和蔗糖浓度对重组左聚糖蔗糖酶聚合活力及转化率的影响 底物浓度影响重组左聚糖蔗糖酶聚合活力的耐热性,当蔗糖浓度为20%~40%时,其最适聚合反应温度为35 ℃,而蔗糖浓度达50%时的最适聚合反应温度上升至40 ℃,此时左聚糖产量达最大值,为183.00±1.73 g/L(图13-A),并保持较高的转化率(36.76±1.84)%(图13-B)。说明底物浓度较高时可对重组左聚糖蔗糖酶起到一定的保护作用。但从蔗糖转化率来看,底物浓度40%、35 ℃反应时可达最高转化率,为(39.80±2.95)%。
3 讨论
由于耐热菌的最适生长温度较高,致使其代谢酶系通常也具有较高的热稳定性,因此从耐热微生物寻找耐热酶很有意义。本研究首次克隆来自耐热菌B. paralicheniformis的左聚糖蔗糖酶基因,重组左聚糖蔗糖酶在50%底物浓度下的最适聚合温度达40 ℃,虽然与嗜热芽孢杆菌(Bacillus sp. TH4-2)(Ammar et al.,2002)和地衣芽孢杆菌RN-01(Nakapong et al.,2013)的50 ℃有差距,但高于目前多数已报道其他菌种的左聚糖蔗糖酶。例如,来源于枯草芽孢杆菌(B. subtilis NRC 33a)的左聚糖蔗糖酶在30 ℃时果糖转化为左聚糖的效果最佳(Abdel-Fattah et al.,2005);来源于运动发酵单细菌(Zymomonas mobilis)的左聚糖蔗糖酶在4 ℃下反应时左聚糖产量最高,而在40 ℃下反应时左聚糖产量明显降低,低聚果糖的含量却很高(Santos-Moriano et al.,2015)。值得注意的是,菌株LN-05与地衣芽孢杆菌RN-01的左聚糖蔗糖酶氨基酸序列虽然高度相似,但在高底物浓度下两者的最适聚合反应温度相差10 ℃,且本研究中的重组左聚糖蔗糖酶最适聚合pH为5.0,而后者为6.0;Mn2+对后者的聚合反应有促进作用,但对本研究中的重组左聚糖蔗糖酶表现为抑制作用。氨基酸序列分析结果表明,本研究的B. paralicheniformis左聚糖蔗糖酶与地衣芽孢杆菌RN-01的左聚糖蔗糖酶仅存在19个氨基酸残基的差异,但导致明显的酶学性质变化,说明这些差异氨基酸残基中可能包含显著影响聚合反应性能及热稳定性的关键氨基酸残基,有待进一步通过定点突变技术加以分析,并借此对左聚糖蔗糖酶进行分子改造,使其酶学性能进一步提高。
此外,许多研究表明高底物浓度不利于左聚糖合成。例如,来源于丁香假单胞菌(Pseudomonas syringae pv. Phaseolicola)的左聚糖蔗糖酶在较高底物浓度条件下水解反应优先左聚糖的形成,蔗糖浓度超过10%时,左聚糖产量开始下降(Hettwer et al.,1995);运动发酵单胞菌(Z. mobilis B-14023)来源的左聚糖蔗糖酶在28 ℃、30%蔗糖浓度条件下左聚糖产量最高,当蔗糖浓度高于30%时,随着碳源浓度的增加,左聚糖的合成逐渐减少(Silbir et al.,2014)。本研究的重組左聚糖蔗糖酶在40 ℃、底物浓度50%的条件下合成左聚糖的蔗糖转化率仍为(36.76±1.84)%,说明该酶具有良好的热稳定性和较强的底物浓度耐受性,即具有较高的生产应用潜力。但以产量为基准的最适反应条件下,转化率并不是最高,说明酶的性能仍有提升空间,今后在酶分子改造和高底物下酶促反应机制方面还值得深入研究。
4 结论
B. paralicheniformis左聚糖蔗糖酶的热稳定性较好,左聚糖产量高,具有转化蔗糖生产高附加值左聚糖的应用潜力。
参考文献:
侯佳. 2014. 广西蔗糖产业发展现状与分析[J]. 新经济,(4):18-20. [Hou J. 2014. Present situation and analysis of Guangxi sucrose industry[J]. New Economy,(4):18-20.]
陆娟,唐俊,肖敏,屈长青. 2013. Levan果聚糖的应用与生产研究进展[J]. 生物学杂志,30(6):86-90. [Lu J,Tang J,Xiao M,Qu C Q. 2013. Progress on the application and production of levan[J]. Journal of Biology,30(6):86-90.]
王涵,汤日玲,姬胜利. 2009. 左聚糖的生物合成及生物学功能[J]. 生命的化学,29(6):860-864. [Wang H,Tang R L,Ji S L. 2009. Biosynthesis and biological functions of levan[J]. Chemistry of Life,29(6):860-864.]
杨辉. 2012. 芽孢杆菌左聚糖蔗糖酶基因克隆、表达及分子改造[D]. 南宁:广西大学. [Yang H. 2012. Cloning,expre-ssion and molecular modification of levansucrase from Bacillus[D]. Nanning:Guangxi University.]
Abdel-Fattah A F,Mahmoud D A R,Esawy M A T. 2005. Production of levansucrase from Bacillus subtilis NRC 33a and enzymic synthesis of levan and fructo-oligosaccharides[J]. Current Microbiology,51(6):402-407.
Ammar Y B,Matsubara T,Ito K,Iizuka M,Limpaseni T,Pongsawasdi P,Minamiura N. 2002. Characterization of a thermostable levansucrase from Bacillus sp. TH4-2 capable of producing high molecular weight levan at high temperature[J]. Journal of Biotechnology,99(2):111-119.
Bae I Y,Oh I K,Lee S,Yoo S H,Lee H G. 2008. Rheological characterization of levan polysaccharides from Microbacterium laevaniformans[J]. International Journal of Bio-logical Macromolecules,42(1):10-13.
Barone J R,Medynets M. 2007. Thermally processed levan polymers[J]. Carbohydrate Polymers,69(3):554-561.
Belghith K S,Dahech I,Belghith H,Mejdoub H. 2012. Microbial production of levansucrase for synthesis of fructooligosaccharides and levan[J]. International Journal of Biological Macromolecules,50(2):451-458.
Bello F D,Walter J,Hertel C,Hammes W P. 2001. In vitro study of prebiotic properties of levan-type exopolysaccharides from Lactobacilli and non-digestible carbohydrates using denaturing gradient gel electrophoresis[J]. Systema-tic & Applied Microbiology,24(2):232-237.
Bersaneti G T,Pan N C,Baldo C,Celligoi M A P C. 2018. Co-production of fructooligosaccharides and levan by le-vansucrase from Bacillus subtilis natto with potential app-lication in the food industry[J]. Applied Biochemistry & Biotechnology,184(3):838-851.
Dunlap C A,Kwon S W,Rooney A P,Kim S J. 2015. Baci-llus paralicheniformis sp. nov.,isolated from fermented soybean paste[J]. International Journal of Systematic & Evolutionary Microbiology,65(10):3487-3492.
Erden-Karao?lan F,Karaka?-Budak B,Karao?lan M,Inan M. 2019. Cloning and expression of pullulanase from Baci-llus subtilis BK07 and PY22 in Pichia pastoris[J]. Protein Expression & Purification,162:83-88.
González-Garcinu O ?,Tabernero A,Domínguez ?,Galán M A,Martin D V E M. 2017. Levan and levansucrases:Polymer, enzyme,micro-organisms and biomedical applications[J]. Biocatalysis & Biotransformation,36(3):1-12.
Han W C,Byun S H,Kim M H,Sohn E H,Jang K H,Lim J D,Um B H,Kim C H,Kang S A,Jang K H. 2009. Production of lactosucrose from sucrose and lactose by a levansucrase from Zymomonas mobilis[J]. Journal of Microbiology and Biotechnology,19(10):1153-1160.
Hernandez L,Arrieta J,Menendez C,Vazquez R,Coego A,Suarez V,Selman G,Petit-Glatron M F,Chambert R. 1995. Isolation and enzymic properties of levansucrase secreted by Acetobacter diazotrophicus SRT4,a bacterium associated with sugar cane[J]. Biochemical Journal,309(1):113-118.
Hettwer U,Gross M,Rudolph K. 1995. Purification and cha-racterization of an extracellular levansucrase from Pseudomonas syringae pv. phaseolicola[J]. Journal of Bacterio-logy,177(10):2834-2839.
Korakli M,Pavlovic M,Ganzle M G,Vogel R F. 2003. Exopolysaccharide and kestose production by Lactobacillus sanfranciscensis LTH2590[J]. Applied & Environmental Microbiology,69(4):2073-2079.
Li W J,Yu S H,Zhang T,Jiang B,Mu W M. 2015. Recent novel applications of levansucrases[J]. Applied Microbio-logy & Biotechnology,99(17):6959-6969.
Lorenzetti M F S,Moro M R,García-Cruz C H. 2015. Alginate/PVA beads for levan production by Zymomonas mobilis[J]. Journal of Food Process Engineering,38(1):31-36.
Méndez-Lorenzo L,Porras-Domínguez J R,Raga-Carbajal E,Olvera C,Rodríguez-Alegría M E,Carrillo-Nava E,Costas M,Munguía A L. 2015. Intrinsic levanase activity of Bacillus subtilis 168 levansucrase(SacB)[J]. PLoS One,10(11):e0143394.
Nakapong S,Pichyangkura R,Ito K,Iizuka M,Pongsawasdi P. 2013. High expression level of levansucrase from Bacillus licheniformis RN-01 and synthesis of levan nanoparticles[J]. International Journal of Biological Macromolecules,54:30-36.
?ner E T,Hernández L,Combie J. 2016. Review of Levan polysaccharide:From a century of past experiences to future prospects[J]. Biotechnology Advances,34(5):827-844.
Ortiz-Soto M E,Porras-Domínguez J R,Seibel J,López-Munguía A L M. 2019. A close look at the structural features and reaction conditions that modulate the synthesis of low and high molecular weight fructans by levansucrases[J]. Carbohydrate Polymers,219:130-142.
Santos-Moriano P,Fernandez-Arrojo L,Poveda A,Jimenez-Barbero J,Ballesteros A O,Plou F J. 2015. Levan versus fructooligosaccharide synthesis using the levansucrase from Zymomonas mobilis:Effect of reaction conditions[J]. Journal of Molecular Catalysis B:Enzymatic,119:18-25.
Silbir S,Dagbagli S,Yegin S,Baysal T,Goksungur Y. 2014. Levan production by Zymomonas mobilis in batch and continuous fermentation systems[J]. Carbohydrate Polymers,99:454-461.
Srikanth R,Reddy C H S S,Siddartha G,Ramaiah M J,Uppuluri K B. 2015. Review on production,characterization and applications of microbial levan[J]. Carbohydrate Polymers,120:102-114.
Xu W,Ni D W,Zhang W L,Guang C,Zhang T,Mu W M. 2018. Recent advances in Levansucrase and Inulosucrase:Evolution, characteristics,and application[J]. Critical Reviews in Food Science & Nutrition,59(22):3630-3647.
Yoo S H,Yoon E J,Cha J,Lee H G. 2004. Erratum to “Antitumor activity of levan polysaccharides from selected microorganisms”[J]. International Journal of Biological Ma-cromolecules,34(1-2):149.
(責任编辑 罗 丽)
收稿日期:2020-04-07
基金项目:广西自然科学基金项目(2017GXNSFAA198128);南宁市科学研究与技术开发计划项目(20141015)
作者简介:*为通讯作者,杨辉(1972-),博士,高级工程师,主要从事食品发酵和酶工程方面研究工作,E-mail:huiy422@gxu.edu.cn。丛豪(1997-),研究方向为发酵与酶工程应用,E-mail:www.hao97.cn@qq.com

