链霉菌CPCC 203577产生的napyradiomycins的分离与鉴定
李书芬,胡辛欣,胡晓敏,江冰娅,刘晓岩,刘红宇,余利岩,武临专
论著
链霉菌CPCC 203577产生的napyradiomycins的分离与鉴定
李书芬,胡辛欣,胡晓敏,江冰娅,刘晓岩,刘红宇,余利岩,武临专
100050 北京,中国医学科学院北京协和医学院医药生物技术研究所卫健委抗生素生物工程重点实验室/中国医学科学院药物合成生物学重点实验室
对一株具有抗菌活性的链霉菌CPCC 203577 产生的次级代谢产物进行系统研究。
采用 ISP2 琼脂平板发酵培养链霉菌CPCC 203577,乙酸乙酯提取发酵培养物,获得粗提物;粗提物经反相色谱柱、凝胶色谱柱、制备型 TLC 和半制备 HPLC 等分离纯化获得目标化合物纯品;MS 和 NMR 等确定化合物结构;琼脂稀释法测定抗菌活性。
从链霉菌CPCC 203577 中分离鉴定了含萘醌并吡喃母核的 3 个已知化合物,3-chloro-6,8-dihydroxy-8-α- lapachone(1)、16-dechloro-16-hydroxynapyradiomycin C2(2)和 napyradiomycin A2(3)。化合物1具有较强的抗革兰氏阳性细菌活性,最低抑菌浓度(MIC)值为 4 ~ 8 μg/ml;化合物2和3没有抗菌活性。
链霉菌 CPCC 203577 具有丰富的次级代谢产物合成能力,产生napyradiomycins 类化合物。
链霉菌CPCC 203577; napyradiomycins; 抗菌活性
链霉菌是一类可产生结构多样、生物活性丰富的次级代谢产物的放线菌;临床使用的链霉素和达托霉素(daptomycin)等抗菌药物均来源于链霉菌。随着细菌耐药性的日趋严重,急需发现具有新结构和作用机制的抗生素。对链霉菌产生的次级代谢产物进行系统挖掘,有望为新型抗生素的研发提供先导化合物。
Napyradiomycins 是链霉菌产生的一类具有显著抗菌、抗细菌生物膜与肿瘤细胞毒活性的化合物[1-7]。Napyradiomycins 的分子中含有一个萘醌并吡喃母核,该母核可连接不同结构修饰的萜链。
链霉菌 CPCC 203577 是分离自云南省景洪曼亭的一株土壤链霉菌,具有显著的抗菌及抗肿瘤细胞活性。本文作者前期研究表明,该菌株产生衣草花青菌素等吩嗪类化合物,并且微生物化学分析提示菌株还产生其他结构类型的活性次级代谢产物。本文作者对该菌株产生的脂溶性次级代谢产物进行挖掘,发现并鉴定了 3 个含有萘醌并吡喃母核的 napyradiomycins 类化合物,具体报道如下。
1 材料和方法
1.1 材料
1.1.1 菌株 链霉菌CPCC 203577,中国药学微生物菌种保藏中心提供。
1.1.2 培养基 种子培养基:葡萄糖 2.8 g/L、酵母提取物 2.8 g/L、麦芽提取物 7.0 g/L、甘露醇6.0 g/L、豆粉 6.0 g/L、琼脂粉 15.0 g/L,pH 自然。发酵培养基:ISP2(葡萄糖 4.0 g/L、酵母提取物4.0 g/L、麦芽提取物 10.0 g/L、琼脂粉 15.0 g/L,pH 自然)。
1.1.3 仪器与试剂 酵母提取物和麦芽提取物均为英国 Oxoid 公司产品;微生物培养所需的其他原料均为国产试剂;乙酸乙酯、甲醇等有机试剂为国产分析纯试剂;乙腈为美国 Fisher 公司产品;液相用水为屈臣氏蒸馏水;ODS 预装柱为瑞典 Biotage 公司产品;Sephadex LH-20 凝胶为美国 GE Healthcare 公司产品;HPLC 分析色谱柱 Diamonsil C18(4.6 mm × 250 mm,5 μm)与 HPLC 半制备色谱柱 Diamonsil C18(10.0 mm × 250 mm,5 μm)购自北京迪科马科技有限公司;薄层色谱硅胶板购自烟台江友硅胶开发有限公司。
样品浓缩使用 EYELAN-1100 型旋转蒸发仪;化合物HPLC 分析和半制备使用安捷伦 1260 高效液相色谱仪;LC-MS 分析使用 Thermo Fisher Scientific 公司 LTQ XL 质谱分析仪;化合物 NMR 测试使用 Bruker Aviiihd 公司核磁共振仪(600 MHz,TMS 为内标)。
1.2 方法
1.2.1 链霉菌 CPCC 203577 培养与发酵 将保藏的链霉菌 CPCC 203577 孢子悬液涂布于种子培养基平板,28 ℃静置培养 8 ~ 10 d 后,用适量无菌水洗下平板上的孢子。孢子悬液均匀涂布于发酵培养基平板(ISP2),28℃静置培养 20 d,获得发酵培养物共 20 L。
1.2.2 化合物分离纯化 链霉菌 CPCC 203577 发酵培养物用乙酸乙酯浸泡提取 3 次,合并提取液,减压浓缩获得发酵培养物的提取物。提取物经 ODS 反相柱层析、Sephadex LH-20 层析、硅胶板 TLC 与半制备反相 HPLC 后,分别得到化合物1~3。
1.2.3 抗菌活性测定 参照 CLSI 标准[8-9],采用平皿二倍稀释法进行 MIC 测定实验。试验菌包括表皮葡萄球菌(ATCC 12228,甲氧西林敏感株)、表皮葡萄球菌(13-3,甲氧西林耐药株)、金黄色葡萄球菌(ATCC 29213,甲氧西林敏感株)、金黄色葡萄球菌(16-30,甲氧西林耐药株)、金黄色葡萄球菌(ATCC BAA-976,克林霉素耐药株)、人葡萄球菌(ATCC 35982)、大肠埃希菌(ATCC 25922)、肺炎克雷伯杆菌(ATCC 700603)与鲍曼不动杆菌(ATCC 19606)等。试验菌用 MH 肉汤增菌,化合物1 ~ 3用 MH 肉汤二倍稀释成各个所需浓度,分别加适量到平皿中,MH 琼脂培养基熔化后定量注入含待测化合物的平皿内混匀。化合物1的样品终浓度为 16、8、4、2 和 1 μg/ml 等,化合物2和3的样品终浓度为 64、32、16、8、4、2 和 1 μg/ml 等。接种试验菌(接种量为104CFU/点)后置 35 ℃恒温培养 18 h 后观察结果,无菌生长的平皿中所含药物最小的浓度即为最低抑菌浓度(MIC)。
2 结果
2.1 化合物 1 ~ 3 分离纯化
采用图 1 所示分离纯化流程,得到了化合物1~ 3纯品。其中,ODS 反相柱层析采用 120 g 预装柱,甲醇-水梯度(50:50、60:40、70:30、80:20、90:10、100:0,V/V)洗脱,流速 20 ml/min。化合物2和3的 HPLC 半制备分析条件为 62% 乙腈-水等度洗脱,流速 1.8 ml/min,保留时间分别为 43 min 与 71 min。化合物1的硅胶板制备 TLC 展层体系为二氯甲烷-甲醇(9:1),HPLC 半制备分析条件为 60% 乙腈-水等度洗脱,流速 1.8 ml/min,保留时间为 18 min。

图 1 化合物1~3的分离纯化流程
Figure 1 Purification flowchart of compounds 1 - 3
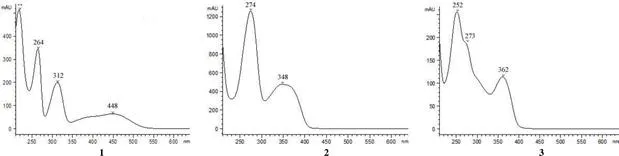
图 2 化合物1~3的紫外吸收光谱
Figure 2 UV spectra of compounds 1 - 3
2.2 结构解析
化合物1为橙色针状结晶,电喷雾质谱(ESIMS)确定其分子量为 308;结合其 NMR(600 MHz,DMSO-6)数据,确定其分子式为 C15H13ClO5。化合物1 的吸收光谱在 264、312 与 448 nm 有最大吸收(乙腈中,图 2)。经化合物微谱数据库查询和文献检索,发现化合物1的核磁数据与文献[10]报道的 3-chloro-6,8-dihydroxy- 8-α-lapachone 一致,因此确定化合物1为 3-chloro-6,8-dihydroxy-8-α-lapachone(图 3)。化合物1的核磁数据见表 1。

图 3 化合物1~3的结构
Figure 3 Structures of compounds 1 - 3

表 1 化合物1 ~ 3的 NMR 数据
化合物2为黄色粉末,ESIMS 确定其分子量为 494;结合其 NMR(600 MHz,CDCl3)数据(表 1),确定其分子式为 C25H28Cl2O6。化合物2的紫外吸收光谱在 274 与 348 nm 有最大吸收(乙腈中,图 2)。经化合物微谱数据库查询和文献检索,发现化合物2的核磁数据与文献[11]报道的16-dechloro-16-hydroxynapyradiomycin C2 一致,因此确定化合物2为16-dechloro-16- hydroxynapyradiomycin C2(图 3)。
化合物3为黄色油状,ESIMS 确定其分子量为 496,结合其 NMR(600 MHz,CDCl3)数据(表 1),确定其分子式为 C25H30Cl2O6。化合物3的紫外吸收光谱在 252、273 与 362 nm 有最大吸收(乙腈中,图 2),与文献[11]报道的napyradiomycins 类化合物的紫外吸收光谱相似,并且其核磁数据与napyradiomycin A2 一致,因此确定化合物3为 napyradiomycin A2(图 3)。
2.3 抗菌活性
以左氧氟沙星(levofloxacin)为阳性对照,对化合物1~3进行了体外抗菌活性测定。化合物1对多数革兰氏阳性细菌显示较强活性,其中对表皮葡萄球菌的 MIC 值为 4 μg/ml,对金黄色葡萄球菌和人葡萄球菌的 MIC 值为 4 ~ 8 μg/ml;而化合物2和3没有抗菌活性(MIC 值≥ 64 μg/ml)。化合物1~3对大肠埃希菌、肺炎克雷伯杆菌与鲍曼不动杆菌等革兰氏阴性细菌均没有活性。
3 讨论
Napyradiomycins 是一类由芳香聚酮和萜类组分组成的杂萜类化合物,1986 年首次从采自日本土样中的放线菌G802-AF1 中分离得到[1-3];随后从链霉菌中发现了在萘醌母核或萜类组分具有不同修饰的多个 napyradiomycins 类化合物[10-16]。虽然文献报道的napyradiomycins 类化合物达 40 多个,但从同一株链霉菌中同时发现化合物1~3系首次报道。
本文作者对化合物1~3的抗菌活性测定结果表明,1具有较强的抗革兰氏阳性菌活性,而2和3没有抗菌活性。文献报道化合物1的 C-8 位-甲基化类似物()-3-chloro-6-hydroxy-8- methoxy-α-lapachone 没有抗菌活性[11],提示萘醌并吡喃母核发生取代修饰可能会导致抗菌活性丢失。化合物2与文献报道的 napyradiomycin C2 均发生了单萜组分修饰(与萘醌并吡喃母核成环,以及C-16 位的羟基或氯取代),它们均没有抗菌活性[17]。化合物3与具有显著抗菌活性的 napyradiomycin A1 相比较,其单萜部分发生了 C-16 位的羟基修饰和 C-17 位双键位置变化,导致化合物抗菌活性丢失。
链霉菌 CPCC 203577 除了产生吩嗪类和 napyradiomycins 类化合物之外,可能还产生其他结构类型的次级代谢产物,值得继续挖掘。
[1] Shiomi K, Iinuma H, Hamada M, et al. Novel antibiotics napyradiomycins. Production, isolation, physico-chemical properties and biological activity. J Antibiot (Tokyo), 1986, 39(4):487-493.
[2] Shiomi K, Nakamura H, Iinuma H, et al. Structures of new antibiotics napyradiomycins. J Antibiot (Tokyo), 1986, 39(4):494-501.
[3] Shiomi K, Nakamura H, Iinuma H, et al. New antibiotic napyradiomycins A2 and B4 and stereochemistry of napyradiomycins. J Antibiot (Tokyo), 1987, 40(9):1213-1219.
[4] Haste NM, Farnaes L, Perera VR, et al. Bactericidal kinetics of marine-derived napyradiomycins against contemporary methicillin- resistant Staphylococcus aureus. Mar Drugs, 2011, 9(4):680-689.
[5] Yamamoto K, Tashiro E, Motohashi K, et al. Napyradiomycin A1, an inhibitor of mitochondrial complexes I and II. J Antibiot (Tokyo), 2012, 65(4):211-214.
[6] Farnaes L, La Clair JJ, Fenical W. Napyradiomycins CNQ525.510B and A80915C target the Hsp90 paralogue Grp94. Org Biomol Chem, 2014, 12(3):418-423.
[7] Bauermeister A, Pereira F, Grilo IR, et al. Intra-clade metabolomic profiling of MAR4 Streptomyces from the Macaronesia Atlantic region reveals a source of anti-biofilm metabolites. Environ Microbiol, 2019, 21(3):1099-1112.
[8] Clinical and Laboratory Standards Institute. Performance standards for antimicrobial susceptibility testing. 29th ed. CLSI supplement M100. Wayne, PA:Clinical and Laboratory Standards Institute, 2017.
[9] Clinical and Laboratory Standards Institute. Methods for dilution antimicrobial susceptibility tests for bacteria that grow aerobically. 11th ed. CLSI standard M07. Wayne, PA:Clinical and Laboratory Standards Institute, 2015.
[10] Wu Z, Li S, Li J, et al. Antibacterial and cytotoxic new napyradiomycins from the marine-derived Streptomyces sp. SCSIO 10428. Mar Drugs, 2013, 11(6):2113-2125.
[11] Motohashi K, Sue M, Furihata K, et al. Terpenoids produced by actinomycetes:napyradiomycins from Streptomyces antimycoticus NT17. J Nat Prod, 2008, 71(4):595-601.
[12] Soria-Mercado IE, Prieto-Davo A, Jensen PR, et al. Antibiotic terpenoid chloro-dihydroquinones from a new marine actinomycete.
J Nat Prod, 2005, 68(6):904-910.
[13] Farnaes L, Coufal NG, Kauffman CA, et al. Napyradiomycin derivatives, produced by a marine-derived actinomycete, illustrate cytotoxicity by induction of apoptosis. J Nat Prod, 2014, 77(1):15-21.
[14] Cheng YB, Jensen PR, Fenical W. Cytotoxic and antimicrobial napyradiomycins from two marine-derived, MAR 4 Streptomyces strains. European J Org Chem, 2013, 2013(18):3751-3757.
[15] Lacret R, Pérez-Victoria I, Oves-Costales D, et al. MDN-0170, a new napyradiomycin from Streptomyces sp. strain CA-271078. Mar Drugs, 2016, 14(10):E188.
[16] Fukuda DS, Mynderse JS, Baker PJ, et al. A80915, a new antibiotic complex produced by Streptomyces aculeolatus. Discovery, taxonomy,fermentation, isolation, characterization, and antibacterial evaluation. J Antibiot (Tokyo), 1990, 43(6):623-633.
[17] Shiomi K, Linuma H, Hamada M, et al. Novel antibiotics napyradiomycins. Production, isolation, physico-chemical properties and biological activity. J Antibiot (Tokyo), 1986, 39(4):487-493.
Isolation and identification of napyradiomycins fromsp.CPCC 203577
LI Shu-fen, HU Xin-xin, HU Xiao-min, JIANG Bing-ya,LIU Xiao-yan, LIU Hong-yu, YU Li-yan, WU Lin-zhuan
To investigate the secondary metabolites fromspCPCC 203577.
spCPCC 203577 was cultured on agar plates and then extracted with EtOAc. The extracts were fractionated by ODS and Sephadex LH-20 column chromatography, followed by preparative TLC and/or semi-preparative HPLC, which yielded compounds 1 - 3. MS and NMR were used to elucidate the structures of 1 - 3. Agar dilution method was used to assay the antibacterial activities of 1 - 3.
Three napyradiomycins were characterized fromspCPCC 203577. Their structures were confirmed to be 3-chloro-6, 8-dihydroxy-8-α-lapachone (1), 16-dechloro-16-hydroxynapyradiomycin C2 (2) and napyradiomycin A2 (3), respectively. Compound 1 showedactivity against Gram-positive bacteria, while 2 - 3 were inactive against both Gram-positive and Gram-negative bacteria.
spCPCC 203577 produces napyradiomycins, a group of secondary metabolites with a pyranonaphthoquinone core.
spCPCC 203577; Napyradiomycins; Antibacterial activities
WU Lin-zhuan, Email:wulinzhuan@imb.pumc.edu.cn
10.3969/j.issn.1673-713X.2020.01.004
Author Affiliation:NHC Key Laboratory of Biotechnology of Antibiotics, CAMS Key Laboratory of Synthetic Biology for Drug Innovation, Institute of Medicinal Biotechnology, Chinese Academy of Medical Sciences & Peking Union Medical College, Beijing 100050, China
国家微生物资源基础平台(NIMR-2018-3);中国医学科学院医学与健康科技创新工程(2016-I2M-3-012)
武临专,Email:wulinzhuan@imb.pumc.edu.cn
2019-07-17

