Na2SO4中毒SCR催化剂对SO3生成特性的影响
叶云云
神华浙江国华浙能发电有限公司, 浙江 宁波 315612
化石燃料的燃烧会生成一系列的大气污染物,NOx(NO占95%左右)作为主要的大气污染物直接排放会造成光化学烟雾、破坏臭氧层和危害人体健康等[1-2]. 目前,氨法SCR烟气脱硝技术因其脱硝效率高,运行稳定而被广泛应用于我国燃煤电站[3-5]. 使用最广泛的催化剂为V2O5-WO3TiO2催化剂,其工作温度区间为300~450 ℃,由于工作温度的限制,反应器通常布置在省煤器和空气预热器之间,长期使用会造成催化剂及空气预热器等下游设备的堵塞[6-7].
由于特殊地理环境,新疆维吾尔自治区的高钠煤储量很大,这种煤具有低灰分、高含水量和高碱金属含量等特点[8-9]. 煤中Na的总含量超过2%,高钠煤燃烧会出现结渣、结垢和腐蚀等现象[10-11]. 此外,燃用高钠煤时将影响催化剂性能. 研究[12-14]表明,硫和碱金属是对SCR催化剂毒害作用最大的两种物质. 碱金属与催化剂活性位点发生强烈的化学反应,导致催化剂反应能力下降[15-17]. 近几年,碱金属对催化剂的毒害作用被广泛研究. PENG等[18]研究了碱金属的中毒机理,其认为催化剂失活的主要原因是碱金属的加入会与V物种相互作用,降低表面酸度,抑制NH3的吸附,从而降低催化剂的活性. CHEN等[19]研究表明,Na2O的加入会降低催化剂表面化学吸附氧和活性成分的数量,抑制NH3的吸附和氧化还原过程. 关于碱金属中毒催化剂大多研究者关注的是不同形式碱金属对催化剂的毒害作用,但HU等[20]专门研究了SO42-在催化剂失活中所起的作用,发现SO42-的加入能够为催化剂表面提供更多的酸性位,充当了Brønsted 酸性位,能够吸附更多的NH3,增强了催化剂的性能. Khodayari等[21]研究了失活催化剂的再生,通过水洗和酸洗的方法,发现用0.5 molL H2SO4清洗的效果最好,SO42-的加入能够使催化剂表面硫酸化,增强了催化剂的活性. 然而,催化剂在还原NOx的同时还会将部分SO2催化生成SO3,SO3进一步与烟气中的成分发生反应. 生成的NH4HSO4和(NH4)2SO4具有黏性和腐蚀性,在低温下会附着在催化剂表面,堵塞催化剂[22]. 尽管SO3的生成会产生一系列的危害,但是,大多数研究者主要集中于研究碱金属中毒对脱硝性能的影响以及如何使催化剂再生,却忽略了提高催化剂脱硝性能后SO3的生成特性[23-24]. 因此,研究燃烧高钠煤过程中Na2SO4中毒SCR催化剂对SO3生成特性的影响十分必要.
SCR脱硝催化剂性能评价指标除脱硝效率外,还包括SO3生成率. 该研究通过湿式浸渍法制备w(Na)为3%的Na2SO4中毒SCR催化剂,通过试验手段和一系列表征方法重点研究了其对SO3生成特性的影响,为实际工作提供了理论基础和试验依据.
1 材料与方法
1.1 试验装置
试验装置示意图如图1所示. 由图1可见:试验所需催化剂〔用量为2 mL,粒度为40~60目(1目=1.5 μm)〕分别被置于石英管反应器中;使用气体混合器确保不同气体进入反应器之前均匀混合,为防止NH3与NO和SO2提前反应,NH3不会通过气体混合器;气体的体积流速由质量流量控制器调节,入口气体体积分数使用烟气分析仪(Testo350,德图集团,德国)进行监测;SO3通过放置于恒温80 ℃水浴锅中的格雷厄姆冷凝器收集,使用80%异丙醇溶液将收集的SO3转化为SO42-,然后使用离子色谱仪测定溶液中的ρ(SO42-),进而求得ρ(SO3),多次测量求平均值. 烟气工况的气体总流量为1.5 Lmin,空速为 45 000 h-1,其中,φ(NH3)、φ(NO)、φ(O2)、φ(H2O)分别为500×10-6、500×10-6、5%和2%,入口ρ(SO2)为 1 000~5 000 mgm3,根据试验工况调节平衡气为N2,试验温度为250~490 ℃.

注: 1—NON2; 2—O2; 3—N2; 4—SO2CO2; 5—NH3N2; 6—质量流量计; 7—气体混合器; 8—蠕动泵; 9—管式电阻炉; 10—温度控制仪; 11—催化剂; 12—石英管; 13—恒温水浴锅; 14—冷凝管收集器; 15—烟气分析仪; 16—吸收液.
SO3的生成率用于表示其对SO2的氧化能力,计算公式:
(1)
式中:ASO3为SO3生成率,%;Coutlet为反应后ρ(SO3),mgm3;Cinlet为反应前ρ(SO2),mgm3.
1.2 催化剂的制备
该研究使用的样品是中国某商业SCR催化剂(V2O5-WO3TiO2催化剂),其中,w(TiO2)占65.97%,w(WO3)占10.14%,w(V2O5)占1.56%,w(黏合剂)占22.33%. 采用湿式浸渍法制备Na2SO4中毒SCR催化剂,其中,Na2SO4中毒SCR催化剂中w(Na)为3%. 称取一定量的Na2SO4,配制成水溶液后与催化剂混合,然后将混合物在超声波下振荡4 h,随后在鼓风干燥箱中110 ℃下干燥12 h,最后,将中毒催化剂在马弗炉中450 ℃下煅烧5 h,将其研磨至40~60目(1目=1.5 μm)得到3% Na2SO4中毒SCR催化剂.
1.3 催化剂的表征
使用比表面积及孔径分析仪(ASAP 2010,麦克仪器公司,美国)来确定催化剂的孔结构和比表面积,其中,催化剂的比表面积利用BET(Brunauer-Emmett-Teller)方程求得,孔径分布采用BJH(Barrett-Joyner-Halenda)模型计算得到.
使用Bruker D8 Advance仪器来测定催化剂样品的XRD(X射线衍射)图谱,分析样品表面物质的结晶度和分散度,其中,测试使用的是Cu Kα辐射源,扫描范围为10°~80°,工作电压为40 kV,工作电流为40 mA.
催化剂的表面形貌使用SEM(发射扫描电子显微镜)对其进行扫描成像,仪器为捷克TESCAN公司生产的VEGA TS 5136MM,其工作电压为1 kV.
使用X射线光电子能谱仪(AXIS ULTRADLD,Kratos公司,日本)来测定催化剂样品的XPS(X射线光电子能谱),其中使用的X射线源为单色化Al靶,进行峰拟合时使用C1s(284.8 eV)进行校正.
2 结果与讨论
2.1 温度对SO3生成率的影响
温度对不同催化剂上SO3生成率的影响如图2所示. 由图2可见,入口ρ(SO2)为 2 000 mgm3时,在反应温度区间(250~490 ℃)内,2种催化剂上SO3生成率随温度的升高逐渐增加. SCR催化剂上SO3生成率在250 ℃时为0.38%,当温度升至490 ℃时,SO3生成率增至0.85%,而3% Na2SO4中毒SCR催化剂上SO3生成率则从0.47%增至1.36%. 结果表明,Na2SO4的加入明显提高了催化剂上SO3生成率. Dunn等[25-26]研究发现,SO2和Na2SO4等物质中的S元素会替代V元素,生成V—O—S,V—O进一步断裂生成SO3. V基催化剂对SO2的氧化仅需要单个表面V反应位点,并且V—O—S是使SO2转化为SO3的关键活性位. 所以,Na2SO4中S元素的存在导致更多活性位的生成,从而导致SO3生成率明显提高.
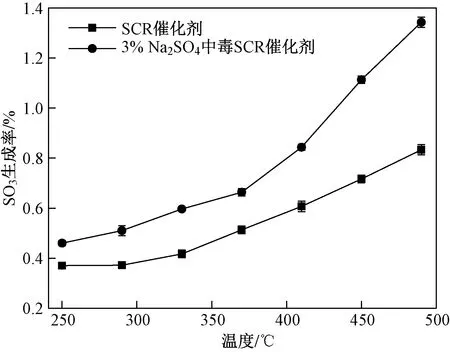
图2 温度对SO3生成率的影响Fig.2 Effect of temperature on SO3 generation ratio
2.2 ρ(SO2)对SO3生成率的影响
图3为不同催化剂上SO3生成率随入口ρ(SO2)的变化规律. 由图3可见,反应温度为330 ℃时,SO3生成率随入口ρ(SO2)的增加均呈下降的趋势. 与3% Na2SO4中毒SCR催化剂相比,相同工况下,SCR催化剂上SO3生成率较小,变化比较平缓. 然而,当入口ρ(SO2)较低时,3% Na2SO4中毒SCR催化剂上SO3生成率的下降趋势很快;当入口ρ(SO2)为 1 000 mgm3时,该催化剂上SO3生成率为1.02%,而SCR催化剂上SO3生成率较低,仅为0.60%.ρ(SO2)的增加会影响V—O—V的含量,导致V—O—S的生成量增加,但随ρ(SO2)的增加SO2扩散速度远大于其反应速度,SO2的增加量大于已反应的SO2量,导致SO3生成率降低,因此决定SO3生成率的主要因素为SO2氧化过程. 催化剂表面有限的活性位点限制了SO2的吸附,从而导致高ρ(SO2)下较低的SO3生成率[27]. 因此,在研究催化剂对SO2的氧化作用时,SO3生成量也应受到高度关注.

图3 ρ(SO2)对SO3生成率的影响Fig.3 Effect of SO2 concentration on SO3generation ratio
2.3 表征分析
2.3.1BET和XRD分析
催化剂的孔结构和比表面积是用N2物理吸附脱附试验来测定的,比表面积和孔结构在一定程度上也影响着催化剂的催化性能. 其中,SCR催化剂的比表面积、孔容和平均孔径分别为91.10 m2g、0.21 cm3g和9.20 nm. 而3% Na2SO4中毒SCR催化剂的比表面积、孔容和平均孔径分别为56.50 m2g、0.19 cm3g、11.10 nm,可见催化剂的比表面积和孔容都明显减小,但是,平均孔径却有所增加,这是因为3% Na2SO4中毒SCR催化剂的小孔被堵塞而使得大孔的比例提高. 这些变化在一定程度上影响了SO2在催化剂表面的吸附效果.
图4为不同催化剂的XRD谱图. 由图4可见:SCR催化剂仅检测到TiO2的峰,说明其他物质都高度分散在催化剂表面;3% Na2SO4中毒SCR催化剂可检测到Na2SO4的特征峰,说明Na2SO4的加入会使催化剂表面产生结晶物质. XIAO等[28]研究发现,烟气通过催化剂时,烟气中的SO2和O2与Na2SO4发生反应生成焦硫酸钠,中间产物焦硫酸钠会分解生成SO3和Na2SO4,从而促进了SO3的生成. 因此,3% Na2SO4中毒SCR催化剂上SO3生成率有所增加.
2.3.2SEM分析

图4 不同催化剂的XRD谱Fig.4 XRD spectrums of different catalysts
催化剂的表面形貌使用扫描电镜扫描获得,不同催化剂的SEM如图5所示. 由图5可见,3% Na2SO4中毒SCR催化剂表面发生很大变化,出现了裂纹和较大孔隙. 这一现象的出现与BET测试得出的结果完全一致,推测是在浸渍过程中Na2SO4导致催化剂中毒,使部分小孔堵塞,增加了大孔的数量. 3% Na2SO4中毒SCR催化剂表面出现了部分结晶产物,这一现象与XRD结果中Na2SO4特征峰的出现相对应.
2.3.3XPS分析

图5 不同催化剂的SEMFig.5 SEM images of different catalysts
通过XPS方法分析催化剂表面几种主要元素的化学形态及其表面原子含量. 表1为不同催化剂表面原子含量的定量结果. 由表1可见,3% Na2SO4中毒SCR催化剂表面的有效成分对应的原子含量明显减少,w(Na)明显增加,表明会有一部分Na2SO4聚集在催化剂表面. 表2为催化剂表面不同形态氧和钒的含量. 其中,定义表面化学吸附氧为Oα,定义晶格氧为Oβ. 由表2可见,3% Na2SO4中毒SCR催化剂w(Oα)增加. 表面化学吸附氧的活性非常强,其在氧化反应过程中起着决定性作用,催化剂的氧化性能和w(Oα)呈一定的正相关性[29]. 因此,3% Na2SO4中毒SCR催化剂表面较高的w(Oα)导致SO3生成率增加.
由表2可见:SCR催化剂中,w(V4+)为 42.50%,w(V4+)w(V5+)为0.74;3% Na2SO4中毒SCR催化剂中,w(V4+)都有所减少,相对应的w(V4+)w(V5+)为0.67. 研究[30-31]表明,w(V4+)w(V5+)在催化剂的氧化还原反应中也扮演着非常重要的角色,在一定范围内,提高w(V4+)w(V5+)会增加催化剂活性,促进SO2氧化. 但是过高和过低的比例都会降低氧化还原反应速率和催化剂的活性. 因为在氧化还原反应进程中,低价和高价V之间会发生电子转移. 只有当低价和高价V之间电子转移平衡时,SO2氧化速率和催化剂活性才会得到提高. 所以也就有可能存在Na2SO4的加入虽然降低了w(V4+)w(V5+),但是使得低价和高价V之间电子转移更加趋于平衡,更有利于SO2的氧化.

表1 不同催化剂的表面原子含量

表2 催化剂表面不同形态O和V的质量分数
3 结论
a) 不同催化剂上SO3生成率随温度的升高而增加. 对于3% Na2SO4中毒SCR催化剂而言,由于SO42-的存在,初始催化剂中V—O—S会被部分替换为V—O—S,从而导致SO3生成率大大增加,温度升至490 ℃时,SO3生成率高达1.36%.
b) 不同催化剂上SO3生成率随入口ρ(SO2)的增加而降低,当入口ρ(SO2)为 1 000 mgm3时,3% Na2SO4中毒SCR催化剂上SO3生成率为1.02%,但是ρ(SO2)的增加会抑制SO3的分解,导致SO3的生成浓度增加. 所以,不仅要关注SO3生成率,还要关注SO3的生成量.
c) BET、XRD和SEM表征结果显示,3% Na2SO4中毒SCR催化剂的比表面积和孔容减小,表面出现裂纹和大孔隙,而且还会出现Na2SO4结晶产物,导致SO3生成率增加.
d) XPS结果表明,3% Na2SO4中毒SCR催化剂表面w(Oα)增加,从而导致SO3生成率的大幅增加.

