产甲胎蛋白伴神经内分泌分化的胃腺鳞癌一例
杨力,汤绍辉
暨南大学附属第一医院消化内科,广东 广州 510630
胃癌(carcinoma of stomach)是发生于胃黏膜上皮和腺上皮的恶性肿瘤,发病率占我国恶性肿瘤的第二位,好发于40~60岁,且男性多于女性,主要好发胃窦部小弯侧。早期胃癌多无症状,部分可出现消化不良、上腹不适、嗳气等非特异性症状,常与胃炎、胃溃疡等胃慢性疾病症状相似,易被忽略。因此,目前我国胃癌的早期诊断率仍较低。本文报道1例特殊类型的胃癌,其具有恶性度高、进展快、易转移、预后差等特点;需引起临床医师重视,以防漏诊,延误疾病治疗。
1 病例简介
患者男,82岁。因“腹部胀痛20+d”于2019年3月31日入院。患者20 d前无明显诱因出现腹部胀痛,主要位于中上腹部,进食后明显,伴恶心、干呕,遂至当地医院就诊。入院后查血常规,血红蛋白74 g/L,肿瘤标志物中甲胎蛋白(AFP)4 432.1 ng/mL、癌胚蛋白(CEA)13.0 ng/mL。胃镜示胃体、胃角、胃窦的前后壁及大弯侧见大片状不规则肿物,质脆易出血;(胃窦、胃体)病变黏膜病理活检诊断伴神经内分泌分化的中分化腺癌、中分化鳞状细胞癌。全腹CT示胃窦病变,胃癌可能性大,伴周边腹腔多发淋巴结稍肿大。予以护胃、补液等对症支持治疗,但仍有腹部胀痛、恶心、干呕、食欲不振。起病以来,患者精神、胃纳、睡眠欠佳,大小便正常,近20 d体质量下降约3 kg。既往有高血压病史6年余,最高血压约160/90 mmHg(1 mmHg=0.133 kPa),未规律服用降压药物,平素血压控制不详;否认肝炎、糖尿病、结核病等病史。
入院体格检查:体温36.5℃,脉搏89次/min,呼吸16次/min,血压137/70 mmHg;神志清楚,全身皮肤、黏膜无黄染,无皮下出血点及瘀斑;浅表淋巴结未触及肿大;双肺呼吸音粗,未闻及干湿性啰音;心律齐,各瓣膜听诊区未闻及病理性杂音;腹部平坦,腹壁未见静脉曲张,腹软,剑突下压痛,无反跳痛,肝脾肋下未触及,Murphy征(-),移动性浊音(-),肠鸣音3~5次/min;双下肢无水肿;四肢肌力、肌张力正常。入院后行相关检查:(1)血常规,血红蛋白65.60 g/L,红细胞计数2.94×1012/L;(2)生化白蛋白26.5 g/L;(3)肿瘤标志物,AFP 3 983.18 ng/mL、CEA 14.89 ng/mL、鳞状细胞癌相关抗原(SCC)4.8 ng/mL;(4)粪便常规潜血阳性;(5)甲乙丙丁戊型病毒标志物阴性。入院诊断:(1)胃占位性病变;(2)高血压病3级,高危组。
入院后进一步完善相关检查:行全身PECT示(1)胃体、胃窦部胃壁明显不均匀增厚,糖代谢增高,考虑胃癌;腹腔多发淋巴结,糖代谢增高,考虑转移瘤;(2)右肺中外侧段磨玻璃结节,糖代谢增高,疑周围型肺癌可能。会诊南医大附属医院病理切片(1902659,HE×1,IHC×9)镜下见微粒组织4小粒,其中2粒见伴神经内分泌分化的中分化腺鳞癌(图1、图2);免疫组化显示CK8/CK5/6/P63部分(+),绒毛蛋白(Villin)弥漫(+),癌细胞突触素(syn)部分(+),嗜铬粒素A(CgA)阴性,AFP阳性,p53阳性指数约40%,ki-67阳性指数约50%,MSH2/MLH1(+)(图3、图4、图5)。综合患者病史、临床表现及相关检查,最后诊断为产甲胎蛋白伴神经内分泌分化的胃腺鳞癌。
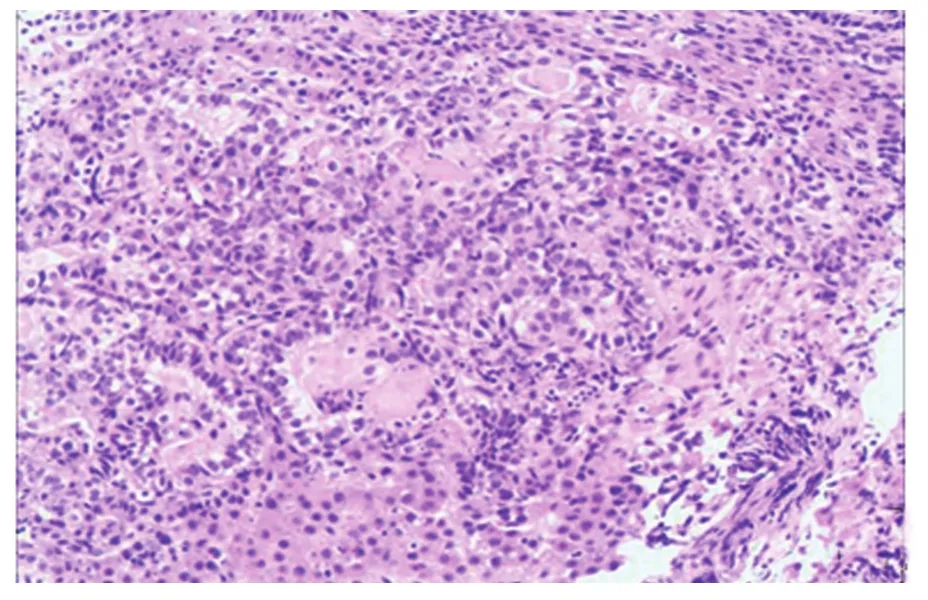
图1 病理组织显示胃中分化腺鳞癌(苏木精-伊红染色×100)

图2 病理组织显示胃中分化腺鳞癌病理组织(苏木精-伊红染色×200)

图3 免疫组织化学显示Ki67(+)(免疫组织化学染色×100)
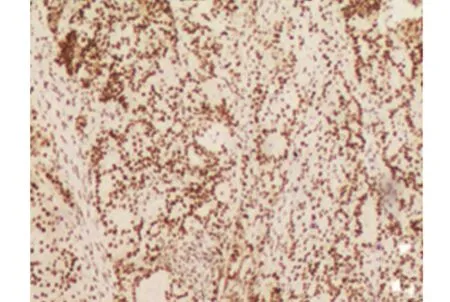
图4 免疫组织化学显示syn(+)(免疫组织化学染色×100)
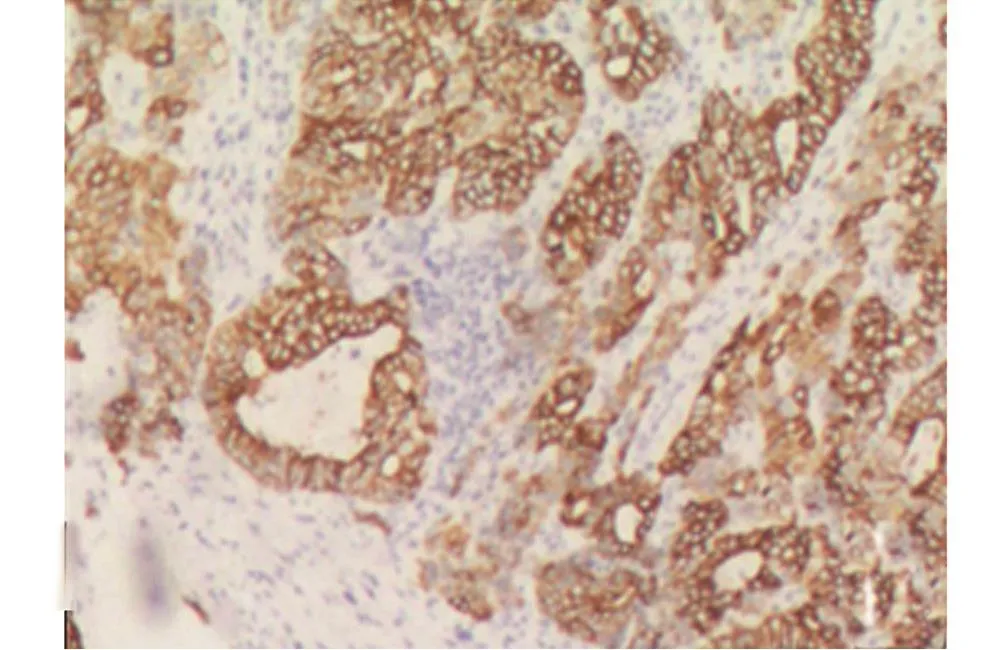
图5 免疫组织化学显示AFP(+)(免疫组织化学染色×100)
2 讨论
神经内分泌肿瘤(neuroendocrine neoplasms,NENs)是一类起源于胚胎的神经内分泌细胞和肽能神经元,且具有神经内分泌标记物、能够产生生物活性胺和(或)多肽激素的肿瘤。其属于异质性肿瘤家族。具有缓慢生长,从低度恶性到高转移性、惰性生长等明显恶性的一系列特征。因被认为具有较低的侵袭性,总的5年生存率为38%~100%,主要取决于肿瘤部位和分期[1]。NENs可以发生在人体任何部位,其中以胃肠胰神经内分泌肿瘤(gastroenteropancreatic neurendocrine neoplasm,GEP-NENs)最常见,占所有NENs的65%~75%。根据2010年世界卫生组织(WHO)分类标准,神经内分泌肿瘤(NENs)按组织学及增殖活性进行分级,可将其分为3级,即G1(低级别):ki-67指数≤2%;G2(中级别):ki-67指数3%~20%;G3(高级别):ki-67指数>20%。在病理学上认为:G1和G2为高分化的神经内分泌肿瘤(NET),呈低度或中度恶性;它们显示了两种一般免疫组化神经内分泌标志物,即嗜铬粒素A(CgA)和突触素(syn),这两种标志物呈弥散或强烈表达。G3表示低分化的神经内分泌癌(NEC),大多数为高度恶性;它具有高有丝分裂计数/Ki-67指数,通常与坏死区域相关,且显示出显著降低的CgA的表达,同时保持对syn的强烈染色[2]。胃神经内分泌肿瘤(g-NENs)在临床上又可分为四型:1型g-NENs是由萎缩性胃炎继发胃酸缺乏引起,其复发率高,在临床上通常表现为消化不良、大细胞或缺铁性贫血。多数预后良好,而>1 cm的肿瘤容易出现转移,往往经过胃镜检查发现。其中2型是由于胃泌素瘤分泌大量激素导致高胃泌素血症(Zollinger-Ellison综合征)引起,具有体积小(直径一般<2 cm)而多发、恶性率高、且常有水样泻及脂性腹泻等特点。此型肿瘤特异表达抗胃泌素抗体。3型可以是G1、G2或 G3,常表现为单发、较大(>2 cm),呈息肉样或溃疡型;它与高胃泌素血症无关,占所有g-NENs的10%~20%。在临床上可表现为贫血、消化不良、消化道出血和梗阻等症状。诊断时,50%以上的患者常出现局部或肝转移。而4型较少见,且其恶性程度较高,分化程度差,常表现为巨大溃疡或球形息肉,80%~100%可发生转移。g-NENs的主要治疗方式仍以手术治疗为主[3]。
产甲胎蛋白胃癌(alpha-fetoprotein producing gastric carcinoma,AFPGC)[4]是指经过病理或组织学检查确诊,伴有血清AFP升高,并排除肝炎、肝硬化、肝细胞癌、生殖细胞恶性肿瘤及Wiskott-Aldrich综合征等其他疾病的胃癌[5]。其临床病理学特征与普通型胃癌有较大不同,特点是好发于中老年男性,更易发生肝转移和早期淋巴道转移,具有明显的侵袭性和恶性生物学行为,常在疾病的晚期阶段被诊断出来。因其恶性度高、进展快、易转移、预后差等特点,逐渐在临床上受到重视,被认为是一种特殊类型的胃癌[6]。AFPGC可分为两种亚型,即产生AFP的非肝样腺癌和肝样腺癌。其预后与肿瘤分期密切相关,其他因素(包括肿瘤侵袭深度、淋巴结转移程度、AFP的表达及p21的表达)也被认为对预测AFPGC患者的预后非常重要。肿瘤细胞增加的有丝分裂、增殖活性、肿瘤进展、肝细胞和受体生长因子、c-Met、血管内皮生长因子(VEGF)和同型VEGF-C的表达等因素也被鉴定为与AFP-GC相关,并且作为癌症的不良预后因素[7]。检索国内外文献,关于AFP阳性胃癌的发病率,国外文献报道为1.3%~15%[8],其5年生存率的报道不尽相同,从8.3%到34.0%不等[9]。而以甲胎蛋白阳性伴神经内分泌分化的胃腺鳞癌未曾有报道。
本病例有如下特点:(1)老年男性患者,亚急性病程,临床症状不显著。(2)鳞状细胞癌(squamous cell carcino-ma)简称鳞癌,是发生于表皮或附属器细胞的一种恶性肿瘤,多见于鳞状上皮覆盖的部位,如皮肤、口腔、食管、喉、子宫颈、阴道及阴茎等处,而胃窦则罕见。本病例中同时存在神经内分泌肿瘤、胃腺癌、胃鳞癌三种肿瘤。(3)该肿瘤恶性程度高,易转移,主要转移至肝脏及淋巴结;本例发现时已存在腹腔多发淋巴结转移,由于患者高龄,且一般情况较差,其家属放弃正规化疗。(4)AFP是一种癌胚糖蛋白,主要由胎儿发育期间的卵黄囊和肝脏产生,且在较小程度上在胎儿胃肠道中产生,最高血清水平出现在妊娠12~15周之间,大约在一年后降至正常成人水平。而此患者血清AFP水平非常高,CEA升高,其他肿瘤标志物不高,容易误诊为肝细胞癌;同时也需与AFP增高的肿瘤鉴别:如肝细胞癌胃转移、生殖细胞肿瘤等。对于临床症状不显著、检查证据不充分、诊断不明确的消化道恶性肿瘤,单一检测某种肿瘤标志物都存在的一定的误诊和漏诊,笔者应该检测多种肿瘤标志物,并结合其他相关辅助检查以尽早明确诊断。而各肿瘤标志物在诊断消化道恶性肿瘤中表现不同,其中AFP在肝癌中最敏感(阳性率为84.8%),而胃癌对所有肿瘤标志物的检测均不敏感[10]。因此,在临床应用中结合其他辅助检查对提高疾病临床诊断水平非常必要,如消化系统中胃肠镜检查,以达到对早癌的筛查,得到有效治疗方案,明显提高预后生存率。在临床工作中对于恶性程度高、进展快、易转移、预后差的一类肿瘤,笔者应该早诊断,保证患者尽早得到有效治疗,而且能够降低消化道恶性肿瘤患者的误诊、漏诊率,延长恶性肿瘤患者的生存期。

