两 个 钒 同 多 酸 化 合 物 的 光 谱 测 试
陈义平, 孙瑞卿, 杨 珍
(1.福州大学 化学学院,福州 350116; 2.福州大学 结构化学国家重点实验室,福州 350002)
0 引 言
钒(V)同多酸化合物属于多核金属-氧簇化合物。钒在形成多酸化合物时通常有VIII、VIV和VV,它们以四方锥、八面体、三角双锥等形式通过共点、共边或共面的方式连接[1],组成钒多酸化合物中簇单元的基本构造单元。由于钒具有多种价态,并且配位方式灵活,导致其多酸化合物的结构多样,表现出丰富的理化性质,在光学[2-3]、磁学[4-5]、离子交换[6]、催化[7-9]和药物化学[10]等方面具有较好的应用前景。
近年来,部分学者尝试采用多种方法对多酸化合物进行表征,研究结构与性能的关系。笔者曾对多酸化合物的水热合成条件进行了探索[11],在此基础上,本文利用X射线粉末衍射、红外光谱、二维红外相关光谱、固体紫外漫反射光谱、热重及高温红外光谱等技术对本文所合成的多酸化合物1和2进行研究。
1 实验部分
1.1 化合物的合成
1.1.1 化合物1的合成
(1) 原料。Na2TeO30.51 mmol,Na3VO4·12H2O 1.99 mmol,LiOH·H2O 1.02 mmol,NH4Cl 2.01 mmol,乙二胺0.2 mL,乙醇6.00 mL(体积分数为50%的溶液)。
(2) 反应条件。用浓盐酸调节上述混合液pH为6.6,在不锈钢高压反应釜中130 ℃恒温82 h。
(3) 结果。暗红色块状晶体,按钒计算产率约为42%。
1.1.2 化合物2的合成
(1) 原料。Na3VO4·12H2O 0.45 mmol,Cu(NO3)2·3H2O 0.64 mmol,CsOH 1.24 mmol,乙二胺0.12 mL,H2O 6.00 mL。
(2) 反应条件。用浓盐酸和氢氧化钠溶液调节pH为5.3,在不锈钢高压反应釜中100 ℃恒温11 h。
(3) 结果。棕褐色片状晶体,按钒计算产率约为31%。
1.2 测试仪器与条件
表1为测试仪器及测试内容与测试条件。

表1 测试仪器及测试内容、测试条件
2 测试结果分析
2.1 化合物的结构特征

化合物[Cu(en)2]3[V10O28]·6H2O为单斜晶系,P21/c空间群。最小不对称单元由1/2个[V10O28]6-阴离子和3/2个[Cu(en)2]2+阳离子构成。Cu2位于对称轴上,其他原子位于一般等效点上。在化合物2中,[V10O28]6-由2个{VO6}共用6条边、4个{VO6}共用5条边、4个{VO6}共用4条边连接而成,其中V=Ot键长0.160 8~0.161 9 nm,V—Oμ键长0.169 1~0.223 7 nm,V—O—V键角83.36°~175.94°,如图3所示。根据价键(BVS)[13]计算结果,V的价态为+5价。每个[V10O28]6-通过与周围8个[Cu(en)2]2+及游离的水分子形成N—H…O、C—H…O和O—H…O氢键而互相连接,形成三维超分子网络结构(见图4),部分氢键列于表3,其中O11、O12、O13、O14为端氧,O4和O10为桥氧。
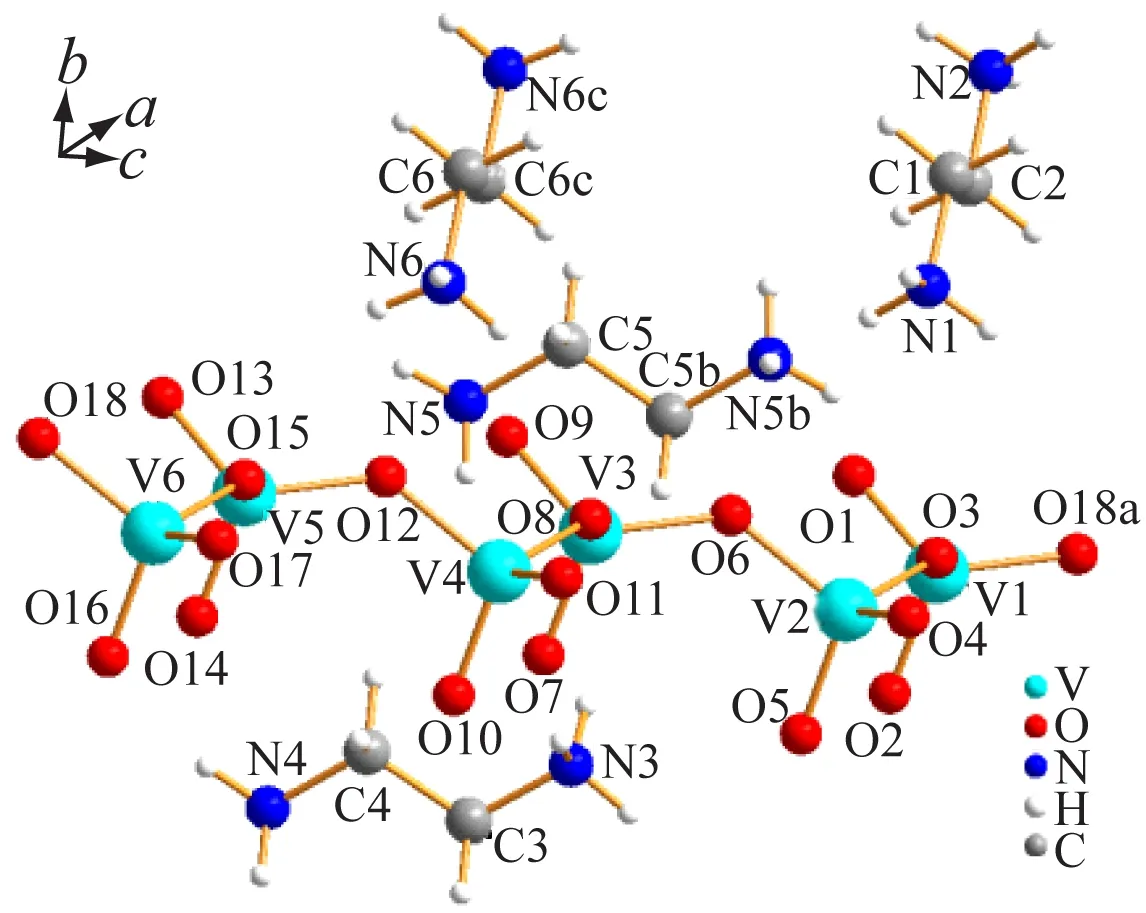
图1 化合物1不对称单元图
对称操作符:a) 2+x,-1+y,z;b) 1-x,1-y,1-z;c) 2-x,1-y,-z
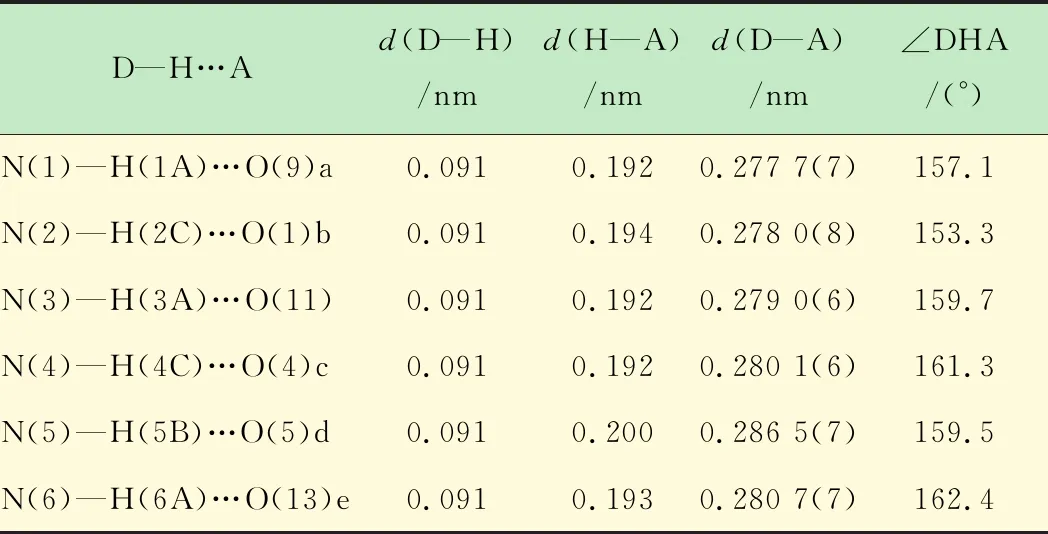
表2 化合物1部分氢键列表
对称操作符:a) -x,1-y,1-z;b)x-1,y+1,z+1;
c) 1-x,-y,1-z;d) 1,y+1,z;e) -x,1-y,-z
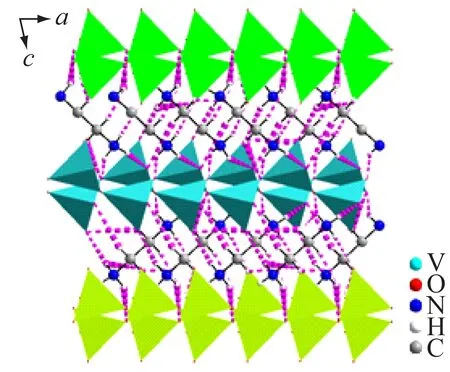
绿、蓝绿、黄绿色多体面代表{VO4}四面体,粉红点线代表N—H…O和C—H…O氢键(省略氢原子)
图2 化合物1三维堆积图
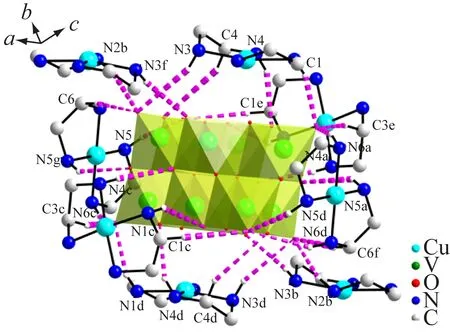
对称操作符:a)x-1,y,z;b)x,y-1,z;c)x,0.5-y,z-0.5;d) 1-x,-y,-z;e) 1-x,y-0.5,0.5-z;f) 1-x,1-y,-z;g) 2-x,-y,-z
图3 化合物2的配位环境图和氢键
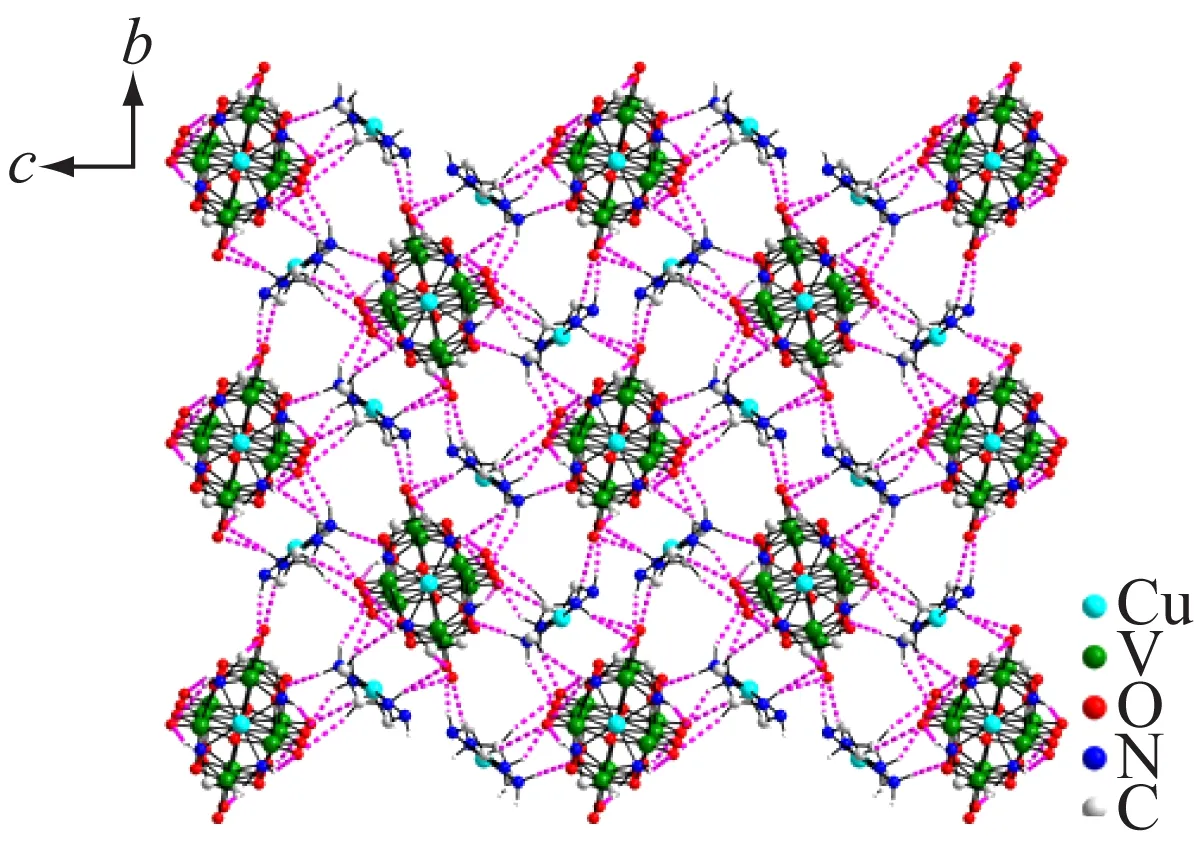
图4 化合物2沿a轴方向的三维堆积图
2.2 化合物的X-射线粉末衍射
X-射线粉末衍射是确定化合物晶体结构及物相分析的有效手段。化合物1、2的实验数据图和模拟衍射图(见图5)显示,实验数据主要衍射峰位置与模拟衍射峰位基本一致,表明所制备的化合物为纯相[14],可用于其他性质的表征。
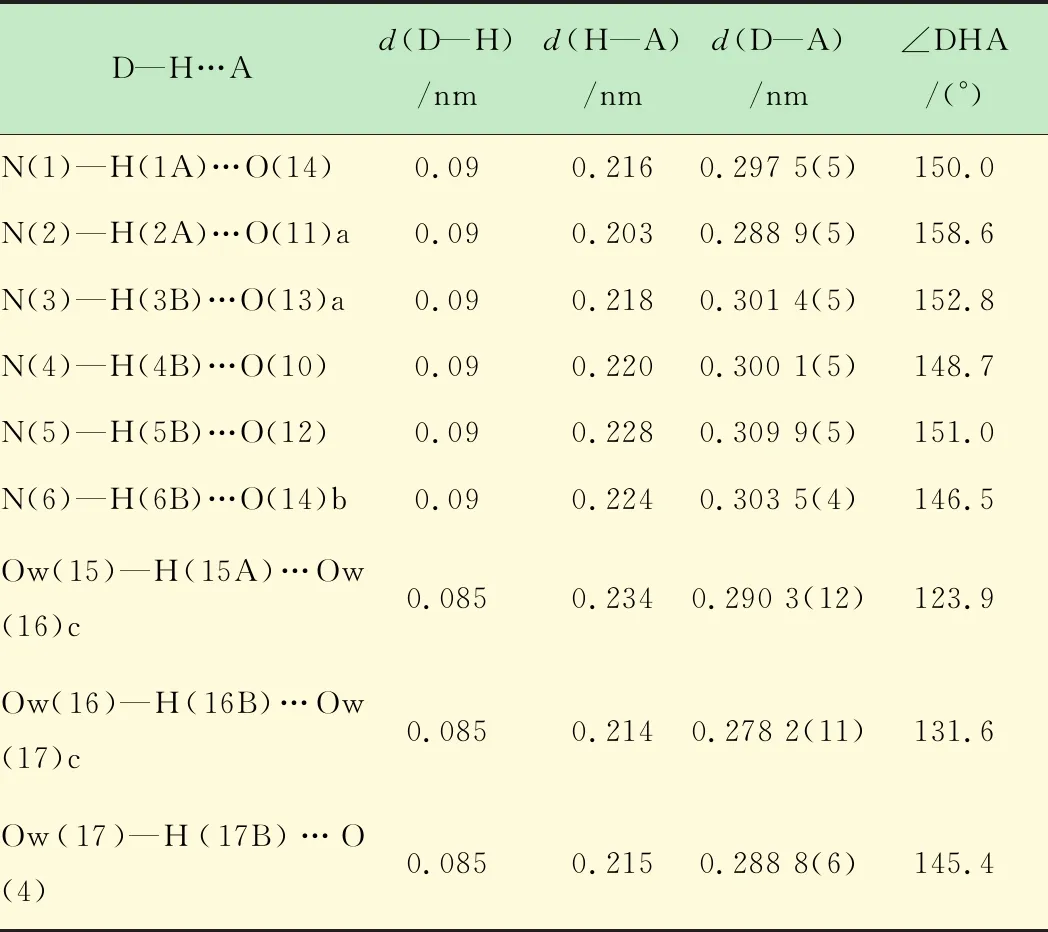
表3 化合物2部分氢键列表
对称操作符:a) -x+1,-y+1,-z;b)x+1,y,z/2;c) -x+2,y-1/2,-z+1/2
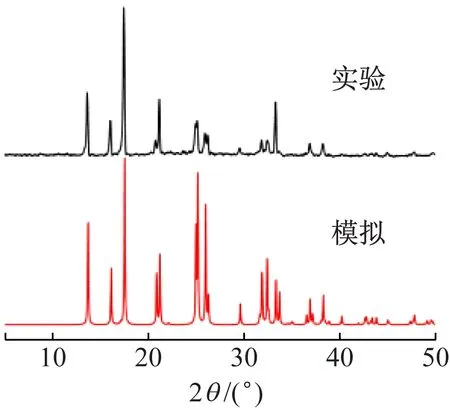
(a) 化合物1
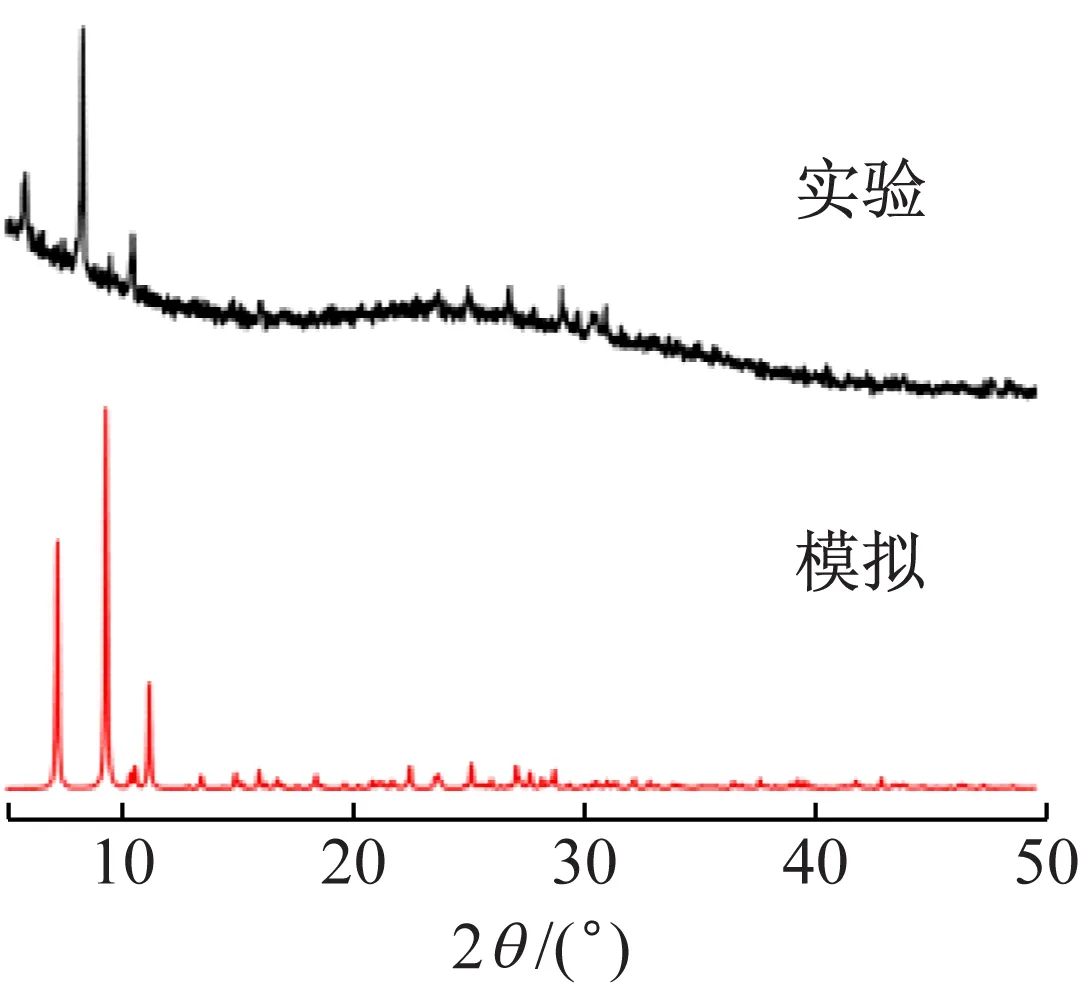
(b) 化合物2
2.3 化合物的红外光谱和二维红外相关光谱
化合物1,2的红外光谱如图6所示,两个化合物中的钒均为+5价。化合物1钒为四配位,V=Ot和V—Oμ均与乙二胺形成N—H…O或C—H…O氢键,V=Ot和V—Oμ的伸缩振动吸收峰分别位于931、907 cm-1及820、770、674 cm-1。化合物2钒为五配位,所有V=Ot和部分V—Oμ与胺合金属阳离子或游离的水分子形成N—H…O或C—H…O或O—H…O氢键,V=Ot和V—Oμ的伸缩振动吸收峰分别位于947、926、907 cm-1及818、725 cm-1[15]。两个化合物的钒氧伸缩振动吸收峰位均向低波数方向移动。配体乙二胺及化合物1、2的红外伸缩振动吸收峰见表4。
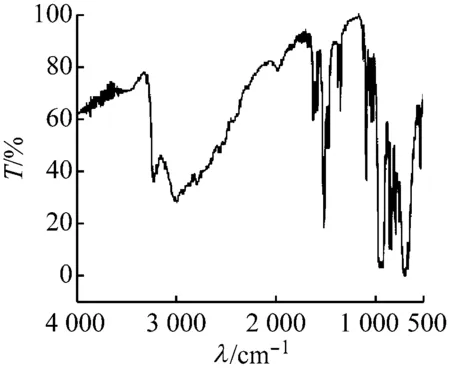
(a) 化合物1
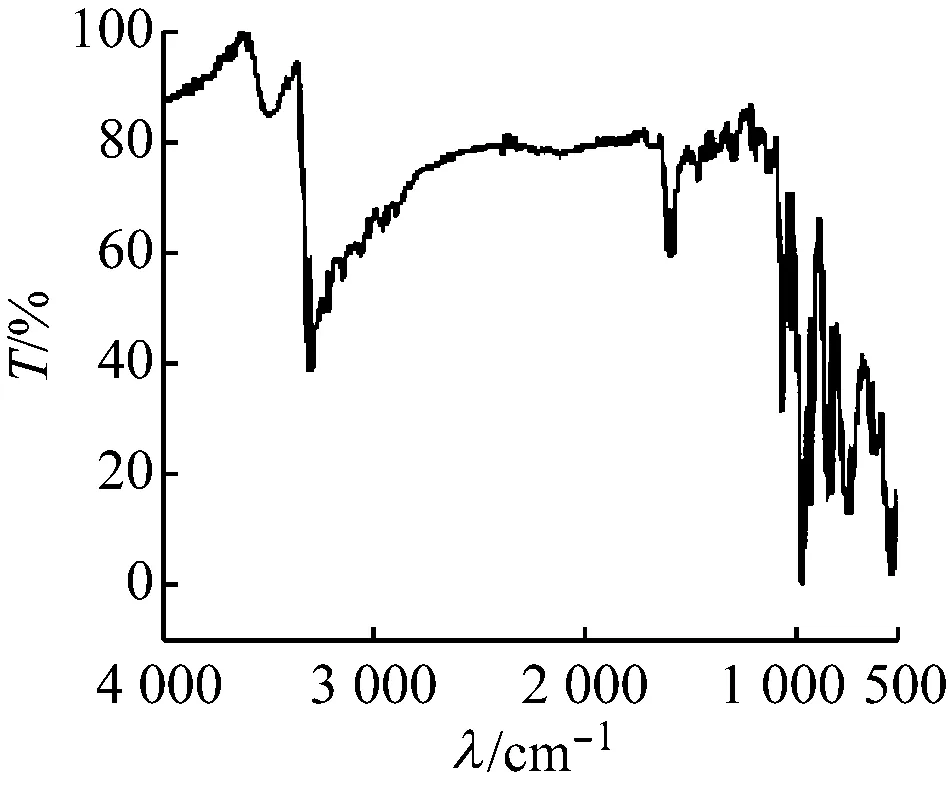
(b) 化合物2
图6 化合物 1,2的红外光谱图
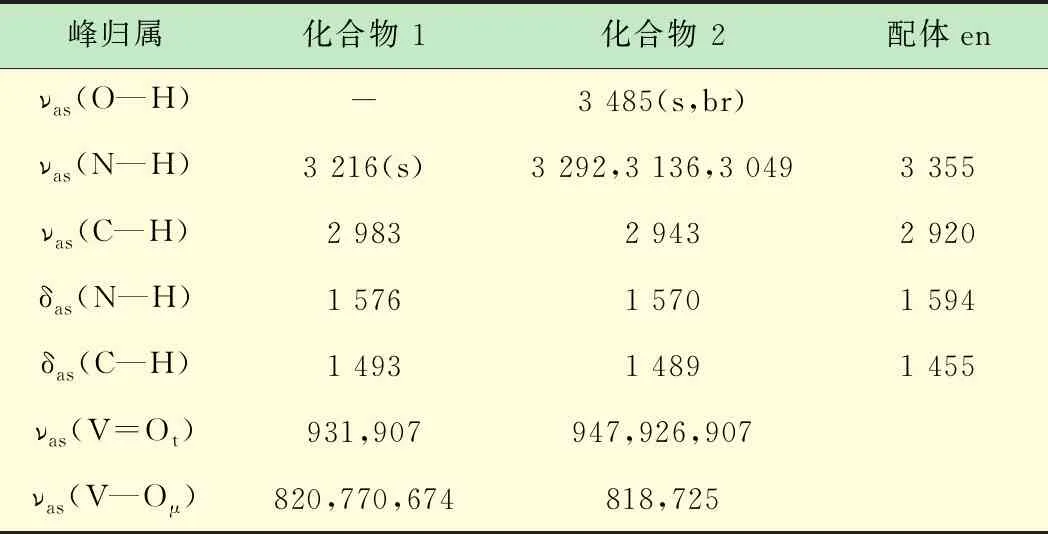
表4 化合物1、2及配体的部分红外振动吸收峰
由于一维红外光谱较难区分钒多酸化合物不同簇笼的振动信息,因此,利用热微扰附件,在50~120 ℃对化合物进行二维红外相关光谱的测试并进行分析。图7(a)化合物1的同步相关图显示,在主对角线上的3 225、3 118 cm-1出现了很强的自动峰,表明N—H的伸缩振动对热微扰比较敏感,(3 225,3 118 cm-1)的交叉峰为负,说明N—H的反对称和对称伸缩振动不同步,结合图7(b)的异步图,(3 225,3 118 cm-1)的交叉峰亦为负,根据Noda[16]规则,可判断νas(N—H)对热变化响应先于νs(N—H)发生。在图7(c)的主对角线上出现了较强的V—Oμ自动峰,位于824、801、632 cm-1,而V=Ot的自动峰位于943,884 cm-1,同步图中(824,884 cm-1)的交叉峰为负,图7(d)异步图中,交叉峰亦为负,通过自动峰的强度及同步异步图正负相关性[16]比较,可知ν(V—Oμ)比ν(V=Ot)对外界的热微扰更敏感,且ν(V—Oμ)对热微扰的响应先于ν(V=Ot)进行。
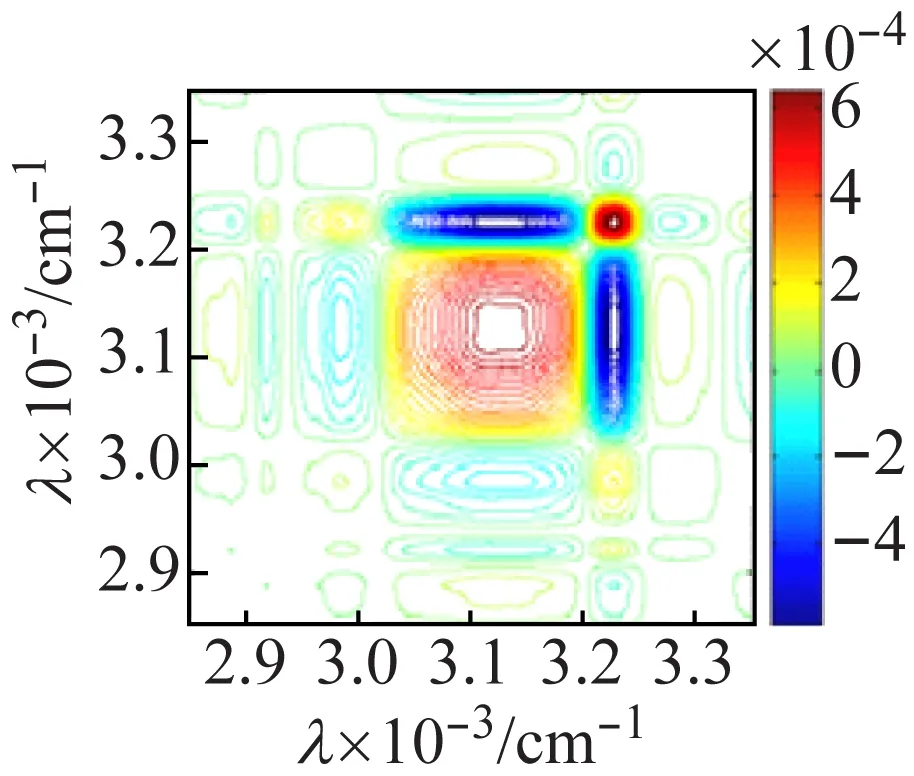
(a) 同步图
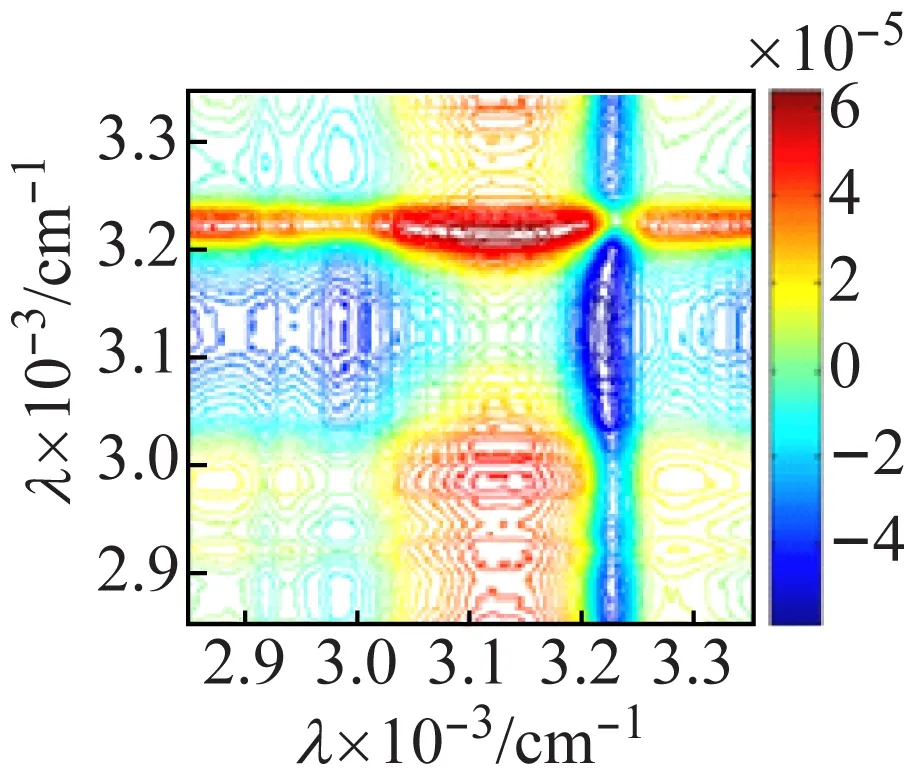
(b) 异步图
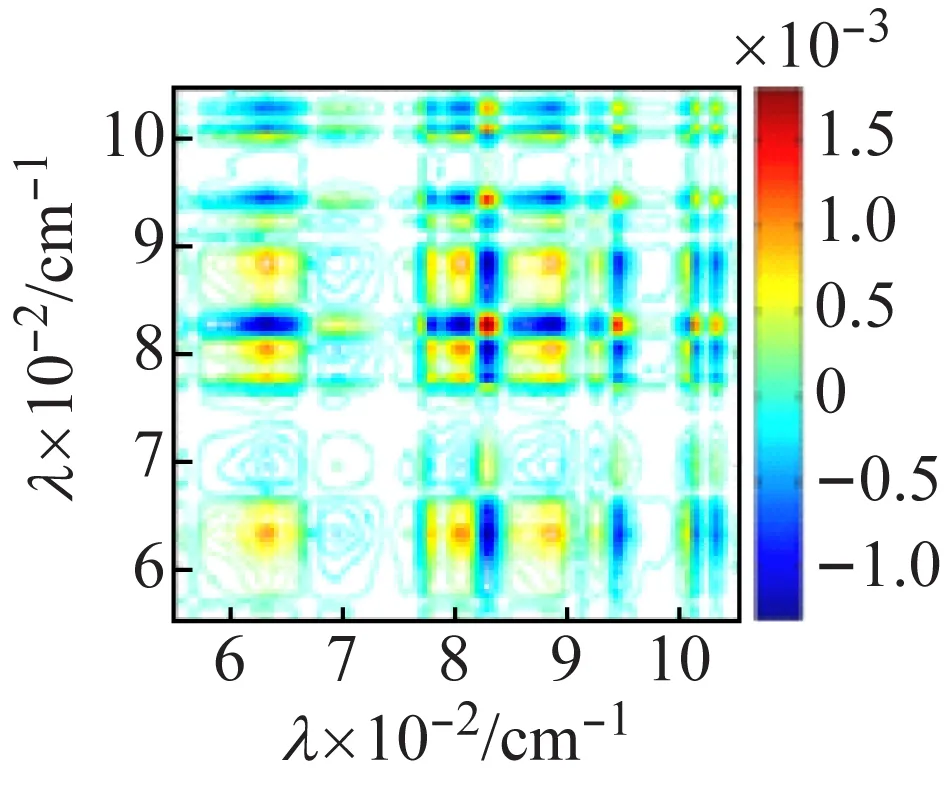
(c) 同步图
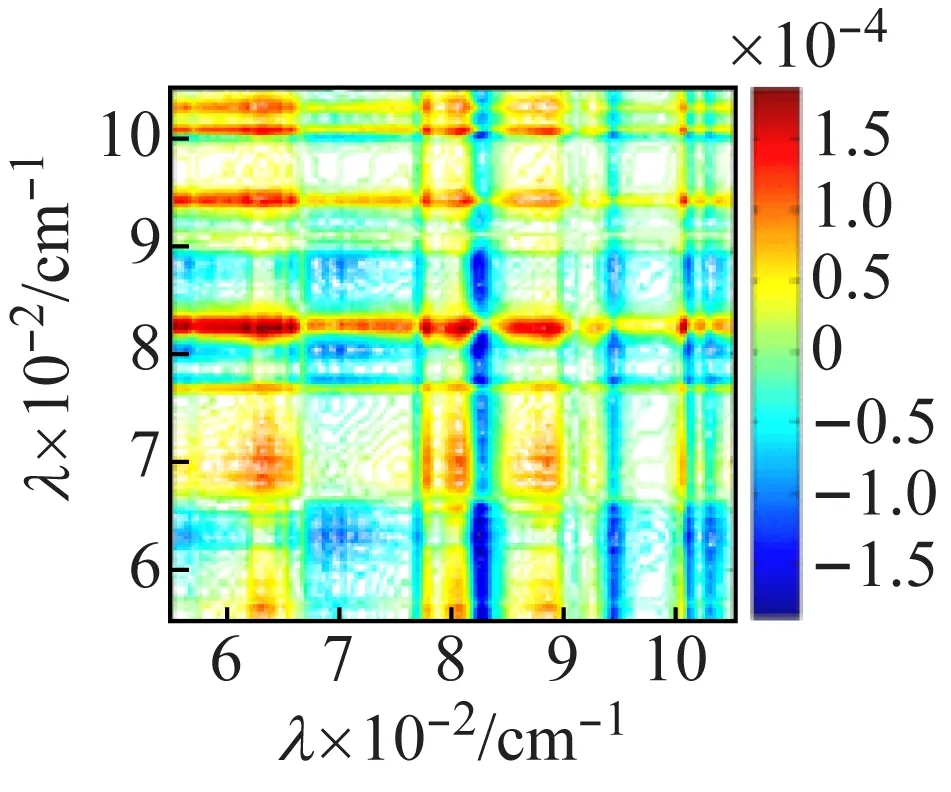
(d) 异步图
图8(a)的同步图中,化合物2在3 265、3 200 cm-1处有很强的热响应,对应于ν(O—H);在3 120、3 076 cm-1处的自动峰对应于ν(N—H)的热响应。由于与多酸阴离子[V10O28]6-上的O原子形成较强的氢键,使O—H和N—H的热响应均向低波数方向移动,同步图(a)和异图步(b)中(3 265,3 120 cm-1)处交叉峰均为正,说明ν(O—H)对外界热微扰的响应先于ν(N—H)发生。图8(c)中,ν(V=Ot)热响应峰位于971、916 cm-1处;ν(V—Oμ) 热响应峰位于801、714 cm-1处。根据Noda[16]规则,结合同步异步图各交叉峰的强度和正负号,可判断V=Ot比V—Oμ对热微扰更敏感且对热微扰的响应也更快。化合物1和化合物2的V=Ot、V—Oμ对热微扰的敏感性及响应速度差异,是由于化合物1形成一维链状结构,簇笼是无限的,因此钒桥氧对热响应更敏感;而化合物2中所有钒端氧均与乙二胺或水形成很强的氢键,呈孤立结构,簇笼是有限的,因此在热微扰中,氢键起主要作用,故钒端氧比钒桥氧对热响应更敏感更快。
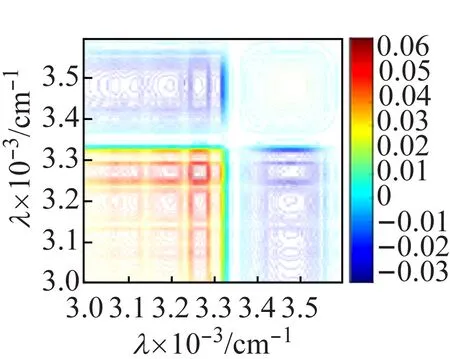
(a) 同步图
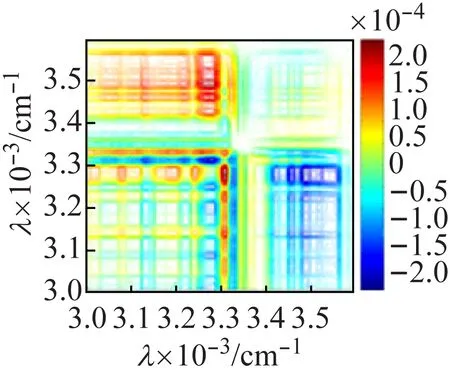
(b) 异步图
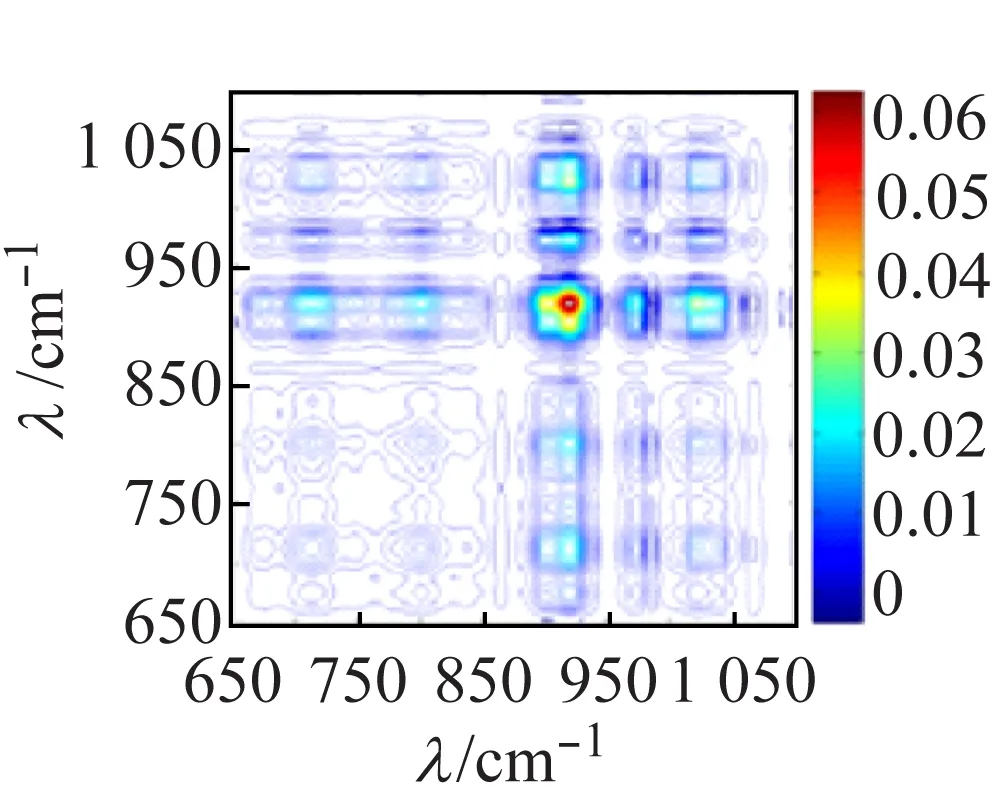
(c) 同步图
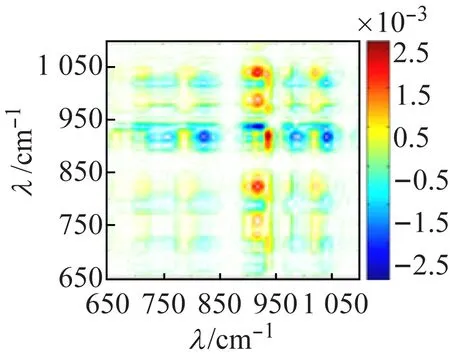
(d) 异步图
2.4 化合物的固体紫外-可见漫反射光谱
化合物1在200~400 nm间有3个比较明显的漫反射峰,分别位于230、291、328 nm处,为O→V的荷移跃迁(见图9,表5)。化合物2在298、359 nm处有2个宽化的漫反射峰,为O→V的荷移跃迁;在550~650 nm 处还出现了Cu2+的d→d跃迁。
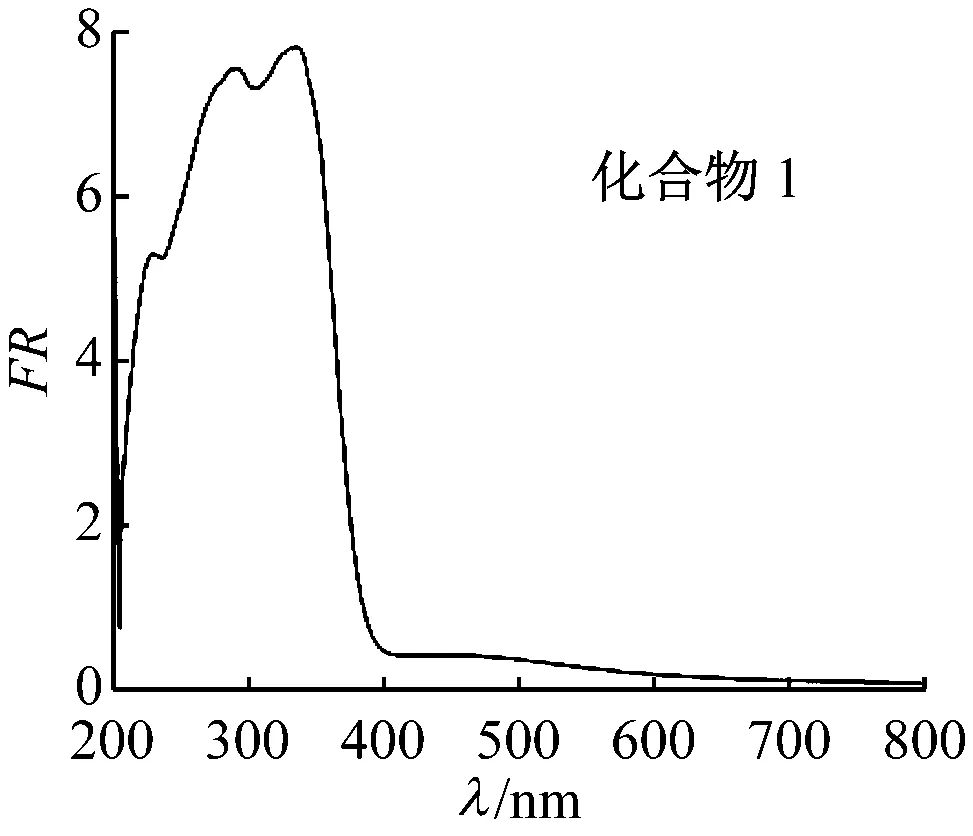
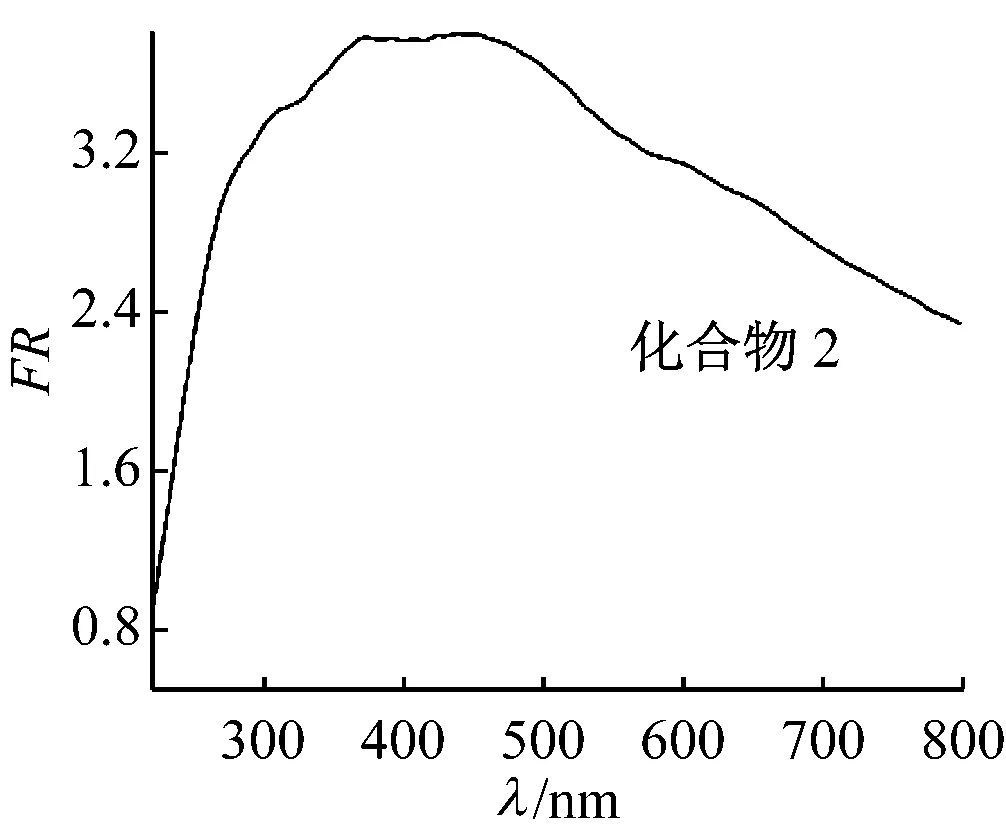
图9 化合物1,2的固体紫外漫反射光谱
2.5 化合物的热重分析
化合物1在50~600 ℃的热失重分2个阶段。第1阶段失去3个双质子化的乙二胺分子(160~390 ℃),失重为20.8% ,理论失重为23.8%。第2阶段为钒多酸阴离子骨架坍塌(410~600 ℃),失重为12.6%,整个过程总失重为33.4%,理论总失重为30%(见图10、表6)。

表5 化合物的固体紫外漫反射光谱带
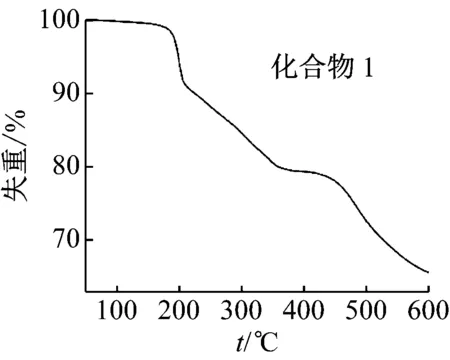
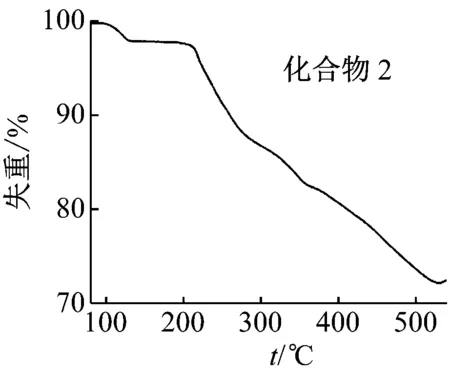
图10 化合物1,2的热重曲线
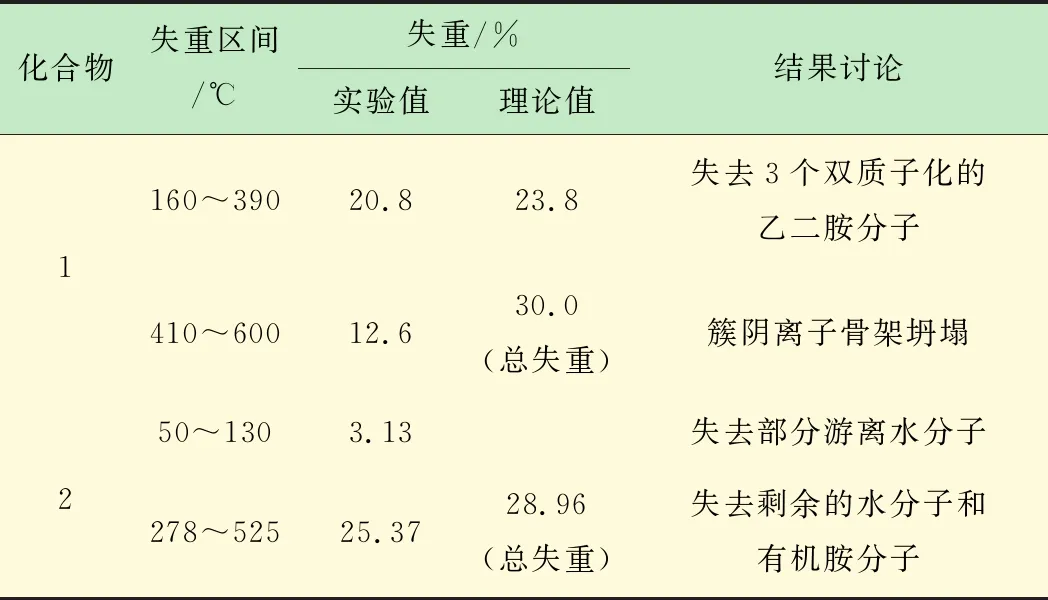
表6 化合物的热失重值
化合物2在50~530 ℃的热失重分2个阶段。第1阶段失去部分游离水分子(50~130 ℃),失重3.13%;第2阶段失去剩余的水分子和[Cu(en)2]2+上的乙二胺分子,失重25.37%,整个过程总失重为28.50%,理论总失重为28.96%(见图10、表6)。
热重分析表明,钒同多酸化合物中的游离水分子最先失去,其次是质子化的乙二胺,再次为[Cu(en)2]2+上的乙二胺分子,达到一定温度后,钒多酸骨架坍塌。
2.6 化合物的高温红外光谱
高温红外光谱分析可以进一步检验二维红外相关光谱、热重分析结果。
根据图11(a),随着温度的升高,化合物1的N—H和C—H伸缩振动吸收峰逐渐变小,峰形宽化变平,当温度升至300 ℃时,则不再出现;当温度升至400 ℃时,在820、770、674 cm-1处,钒簇单元的V—Oμ的伸缩振动吸收峰不再出现;当温度升至540 ℃时,931 cm-1处还存在V=Ot伸缩振动吸收峰,说明V—Oμ比V=Ot先断裂失去。
根据图11(b),当温度升至300 ℃时,化合物2的N—H和C—H伸缩振动吸收峰不再出现;当温度升至355 ℃时,在818、725 cm-1处,钒簇单元的V—Oμ的伸缩振动吸收峰不再出现;当温度升至500 ℃时,947 cm-1处还存在V=Ot的伸缩振动吸收峰,说明钒桥氧键比钒端氧键先断裂。
高温红外光谱显示,随着温度上升,化合物结构发生变化、失去小分子的次序为:游离水分子、游离有机胺分子、[Cu(en)2]2+上的有机胺分子,在较高温度时,簇阴离子骨架坍塌。化合物高温红外光谱特征与热重分析基本吻合。
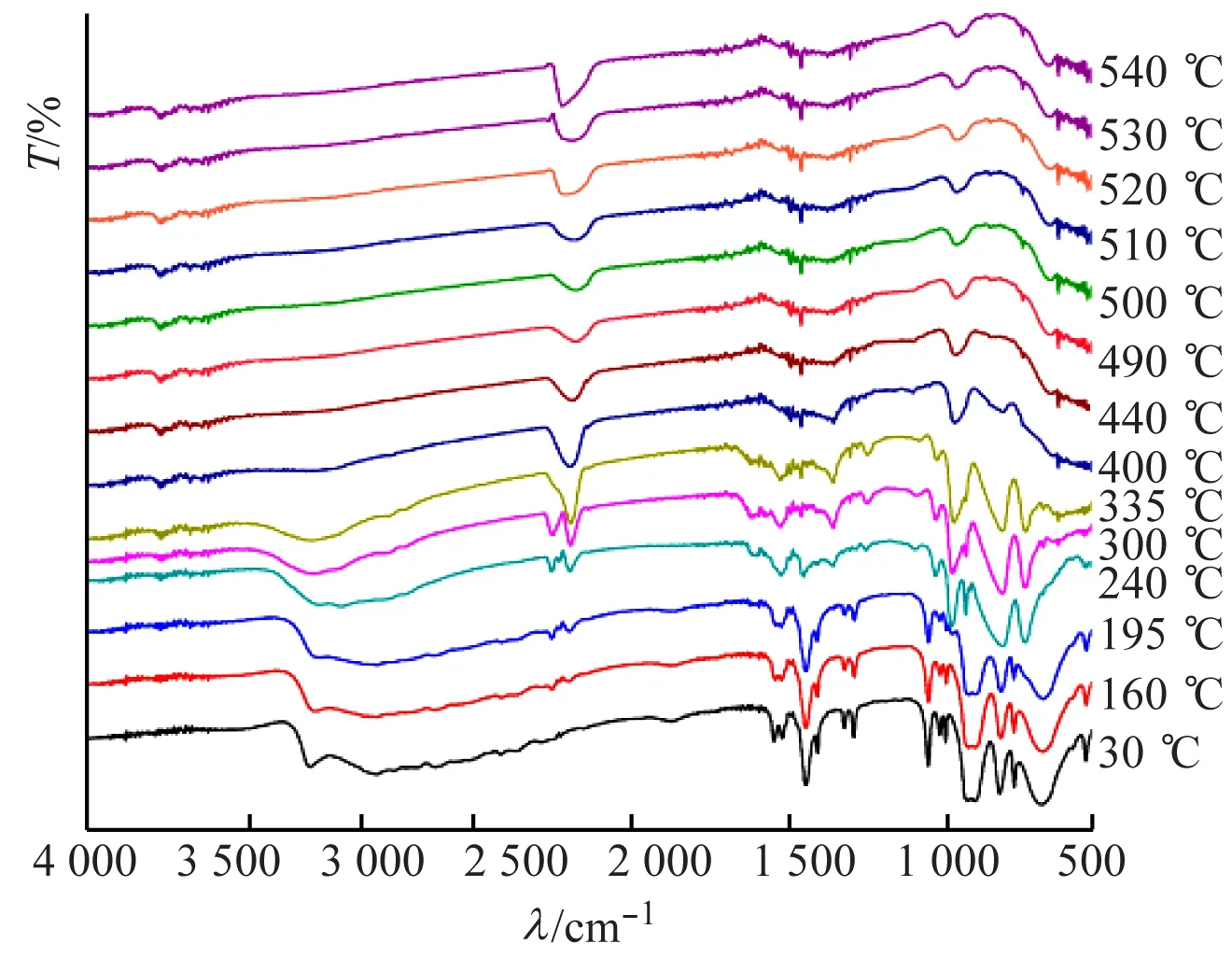
(a) 化合物1
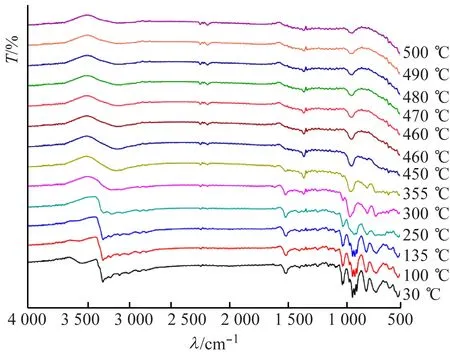
(b) 化合物2
3 结 语
光谱测试技术是研究钒多酸化合物结构与性能间关系的重要手段[17]。本文通过对合成化合物的光谱分析,让学生掌握多种谱学性质分析方法的适用范围及特点,包括X-射线单晶衍射确定晶体结构,X-射线粉末衍射进行物相分析,红外光谱获得官能团特征频率,二维红外相关光谱研究化合物对外界微扰的响应及官能团对外界微扰的响应次序,紫外-可见漫反射光谱显示电子能级及LMCT跃迁,热重分析获得化合物在升温过程中质量变化,高温红外光谱进一步显示化合物热稳定性等。通过光谱测试分析,验证化合物结构的准确性,并进一步探索研究结构与性能间的关系。
——以高中化学“氢键”的教学为例

