原发性肝脏非霍奇金淋巴瘤1例
吴晓天
(浙江大学医学院附属第一医院 浙江 杭州 310003)
1 病例
患者女性,69岁,2月前无明显诱因下出现间断性中下腹隐痛,不剧能忍,持续数分钟可自行缓解,无头晕头痛,无畏寒发热,无腹痛腹泻等不适。外院彩超示“肝内低回声团,占位性病变”。PET-CT示:“1肝左叶部分切除术,肝左叶占位,18-FDG代谢增高,考虑恶性病变”。3年前行“左肝外侧叶切除+开腹胆总管切开经胆道镜取石术+T管流术”,余既往史、个人史、家族史无殊。查体:中下腹压痛,无反跳痛,肝脾肋下未及,全身浅表淋巴结未及肿大。血常规示:白细胞计数 9.0×109/L。生化示:碱性磷酸酶173U/L,直接胆红素7.0μmol/L,谷氨酰转酞酶137U/L。超敏C反应蛋白144.80mg/L。肿瘤标志物示:糖抗原199 66.2U/ml。
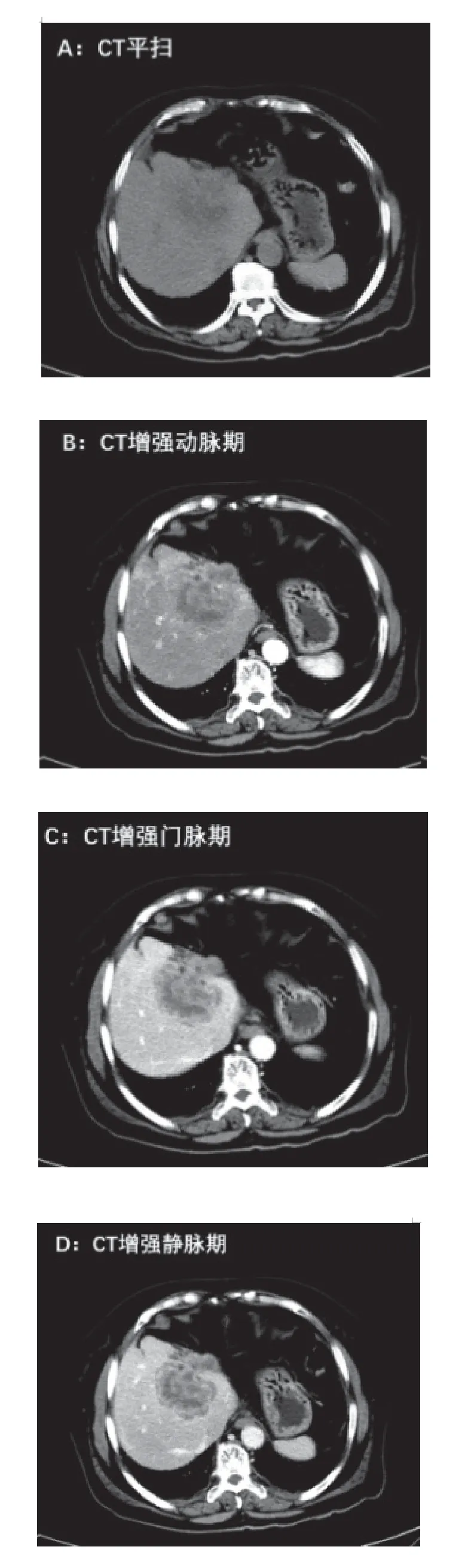
行肝脏CT增强检查示:右肝近肝门部见团片状稍低密度影,边缘模糊,动态增强扫描动脉期病灶边缘轻度环状增强,门静脉及延迟期病灶进行性不规则强化,临近肝内胆管轻度扩张。右肝占位,考虑“慢性脓肿可能”。
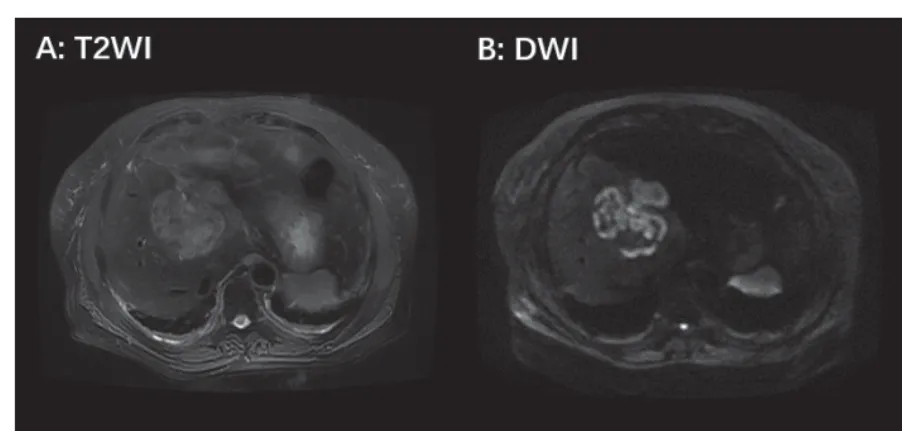
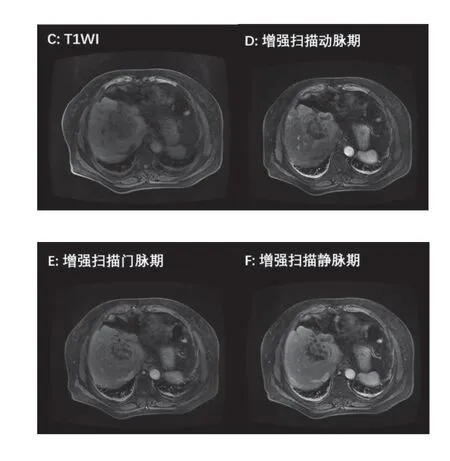
行肝脏MRI增强扫描示:右肝近肝门见圆形异常信号灶,直径约6.3cm,T1WI呈稍低信号,T2WI呈稍高信号,DWI呈环状不均匀高信号,增强扫描动脉期病灶呈花环状强化,超过同期肝组织,门脉期及平衡期持续强化,病灶边缘不规则,内见片状无强化区。右肝包膜下动脉期可见斑片状强化,余期未见明确显示。肝内胆管未见扩张;肝静脉及门脉主干血管流空信号正常,未见明显充盈缺损。右肝占位,考虑肝胆管细胞癌可能。
行肝穿刺活检示:T淋巴细胞异常增生,CD2+,CD4部分+,CD8+,CD5+,CD7+,TIA-1+,CD56-,CD31-,CD3+,CK-,CD79a-,CD30-,Ki67(70%+),CD20-,Hep-,S-100-,DOG-1-,CD23-,EBER-,CD21-,ALK-,CK19-,CK7-,CD34-,GPC-3-,CD117-,结合免疫组化符合外周T细胞性淋巴瘤。
行骨髓活检示:造血组织增生活跃,CD3(散+),CD20(少+),CD45(散+),MPO(+),CD138(散+),CD235(+),CD117(-),CD34(-)。
最后诊断:非霍奇金淋巴瘤(外周T细胞性淋巴瘤,IV期A组)。
2 讨论
原发性肝脏淋巴瘤(primary hepatic lymphoma,PHL)是起源于肝脏淋巴组织和残留造血组织的罕见恶性肿瘤,以肝窦内大量单一形态的中等大小淋巴细胞浸润为特征,占非霍奇金淋巴瘤的0.016%,占所有结外淋巴瘤的0.4%,占肝脏恶性肿瘤的0.1%[1]。
PHL的病因和发病机制尚不明确,近年研究表明乙肝或丙肝肝炎病毒感染、EB 病毒及人类免疫缺陷病毒(HIV)感染、免疫抑制治疗、器官移植患者发病率高,慢性感染及免疫抑制可能导致淋巴细胞持续性单克隆扩增和细胞凋亡的抑制,进而诱发PHL的发生[2,3]。通过对90例PHL病理分型回顾研究得到22种亚型分型,以弥漫性大B淋巴瘤(DLBcL)最为常见[4]。
PHL可发生于任何年龄,以中老年人较为多见,平均发病年龄为50岁,男女比例为2~3:1[1];其临床表现缺乏特征性,较为常见的症状有上腹部隐痛不适,也可以表现为全身乏力、食欲减退、发热、盗汗、体重减轻等淋巴瘤症状,体格可触及肿大的肝脏,10%~20%的患者可出现黄疸。实验室检查肿瘤标志物如AFP、CEA无增高,LDH可有增高。有学者[5]认为乳酸脱氢酶能帮助诊断 PHL,并是判断其预后的敏感指标,但目前PHL患者LDH升高的具体机制尚不明确。
原发性肝脏淋巴瘤的诊断标准为:(1)临床症状由肝脏病变引起;(2)无全身浅表或远处淋巴结肿大,无脾脏肿大;(3)无白血病的骨髓和血清学表现[6]。
PHL大体病理分型与肝脏常见肿瘤类似,大致可分为 3型:(1)单发结节型或肿块型:直径>3cm;(2)多发结节型:肝内多发大小不等病灶,直径<3cm;(3)弥漫型或肝肿大型:未见明确的病灶存在;最常见的为肝脏孤立性病变,见于55%~60%的病例[7]。
淋巴瘤在CT平扫呈单发或多发性肝内低密度肿块或结节,多数边缘清楚,病灶可呈类圆形或分叶状。病灶密度及信号均匀度与肿瘤内坏死、出血、纤维化及钙化成分的存在有关,多数病灶密度及信号较均匀[8]。行MRI检查,病灶在T1WI为等低信号,T2WI信号表现多样,可呈等低信号、等信号或中高信号,偶可见低信号包膜,肿瘤在T2WI呈等低信号时,对PHL的诊断有一定价值;DWI多为稍高或高信号,ADC值减低[9]。肝淋巴瘤为乏血供肿瘤,动态增强扫描大多数病灶呈进行性轻至中度延迟强化,部分病例可表现为边缘强化,这可能与病灶邻近肝实质的脉管炎症有关[8]。由于淋巴瘤起源于肝脏间质,肿瘤跨越或沿脏器解剖结构生长,而原有的解剖结构残留,因此病灶内可见细小血管穿行,而血管本身无狭窄、扭曲,这一特征性表现称为“血管漂浮征”[11]。肝脏弥漫型PHL表现为肝脏肿大而无明显密度及信号的改变时,MRI及CT难以发现病灶。
PHL的鉴别诊断:(1)肝细胞肝癌(hepatocellular carcinoma,HCC):HCC大多数属于富血供肿瘤,增强扫描动脉期明显强化,门脉期快速廓清,呈“快进快出”表现,典型病灶可见假包膜样强化;部分肝癌为乏血供病变,动脉期病变呈轻度强化或不强化,门脉期及延迟扫描病变呈低信号;PHL与乏血供肝癌鉴别困难,但不典型HCC通常相对体积较小,呈结节性[12],且可伴有AFP升高,合并肝硬化背景、门静脉癌栓形成、周边血管受累等。(2)胆管细胞癌:好发于肝脏左叶,常伴有临近肝实质的萎缩、包膜凹陷、远端肝内胆管扩张,增强后病灶内部可有延迟强化,有助于与PHL进行鉴别诊断。(3)肝脓肿:患者多有发热、白细胞增高等感染的表现,病程较急,DWI序列典型病灶脓腔呈高信号,增强扫描脓肿壁呈环状强化,可通过诊断性抗感染治疗进行鉴别。(4)转移瘤:患者有原发恶性肿瘤病史,肝内转移瘤多表现为多发结节,增强后呈典型的厚壁环形强化,病灶内坏死区域相对较大。(5)上皮样血管内皮瘤:增强扫描二者都无明显强化,但上皮样血管内皮瘤好发于肝脏包膜下,可出现包膜皱缩,肝内静脉进入并止于病灶呈“棒棒糖征”,增强可表现为中层环形强化伴周围低密度晕环[13]。

