右美托咪啶复合地佐辛对剖宫产高危产妇术后疼痛及泌乳功能的影响
董晓筠,程 梅,郑彩虹
(杭州市妇产科医院麻醉科 310000)
产妇术后切口疼痛、宫缩痛是麻醉医生关切的重点,手术、疼痛、负性情绪等均抑制产妇的泌乳功能,且不利高危产妇的术后康复。硬膜外镇痛是产妇术后镇痛的有效方式,但存在易发生导管脱落、硬膜外腔感染及脓肿等缺点[1]。近年来,患者自控静脉镇痛(patient- controlled intravenous analgesia,PCIA)已广泛用于产科术后镇痛,效果显著,其中阿片类药物是主要的镇痛药物。研究显示,阿片类药物虽然具有良好的镇痛效果,但恶心、呕吐、呼吸抑制、皮肤瘙痒、便秘等不良反应常限制了其临床应用[2]。因此,选择合适的镇痛药物行多模式镇痛是产科镇痛的基本方案。右美托咪定(dexmedetomidine,Dex)是α2受体激动剂,具有镇痛、镇静作用[3],地佐辛是阿片受体激动(主要激动μ受体)- 拮抗(部分拮抗μ受体)剂,治疗中等程度疼痛效果优于阿片类药物[4],二者复合用于剖宫产术后镇痛的研究报道较少。本研究拟观察Dex复合地佐辛对剖宫产高危产妇术后疼痛及泌乳功能的影响,为产科镇痛提供借鉴。
1 资料与方法
1.1一般资料 选取2017年1月至2019年1月90例剖宫产高危产妇,美国麻醉医师协会(ASA)评级Ⅱ~Ⅲ级。纳入标准:(1)符合《妇产科学(第7版)》[5]中高危妊娠的诊断标准,且在腰硬联合麻醉下行子宫下段横切口剖宫产术;(2)肝、肾、脑、肺等脏器功能正常;(3)产妇认知能力正常,无心理、精神疾病,可独立完成量表填写;(4)临床资料齐全,并签署同意书。排除标准:(1)全身麻醉、局部麻醉及腰硬联合麻醉效果不佳;(2)妊娠高血压综合征、内分泌疾病、血液系统疾病等;(3)药物过敏、吸毒、阿片类药物滥用、心动过缓、房室传导阻滞等;(4)乳房缺陷、母乳喂养禁忌证;(5)连续按压PCIA泵5次及以上,疼痛视觉模拟评分法(VAS)评分大于或等于5分。采用随机数字表法将产妇分为硬膜外腔组(E组)、静脉组(I组)和对照组(C组),各30例。3组年龄、体质量指数(BMI)、孕周、手术时间、术中出血量等一般资料比较,差异均无统计学意义(P>0.05),具有可比性,见表1。本研究经本院伦理委员会批准实施,并与产妇及其配偶签署知情同意书。
1.2方法 入室后开放外周静脉,监测血压、心电图、脉搏氧饱和度,鼻导管吸氧2 L/min,快速静脉输注乳酸钠林格液6 mL/kg,左侧卧位下行第3~4腰椎(L3~4)穿刺,见脑脊液流出后,于60 s匀速注射0.5%罗哌卡因2.5 mL(0.75%罗哌卡因2 mL+脑脊液1 mL,注射2.5 mL),置入硬膜外导管转为仰卧位,调整体位使阻滞平面不超过第6胸椎(T6),平面固定后垫高左侧臀部15°。若手术时间超过60 min,硬膜外腔注射2%利多卡因5 mL。术中收缩压小于90 mm Hg,静脉注射麻黄碱15 mg,心率小于55次/分钟,静脉注射阿托品0.5 mg。胎儿娩出后,E组硬膜外腔注射Dex(江苏恒瑞医药股份有限公司,200 μg/2 mL,批号:161248BP)0.5 μg/kg+地佐辛(扬子江药业集团有限公司,5 mg/1 mL,批号:16122718)5 mg,共5 mL;I组静脉泵注Dex 0.5 μg/kg+地佐辛5 mg 15 min;C组注射等量生理盐水。术毕,3组均行PCIA镇痛,其中E、I组配方为Dex 0.5 μg/kg+地佐辛0.5 mg/kg+托烷司琼(江苏恒瑞医药有限公司,5 mg/5 mL,批号:16121328)10 mg,C组配方为舒芬太尼(宜昌人福药业有限责任公司,50 μg/1 mL,批号:1170208)2 μg/kg+托烷司琼10 mg。3组均用生理盐水稀释至100 mL,背景输注量2 mL/h,一次追加量1 mL,负荷量2 mL,锁定时间为10 min。3组麻醉操作均为作者操作,手术医生均为同一组医生,数据记录均由一名不知情麻醉医生执行。回病房后3组均实行母婴同室、早接触、早吸吮,按需哺乳。
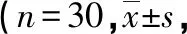
表2 3组术后疼痛评分比较分)
a:P<0.05,与C组比较;b:P<0.05,与I组比较
1.3观察指标 比较3组术后6、12、24、48 h静息、运动和宫缩VAS评分及Ramsay镇静评分,记录3组术前、术后第1、2天泌乳素(PRL)水平,比较3组不良反应(恶心、呕吐、头晕、嗜睡、瘙痒、呼吸抑制等)及新生儿哺乳12 h神经行为评分。VAS用10 cm长标尺表示疼痛程度,0分表示无痛,10分表示最痛,疼痛判定:0分无痛,1~3分轻度疼痛,4~6分中度疼痛,7~10分重度疼痛。Ramsay评分:躁动、焦虑计1分;安静合作计2分;嗜睡,但可听从指令计3分;入睡,但可唤醒计4分;入睡,对刺激有反应计5分;入睡,不可唤醒计6分;其中2~4分为镇静满意,5~6分为镇静过度。PRL采用化学发光法测定,抽取外周静脉血3 mL,3 000 r/min离心5 min,分离血清,置于-20 ℃冰箱待测。神经行为评分总分40分,包括一般评估3项、主动及被动肌张力各4项、原始反射3项,行为能力6项,每项评分为0~2分,总分小于35分表示存在神经行为异常。

2 结 果
2.13组术后疼痛情况比较 3组术后6、48 h静息、运动及宫缩VAS评分比较,差异均无统计学意义(P>0.05);3组术后12、24 h静息、运动及宫缩VAS评分比较,差异均有统计学意义(P<0.05)。E组、I组术后12、24 h静息、运动和宫缩VAS评分均明显低于C组(P<0.05);E组、I组术后12、24 h静息VAS评分比较,差异无统计学意义(P>0.05);E组术后12、24 h运动和宫缩VAS评分均明显低于I组(P<0.05),见表2。
2.23组术后镇静程度比较 3组术后6、12、24 h Ramsay评分比较,差异均有统计学意义(P<0.05),且E组、I组术后6、12、24 h Ramsay评分均明显低于C组(P<0.05);3组术后48 h Ramsay评分比较,差异无统计学意义(P>0.05);E组、I组各时间点Ramsay评分比较,差异均无统计学意义(P>0.05),见表3。
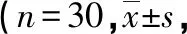
表3 3组Ramsay评分比较分)
a:P<0.05,与C组比较
2.33组泌乳功能比较 3组术前PRL水平比较,差异无统计学意义(P>0.05);3组术后第1、2天PRL水平比较,差异均有统计学意义(P<0.05),且E组、I组均明显高于C组(P<0.05),E组明显高于I组(P<0.05),见表4。
2.4不良反应及神经行为评分比较 3组无1例患者发生呼吸抑制;3组恶心、呕吐发生率比较,差异有统计学意义(P<0.05),E组、I组恶心、呕吐发生率低于C组;3组其余不良反应及新生儿哺乳12 h神经行为评分比较,差异均无统计学意义(P>0.05),见表5。
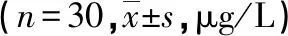
表4 3组手术前后PRL水平比较
a:P<0.05,与C组比较;b:P<0.05,与I组比较

表5 3组不良反应及神经行为评分比较(n=30)
3 讨 论
切口疼痛、宫缩痛是剖宫产术后疼痛的主要来源,引起交感神经兴奋,抑制泌乳功能,严重还可抑制宫缩,增加术后出血风险等。阿片类药物是术后静脉镇痛的主要药物,主要作用于μ受体产生脊髓及其以上水平的镇痛,但所需剂量较大,存在恶心、呕吐、呼吸抑制等风险[6],而地佐辛主要激动κ受体产生脊髓水平的镇痛,部分激动- 拮抗μ受体,镇痛效果安全、确切。Dex具有镇痛、镇静效果,与阿片类药物合用可增强镇痛效果,减少其需要量,无呼吸抑制风险。因此,本研究选择Dex复合地佐辛用于上述剖宫产高危产妇的研究,以期达到减轻术后疼痛、改善泌乳功能的效果。
手术损伤刺激外周和内脏的伤害性感受器,降低痛阈,增强痛反应,引起外周及中枢敏化,产生疼痛,其中切口痛体表定位明确,而宫缩痛属内脏痛,定位模糊。本研究表明,3组术后6、48 h静息、运动及宫缩VAS评分比较无明显差异(P>0.05),E组、I组术后12、24 h静息、运动和宫缩VAS评分均低于C组,E组术后12、24 h运动和宫缩VAS评分均低于I组,说明Dex复合地佐辛的镇痛效果优于舒芬太尼,而硬膜外腔给药的镇痛效果优于静脉给药。地佐辛镇痛强度和吗啡相当,是哌替啶的5~9倍,部分激动大脑皮层的μ受体和脊髓的κ受体产生镇痛效应,其中激动κ受体还可减轻内脏痛,缓解焦虑、紧张等负性情绪。另外,地佐辛还通过抑制5- 羟色胺(5- HT)及去甲肾上腺素的再摄取而产生镇痛作用[7]。Dex激动脊髓后角α2受体抑制去甲肾上腺素释放,还可使脊髓水平的去甲肾上腺素能传导通路的突触前膜产生去极化,抑制Aδ纤维及C纤维活性,减少外周神经释放伤害性肽类物质,从而产生中枢及外周的双重镇痛效果[8]。本研究E组、I组镇痛效果优于C组,可能是地佐辛与Dex合用有关,不仅发挥Dex的镇痛、镇静效果,还可能协同增强地佐辛的镇痛作用。E组镇痛效果优于I组,其原因可能是:(1)地佐辛激动脊髓水平κ受体产生镇痛作用,硬膜外腔注射可更好地发挥脊髓水平镇痛;(2)硬膜外腔注射Dex可直接与脊髓神经元的突触前后膜α2受体结合,开放钾离子(K+)通道,使细胞膜超极化,抑制伤害性递质释放;(3)Dex通过硬脊膜弥散至脑脊液,与局部麻醉药产生协同镇痛作用;(4)Dex经硬膜外腔脂肪吸收入血,与蓝斑核α2受体结合产生镇静作用,降低痛感等。3组术后6、48 h静息、运动及宫缩VAS评分无明显差异(P>0.05),原因可能是术后6 h还存在残余的腰硬联合麻醉作用,减轻术后疼痛,而术后24 h是宫缩痛最剧烈时刻[9- 10],到术后48 h切口疼痛及宫缩痛强度降低,3组均能产生相似的镇痛作用。
本研究还显示,E组、I组术后6、12、24 h Ramsay评分均明显优于C组(P<0.05),3组术后48 h Ramsay评分无明显差异(P>0.05),E组、I组各时间点Ramsay评分无明显差异(P>0.05),提示Dex复合地佐辛可产生良好的镇静效应,机制与各自的镇静作用有关,亦可能与二者的协同镇静作用有关,而与给药途径没有明显关系,具体机制有待进一步研究。PRL的功能主要是刺激泌乳和维持泌乳,产后24 h维持较高浓度可促进早期泌乳,提高泌乳量[11]。研究显示,切口疼痛及宫缩痛抑制泌乳功能[12],焦虑、抑郁等负性情绪亦可抑制PRL分泌等[13]。本研究表明,3组术前PRL水平无明显差异(P>0.05);术后第1、2天PRL水平比较,差异有统计学意义(P<0.04),E组、I组均高于C组,E组高于I组,提示Dex复合地佐辛可促进PRL分泌,改善泌乳功能,效果以硬膜外腔途径为佳。分析其可能的原因:(1)疼痛是抑制术后PRL分泌的主要因素,减轻疼痛可提高PRL水平[14],本研究E组、I组镇痛效果优于C组,且E组镇痛效果优于I组;(2)焦虑、紧张等影响休息,交感神经兴奋抑制PRL分泌[15],本研究E组、I组的镇静效果优于C组,有利于提高PRL水平等。由于地佐辛部分拮抗μ受体,Dex作用于胃肠道α2受体减少消化液分泌,降低胃肠动力[16],且Dex复合地佐辛镇静效果好,本研究结果也显示,E组、I组恶心、呕吐发生率低于C组。Dex胎盘滞留性高,输注24 h大部分(约85%)经尿排出,且口服生物利用度低(约16%)[17],故经乳汁进入新生儿的量极少,而地佐辛经乳汁分泌的量亦较少[18]。本研究结果显示,3组新生儿哺乳12 h神经行为评分无明显差异。本研究不足之处为缺乏最佳药物浓度的系列研究,无法获得最佳药物浓度组合,且研究样本量较小,需在后续探索中予以完善。
综上所述,Dex复合地佐辛减少剖宫产高危产妇的术后12、24 h静息、运动和宫缩VAS评分,减轻术后疼痛,改善术后6、12、24 h Ramsay评分,提高镇静水平,提高PRL水平,促进泌乳功能,降低恶心呕吐的发生,效果以硬膜外腔途径为佳,且对新生儿神经行为无明显影响。

