稳定性筛选莪术油亚微乳及体外溶血性评价
杨金兰,陈忠敏,冯丽霖,王富平
(重庆理工大学 药学与生物工程学院, 重庆 400054)
中药注射剂是中药现代化的重要产物,也是传统医药理论与现代生产工艺相结合的产物[1]。与其他传统药物剂型相比,注射剂的生物利用度更高、起效更快、疗效较好,特别是在一些危重症患者和不能口服给药患者的临床治疗中,发挥了重要的作用[2]。尽管国家对于中药注射剂的提取技术没有统一标准,同一产品在不同提取方式、不同批次、不同厂家获得指纹图谱相似性存在差异,但目前依然在临床中应用广泛,在许多疾病的治疗中发挥着重要的作用。中药注射剂常使用增溶剂提高中药有效成分的稳定性、溶解性,降低刺激性等,但其临床应用依然有限。如莪术油注射液,尽管莪术油具有抗肿瘤[3]、病原体、抗血栓、抗溃疡、抗早孕等多种作用[4],但由于其处方中主要通过吐温-80增溶[5],吐温-80会引起家兔红细胞溶血和形变,且溶血率呈浓度和时间相关性增加[6],同时有较大的刺激和过敏作用,其使用浓度和应用范围受限[7],导致莪术油注射液目前只被应用于消炎、抗病毒领域[8]。
为解决此问题,大量研究集中在用其他药用辅料替代吐温-80,如林海东在制备莪术油亚微乳注射液中,采用大豆油、精制蛋黄磷脂、油酸、伯洛沙姆(F68)为辅料,可室温下放置6个月基本稳定,以期避免原注射剂辅料所引起的副作用[9]。祁鸣[10]用大豆油、蛋黄卵磷脂、F68、油酸、维E、甘油为辅料,稳定常数Ke平均最低为58.2%,加速试验和长期留样试验结果显示稳定性良好,至少可储存12个月,体外无明显溶血作用,对兔耳静脉血管无明显不良刺激。黄尊动[11]用大豆油、中链油、F68、维E、甘油为辅料,30 ℃和40 ℃加速实验6个月后,莪术油亚微乳外观性状不发生变化,主药含量不下降,各项参数不发生变化,基本无局部刺激性、溶血性。由于大部分莪术油乳剂中常存在大豆油、甘油,在长期放置时游离脂肪酸和过氧化脂质含量会升高,导致保质期缩短,副作用增加[12],为了防止脂质氧化,通常需加入抗氧剂,但增加了安全不确定性。另外,甘油会被氧化成丙烯醛而具有刺激性。为此,本研究排除大豆油、甘油,采用泊洛沙姆188(Poloxamer 188,F68)、海藻酸钠(sodium alginate,SA)和聚乙二醇(polyethylene glycol,PEG)。其中,F68作为一种水包油乳化剂是目前用于静脉乳剂极少数合成乳化剂之一,用F68能够制备出粒径小、稳定、吸收率高的乳剂。SA可用作助乳化剂,具有药物制剂辅料所需的稳定性、溶解性、黏性和安全性。PEG可用作稳定剂,能提高难溶药物的溶解度及加强药物在水中的稳定性,将其用作修饰乳剂稳定性,用3种生物相容性良好的材料替代Tween-80对莪术油的增溶作用和稳定作用,对其市售型的莪术油亚微乳进行改性,制备一种高稳定性、低溶血风险莪术油亚微乳,为扩大莪术油亚微乳注射液临床应用提供基础依据。
1 仪器与药品试剂
1.1 仪器
D3024R台式高速微量离心机(北京科博赛尔科技有限公司)、AR1530精密电子天平(岛津企业管理(中国)有限公司)、SHX150ⅡI生化培养箱(上海树立仪器仪表有限公司)、PR-310酶标分析仪( 深圳市普康电子有限公司)、Bettersize2000智能激光粒度仪(中国辽宁省丹东市百特)、JRJ300-S型实验室剪切乳化机(上海索映仪器设备有限公司)、OS20-PRO机械搅拌器(北京科博赛尔科技有限公司)、752N紫外可见分光光度计(上海仪电分析仪器有限公司)、TU-1901紫外-可见分光光度仪(北京普析通用仪器有限责任公司)、实验室pH计(梅特勒-托利多仪器(上海)有限公司)。
1.2 药品与试剂
莪术油(吉安市青原区绿源天然香料油提炼厂)、海藻酸钠、香兰素(香草醛)、浓硫酸、聚氧乙烯脱水山梨醇单油酸酯(简称聚山梨酯-80、吐温-80)、聚乙二醇400(PEG)(成都市科龙化工试剂厂)、泊洛沙姆188(F68)(中国阿达马斯试剂)为市售分析纯,水为注射用水。
2 方法与结果
2.1 亚微乳的制备
2.1.1莪术油亚微乳剂的制备
在搅拌条件下,将F68、Tween-80、SA、PEG依次分散于注射用水中,后将莪术油缓慢滴入进行预溶,再进行高速剪切乳化(8 000 r/min,1 h),最后将莪术油亚微乳置于-20 ℃冷冻24 h,取出冷冻乳剂进行溶化即得。
2.1.2离心稳定常数(Ke)的计算
乳剂因在长期静置时稳定性变化导致分层、絮凝、合并、破乳等。将乳剂在一定转速下离心一段时间,可相当于自然静置较长时间。因此,用离心分光法测定Ke是评价乳剂稳定性常用的一种方法,Ke越小,制剂越稳定。
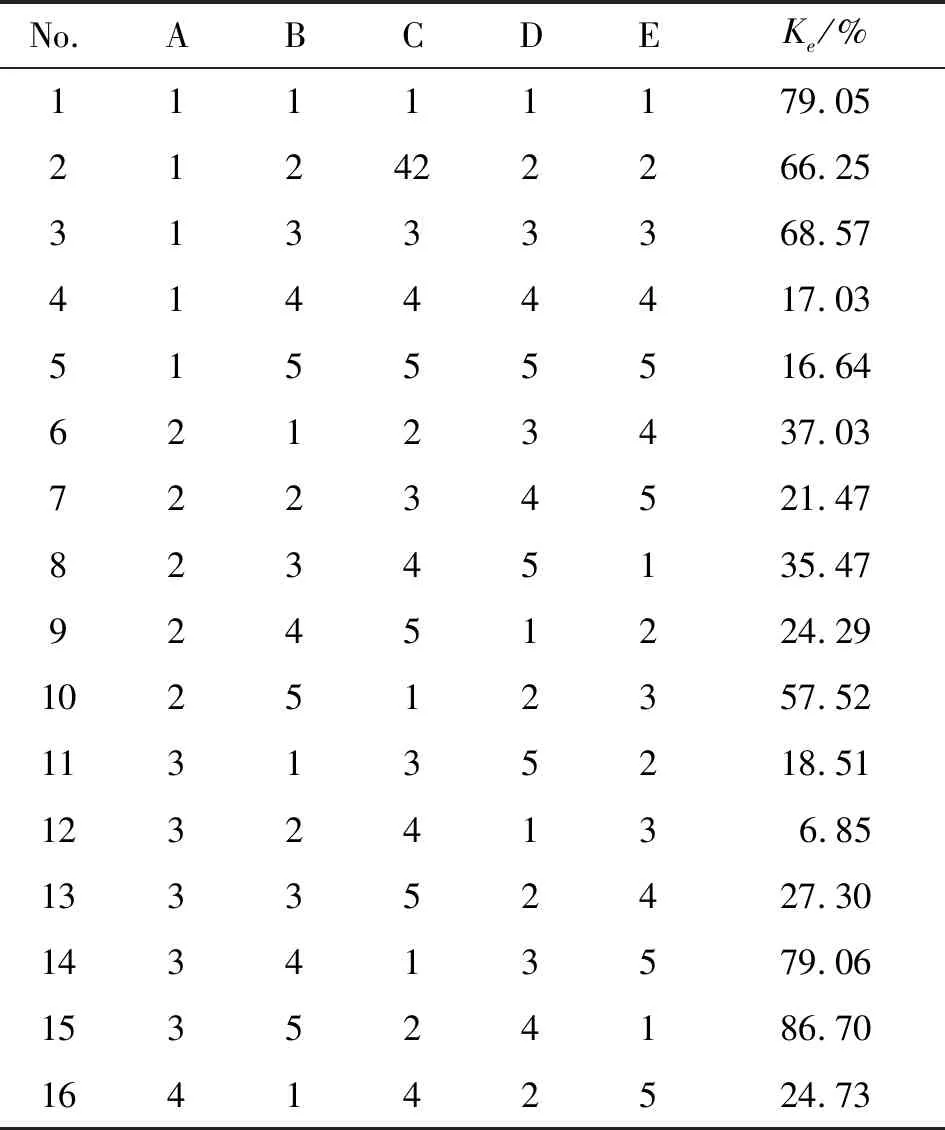
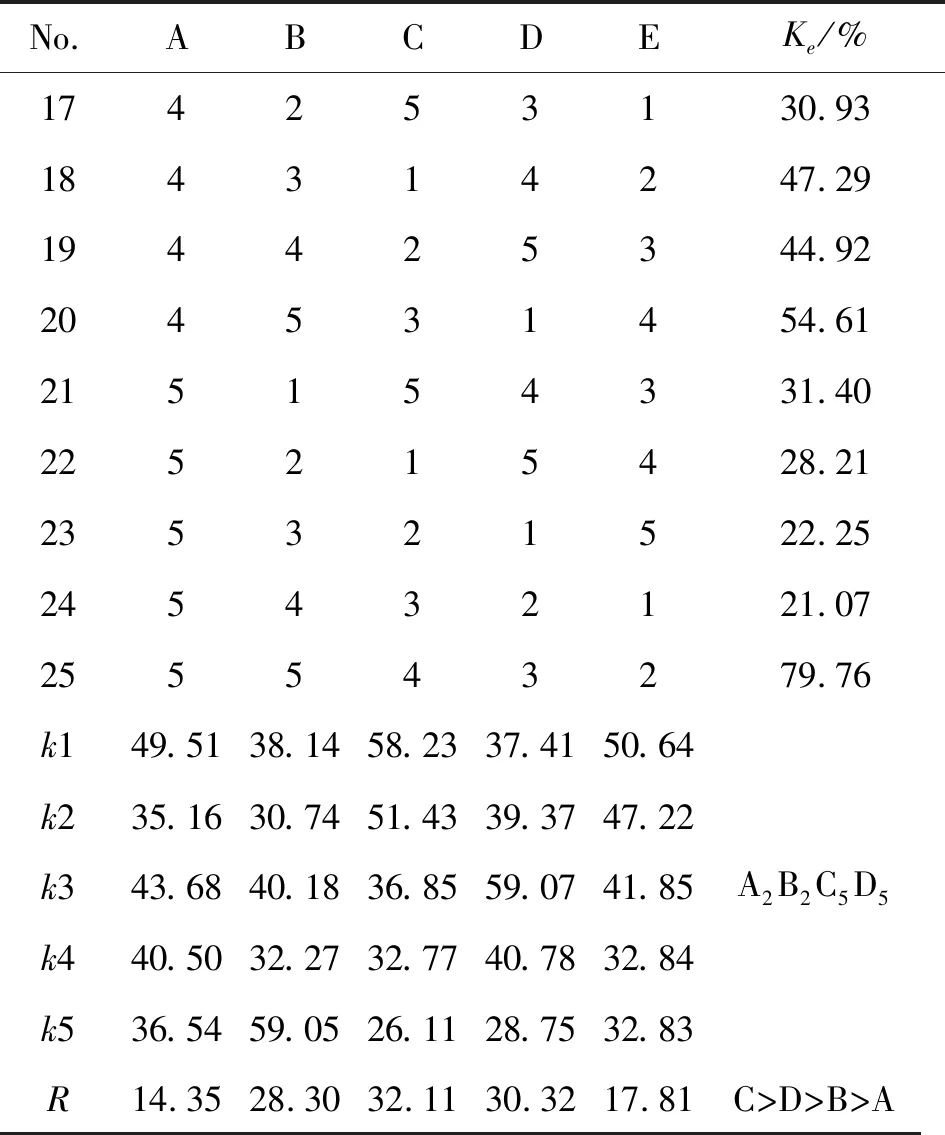
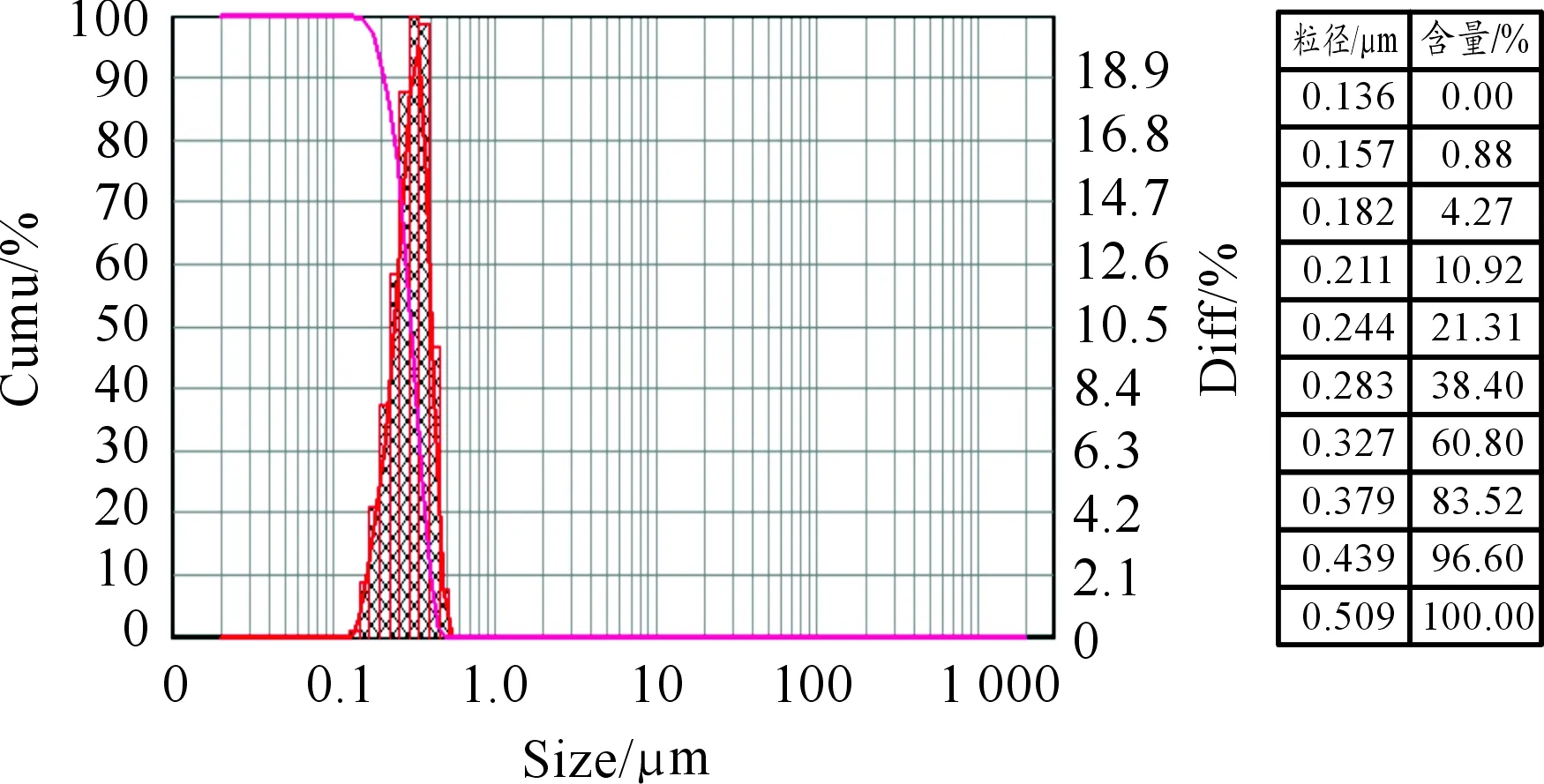
取乳剂3 mL置5 mL离心试管中,4 000 r/min离心15 min后,精密量取试管底部样品50 μL至10 mL量瓶中,用经0.22 μm微孔滤膜滤过的蒸馏水稀释至刻度,摇匀,以蒸馏水为空白,在波长500 nm处测定吸光度(A)。同法精密量取未离心乳剂样品50 μL至10 mL量瓶中,同法测定吸光度(A0),按式(1)计算Ke(0 Ke=(A0-A)/A×100% (1) 2.1.3正交试验处方优化 以单因素实验为基础,取对乳剂稳定性影响较大的辅料含量(A)、SA占辅料含量(B)、乳化剂中F68与Tween-80的比例(C)、PEG添加量(D)作为正交设计因素,以Ke为评价指标,筛选最优处方。正交试验设计的因素、水平安排见表1,用L25(55)正交表安排实验,结果见表2。 表1 正交实验安排 水平因素Aw(辅料)/%BSA占辅料的含量/%CF68:Tween-80DPEG/g10.50804∶10.0520.75703∶10.1031.00602∶10.2041.25501∶10.5051.50401∶21.00 根据表2中极差值(R)可知:各因素对亚微乳稳定性影响主次顺序是C、D、B、E、A,即乳化剂中F68与Tween-80的比例、PEG添加量、SA占辅料含量、辅料的含量的影响依次减弱。同时,通过分析正交设计表及综合因素筛选得各因素最优化组合为A2B2C5D5,最优处方为辅料含量为0.75%,其中SA占辅料含量的70%,乳化剂中F68占辅料的10%,Tween-80占辅料的20%,PEG添加量为1 g。 表2 正交实验设计 No.AB C D E Ke/%11111179.05212422266.2531333368.5741444417.0351555516.6462123437.0372234521.4782345135.4792451224.29102512357.52113135218.5112324136.85133352427.30143413579.06153524186.70164142524.73 No.AB C D E Ke/%174253130.93184314247.29194425344.92204531454.61215154331.40225215428.21235321522.25245432121.07255543279.76k149.5138.1458.2337.4150.64k235.1630.7451.4339.3747.22k343.6840.1836.8559.0741.85k440.5032.2732.7740.7832.84k536.5459.0526.1128.7532.83A2B2C5D5R14.3528.3032.1130.3217.81C>D>B>A 由于A2B2C5D5组合不在25次正交实验中,而A3B2C4D1在25组实验中稳定性高,按此2组较优处方,在固定工艺条件下制备亚微乳,平行6次,结果见表3。 表3 重复验证实验表 由表3可知:正交实验优化实验所得的单因素最优实验方案A2B2C5D5的稳定性高于正交设计实验中最优组A2B3C4D1。综合单因素实验和正交实验最优处方为辅料含量0.75%,其中SA占辅料含量的70%,乳化剂中F68占辅料的10%,Tween-80占辅料的20%,即莪术油∶SA∶Tween-80∶F68∶PEG=10∶21 ∶6 ∶3 ∶10。其中,本处方莪术油亚微乳中Tween-80所加含量为0.15%,占所用辅料的20%。 将最优处方制备的莪术油亚微乳用粒度分析仪测定其粒径大小分布,对莪术油亚微乳粒径大小进行统计,评价莪术油亚微乳粒径的均一度。结果如图1所示,莪术油亚微乳的粒径范围在0.136~0.509 μm,其平均粒径大小为0.306 μm,97%的粒径小于0.443 μm,面积平均径D[3,2]=0.288 μm,D(4,3)=D50=0.306 μm,显示D(3,2)和D(4,3)结果接近,样品颗粒的形状规则,呈圆球型,并且粒度分布集中。 按中国药典2010年版二部采用紫外-可见分光光度法测定莪术油的含量[15],再以乙醇与香草醛显色反应后为对照组,如图2所示莪术油亚微乳、莪术油与香草醛显色反应后在442 nm处呈最大吸收峰,空白亚微乳在此无吸收峰,说明辅料在此波长时对莪术油检测无明显干扰。 图1 莪术油亚微乳粒径分布 图2 方法专属性考察 配制95.3 μg/mL的莪术油乙醇溶液作为标准液,分别吸取1、0.8、0.6、0.4、0.2 mL于10 mL容量瓶中,同时用1 mL的无水乙醇为空白对照,用新配制的0.2%香草醛硫酸溶液定容,将定容好的溶液避光静置2 h后在波长为442 nm进行分光光度法测定,记录A值,在1.906~9.53 μg/mL莪术醇浓度范围内,得标准曲线方程:C=108.239 6A-5.712 1,R=0.999 8(其中A吸光度,C代表浓度)。 取亚微乳样品制成供试品溶液进行香草醛显色,经测定A442=0.255±0.004,代入标准方程得载药量为2.188 9±0.043 g·L-1。 2.4.1稀释稳定性 亚微乳剂在临床上通常以5%的葡萄糖注射液和0.9%的NaCl生理盐水稀释,因此考察本品在二者中稀释后的物理稳定性。方法:将莪术油亚微乳剂样品与5%葡萄糖注射液和0.9%的NaCl生理盐水按l∶25分别配伍,室温放置,于0、2、4、8、16和24 h后观察外观,测定其pH值及平均粒径,结果如图3、4所示,pH值无明显变化,但在生理盐水稀释条件放置,乳剂粒径变化显著,说明用5%葡萄糖注射液稀释所得乳剂稳定性较好。 图3 稀释后pH值变化 图4 稀释后平均粒径变化 2.4.2长期稳定性 在试验期间,分别于第3、6、9、12个月末取样1次,对莪术油亚微乳的稳定性常数、pH值、平均粒径、药物含量进行测定,结果如表4所示。在亚微乳外观无分层漂油现象,为乳白色半透明色,与0月状态比较无明显差别,pH值、离心稳定常数、药物含量无明显变化,稳定性良好,有效期至少1年,从而验证高速离心法可代替加速实验完成乳剂稳定性的检测。 表4 长期稳定性测定结果 时间外观 Ke/%pH值平均粒径/nm药物含量/(g·L-1)RSD/%3月乳白色,半透明 5.197.153082.116月乳白色,半透明5.307.153102.089月乳白色,半透明5.557.163112.0512月乳白色,半透明5.607.183232.000.19 按照《中国药典》2010年版2部附录的紫外分光光度测定溶血率法对莪术油亚微乳进行体外溶血评价。依照表5将生理盐水/蒸馏水/莪术油亚微乳/市售型莪术油注射液于含2%的红细胞混悬液的试管中,充分混匀后置37 ℃生化培养箱中。4 h后移至离心管,1 000 r/min离心5 min,取200 μL上清液与96孔板中,设置4个复孔,用540 nm波长测定各组样品的OD值,计算平均值,根据计算结果按照公式(2)计算溶血率[16-17]。 溶血率(%)=(Dt-Dnc)/(Dnc-Dpc)×100% (2) 其中:Dt为实验组莪术油亚微乳样品的吸光值;Dnc为阴性对照组生理盐水样品的吸光值;Dpc为阳性对照组蒸馏水样品的吸光值。 溶血性试验是常用的一种检测注射剂安全性的最基本的方法,可考查到注射剂在血液中的溶血性。通过紫外分光光度测定的溶血率法结果如图4显示。莪术油亚微乳溶血率随着浓度的增加而升高,在莪术油浓度达到0.024 g·L-1后,无明显变化,维持在1.4%左右,最大为1.47%,在试验浓度范围内远远小于安全阈值5%,符合国家标准[18]。而市售型莪术油注射液浓度大于0.024 g·L-1后溶血率出现剧增且超过5%,显示市售型莪术油注射液在浓度较高时具有较大的溶血风险。 表5 溶血实验安排 图5 溶血率随浓度的变化 亚微乳作为注射剂必须具有必要的物理稳定性和化学稳定性,以确保产品在贮存期安全、有效,然而亚微乳又是属于热力学不稳定的一种非均相分散体系,会受到乳化剂用量,乳化时间、温度等影响,因稳定性改变,而在储存过程中出现分层、破乳、析油等现象,因此亚微乳的稳定性考察是制备亚微乳的一个重要指标。本实验稳定性的测定选择离心分光法,高速离心增加了乳滴之间的碰撞几率,可以在短时间模拟乳剂长时间存放过程中乳滴之间的碰撞、合并的结果,在一定程度上等同于长期存储,从而提高了实验效率。 本实验在单因素实验基础上通过正交试验筛选莪术油亚微乳制备最佳处方,制备出的亚微乳稳定常数达到(5.42±0.47)%,且重复性高,远远低于已有文献报道的莪术油亚微乳(稳定常数Ke平均最低为58.2%)[10],表明在相同的储存时间内,本处方莪术油亚微乳稳定性应更高,原因可能是由于本研究选择SA、F68作为乳化剂和助乳化剂,让SA与F68两者在油水界面产生了稳定的乳化膜,且F68可在小油滴周围形成空间立体屏障,增加液滴表面的亲水性,避免莪术油吸附在乳滴表面。F68,SA可提高乳化效果,莪术油的油水表面张力得到缓解和释放,提高了稳定性[21],同时PEG可增加溶液的稳定性作用。 本处方制备的亚微乳粒径分布在0.136~0.509 μm之间,属于亚微米级,粒径分布窄且连续,颗粒的形状规则,呈圆球型。有研究表明:亚微乳剂的稳定性与粒径及其分布有关,粒径越小、粒径分布越窄,亚微乳剂越稳定[22]。原因可能在于本处方选择SA作为包裹莪术油的主要成分,SA插入乳化剂F68和吐温-80的界面膜中,形成复合凝聚膜,提高了牢固性和柔顺性,促进曲率半径很小的膜形成,增大了乳化剂的溶解度,降低界面张力,以致在高速乳化切割时,能形成粒径大小均一乳剂。 本处方莪术油浓度为(2.188 9±0.43) g·L-1是市售型莪术油注射液(浓度为0.4 g·L-1)的5倍左右。尽管文献[9]制备的纳米乳剂粒径为(76.5±10.1) nm,然而其浓度(1.76±0.09) g·L-1与本处方相近,低于祁鸣[10]的莪术油亚微乳浓度(10 g·L-1),原因在于其辅料用量质量分数达到13.83%,远高于本处方(0.75%),辅料与莪术油的之比达到13.83∶1,而本处方此比例仅为3∶1,单位质量辅料包裹莪术油量更大。 本处方用F68/SA/PEG替换80%的吐温-80以后,在试验条件下显著降低了由吐温-80引起的溶血率急剧增加的风险,且即使继续提高浓度,溶血风险也能控制在安全范围内。这可能与处方中的具有良好血液相容性的SA、F68、PEG对含量较少的吐温-80起到了遮蔽作用有关,使其无法大量接触红细胞,还有可能在亚微乳乳滴表面被柔顺而亲水的PEG链覆盖,提高亚微乳膜的亲水性,降低表面自由能,使表面自由能降低到接近血管内膜的表面自由能值,降低溶血风险。正常人体血管壁内皮细胞的电位值为负,血液中的红细胞、白细胞及血小板等均带负电荷,因此不易发生粘附[23]。SA在水溶液中可表现出聚阴离子行为,使亚微乳膜表面带负电,从而减少血栓的形成,提高了血液相容性。 本研究筛选制备莪术油亚微乳的最佳处方具有较高的稳定性和载药量。本处方莪术油亚微乳从稳定性、pH值、粒径、溶血性方面符合国家中药亚微乳注射液的标准要求,且在较高浓度下风险可控,为扩大其在临床应用提供基础依据,同时也可为其他中药注射液的制备提供参考。

2.2 亚微乳乳剂粒径大小分布测定
2.3 亚微乳剂含量测定
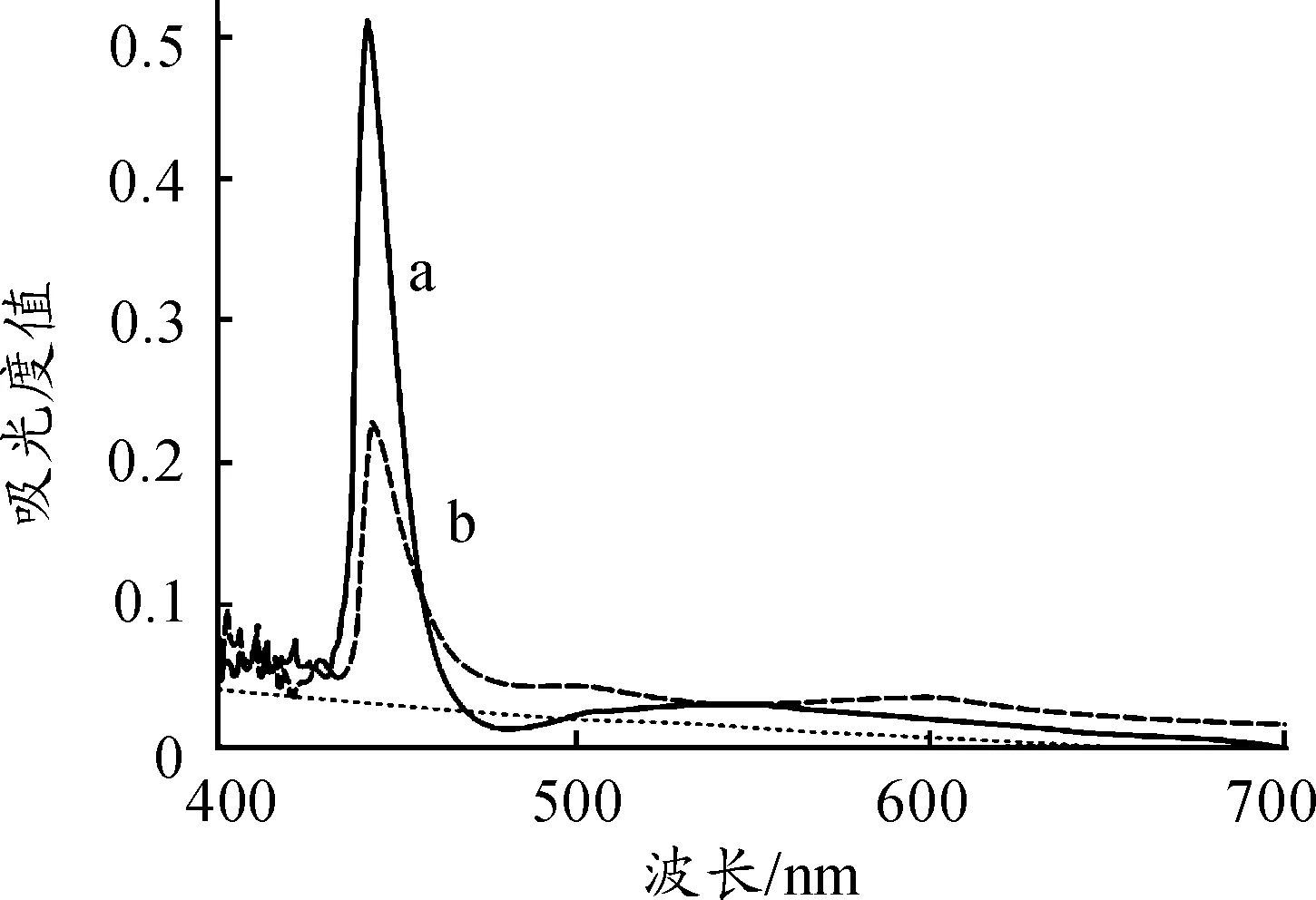
2.4 亚微乳剂稳定性验证
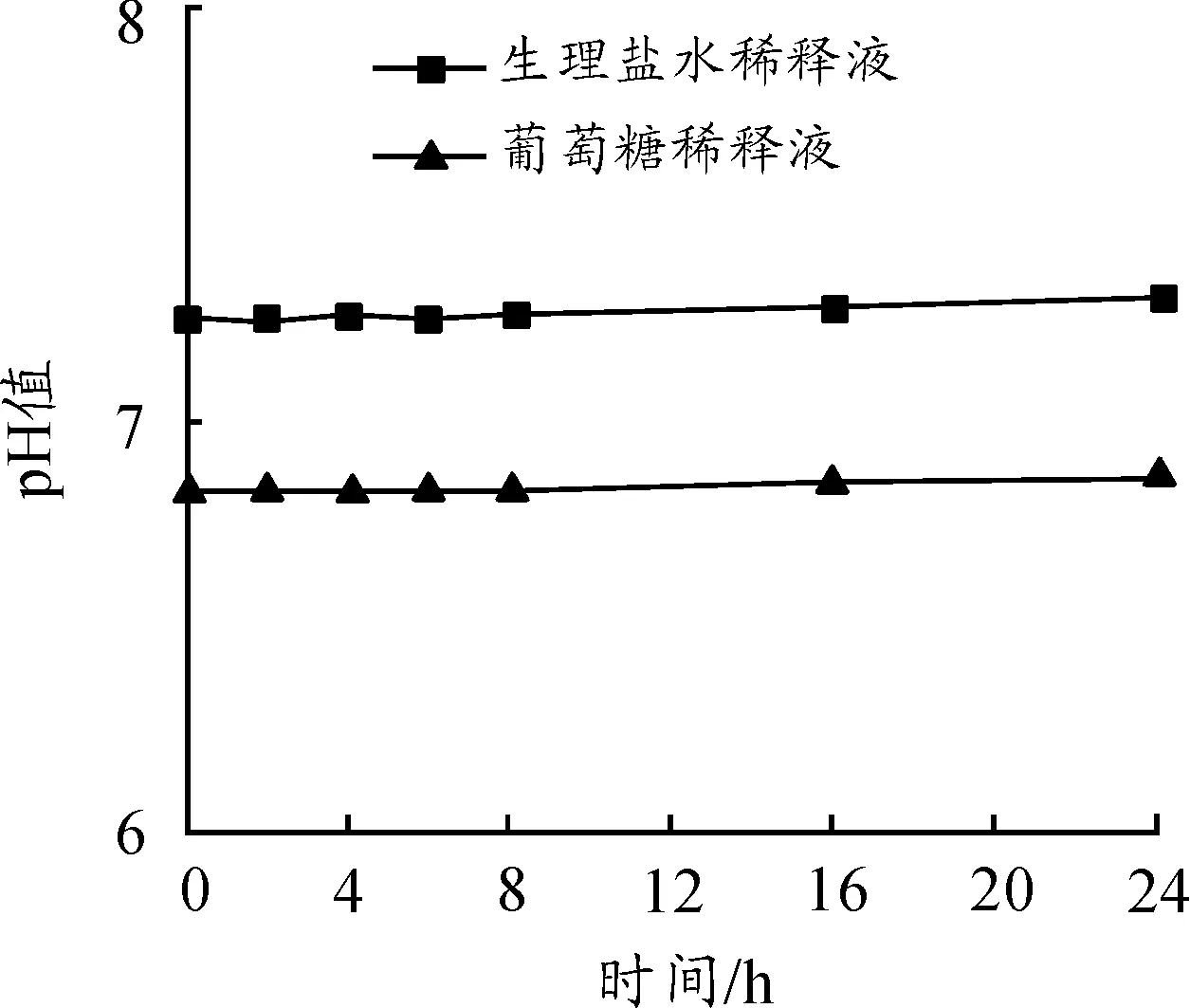

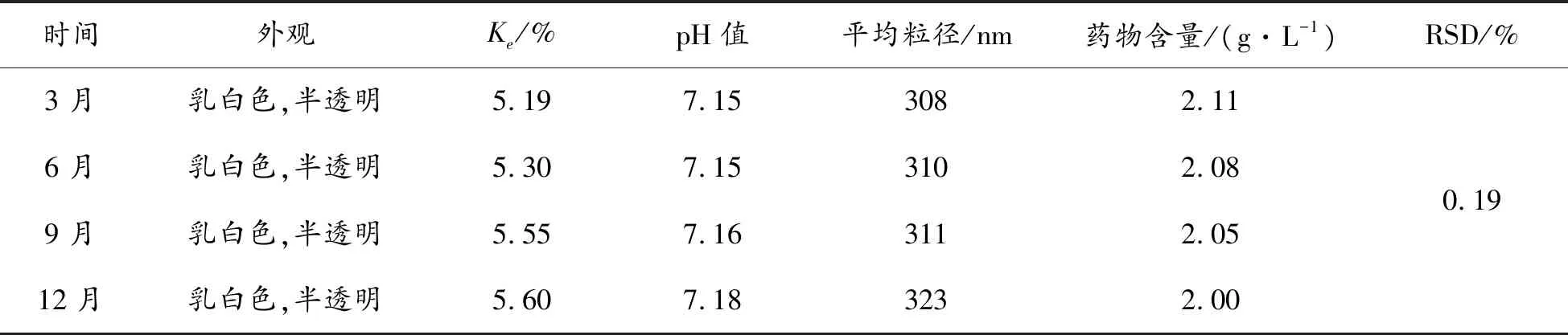
2.5 亚微乳体外溶血性评价
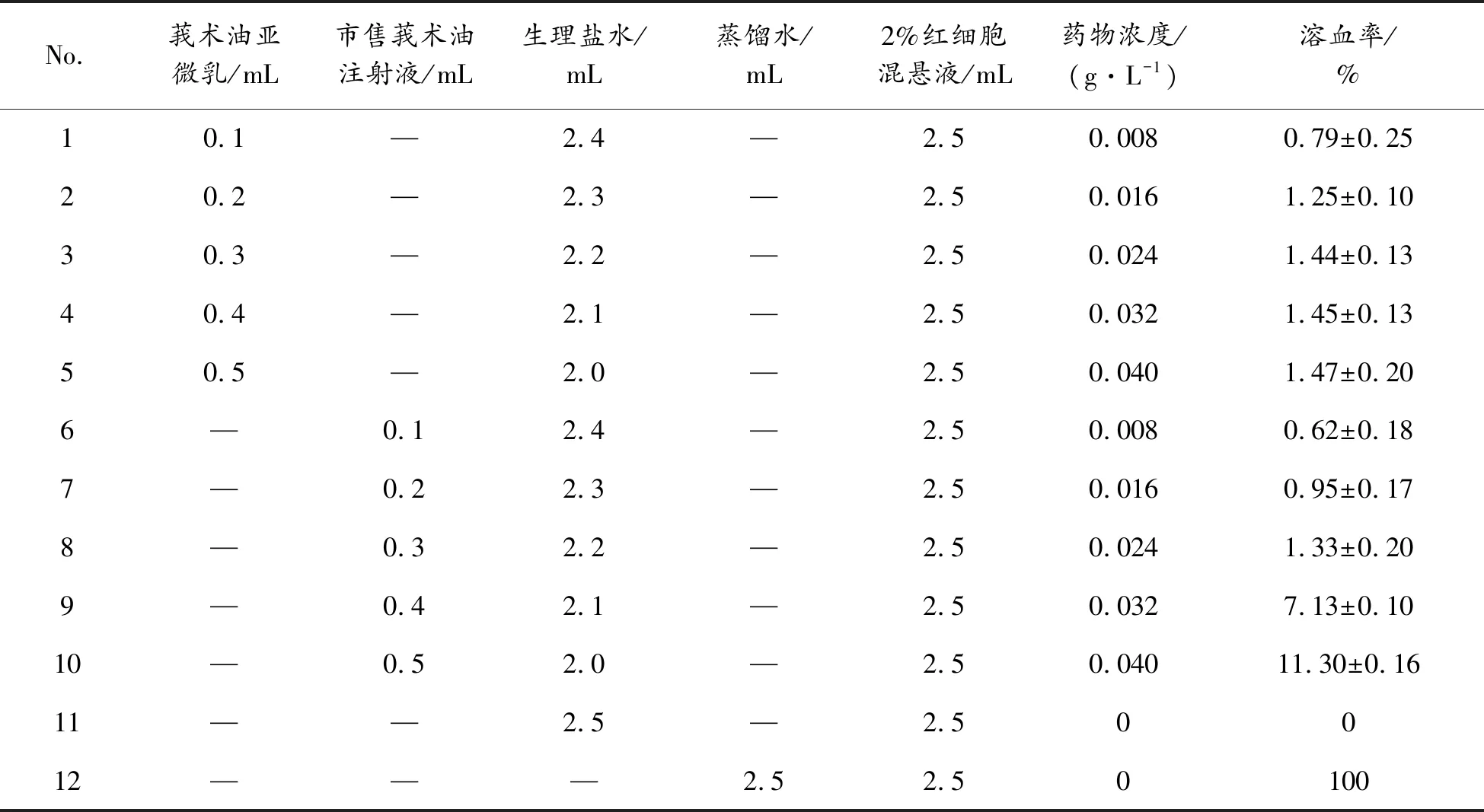

3 讨论
4 结束语

