康柏西普辅助玻璃体切除治疗PDR及对炎症因子及ANGPTL4的影响
程四华,童巧珍,赵 艳,卓 晓
0引言
糖尿病是一种常见的代谢性疾病,据统计,直至2015年,全球糖尿病患病人数达4.15亿,预计到2040年将达到6.42亿[1]。我国是糖尿病患病人数最多的国家,患病人数达到1.09亿,且随着人口老龄化的加剧,患病人数将继续增长。增生型糖尿病视网膜病变(proliferative diabetic retinopathy,PDR)是一种由糖尿病引发的严重并发症,病理改变为血管代谢微循环障碍,严重影响患者的视力,甚至出现失明等现象[2-3]。据统计,1型糖尿病患者几乎全部出现眼部并发症,2型糖尿病患者中,病程超过20a的患者出现视网膜病变的几率超过60%[4]。因此,寻找治疗PDR的合理方法具有显著的临床价值。玻璃体切除术(pars plana vitrectomy,PPV)是治疗PDR的有效手段,其通过剥离新生血管,清除玻璃体内的积血,消除视网膜显微血管膜的牵拉,从而达到改善视网膜的缺血,促进视力恢复的作用[5-6]。但是由于PDR患者新生血管膜、视网膜前增殖膜与视网膜的连接较为紧密,剥离困难,常常在手术过程中出现出血及医源性裂孔等症状[7]。康柏西普(conbercept)是一种抗血管内皮生长(vascular endothelial growth factor,VEGF)的药物,能够显著抑制DR患者新生血管的生长,并促进纤维组织萎缩,从而减少术中出血等情况的发生[8]。因此,本研究选取2016-01/2018-12我院收治的行PPV治疗的PDR患者90例99眼作为研究对象,探究玻璃体内注射康柏西普辅助PPV治疗PDR的临床效果,现汇报如下。
1对象和方法
1.1对象选取2016-01/2018-12我院收治的行PPV治疗的PDR患者90例99眼作为研究对象。根据是否采用玻璃体内注射康柏西普(intravitreal conbercept,IVC)将患者分为PPV组和IVC辅助PPV组。PPV组患者46例50眼,其中男30例32眼,女16例18眼;年龄41~79(平均57.46±6.39)岁;按照糖尿病视网膜病变临床分期的相关标准,Ⅳ期患者28例32眼,Ⅴ期患者10例10眼,Ⅵ期患者8例8眼;术前平均眼压13.05±3.58mmHg。IVC辅助PPV组患者44例49眼,其中男26例30眼,女18例19眼;年龄43~77(平均58.46±7.10)岁;按照糖尿病视网膜病变临床分期的相关标准,Ⅳ期患者27例30眼,Ⅴ期患者11例12眼,Ⅵ期患者6例7眼;术前平均眼压13.28±3.52mmHg。两组患者在性别、年龄、临床分期及眼压等一般临床资料的比较上均无统计学意义(P>0.05),具有可比性。本研究通过我院伦理委员会审核,且所有患者均签署知情同意书。
1.1.1纳入标准(1)所有患者临床指标及功能检测等符合我国糖尿病视网膜病变的相关标准;(2)增生膜样组织新生血管旺盛导致牵引性视网膜脱落,出现黄斑或伴有视网膜前出血或玻璃体积血;(3)眼底镜检查可窥入。
1.1.2排除标准(1)晶状体严重混浊,影响手术,需进行晶状体超声乳化吸除手术的患者;(2)具有眼科手术史的患者;(3)既往向玻璃体内注射过康柏西普或其他抗VEGF药物的患者;(4)合并严重的其他疾病,如肝肾功能严重不良、脑血管疾病等;(5)具有手术禁忌证的患者。
1.2方法
1.2.1治疗方法收集两组患者的一般临床资料、病史资料并进行详尽的眼科检查及体质检查,合并其他基础疾病的患者,进行基础疾病治疗,如高血糖患者控制空腹血糖水平在7.8mmol/L以下,高血压患者控制收缩压在140mmHg以下。
玻璃体内注射康柏西普方法:患者术前眼部滴加抗生素,行仰卧位,采用内眼手术常规消毒铺巾,表面麻醉后,对结膜囊行聚维酮碘冲洗。康柏西普(成都康弘生物科技有限公司生产,国药准字S20130012,规格10mg/mL)自带注射针于颞上角膜缘后3.5mm睫状体的扁平处平坦进针,向玻璃体内注射0.05mL。注射过程中使用消毒棉签按压穿刺口,避免药物溢出。术后观察是否有出血,采用抗生素滴眼液防治感染。
PPV手术:两组患者的手术均由我院一名经验丰富的医生完成,患者入院后行血常规及眼部检查,由眼科医生、神经外科医生等组成小组,进行会诊,根据患者情况确定手术时间,术前3~5d康柏西普注射。托吡卡胺滴眼液散瞳,20g/L利多卡因和布比卡因等量混合,进行球后麻醉。采用白内障超声乳化玻璃体切割一体机进行手术,对角膜缘后4.0mm左右处的结膜以23G穿刺刀斜行穿刺,将套管针置入到睫状体扁平部,切割轴心部玻璃体,切除范围为中央区、基底部玻璃体及周边部,切速控制在3600~3900r/min,负压为360~400mmHg。术中清除玻璃体积血,将玻璃体剥离后注入少量曲安奈德。如果患者的视网膜前增殖膜与视盘或视网膜紧密相连,对两者之间的粘连进行钝性分离,松解视网膜的牵拉,复位视网膜。532nm眼底激光对视网膜进行广泛光凝,黄斑区和颞侧上下血管弓范围不进行光凝。玻璃体切除后如发现新生血管或血管壁残端出血,等待其自主凝血,如果仍反复出血则采用23G眼内双极电凝血管进行止血。如果视网膜牵拉严重或视网膜出现变性、裂孔,气液交换后进行硅油或C3F8填充。所有操作结束后用8-0尼龙线缝合切口。
1.2.2观察指标(1)观察两组患者的手术指标,包括手术时间、术中出现严重出血(需用电凝笔的出血)、医源性视网膜裂孔及术后硅油填充的几率;(2)术后随访3mo,对两组患者进行最佳矫正视力(BCVA)及眼底检查并进行比较,其中BCVA采用LogMAR视力表示。如果患者发现玻璃体恢复透明之后再次出现玻璃体内血性混浊则定义为PPV术后玻璃体内积血(POVCH),等级分为3级:轻度:眼底结构细节能够清晰观察到,且视网膜前>3PD,玻璃体出现轻度血性混浊;中度:眼底结构细节能够被观测但不清晰,仅视盘或大血管轮廓可见;重度:POVCH表现为玻璃体内出现显著血性混浊,伴有前房积血,眼底情况无法观测到;(3)采用酶联免疫吸附法(ELISA)测定两组患者玻璃体中白介素-6(IL-6)、白介素-10(IL-10)及C反应蛋白(CRP)等炎症因子的含量;同样采用ELISA法测定两组患者玻璃体中血管生成素样蛋白4(ANGPTL4)的含量。
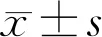
表1 两组患者手术指标比较眼

组别眼数手术时间(x±s,min)术中出现严重出血(眼,%)医源性视网膜裂孔(眼,%)术后硅油填充(眼,%)PPV组5098.25±12.2514(28)16(32)20(40)IVC辅助PPV组4960.58±10.843(6)6(12)10(20) t/χ216.1908.3285.5884.498P<0.010.0040.0180.034


组别眼数术前术后1mo术后3moPPV组501.02±0.030.41±0.080.34±0.08IVC辅助PPV组491.01±0.070.35±0.090.22±0.04t0.9273.5089.410P0.356<0.001<0.001
表3 两组患者术后3mo POVCH情况比较眼(%)

组别眼数发生率轻度中度重度PPV组5021(42)16(32)3(6)2(4)IVC辅助PPV组4911(22)9(18)2(4)0 χ2/Z4.3241.147P0.0380.056
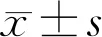

组别眼数IL-6(ng/L)IL-10(ng/L)CRP(mg/L)ANGPTL4(ng/mL)PPV组5036.97±8.7918.79±6.4113.45±3.7428.69±5.14IVC辅助PPV组4932.14±6.8413.74±5.6710.47±2.5530.85±4.57 t3.0474.1494.6232.208P<0.01<0.01<0.01<0.01
2结果
2.1两组患者手术指标比较与PPV组患者相比,IVC辅助PPV组患者的手术时间显著缩短,术中出现严重出血(需用电凝笔的出血)、医源性视网膜裂孔及术后硅油填充的几率显著缩短,差异均有统计学意义(P<0.05),见表1。
2.2两组患者术前及术后BCVA比较两组患者术前及术后不同时间BCVA比较,差异有统计学意义(P<0.05)。两组患者术前BCVA相比,差异无统计学意义(t=0.927,P=0.356);与手术前相比,两组患者术后BCVA值显著降低, 差异均有统计学意义(PPV组:t术后1mo=33.517,P术后1mo<0.001;t术后3mo=35.470,P术后3mo<0.001;IVC辅助PPV组:t术后1mo=42.017,P术后1mo<0.001;t术后3mo=47.221,P术后3mo<0.001);且与PPV组患者相比,IVC辅助PPV组患者术后1、3mo BCVA值显著降低, 差异均有统计学意义(P<0.001),见表2。
2.3两组患者术后3mo POVCH情况比较与PPV组患者相比,IVC辅助PPV组患者术后3mo POVCH的发生率显著降低(P<0.05),但两组患者POVCH的严重程度相比,差异无统计学意义(P>0.05),见表3。
2.4两组患者玻璃体中炎症因子及ANGPTL4含量比较与PPV组患者相比,IVC辅助PPV组患者玻璃体中IL-6、IL-10及CRP的含量显著降低,差异均有统计学意义(P<0.01),ANGPTL4含量显著升高,差异有统计学意义(P<0.01),见表4。
3讨论
通过临床观测显示,PDR患者主要表现为玻璃体出血、牵拉性视网膜脱离及增生膜样组织,主要治疗方法为玻璃体切除术,但由于患者增生膜样组织与视网膜之间的空隙较小,连接紧密,大大增加了手术难度,并易导致医源性裂孔等并发症的发生[9]。除此之外,手术过程中新生血管出血也是常见并发症之一,需要采用电凝止血的严重出血不仅影响手术进程,而且会增加机械损伤[10]。大量研究表明VEGF是PDR发生发展的关键因子之一,也是促进新生血管生长的必要因素[11],因此,阻断VEGF的产生对于减少PDR患者新生血管的生长等具有重要意义。
康柏西普是我国首个获得世界卫生组织国际通用名的拥有全自主知识产权的生物I类新药。是新一代的抗VEGF融合蛋白,能够显著抑制病理性的血管生长。与其他抗VEGF药物相比,康柏西普具有半衰期长、亲和力高及作用靶点多的优点,被广泛应用于临床。韩姬等的研究显示,对糖尿病视网膜病变患者采用玻璃体腔注射康柏西普治疗,能够显著改善视网膜病变,促进视力恢复[12];邢凯等[13]研究分析玻璃体腔内注射康柏西普治疗视网膜分支静脉阻塞继发黄斑水肿的临床疗效,结果显示,基于光学相干断层扫描技术采用玻璃体腔内注射康柏西普,能够显著改善患者的视力,且安全性良好。国外的研究[14]也显示,新生血管性年龄相关性黄斑变性患者采用康柏西普治疗能够显著延长治疗间隔,促进最佳矫正视力的改善。本研究采用PPV术前玻璃体注射康柏西普治疗PDR,结果显示,术前玻璃体注射康柏西普能够显著缩短手术时间,减少术中严重出血、医源性视网膜裂孔及术后硅油填充的发生率,并能够显著改善术后BCVA,减少POVCH的发生率, 以上结论与以前的研究结果相似,充分显示出PPV术前玻璃体注射康柏西普治疗PDR的优势。为了探究PPV术前玻璃体注射康柏西普治疗PDR疗效的机制,本研究从炎症及血管生成两方面进行探究。
PDR患者眼内病理状态,势必造成眼部慢性炎症的发生,炎症反应能够促进巨噬细胞等反应细胞分泌促炎介质,吞噬受损部分的细胞及组织,起到损伤的调控作用。但如果这种炎症反应得不到及时控制,则会对正常组织产生毒害作用,加速疾病进程[15-16]。IL-6及IL-10是两种主要的促炎介质,参与炎症的发生发展;CRP是一种主要的急性时相反应蛋白,大量研究表明,其在炎症发生时含量显著升高。刘珍容等[17]的研究探究2型糖尿病增生性视网膜病变患者血清中IL-6、IL-10及CRP的水平,结果显示只有IL-6的水平显著升高。徐芳[18]的研究提示,2型糖尿病视网膜病变患者血清炎症因子水平显著升高,且与血清氧化水平存在一定的相关性。本研究结果显示,与PPV组患者相比,IVC辅助PPV组患者玻璃体中IL-6、IL-10及CRP的含量显著降低,但未与正常对照组患者进行比较,在以后的研究中可以进行探究。究其原因,可能是因为玻璃体是直接病变部位,炎症反应相对于血清来说更加剧烈,炎症因子水平显著升高。ANGPTL4是血管生成素样蛋白家族中的一员,在细胞凋亡、血管生成及机体代谢中发挥重要作用,在糖尿病的发生发展中起重要作用。近年来,有报道显示,ANGPTL4与PDR的形成有关,此结果提示,PPV术前玻璃体注射康柏西普能够一定程度上改善PDR患者玻璃体中ANGPTL4含量的缺失。
综上所述,PPV术前玻璃体注射康柏西普治疗PDR,能够减少术中及术后并发症的发生,促进患者视力的康复,并减轻玻璃体中炎症反应,增加ANGPTL4的含量。

