锌在生物磷灰石中的晶体化学研究进展
程 潇,王长秋,王 卉
(1. 造山带与地壳演化教育部重点实验室, 矿物环境功能北京重点实验室, 北京大学地球与空间科学学院, 北京 100871;2. 北京经济管理职业学院 珠宝与艺术设计学院, 北京 100102)
与纯磷灰石相比,作为构成脊椎动物硬组织的主要无机相,生物磷灰石存在结晶度低、非化学计量性和热稳定性差的特点(Legeros and Legeros, 1984; Bigietal., 1992)。人们熟知的骨和牙齿,其主要无机成分为羟基磷灰石(HAP)(秦善等, 2008; 张爱娟, 2009; 崔福斋, 2012)。肾结石患者的肾乳头尖部常见一种被称作Randall ’s plaque(RP)的斑块,该斑块被认为是肾结石形成的一个初始点和滞留点,其主要无机成分亦为HAP(Randall, 1944; Evanetal., 2006)。实际上,人体几种常见肿瘤(乳腺癌、甲状腺癌、卵巢癌、脑膜瘤)等中常伴有一定的微钙化,钙化的最常见物相也为HAP(Frappartetal., 1986; Hakaetal., 2002; 杨若晨等, 2008; 赵文雯等, 2009; 王长秋等, 2011; 熊翠娥等, 2011a, 2011b; 孟繁露等, 2015)。上述生物磷灰石中常常可以检测到Zn元素的存在(Beattie and Avenell, 1992; Tvinnereimetal., 1999; 崔福斋, 2012; 孟繁露等, 2013b, 2015),且浓度高于100×10-6(马丽英, 1998; Merlinetal., 2012)。
在生物医学材料领域,HAP因具有良好的生物相容性、生物活性,能与人体骨骼组织形成化学键结合等,而被人工大量合成并广泛应用于整形外科和牙科领域(Suchapnek and Yoshimura, 1998; Sanoshetal., 2009),还可进一步制成性能优良的HAP陶瓷和骨组织工程支架材料等(Itoetal., 2000; Tampierietal., 2001; 张爱娟,2009; Zhangetal., 2018)。为了满足临床应用的需要,常需在HAP中添加一些元素以改善其性能,含Zn羟基磷灰石(Zn-HAP)就是其中非常重要的一类改性材料,且有望成为新一代的骨修复和替换材料(李明鸥等,2008,2009; Zhangetal., 2018)。研究报道的合成Zn-HAP中Zn2+替代上限存在一定差异,摩尔分数为15%~25%(Bigietal., 1995; Miyajietal., 2005; Tangetal., 2009; Renetal., 2009)。
Zn在地壳中的丰度不足100×10-6,且Zn和Ca的离子半径相差较大,地质条件下不易发生Zn2+对磷灰石中Ca2+的替代(陈振宇等, 2009),因此,生物磷灰石中的Ca位替换具有特殊性,传统的磷灰石类质同像替换理论对其Ca位替换并不完全适用。近年来,由于人体病理性钙化及生物医学材料的研究需求,Zn在HAP中的存在及其晶体化学行为引起了广泛关注(孟繁露等,2013b,2015;Zhangetal., 2018)。
生物磷灰石的新陈代谢和/或物理化学行为与其所含离子的空间配位密切相关,Zn占据Ca的位置,会对其晶体结构、结晶度和物理化学性质等造成一定影响(Legerosetal., 1999; Miyajietal., 2005; Hayakawaetal., 2007),因此了解Zn掺入HAP的具体机制以及Zn在生物磷灰石中的晶体化学行为非常重要。HAP结构中存在适合于Zn取代的两个不同的阳离子位点Ca1和Ca2(Tangetal., 2009; Matsunagaetal., 2010),尽管目前有广泛的研究集中在Zn-HAP上,但结果和数据相当不一致(Barreaetal., 2001; Hayakawaetal., 2007; Tangetal., 2009; Matsunagaetal., 2010),HAP中Zn的掺入模式,尤其是结合位点及其局部结构仍不确定。本文综述了国内外关于生物磷灰石中Zn的存在状况、Zn对Ca的替代机制及Zn替代对生物磷灰石的影响等方面的研究进展与现状,并讨论了Zn在生物磷灰石中的晶体化学研究对人体肿瘤诊疗的启示作用。
1 传统的磷灰石类质同像替换理论
羟基磷灰石(HAP),理想化学式为Ca5[PO4]3(OH),属于一类孔道结构矿物,可以发生多种阴阳离子替代。关于磷灰石的类质同像替代问题,刘羽等(2003)进行过较为详尽的综述:在Ca位上存在两种不同的阳离子位置: 相对较大的Ca1位和较小的Ca2位,多种不同类型、不同半径的金属离子可以进入这两种结构位置,除了2价的Sr2+、Mn2+、Fe2+、Ba2+等外,还经常出现Ce3+、La3+、Nd3+、Sm3+、Y3+等3价稀土元素离子和Na+等1价金属离子。关于Zn2+替代的报道少见,仅有陈振宇等(2006)对中国大陆科学钻探(CCSD)榴辉岩中磷灰石的研究表明,磷灰石中含有微量的Zn。
普遍认为,晶体中类质同像的形成必须具备以下条件:相互替代的原子(离子)大小相近、离子化合物的电价总和平衡、相似的化学键性、适当的热力学条件。晶体化学上,Zn3+与Ca3+属于不同离子类型,前者为铜型离子,后者为惰性气体型离子;Zn3+和Ca3+的半径相差较大,分别为0.074 nm和0.099 nm,理论上两者不易互相取代,地质作用中通常只在高温条件下才能形成有限的类质同像替代(陈振宇等, 2009),加之Zn在地壳中的丰度不足100×10-6,因此Zn在HAP中的存在往往被忽视。
2 Zn在生物磷灰石中广泛存在
在通常不足40℃的人体体温的低温条件下,Zn富集于骨骼(Murray and Messer, 1981)和牙齿(Tvinnereimetal., 1999; Milaimetal., 2018)以及潜在的病理性钙化(Carpentieretal., 2011; Merlinetal., 2012; 孟繁露等, 2013b)中。Zn广泛存在于骨骼中,质量分数为0.0126%~0.0217%(Beattie and Avenell, 1992),可以刺激动物骨的发育和矿化(Yamaguchietal., 1987)。牙齿被发现含有一定量的Zn,且被用作环境暴露的指示剂(Tvinnereimetal.,1999),Takatsuka等(2005)通过实验验证了ZnO对牙本质脱矿的抑制作用,Zn亦被证明对硬牙组织的矿化和成熟及对减少龋病有积极意义(Milaimetal., 2018)。Carpentier等(2011)对多个RP的Zn含量进行了测试,得出其平均含量﹥5 000×10-6,明显高于肾结石中的Zn含量,提示Zn可以促进髓质间质中磷酸钙的沉积(Negri and Luis, 2018),肾结石患者的Zn排泄量显著高于正常受试者(Trincherietal., 1992),饮食中高Zn摄入量也被认为与较高的成人肾结石风险相关(Turneyetal., 2014)。Merlin等(2012)利用电感耦合等离子体光谱(ICP)对卵巢癌和甲状腺癌砂粒体钙化中的无机元素进行了研究,测得其中微量元素Zn的浓度高于100×10-6。孟繁露等(2013b)利用显微同步辐射X射线荧光(μ-SRXRF)对乳腺不同类型病变钙化物进行了元素分析,拟合图谱显示这些钙化物中均含元素Zn。
在生物医学材料领域,学者们采用溶胶-凝胶法(Jallotetal., 2005; Miaoetal., 2005; 李明欧等, 2009)、湿化学法(Renetal., 2009)、水热法(Lietal., 2008; 李明欧等, 2008; Xiaoetal., 2008)以及化学沉淀法(Bigietal., 1995; Legerosetal., 1999; 刘榕芳等,2003; Miyajietal., 2005; 李明欧等, 2008; Tangetal., 2009; 董胜敏等, 2010;Matsunagaetal., 2010; Aliouietal., 2019)等方法均合成了含有Zn的HAP。
3 Zn掺入生物磷灰石的具体机制
从矿物学角度看,HAP具有一种适应性的骨架结构(Whiteetal., 2005),且在两种Ca位点(Ca1和Ca2)上可容纳一定量的Zn(Ma and Ellis, 2008; Matsunaga, 2008; Tangetal., 2009; Matsunagaetal., 2010)。对于Zn掺入HAP的具体机制,主要存在以下3种观点。
3.1 吸附作用
Bigi等(1995)实验合成的HAP粉末的Ca/Zn值与初始溶液中的Ca/Zn值几乎相等,且晶胞参数变化与Zn浓度的关系并不明显,其认为大部分Zn与磷灰石相的相互作用仅限于晶体表面和/或无定形部分。Barrea等(2001)利用扩展X射线吸收精细结构谱(EXAFS)研究了Zn在人体牙龈中的第一壳层配位,发现上牙龈样品中的Zn呈四面体配位,将其解释为Zn吸附于HAP表面。唐文清等(2007)、张昱等(2008)利用废弃蛋壳制备HAP,对废水中的Zn2+进行了吸附研究,发现当HAP对Zn2+的吸附达到平衡时,延长搅拌时间,去除率一直保持而没有下降,且HAP对Zn2+的吸附符合Freundlich和 Langmuir吸附方程,据此认为HAP对Zn2+发生了以离子交换吸附和表面吸附为主的吸附作用。
3.2 Zn进入晶格替代Ca
Takatsuka等(2005)通过对ZnO/ZnO+ZnCl2处理的牛牙样品、胶原蛋白粉末、合成的Zn-HAP、ZnCl2处理的HAP等样品进行X射线近边吸收谱(XANES)和EXAFS对比分析,认为Zn进入HAP晶格中替代了Ca。Barrea等(2001)的EXAFS结果表明下牙龈样品中的Zn呈八面体配位,将其解释为Zn进入了HAP晶格。Matsunaga等(2010)对化学沉淀法合成的Zn-HAP的XRD分析证实形成的是单一物相,且样品在773 K下退火后的XRD和XANES结果没有明显的区别,认为掺杂的Zn2+不是简单地吸附在HAP表面,而是进入了HAP晶格。李明欧等(2008)采用水热法制备纳米Zn-HAP,发现随着Zn2+浓度的增加,沿a轴和c轴方向的HAP晶粒尺寸、晶胞参数a和c以及晶胞体积均呈减小趋势,认为该现象是由Zn进入HAP晶格引起的。Ren等(2009)对湿化学法合成的纳米Zn-HAP进行了多次超声波清洗处理,以排除吸附作用的干扰,相关实验结果均证实Zn进入HAP结构中替代了Ca,而不是简单地吸附在HAP表面或非晶相上。Alioui 等(2019)对沉淀法合成的Zn-HAP进行测试的结果也表明Zn进入了HAP晶格。
如图1所示,在HAP结构中,Ca1平行c轴排列,位于6个分居上下两层的[PO4]四面体之间,与这些[PO4]四面体的9个角顶O相连(图1a、1b),呈9次配位,其中6个较邻近的O原子(3个O1和3个O2原子,分别分布在单位细胞的上下两层)与Ca1形成环状Ca1—PO4骨架,另外3个较远的为O3原子(图1b),Ca1—O9多面体之间共面连接;12个分居上下两层的[PO4]四面体围成沿c轴延伸的较大通道(图1a),配位数为7的Ca2位于通道内(图1a),被5个[PO4]四面体包围,与1个O1、1个O2、4个O3和1个O4原子(属于OH基团)成键(图1a、1c),即Ca2—O7多面体通过5个角顶和1个棱的共用与周围的磷酸基团以及羟基相连。
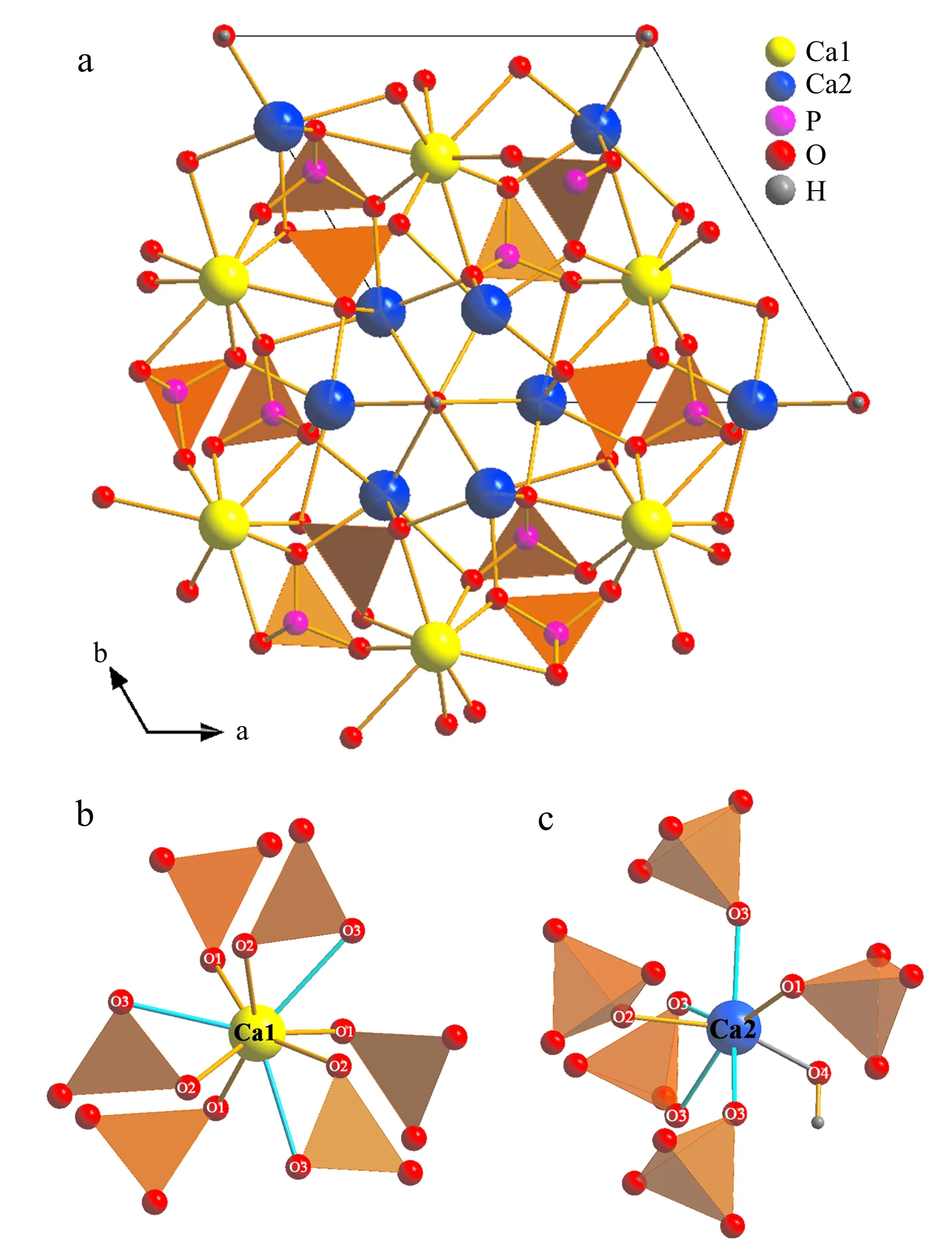
图 1 沿c轴观察的HAP结构(a)以及Ca1(b)、Ca2位点(c)的结构构型(修改自Tang等, 2009)Fig.1 Crystal structure of HAP viewed along the c axis (a) and local atomic structures of Ca1 (b) and Ca2 (c) (modified after Tang et al., 2009)
无论Zn在哪个位点,具有哪种配位,HAP的局部结构都必须变形以适应Zn的替代。如果Zn占据Ca1位点,将破坏Ca1—O9多面体上下面的共面结构,本质上会破坏环状Ca1—PO4骨架;如果Zn占据Ca2位点,Zn—O多面体和通道OH的距离将缩短而引起局部结构发生收缩,使得对相邻Ca1位的影响最小化,并避免对结构造成破坏(Tangetal., 2009)。理论上Ca2位的置换更稳定(Matsunaga, 2008; Matsunagaetal., 2008; Tangetal., 2009)。
XANES通常可以反映一个被关注原子的局部配位结构和化学结合状态,而且很稳定,因而可用于分析Zn-HAP的具体化学环境(Matsunagaetal., 2010),有效研究Zn占据Ca1或Ca2位置的可能性(Tangetal., 2009; Matsunagaetal., 2010)。对Zn具体占位进行的XANES实验研究也一致认为Zn更容易占据Ca2位而非Ca1位(Ma and Ellis, 2008; Matsunaga, 2008; Tangetal., 2009; Matsunagaetal., 2010; 孟繁露等, 2013b)。
3.3 Ca2+空位填充机制
为了研究HAP中取代Ca2+的Zn2+的局部环境,Matsunaga等(2010)在荧光模式下对沉淀法合成的Zn-HAP样品进行了XANES测试,获得了与Tang 等(2009)、Takatsuka等(2010)几乎完全相同的Zn掺杂HAP的实验光谱,并将其与计算模拟的理论光谱进行了归一化和比较(图2)。
如图2所示,“Ca-def HAp”模型中Zn2+取代发生在Ca2位点的理论图谱“Zn@ Ca-2”(图中绿色)与实验图谱“Expt.”(图中黑色)显示出高度的一致性;而“Perfect HAp”模型中Zn占据Ca1位和Ca2位的理论光谱“Zn@Ca-1”和“Zn@Ca-2”(图中蓝色)都显示了与实验光谱“Expt.”明显不同的光谱特征, 峰A(9 662 eV)、峰B(9 665 eV)、峰C(9 674 eV)以及AB之间的峰分裂均存在较大的差异,且“Zn@Ca-1”和“Zn@Ca-2”在B峰值后出现了肩型特征,而没有出现实验图谱“Expt.”在9 656 eV附近的边前峰。这些差异表明Zn2+进入HAP结构不能由完好晶格中的Ca被简单替代来解释。

图 2 Zn占据Ca1、Ca2位的实验和模拟计算XANES图谱(据Matsunaga等, 2010)Fig. 2 Experimental Zn-K XANES for Zn2+-doped HAP in comparison with theoretical ones (after Matsunaga et al., 2010)
另外,Matsunaga等(2010)还得到掺杂Zn2+的HAP含有一定量的Ca2+空位的结论,即掺杂了Zn2+的HAP化学成分倾向于缺失Ca,n(Ca+Zn)/n(P)﹤1.67,与以往的一些研究结果一致(Bigietal., 1995; Miyajietal., 2005)。据此,Matsunaga等(2010)假定了一个Ca2+空位缺陷复合体填充机制: 在Ca2位置的Ca2+空位上(围绕OH垂直于c轴排列的三角形Ca位),电荷由两个质子补偿,形成电荷中性的空位质子缺陷复合体,用“(VCa-2Hi)x”表示,则空位填充机制可表示为(VCa-2Hi)x(HAP) + Zn2+(aq)→ZnCa(HAP) +2H+(aq),即Ca2+空位缺陷复合体不仅是HAP中钙缺陷的来源,而且可充当Zn2+在HAP中的原子位点。相关实验已经确定了Ca2的优先损失(Miyajietal., 2005),理论和实验的XANES结果也证实Ca2+空位缺陷复合体是一种含Ca缺陷的HAP可能存在的模型(Matsunaga, 2008)。替代的Zn2+和缺陷复合体显示出相互吸引作用,且缺陷缔合使得Zn2+对Ca2+空位复合体的替代更加稳定,并可能导致Zn-HAP中钙缺陷的增加(Matsunagaetal., 2010)。
4 Zn的掺入对生物磷灰石的影响
4.1 晶粒尺寸和结晶度的变化
部分研究表明Zn的掺入会抑制生物磷灰石的结晶。Bigi等(1995)发现随着Zn2+浓度的增加,合成Zn-HAP的XRD特征峰逐渐变宽、变弱,(211)和(112)晶面对应的XRD峰分裂也变得模糊,认为Zn2+浓度的增加使得晶粒尺寸减小和(或)晶体应力增加。LeGeros等(1999)认为少量Zn掺入到HAP结构中便会导致磷灰石相的结晶度明显降低,因而结构不能容纳更多的Zn。Miyaji等(2005)使用化学沉淀法合成Zn-HAP,发现当Zn2+摩尔分数为0~15%时,XRD结果显示HAP的特征峰峰宽随着Zn含量的增加而急剧扩大,表明HAP的结晶度随Zn含量的增加而显著减弱。李明欧等(2008)采用水热法制备纳米Zn-HAP时发现随着Zn2+浓度的增加,沿a轴和c轴方向的晶粒尺寸和晶胞体积都呈减小趋势,将其解释为Zn2+和Ca2+半径大小不匹配。Alioui等(2019)发现随着Zn2+浓度的增加,合成的Zn-HAP晶粒尺寸和结晶度明显降低,晶体变得不规则并容易团聚,与Ren等 (2009)的结论一致。
然而,从骨细胞生物学的角度来讲,Zn的掺入会促进生物磷灰石的结晶。Zn可以通过刺激成骨细胞而促进骨骼羟基磷灰石的生长(Yamaguchietal., 1987),Zn亦能促进成骨细胞骨钙素的产生,而骨钙素可促进骨组织的钙化,加快骨基质成熟(Moonga and Dempster, 2010),且对破骨细胞有一定的抑制作用(Itoetal., 2000)。Zn掺入骨骼植入物中被证实可以促进仿骨材料周围的骨形成,从而促进骨折和骨创伤的愈合(Itoetal., 2000; 李明欧等, 2008)。另外,Hayakawa等(2007)报道可通过离子交换反应,在不改变晶粒尺寸和结晶度的情况下将Zn2+引入HAP晶格。
4.2 晶胞参数的变化
Zn被固定在矿物晶格之中时,会对矿物本身的晶胞参数产生影响。大多数研究均认为Zn的掺入会使得HAP的晶胞参数a和c减小(Barreaetal., 2001; Hayakawaetal., 2007; Renetal., 2009)。晶胞参数a减小,是因为羟基从c轴位置向Zn原子移动,Zn原子也偏离Ca2位向羟基移动(Ma and Ellis, 2008; Matsugana, 2008; Tangetal., 2009)。晶胞参数c随Zn含量的增加而减小(Bigietal., 1995; Miyajietal., 2005; Lietal., 2008;李明欧等,2008),与Zn2+半径小于Ca2+半径有关。
也有学者报道了随着Zn2+浓度的增加,晶胞参数a和c发生更加复杂的变化。Li等(2008)报道了水热法制备的Zn-HAP的晶格参数a在Zn2+摩尔分数小于10%时,随Zn2+摩尔分数的增大而减小;当Zn2+摩尔分数大于10%时,随Zn2+摩尔分数的增大而增大。Miyaji等(2005)通过实验得出HAP的晶胞参数a在Zn2+摩尔分数大于5%时会随Zn2+摩尔分数的增大而增大,将其归因于晶格水的增加取代了HAP结构中的羟基。Legeros等(1999)使用沉淀法合成有Ca缺陷的HAP,结果表明Ca位点的Zn替代会使得晶格参数a和c都增大。Ren等(2009)则发现当Zn2+摩尔分数大于10%时,晶格参数a和c都略有增大,推测其与生成了多晶沉淀和(或)新的物相有关。
4.3 其他
相关研究表明,Zn-HAP单一晶相只能在有限的条件下获得。Bigi等(1995)采用化学沉淀法合成Zn-HAP,发现当Zn2+浓度过高时会生成其他晶相如Zn3(PO4)2·2 H2O和CaZn2(PO4)2·2 H2O; Miyaji等(2005)使用化学沉淀法合成Zn-HAP,发现当Zn2+摩尔分数大于18%时,开始出现类磷灰石的无定形相以及磷酸钙锌复合盐CaZn2(PO4)2·2 H2O;李明欧等(2008)采用水热法制备纳米Zn-HAP,发现当Zn2+摩尔分数大于40%时,开始生成CaZn2(PO4)2·2 H2O;Ren等(2009)采用湿化学法在含Zn2+的水溶液中合成纳米HAP晶体,当Zn2+摩尔分数大于20%时,出现了磷酸钙锌复合盐,包括CaZn2(PO4)2·2 H2O、(Ca, Zn)HPO4·2 H2O、Zn2Ca (PO4)3·2 H2O及Zn3(PO4)2·H2O等物相。
另外,不同学者采用不同或相同的合成方法得到的Zn2+替代上限有较大的差异,即Zn2+在HAP中的替代上限仍不确定。LeGeros等(1999)认为,少量Zn2+掺入到HAP结构中便会导致磷灰石相的结晶度明显降低,进而导致结构不能容纳更多的Zn2+;Miyaji等(2005)、Tang等(2009)得出的磷灰石晶格中Ca位的Zn取代上限摩尔分数约为15%, Ren等(2009)认为是20%, Bigi等(1995)认为是25%。Alioui等(2019)则发现当掺杂的Zn2+摩尔分数为15%时,生成的Zn-HAP纳米晶呈现出规则的十二面体形态。
5 Zn的晶体化学行为研究对肿瘤诊疗的启示
肿瘤的早期发现主要依赖医学影像技术对病灶部位组织病变(包括钙化)征象以及化学检验对体液中元素含量等指标异常的筛查,肿瘤中的微钙化在许多情况下是肿瘤的唯一可检测标志(Lingetal., 2013; O’Gradyetal., 2018),而微量元素Zn与肿瘤的发生、发展关系密切(Prasad and Kucuk, 2002; Ho, 2004),是恶性肿瘤转移过程中的关键元素(Kagaraetal., 2007)。不同类型的乳腺病变(乳腺癌、乳腺纤维腺瘤、乳腺增生症和乳腺炎症等)伴随的钙化(物相为HAP)中均含有Zn元素,且乳腺癌钙化中的Zn含量高于乳腺良性病变(孟繁露等, 2013b, 2015),与乳腺良恶性组织中Zn含量的变化趋势一致(顾纪容等, 1994; 柏楠等, 2000; Gerakietal., 2002; Magalhăesetal., 2006, 2008; Siddiquietal., 2006)。荧光成像结果显示不同类型的乳腺病变钙化中Ca与Zn的分布大体一致,在Ca或Zn分布较多的区域有此消彼长之势(孟繁露等, 2013a, 2013b, 2015),提示Zn对Ca的替代。
近几十年来,Zn与癌变的关系逐渐受到生物医学界的关注,不同体液中的Zn含量水平已被用于肿瘤研究之中。相比于乳腺良性病变患者和(或)健康对照组,乳腺癌患者的血浆(Cavalloetal., 1991; Sevenetal., 1998)以及血液(Siddiquietal., 2006)中的Zn含量升高,而血清(Guptaetal., 1991; Yüceletal., 1994; Magalovaetal., 1996; 武力等, 2008)中的Zn含量降低。Larner等(2015)首次采用多接收器电感耦合等离子体质谱(MC-ICP-MS)对乳腺癌患者不同部位的Zn同位素进行了测试,发现肿瘤组织中的66Zn/64Zn值比健康组织以及血液和血清中的66Zn/64Zn值低,且为负值。根据66Zn/64Zn的测试数据,并结合铜同位素的测试结果,他们给出的乳腺癌诊断意见,与病理学诊断结果相符。
上述研究表明,肿瘤形成过程中Zn元素的新陈代谢发生了复杂的变化,不同类型的乳腺病变钙化、不同病理阶段患者的有机组织及体液中的Zn含量水平可以辅助说明病变的良恶性。一般来说,肿瘤患者分布的广泛性表明其病发时Zn的摄入量和排出量与未发病时并无显著区别,患者的长期居住环境和饮食习惯也不是导致体内Zn含量变化的原因,即患者体内的Zn总量在病发前后实际上是一个较为恒定的量。若将病变与成矿作用类比,其机理可假设为:病变导致了体内稳态的破环,元素在体内各个部位的分布平衡也被破坏,进而具有向某一特定部位迁移的倾向,并随着病变的发展在该部位富集。人体是一个庞大而复杂的有机系统,但在人体乳腺病灶中出现了含有Zn元素的无机钙化,且Zn的含量有随病理阶段递增的趋势,当Zn被固定在钙化晶格中时,其又可能对周围组织及体液中的Zn含量及Zn同位素分馏产生影响,即随着病变的发生和发展,钙化作为Zn的储存位置影响人体内Zn的新陈代谢。
6 结语
Zn掺入HAP结构会对其晶粒尺寸、结晶度、晶胞参数等产生较大的影响,选择不同的合成方法并控制合成条件,将不同浓度的Zn2+掺入到HAP结构,可以获得具有理想物理化学性质的Zn-HAP或其他所需物相;Ca2+空位填充机制可以辅助解释某些特殊元素掺入HAP结构的过程,也可以指导掺杂其他金属离子的高性能HAP材料的开发;Zn占据Ca2位点理论上不会破坏结构骨架,因而可以促进生物磷灰石对Zn的吸收和释放,这为今后研究钙化硬组织中Zn的储存和转运以及调控体内Zn的代谢提供了有价值的信息。
另外,Zn在钙化中的存在及含量差异应该引起关注。钙化似乎对Zn元素有富集作用,并作为Zn的储存位置影响Zn的新陈代谢,因而随着病变的发生和发展,不同类型的乳腺病变钙化、不同病理阶段患者的有机组织及体液中的Zn含量水平发生了较大的变化。相比于有机组织或体液,病变伴有的无机钙化具有更强的稳定性,可长期保存Zn元素的相关信息。围绕肿瘤钙化中Zn元素的晶体化学特性和行为,开展矿物学和生物医学交叉研究,可以揭示Zn元素与肿瘤发生和发展的关系,为人体肿瘤的早期发现和危险因素研究提供新的线索和思路。

