HIV阳性患者合并多发骨坏死1例
王 帅,张 强,赵昌松,邱玉金
AIDS是由HIV侵入人体后引起的以免疫系统结构破坏和功能缺陷为主的疾病。1996年开始的高效联合抗反转录病毒治疗(highly active antiretroviral therapy, HAART)延长了AIDS患者的寿命,减少了相关并发症的发生,但其引起的骨骼系统病变长期困扰着患者。HIV与HAART均会引起HIV阳性患者骨坏死,可以发生在任何部位,如膝关节、踝关节、肩关节、股骨头等都是易发部位[1-3],其中以股骨头坏死多见,多为双侧病变,但多发骨坏死较为少见。首都医科大学附属北京地坛医院骨科收治1例HIV阳性多发骨坏死患者,现报告如下。
1 病例报告
1.1 病史及查体 患者,男,33岁,HIV阳性合并双侧股骨头坏死,右肱骨头坏死。患者2016年5月因双髋部疼痛加重,活动及行走明显受限就诊于我院并行手术治疗。既往2009年患者因“间质性肺炎”曾服用激素。2010年因“脑膜炎”住院治疗,并确诊HIV阳性,之后长期口服“拉米夫定、齐多夫定、奈韦拉平”治疗。2013年2月患者无明显诱因出现左髋部疼痛,行走后加重,就诊于山西医科大学附属第一医院,行X线检查,被诊断为“左侧股骨头坏死,右侧股骨头坏死?”,未给予治疗,建议定期复查。2013年8月右髋出现疼痛,再次就诊于山西医科大学第一附属医院,行X线检查,被诊断为:“双侧股骨头坏死”,给与止痛治疗(药名不详),建议定期复查,必要时手术。2014年1月摔伤致右桡骨远端骨折,同时给予右肩X线检查示右肱骨头坏死可能,行石膏固定,右上肢制动。2015年3月双髋部疼痛加重,活动及行走受限,于我院就诊,行X线及CT检查示“双侧股骨头坏死”,建议手术治疗。患者及家属拒绝手术治疗,继续止痛对症治疗。病情逐渐加重。
本次入院骨科查体:患者跛行,蹒跚步态,双肩不等高,右肩较左肩低约1.5 cm,双髋部及右肩部轻度肿胀,双髋轻微屈髋外旋外展畸形;双髋部及右肩部压痛,活动明显受限。左髋关节前屈后伸活动 25°-0°-5°;右髋前屈后伸活动 10°-0°-5°;左髋屈髋位内旋外旋15°-0°-5°;右髋屈髋位内旋外旋 5°-0°-5°;左髋外展内收 5°-0°-10°;右髋外展内收 0°-0°-5°。右肩内旋外旋 25°-0°-15°;右肩外展内收65°-0°-25°。左足跟较右侧短缩约 1.5 cm。入院诊断:双侧股骨头坏死,右肱骨头坏死。分别于2016年5月31日,2016年10月24日行右侧、左侧全髋置换术。术后第14 d拆线出院。术前常规预防应用抗生素,术后3 d停止应用抗生素,患者未出现明显的术区感染及并发症。出院6周内减少髋部屈伸活动,6周后开始髋部肌肉锻炼(具体影像学见图1~4)。
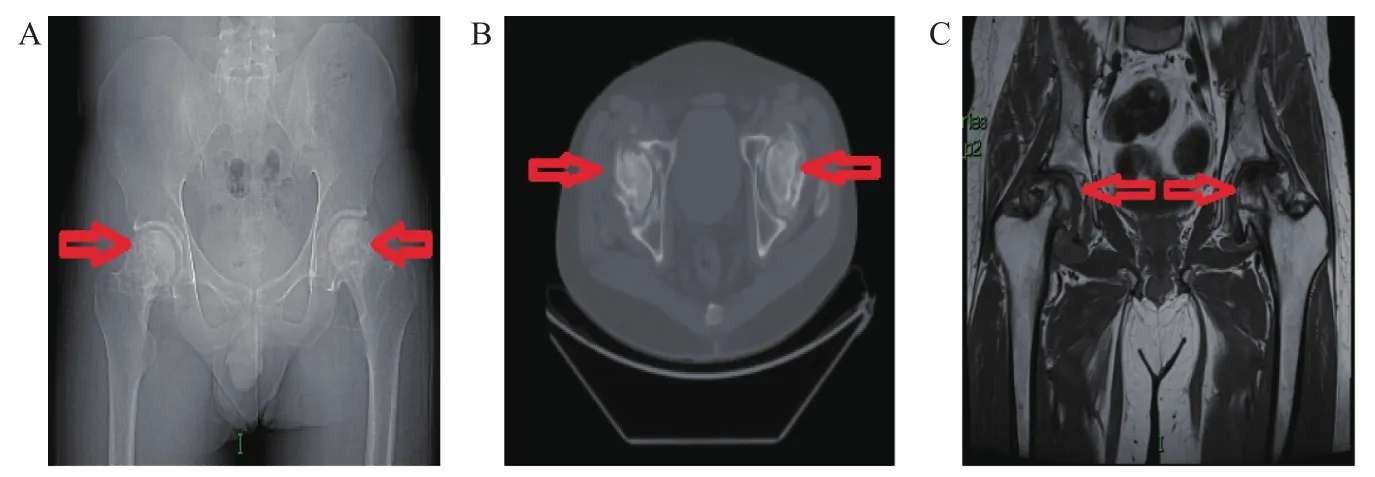
图1 术前双髋关节X线、CT、MRIA.双侧股骨头变扁,关节面欠光整,双侧股骨头关节面下骨质呈不均匀稍高密度,双侧髋关节间隙狭窄。B.多发死骨边缘硬化,周围可见透亮区,髋臼硬化,边缘骨质增生。C.双侧股骨头变扁,关节面稍毛糙,关节面下骨质信号异常Figure 1 X-ray,CT and MRI of hip before surgery
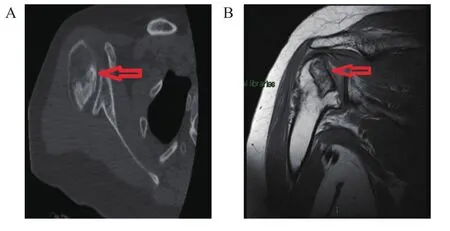
图2 术前右肩关节CT、MRIA.右侧肱骨头略变扁,其内可见小囊性低密度影,肱骨头边缘可见高密度硬化缘,关节面不光滑,关节间隙无明显异常改变。B.右肩关节在位;右肱骨头变形,局部关节面软骨及关节面下骨质缺损,缺损缘硬化,肱骨头骨质缺损面下可见灶性高信号影;关节盂关节面软骨局部变薄、缺损,关节间隙增宽,关节腔及周围少量积液Figure 2 CT and MRI of right shoulder joint before surgery

图3 第1次术后骨盆X线右侧股骨头置换术后,左侧股骨头无菌性坏死Figure 3 Pelvis X-ray after the first surgery

图4 第2次术后骨盆X线双髋关节置换术后,余骨盆组成骨质未见明显异常Figure 4 Pelvis X-ray after the second surgery
1.2 辅助检查 化验检查及影像学资料:入院后检查HIV载量<20 copies/ml,CD4+T淋巴细胞计数475个/μl,TG为1.03 mmol/L,WBC为4.63×109/L,ESR为11 mm/h,CRP为1.3 mg/L,BUN为7.25 mmol/L,CRE 为 52.1 μmol/L,AST 为 20.1 U/L,ALT 为32.4 U/L,PT为11.1 s,APTT为26.3 s。
2 讨 论
1990年第1例HIV阳性患者股骨头坏死被报道后,其发病率逐年增加[4]。Cabrita等[5]研究表明:正常人群股骨头坏死发病率为0.01%~0.14%,而HIV阳性患者股骨头坏死发病率为1.33%~4.40%,显著高于正常人群。Cummins等[6]回顾文献后指出,HIV阳性患者股骨头坏死发病率为1%。
除引起股骨头坏死的常见因素外,HIV阳性患者也存在其他高危因素。常见因素包括高血脂、酒精摄入、激素应用、系统性红斑狼疮等;其他高危因素包括HIV感染、抗病毒药物不良反应、长期应用类固醇激素等。Kieselova等[7]发现,83.3%的HIV阳性股骨头坏死患者有蛋白酶抑制剂(protease inhibitor, PI)应用史;但Hasse等[8]的研究表明PI出现之前就已有HIV阳性患者出现股骨头坏死。Mary-Krause等[9]和Lorkowski等[10]研究显示,HAART是股骨头坏死的高风险因素,接受此类治疗患者的发病率是不接受此类治疗患者的2.5倍,尤其在服用药物超过5年时,该风险升高到5.1倍。关于HIV阳性患者发生股骨头坏死是否归因于病毒对骨结构的直接影响,或通过免疫紊乱间接作用尚不清楚。
本例HIV阳性患者发生多部位(双侧股骨头、右侧肱骨头)骨坏死,考虑与既往应用激素、HIV感染及长期服用抗病毒药物有关。有文献报道,HIV阳性患者骨坏死的发生率随着病毒感染时间和服药时间增加而增加[9]。本研究患者确诊HIV阳性后长期服用抗病毒药物,服药3年后发现双侧股骨头坏死,4年后发现右肱骨头坏死。Whitlock等[11]也发现,15例骨坏死HIV阳性患者中有50%的患者在初诊股骨头坏死后出现了其他部位的骨坏死。因此,HIV阳性股骨头坏死的患者应警惕其他部位发生骨坏死的可能。
临床实践表明,MRI对股骨头坏死诊断的灵敏度和特异度高达95%,而X线对股骨头坏死早期诊断意义不大;骨扫描对早期诊断有一定意义,但是特异性和灵敏度较低,坏死区域的范围和具体位置不能精确量化。
早期的股骨头坏死可暂行保守治疗,减少负重以延缓疾病的进展;应用血管扩张剂药物前列腺素、双磷酸盐类药物,如阿伦磷酸钠均可改善患者的疼痛以及预防疾病的进展。此外,高压氧舱治疗,电刺激和体外冲击治疗也对早期的股骨头坏死有一定的疗效[12-14]。早期手术治疗可行股骨头髓芯减压术,晚期患者主要进行全髋关节置换术。预手术治疗的HIV阳性患者应在术前应用药物,快速降低病毒载量,以增加免疫力、改善机体状态。
总之,HIV阳性患者骨坏死的发病率显著高于正常人群。此类患者应注意避免各种高危因素,预防骨坏死的出现,如出现关节不适,特别是髋关节疼痛,应尽早检查,定期复查,以选择合适的治疗方案,提高患者生活质量。

