子痫前期孕妇子宫动脉彩色多普勒参数与血清内皮损伤标志物、胎盘凋亡基因的相关性研究
于国新,任 蓉
(西安市第九医院妇产科,西安 710000)
子痫前期是一种常见的妊娠期特有的并发症,以妊娠20周后出现的高血压、蛋白尿为主要特征[1]。子痫前期可能会导致孕妇出现肾衰竭、视网膜剥离、短暂失明、脑出血等并发症,同时造成胎儿发育迟缓、胎盘早剥、早产等严重情况。子痫前期若不及时干预,随着病情的不断加重可诱发子痫抽搐发作或昏迷,严重者甚至会造成孕妇和胎儿死亡。有调查显示,子痫前期是目前世界范围内造成孕妇及胎儿死亡的重要因素[2]。目前关于子痫前期的发病机制尚不清楚,但胎盘损伤两阶段学说为大多数学者所接受[3-4]。该学说认为,子痫前期与胎盘有关,胎盘中的滋养细胞浸润过浅,子宫螺旋小动脉产生重构障碍,导致胎盘灌注不足,血流阻力增加,引发孕妇多器官系统损伤[5]。目前临床上并未发现真正有效的治疗方法,现有的治疗方法也只是控制和缓解病情,争取延长孕周[6]。因此,子痫前期的预测显得尤为重要。检测孕妇子宫动脉的血流参数可以为子痫前期的筛查及病情评估提供依据。彩色多普勒超声诊断仪是临床上检测子宫动脉血流参数的常用辅助手段。本研究旨在分析子痫前期孕妇子宫动脉彩色多普勒参数与血清内皮损伤标志物、胎盘凋亡基因的相关性,以期为子痫前期的预测及治疗提供参考。
1 资料与方法
1.1一般资料 选择2014年5月至2017年10月在西安市第九医院分娩的110例孕妇作为研究对象,根据是否患有子痫前期分为子痫前期组(58例)和正常组(52例)。子痫前期组孕妇年龄24~42岁,平均(30.5±4.7)岁;孕周28~33周,平均(27.5±4.0)周。正常组孕妇年龄23~40岁,平均(29.4±4.6)岁;孕周27~32周,平均(27.2±3.7)周。两组孕妇年龄、孕周比较差异无统计学意义(P>0.05)。本研究通过西安市第九医院伦理委员会审批(伦理编号:2018-SR-196),孕妇均签署知情同意书。
1.2纳入与排除标准 纳入标准:①年龄20~40岁;②单胎妊娠初产妇。排除标准:①糖尿病、肝肾疾病、慢性血管性疾病史;②死胎、多胎妊娠史;③无其他产科并发症[7-8]。
1.3方法
1.3.1子宫动脉彩色多普勒参数的检测 超声仪器采用荷兰Philips公司制造的HDI-4000型诊断仪,探头频率为3.5~5.0 MHz,在孕27~32周进行子宫动脉的血流参数检测。具体检测方法如下:孕妇采取仰卧位,控制呼吸频率,待腹部进行常规扇形检查羊水、胎盘及胎儿发育等情况后,将探头放在宫颈两侧1 cm处,连续记录3个以上稳定且清晰的多普勒频谱图像,然后通过软件自动计算出子宫动脉的收缩期及舒张期血流比值(systolic/diastolic ratio,S/D)、搏动指数(pulsatility index,PI)、阻力指数(resistance index,RI)。
1.3.2血清内皮损伤标志物及胎盘凋亡基因的检测 孕妇成功分娩后20 min内取出胎盘组织,避开坏死及钙化区域,切取胎盘母体中央绒毛组织块1 cm×1 cm×1 cm。待充分研磨组织后,采用上海抚生实业有限公司生产的酶联免疫吸附试验试剂盒,对内皮素(endothelin,ET)、血管性血友病因子(von Willebrand factor,vWF)、血栓调节蛋白(thrombomodulin,TM)、一氧化氮合酶(nitric oxide synthase,NOS)进行检测,同时检测胎盘凋亡促进基因(Bax、Fas、caspase-3、caspase-9)和凋亡抑制基因[Bcl-2、Survivin、Livin、X连锁凋亡抑制蛋白(X-linked inhibitor of apoptosis protein,XIAP)]含量。操作步骤严格按照酶联免疫吸附试验试剂盒操作说明书。

2 结 果
2.1两组孕妇子宫动脉多普勒参数比较 子痫前期组孕妇S/D、PI及RI均高于正常组(P<0.01),见表1。

表1 两组孕妇子宫动脉多普勒参数比较
S/D:收缩期及舒张期血流比值;PI:搏动指数;RI:阻力指数
2.2两组孕妇血清内皮损伤标志物比较 子痫前期组孕妇ET、vWF、TM水平高于正常组,NOS水平低于对照组(P<0.01),见表2。

表2 两组孕妇血清内皮损伤标志物比较
ET:内皮素;vWF:血管性血友病因子;TM:血栓调节蛋白;NOS:一氧化氮合酶
2.3两组孕妇胎盘凋亡促进基因比较 子痫前期组Bax、Fas、caspase-3及caspase-9均高于正常组(P<0.01),见表3。
2.4两组孕妇胎盘凋亡抑制基因比较 子痫前期组Bcl-2、Survivin、Livin及XIAP均低于正常组(P<0.01),见表4。
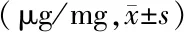
表3 两组孕妇胎盘凋亡促进基因比较

表4 两组孕妇胎盘凋亡抑制基因比较
XIAP:X连锁凋亡抑制蛋白
2.5子痫前期患者子宫动脉多普勒参数与内皮损伤标志物、凋亡基因的相关性分析 子痫前期组子宫动脉多普勒参数S/D、PI、RI与内皮损伤标志物ET、vWF、TM呈正相关(P<0.05),与NOS水平呈负相关(P<0.05),与凋亡促进基因Bax、Fas、caspase-3、caspase-9呈正相关(P<0.05),而与凋亡抑制基因Bcl-2、Survivin、Livin、XIAP呈负相关(P<0.05)。见表5。

表5 子痫前期患者子宫动脉多普勒参数与内皮损伤标志物、凋亡基因的相关性
S/D:收缩期及舒张期血流比值;PI:搏动指数;RI:阻力指数;ET:内皮素;vWF:血管性血友病因子;TM:血栓调节蛋白;NOS:一氧化氮合酶;XIAP:X连锁凋亡抑制蛋白
3 讨 论
子痫前期属于妊娠期高血压疾病的一种特殊类型,有调查显示,子痫前期约占妊娠高血压疾病的0.9%,发病率为2%~7%[9]。子痫前期容易促使孕妇血管收缩,对孕妇心脏、肾脏、大脑等器官造成损伤。当流向孕妇子宫的血液持续减少时,胎儿会出现生长缓慢、发育不良、羊水不足、胎盘早剥等严重问题。目前子痫前期的治疗方法仅能减缓疾病进程,只有终止妊娠才会停止子痫前期,妊娠继续只会加重[10]。即使孕妇及时终止了妊娠,保障了自身安全,疾病本身也会对孕妇及胎儿产生深远影响。
彩色多普勒超声诊断仪是一种无放射性、无创伤性的手段,它可以准确客观地反映子痫前期孕妇子宫动脉血流状况[11-13]。本研究结果显示,子痫前期组子宫动脉多普勒参数S/D、PI及RI均明显高于正常组,说明随着子痫前期病情的发展,子宫动脉的血流量明显减少,阻力明显增大。当胎盘血流灌注不足时,氧化应激反应增加,造成缺血缺氧,容易引发血管内皮功能障碍。ET是由21个氨基酸组成的多肽,它有ET-1、ET-2及ET-3三种形式。Demers和Girard[14]研究发现,当血管内皮受刺激或损伤时,ET-1会释放增加,因此ET-1水平升高可以在一定程度上反映血管内皮受损程度。vWF是由第12号染色体的短臂所编码的糖蛋白,Martínez-Ruiz和Vílchez[15]研究表明,vWF水平升高通常意味着血管内皮受到损伤。TM是使凝血酶由促凝转向抗凝的重要血管内凝血抑制因子,也是内皮损伤的标志物之一[16]。NOS是一种同工酶,其水平降低也反映了血管内皮受到损伤。本研究结果显示,子痫前期组内皮损伤标志物ET、vWF、TM水平高于正常组,而NOS水平低于正常组,说明子痫前期组胎盘组织中血清内皮细胞受到损伤。研究表明[17-18],血管内皮细胞受损后,vWF、TM水平升高,NOS水平下降。进一步分析子宫动脉多普勒参数与内皮损伤标志物水平的相关性发现,子宫动脉多普勒参数S/D、PI、RI与内皮损伤标志物ET、vWF、TM水平呈正相关,与NOS水平呈负相关,说明子宫动脉血流变化情况与血清内皮细胞损伤密切相关。其可能的机制是子宫动脉的血流量减少,阻力增大,抑制了血管舒缩功能,从而导致血管受到损伤,而血管受损又会增加血流阻力,加重胎盘血流灌注不足。
胎盘组织缺血缺氧不仅可抑制血管舒缩功能,导致血管受到损伤,还会引发胎盘细胞凋亡,对孕妇和胎儿带来不利影响。细胞凋亡是由基因控制的细胞自主有序的死亡,它与细胞坏死不同[19]。细胞坏死是病理条件下被动的自我损伤现象,而细胞凋亡是主动过程,是为了更好地适应生存环境而主动争取的一种死亡过程[20]。它涉及一系列基因的激活、表达以及调控。控制细胞凋亡的基因通常分为两类[21]:①凋亡促进基因,如Bax、Fas、caspase-3、caspase-9等。②凋亡抑制基因,如Bcl-2、Survivin、Livin、XIAP等。本研究结果显示,子痫前期组凋亡促进基因Bax、Fas、caspase-3、caspase-9水平明显升高,而凋亡抑制基因Bcl-2、Survivin、Livin、XIAP水平明显降低,说明在子痫前期孕妇胎盘组织内,更多的细胞以凋亡的形式来维持内环境稳定。进一步分析子宫动脉多普勒参数与胎盘凋亡基因的相关性发现,多普勒参数S/D、PI、RI与凋亡促进基因Bax、Fas、caspase-3、caspase-9呈正相关,而与凋亡抑制基因Bcl-2、Survivin、Livin、XIAP呈负相关,说明子宫动脉血流变化情况与胎盘凋亡基因水平密切相关。其可能的机制是子宫动脉重铸障碍引发胎盘组织缺血缺氧,促使细胞凋亡以适应环境,而细胞凋亡又进一步加重了胎盘缺氧缺血,从而影响胎盘发育。
综上所述,子痫前期孕妇子宫动脉彩色多普勒参数与血清内皮损伤标志物、胎盘凋亡基因密切相关,彩色多普勒参数升高,则患者血清内皮损伤增大,胎盘基因加速凋亡,反之,则内皮损伤减小,胎盘凋亡基因受到抑制。

