手助腹腔镜与腹腔镜辅助手术治疗结直肠癌的疗效与安全性比较
杜继明 王燕 赛媛媛
临床主要通过手术进行结直肠癌治疗,传统开腹手术创伤性较大,且术后恢复效果不理想,难以满足微创外科要求[1]。腹腔镜辅助手术治疗结直肠癌具有切口并发症少、疼痛轻、恢复快等优点,但学习曲线长,操作相对复杂,且术中缺少触觉反馈,不利于临床推广[2]。手助腹腔镜手术存在术中手触觉反馈,可在一定程度上缩短学习曲线,降低手术难度,但易引发术者腕部疲劳[3]。为寻找科学有效的治疗方式,维护患者健康,本研究进一步比较手助腹腔镜与腹腔镜辅助手术在结直肠癌治疗中的价值,现报告如下。
1 资料与方法
1.1 一般资料 选取2017年10月至2018年10月我院收治的结直肠癌患者100例,采用随机数表法分为观察组与对照组各50例。本研究经我院医学伦理委员会批准,患者及其家属对本研究均知情,并签署知情同意书。观察组男28例,女22例;年龄32~79岁,平均年龄(60.14±5.16)岁;肿瘤部位:直肠28例,结肠22例。对照组男29例,女21例;年龄33~79岁,平均年龄(60.58±5.09)岁;肿瘤部位:直肠28例,结肠22例。比较两组一般资料,差异无统计学意义(P>0.05),具有可对比性。
1.2 入选标准 纳入标准:①经病理检查、纤维结肠镜检查确诊。②初次手术治疗者。③未合并肿瘤转移。④近期未进行新辅助治疗。排除标准:①合并急性感染疾病、慢性炎症、严重肝肾肺功能障碍、肠梗阻。②存在腹部手术既往史。③采取急诊手术、姑息切除术以及中转开腹手术者。
1.3 方法 所有患者均予以全身麻醉,保持头高足低截石位。对照组予以腹腔镜辅助手术,建立二氧化碳气腹,设置气腹压力为13 ~15 mmHg(1 mmHg=0.133 kPa),依据肿瘤位置设计腹壁切口位置,切除直肠、乙状结肠。利用10 mm Trocar安置超声刀,对结肠旁腹膜进行锐性分割,接着对腹膜间隙进行钝性分离,再游离裸化系膜血管,在根部位置上钛夹,近端为2枚,远端为1枚,通过超声刀慢刀凝固、切断血管。切除右半结肠与左半结肠时,在右或中腹作一3~4 cm的切口,向体外缓慢拉出病变肠管,切除吻合,并在完成吻合后放回肠管。实施直肠癌根治手术时,通过超声刀对全直肠系膜进行锐性切除,清扫腹腔,暴露输尿管,之后锐性分离小骨盆,确保直肠远端的系膜组织被彻底清除,接着裸化直肠到肿瘤下端约3~5 cm位置,再通过直线切割闭合器离断远端直肠。在左下腹壁作纵形切口,长4 cm,向体外拉出病变肠管,切除标本,经肛门置入吻合器,于腹腔中结束吻合。对腹腔进行冲洗,安置引流管,最后关腹。观察组给予手助腹腔镜手术,将正中绕脐切口设计为手助切口,右半结肠切口位于右侧,乙状结肠、直肠以及左半结肠的位于左侧,长度为6 cm。建立气腹,将蓝碟(手助辅助器)置入手助切口,在手辅助器套口位置安放10 mm Trocar,为探查孔,把套口旋紧,维持气腹压力为14 mmHg。探查腹腔,消除气腹,将纱布放入腹腔内,术者经蓝碟以左手伸入气腹,穿刺10 mm Trocar,其次置入操作钳或者超声刀,将其作为主操作孔,术者于监视器下凭借超声刀进行游离,直接将小血管切断,而对于大血管则在钛夹夹闭之后切断。开展乙状结肠以及直肠切除术时,需对肠系膜之下的血管根淋巴结进行彻底清扫,将肠系膜下动、静脉分离,在血管根部位置结扎切断输尿管。游离结肠系膜,近端至肿瘤10 cm位置,远端至双侧系膜以及直肠后方,离肿瘤下缘5 cm。之后,实施平面裸化直肠系膜,凭借腔镜切割吻合器以及钉仓对远端直肠进行操作,并透过蓝碟取出近端肠管,体外切除标本,经患者肛门置入吻合器,于其腹腔中结束吻合。开展右、左半结肠切除手术的操作基本同于对照组,需从手术切口把病变肠管拖出,把吻合切除后再放进腹腔。对腹腔进行冲洗,安置引流管,最后关腹。
1.4 评价指标 ①记录两组手术出血量、手术时间、胃肠功能恢复时间、住院天数。②记录两组并发症,包括切口感染、肠梗阻、腔内感染、吻合口漏以及吻合口出血。③于术后24 h,记录两组VAS评分[4],0为无痛,10为剧痛,分值愈高则疼痛愈严重。
1.5 统计学方法 采用SPSS 20.0统计学软件,计数资料以率表示,组间比较采用χ2检验;计量资料采用(±s)表示,组内用配对本t检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者手术相关指标比较(表1) 观察组出血量低于对照组,手术时间短于对照组,胃肠功能恢复时间长于对照组,差异有统计学意义(P<0.05)。
2.2 两组患者并发症比较(表2) 两组并发症发生率相比,差异无统计学意义(P>0.05)。
表1 两组患者手术相关指标比较(±s)

表1 两组患者手术相关指标比较(±s)
组别 例数 手术出血量/mL 手术时间/min 胃肠功能恢复时间/h 住院天数/d对照组 50 133.62±27.35 137.95±40.58 47.52±9.09 7.02±1.39观察组 50 94.53±11.41 103.21±28.54 58.07±9.58 7.51±1.23 t值 9.327 4.952 5.649 1.867 P值 <0.05 <0.05 <0.05 >0.05
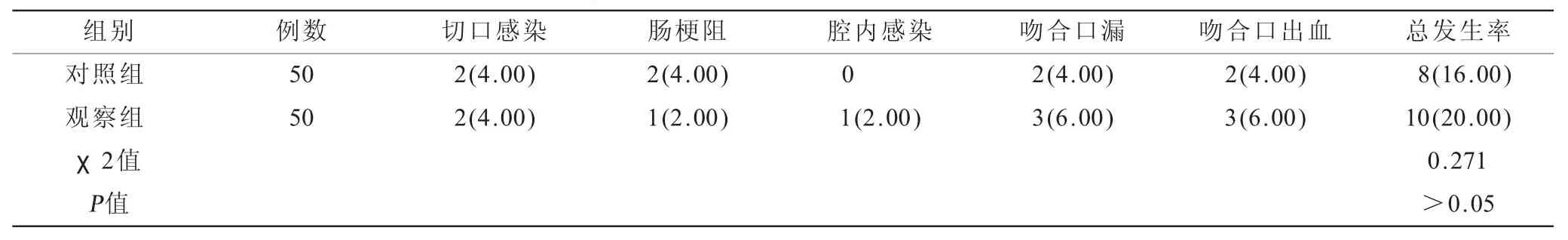
表2 两组患者并发症比较[n(%)]
2.3 两组患者VAS评分比较 观察组VAS评分为(2.77±1.21)分高于对照组(2.13±0.08)分,差异有统计学意义(t=3.732,P=0.000)。
3 讨论
结直肠癌是仅次于胃癌与食管癌的消化道恶性肿瘤,其发病原因与患者长期吸烟、低纤维素高脂肪饮食、遗传以及环境因素等相关[5]。流行病学资料显示,结直肠癌以60~70岁患者为高发人群,其在小于50岁人群中发病率不超过20%[6]。近年来,随着腹腔镜外科的快速发展,微创腹腔镜手术被较为广泛地应用到结直肠癌的治疗中,术式主要为腹腔镜辅助手术以及手助腹腔镜手术,但临床上对其疗效与安全性还存在一定争议。
手术腹腔镜外科产生于1992年,主张在腹腔镜术中把手伸入腹腔,以便辅助治疗,不仅可保留腹腔镜术式的优势,还可有效恢复手触觉,缩短手术时间,降低手术操作难度[7]。其与腹腔镜辅助手术均需对血管根部进行结扎切断处理,将相应的肠系膜与肿瘤两端涉及的肠管切除,与开腹手术治疗效果相当。本研究结果显示,观察组手术出血量低于对照组,手术时间短于对照组,VAS评分高于对照组,胃肠功能恢复时间长于对照组。提示,相较于腹腔镜辅助手术,在结直肠癌治疗中应用手助腹腔镜手术的出血量更低、手术时间更短,但胃肠功能恢复较慢,且术后疼痛较大,各有利弊。这与李伟学等[8]的研究结果一致。究其原因,手助腹腔镜手术过程中使用蓝碟,可将手伸入腹腔,进行各种手术操作,利于提高术者手眼协调性,更为准确地判断转移淋巴结与肿瘤范围,且便于辨认输尿管、血管等重要组织,可明显缩短手术时间,并在发生异常出血时,于清晰的术野下快速进行止血操作,进而降低出血量[9]。另外,手助腹腔镜治疗过程中,将手插入腹腔以及使用蓝碟,易增加对患者肠管的刺激,延长术后胃肠功能的恢复时间,而蓝碟位置切口较长,且需凭借持续压力固定在切口周围,可加重切口组织充血水肿以及组织挫伤情况,同时手腕的反复活动亦可刺激切口,加剧疼痛感[10]。
综上所述,针对结直肠癌手术治疗患者,应用手助腹腔镜手术治疗的出血量较低且时间较短,而腹腔镜辅助手术术后疼痛轻微、胃肠功能恢复快,临床上应依据实际需要加以选择。

