腹腔镜子宫肌瘤剔除术与宫腔镜子宫肌瘤电切术治疗子宫肌瘤伴不孕的效果比较
王君梅, 杜 岚
(陕西省西安安琪儿妇产医院 妇产科, 陕西 西安, 710032)
子宫肌瘤可致患者月经紊乱、月经量增多、经期延长等,并可引发子宫内膜容受性改变、子宫肌层蠕动异常等不良事件,最终导致不孕[1]。研究[2]发现,5%~10%不孕症患者伴子宫肌瘤,临床上多采用手术治疗,包括经腹子宫肌瘤剔除术、腹腔镜子宫肌瘤剔除术、宫腔镜子宫肌瘤电切术等[3]。经腹子宫肌瘤剔除术创伤较大,可能导致较多并发症,不易被患者接受[4]。腹腔镜子宫肌瘤剔除术虽可减少手术创伤,但在治疗部分直径较大肌瘤时也可能出现手术时间延长、出血量增多等问题[5]。近年来,宫腔镜子宫肌瘤电切术具有微创、对宫腔结构及功能的影响较小等优势,受到临床医师的关注[6]。本研究选取88例子宫肌瘤伴不孕患者,分析腹腔镜子宫肌瘤剔除术、宫腔镜子宫肌瘤电切术的效果,报告如下。
1 资料与方法
1.1 一般资料
选取2017年4月—2018年3月本院收治的88例子宫肌瘤伴不孕患者。纳入标准: ① 符合《子宫肌瘤的诊治中国专家共识》[7]中子宫肌瘤诊断标准; ② 符合《妇产科学》[8]中不孕症诊断标准; ③ 意识清晰,有生育意愿; ④ 行腹腔镜子宫肌瘤剔除术或宫腔镜子宫肌瘤电切术; ⑤ 临床及随访资料完整。排除标准: ① 合并严重心、肝、肾脏器疾病; ② 合并严重精神疾病; ③ 其他因素所致不孕,如多囊卵巢、输卵管阻塞、男方因素等; ④ 存在盆腔子宫内膜异位症、盆腔炎等疾病; ⑤ 临床及随访资料不完整。根据治疗方法分为对照组44例,年龄25~40岁,平均(31.85±3.26)岁; 子宫肌瘤病程5个月~3年,平均(1.69±0.24)年; 不孕病程12~23个月,平均(17.95±2.16)个月; 23例为肌壁间肌瘤, 21例为浆膜下肌瘤。研究组44例,年龄24~40岁,平均(31.81±3.22)岁; 子宫肌瘤病程5个月~3年,平均(1.65±0.21)年; 不孕病程12~24个月,平均(18.01±2.14)个月; 24例为肌壁间肌瘤, 20例为浆膜下肌瘤。2组患者一般资料无显著差异(P>0.05)。本研究经医院伦理委员会审核批准。
1.2 方法
对照组行腹腔镜子宫肌瘤剔除术: 术前清洗阴道,排空膀胱。取膀胱截石位,硬膜外麻醉。置入举宫器,暴露肌瘤。采用四孔法,创建CO2气腹,置入腹腔镜,探查子宫肌瘤大小、位置、腹腔是否存在粘连等。瘤蒂较细者行浆膜下肌瘤电凝切断摘除,常规止血; 瘤蒂较粗者切开假包膜,术后常规止血。
研究组行宫腔镜子宫肌瘤电切术: 仪器为日本OlymPus公司27F被动式连续灌流宫腔电切镜。术前清洗阴道,排空膀胱。取膀胱截石位,硬膜外麻醉。以宫颈扩张器扩张阴道,暴露宫颈。置入宫腔镜,探查子宫肌瘤大小、位置、数量等。蒂黏膜下肌瘤体积较小者,电凝切断瘤蒂,取出瘤体; 肌瘤直径>3 cm者,以环形电极分次片状切割或组织剪除后取出; 无蒂黏膜下肌瘤在B超引导下操作。
1.3 观察指标
① 比较2组手术指标,包括手术时间、术中出血量、术后肛门排气时间。② 比较2组术前、术后6个月时卵巢储备功能指标变化,包括黄体生成素(LH)、卵泡刺激素(FSH)、雌二醇(E2)。③ 术后随访12个月,比较2组复发情况。复发标准为再次出现子宫肌瘤,直径>1 cm, 经妇科检查、超声等确诊[9]。④ 术后随访12个月,比较2组妊娠情况及术后首次妊娠时间。随访期间均进行生育指导,不避孕,妊娠标准为受精卵成功着床。
1.4 统计学分析

2 结 果
2.1 2组手术指标比较
研究组手术时间、术后肛门排气时间短于对照组,术中出血量少于对照组,差异均有统计学意义(P<0.05)。见表1。
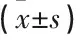
表1 2组相关手术指标比较
与对照组比较, *P<0.05。
2.2 2组卵巢储备功能比较
术后6个月时, 2组LH、FSH、E2均基本恢复到术前水平,差异无统计学意义(P>0.05)。见表2。
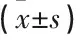
表2 2组不同时点卵巢储备功能比较
LH: 黄体生成素; FSH: 卵泡刺激素; E2: 雌二醇。
2.3 2组术后子宫肌瘤复发情况比较
术后随访12个月,中位随访时间7.5个月。研究组复发率为4.55%(2/44), 对照组复发率为9.09%(4/44), 差异无统计学意义(P>0.05)。
2.4 2组妊娠情况比较
随访期间,研究组妊娠率为77.27%(34/44), 术后首次妊娠时间为(6.96±2.15)个月。对照组妊娠率为68.18%(30/44), 术后首次妊娠时间为(8.36±2.08)个月。2组妊娠率比较,差异无统计学意义(P>0.05); 研究组术后首次妊娠时间早于对照组,差异有统计学意义(P<0.05)。
3 讨 论
子宫肌瘤发病机制较为复杂,与宫角处子宫肌瘤堵塞输卵管开口、宫颈管等因素有关[10]。目前研究[11-12]认为,子宫肌瘤与不孕症发生密切相关,黏膜下肌瘤、肌壁间肌瘤可致使宫腔性质改变,对受精卵着床产生干扰,引发子宫收缩异常,而阔韧带子宫肌瘤可压迫输卵管,致使受精卵无法顺利通过,引发不孕。此外,随着子宫肌瘤病情进展,还可能诱发血管紊乱、子宫内膜感染等现象,使得子宫内膜长时间处于高雄性激素水平状态下,降低子宫内膜容受性,且伴发严重盆腔粘连还可能致使输卵管扭曲、卵巢包裹,影响精子活动,造成不孕[13]。
子宫肌瘤伴不孕症治疗方法较多,以药物保守治疗、手术为主,但多数患者经药物保守治疗效果不佳[14]。研究[15]显示,腹腔镜子宫肌瘤剔除术治疗子宫肌瘤的效果理想,能避免经腹子宫肌瘤剔除术创伤大、并发症多、恢复慢等问题,且有利于维持盆腔正常结构,对腹(盆)腔脏器干扰小,腹壁不留瘢痕。研究[16]发现,腹腔镜子宫肌瘤剔除术在单发、浆膜下、中等大小子宫肌瘤治疗中具有较高的应用价值,但在部分直径较大子宫肌瘤治疗中有一定局限性,所需时间长,出血量多,且创面较大,中转开腹率较高。近年来,临床开始越来越多地关注该病治疗中宫腔镜子宫肌瘤电切术的应用,认为该手术具有微创性特点,可减少盆腔粘连发生,有利于术后正常妊娠[17]。此外,宫腔镜子宫肌瘤电切术在部分直径较大肌瘤治疗中效果也较为理想[18]。
本研究中,与对照组相比,研究组手术时间、术后肛门排气时间显著更短,术中出血量显著更少(P<0.05), 说明宫腔镜子宫肌瘤电切术创伤更小,能控制手术时间,可减少术中出血,促进术后恢复。此外, 2组术后6个月时LH、FSH、E2均基本恢复到术前水平,这说明两种手术对术后卵巢储备功能的影响均较小。考虑原因为两种手术虽可导致短期性激素紊乱,但术中对子宫肌壁深层影响较小,几乎不影响卵巢血供。术后随访12个月, 2组复发率均较低,说明两种手术在控制术后复发上效果相近。目前,临床针对子宫肌瘤是否会给生育能力造成影响仍存在较大争议。腹腔镜子宫肌瘤剔除术与宫腔镜子宫肌瘤电切术均为微创治疗手段,适用于有生育需求或希望保留生育功能者,能满足子宫肌瘤伴不孕患者的治疗需求。本研究结果显示,随访12个月时,研究组妊娠率为77.27%, 对照组则为68.18%, 差异无统计学意义,但研究组术后首次妊娠时间明显早于对照组,分析是因宫腔镜子宫肌瘤电切术创伤更小,术后肌层愈合速度快,可满足患者生育需求。
综上所述,在子宫肌瘤伴不孕治疗中,腹腔镜子宫肌瘤剔除术与宫腔镜子宫肌瘤电切术各具优势,对卵巢储备功能影响小,可改善妊娠率,控制复发。相较于腹腔镜子宫肌瘤剔除术,宫腔镜子宫肌瘤电切术可更好地控制手术创伤,减少术中出血,缩短术后首次妊娠时间。

