聚合反应主催化剂中钛含量的吸光光度测试法
汪东华
摘要:聚合反应的速度主要是通过控制Ti/C3=比值来实现。吸光光度法测试主催化剂中钛含量简便易行,采用回归分析校验标准曲线使曲线更具科学性,结果更加准确可靠。
关键词:催化剂;标准曲线;回归分析
聚合反应的速度主要是通过控制Ti/C3=比值来实现。Ti/C3=比值过大,单位体积内的活性中心数目增大,丙烯的转化率就越大,反应速率也急剧增大,严重时就会引起爆聚,而Ti/C3=比值太小,反应活性中心数目也会减小,引起反应速率过小甚至为零,结果是不聚合。因此,主催化剂中钛含量的测定显得尤为重要。
1.吸光光度法测试主催化剂中钛含量简便易行,采用回归分析检验标准曲线使曲线更具科学性,结果更加准确可靠。
1.1检测原理
吸光光度法是工业分析中的常用方法,其理论依据是朗伯(Lambert)——比尔(Beer)定律[1]即当一束单色光通过均匀溶液时,其吸光度与溶液的浓度和厚度成正比。它的表达式为:
式中:I0—入射光强度
A — 吸光度,无因次量
I — 透射光强度
b — 液层厚度
c — 吸光系数
在生产实践中适量的主催化剂己烷溶液被硫酸溶液分解,加入过氧化氢显色。用分光光度计测定试样的吸收率并且根据标准曲线计算钛含量。
2.实验部分
2.1试剂
硫酸(H2SO4)溶液(1+1) 磷酸(H3PO4)
3%过氯化氢(H2O2)溶液 海绵状钛
2.2 仪器
分光光度计UV-1201 日本岛津
直管吸量管10ml 移液管1ml,5ml和10ml
容量瓶100ml 催化剂取样瓶300ml
2.3实验步骤
2.3.1通过旋塞供入N2,缓缓地打开盛有试样的催化剂取样瓶的塞子,并将一根干净的搅拌棒放入瓶内。将试样瓶放在电磁搅拌器上并搅拌試样。
2.3.2在100ml的容量瓶中用经氮气吹扫过的10ml 移吸管取10ml试样放入,加入10ml的硫酸溶液(1+1)。
2.3.3在容量瓶内加入约20ml的水,并且充分摇晃容量瓶。加入1ml磷酸、5ml 3%过氧化氢,使该液体产生颜色。加水至标记线,然后充分摇晃试样。
2.3.4 20分钟后,在420nm波长处用20mm测定池并用蒸馏水作为参考溶液来测量该试样的吸光度。
2.3.5与事先绘制的标准曲线进行比较,计算试样的钛含量。
2.3.6 标准曲线的绘制
2.3.6.1加热用5N硫酸溶液溶解的海绵状钛,制备钛含量为0.1mg / ml的用作标准溶液
2.3.6.2分别用移液管取5,10,15和20ml的标准溶液,移入相应的100ml容量瓶中,并进行步骤2.3.3~2.3.4。
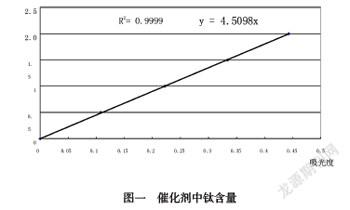
2.3.6.3根据钛含量和吸光度之间的关系绘制一校准曲线。如图一所示:
3.结果与讨论
3.1精密度试验
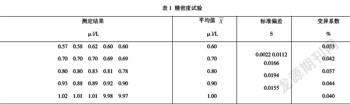
分别配制钛含量为 0.60ppm,0.70ppm,0.80ppm,0.90ppm,1.00ppm试样作为标样,用UV—1201型分光光度计测定,测其精密度,见表1。结果表明,标准偏差(变异系数)小于0.4。
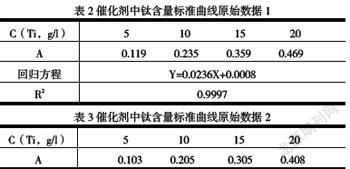
3.2标准曲线的校验
标准曲线使用一段时间后,由于仪器、试剂或其它原因会使吸光系数发生变化,因此标准曲线需要定期重新绘制。用回归分析法[2]校验标准曲线。
3.3分析参数的选择
3.4.1选择吸收池时要考虑溶液度对光的吸收特性的影响。一般说来摩尔系数较小的物质宜采用增大试样浓度使其吸光值增大,以便于测定。
3.4.2选择显色剂浓度要考虑因显色剂的过量使用而可能引起的副作用[4]。
3.4.3吸光度范围一般应在0.2--0.8之间。
3.4.4选择测定波长考虑主体物质对波长的选择性同时还要考虑检测灵敏度。
4结论
采用回归分析校验标准曲线使曲线更具科学性,结果更加准确可靠,能满足生产工艺要求,适用于生产控制分析。
参考文献:
[1]华东化工学院分析化学教研组,成都科学技术大学分析化学教研组,分析化学,高等教育出版社(第三版)1992,330
[2] 宋清 定量分析中的误差和数据评价,人民教育出版社,1982,126
[3]华东化工学院分析化学教研组,成都科学技术大学分析化学教研组,分析化学,高等教育出版社(第三版)1992,346
[4]蒋子刚 顾雪梅 分析测试中的数理统计与质量保证,华东化学工业出版社,1991,160

