Kartagener综合征41例诊治研究*
程克斌,孙晓丽,梁 硕,李惠萍,徐金富
苏州大学附属第三医院(上海市肺科医院呼吸与危重症医学科)(上海200433)
Prognosis
Kartagener综合征是一种纤毛结构和(或)功能异常的常染色体隐性遗传病,是原发性纤毛运动障碍(Primary ciliary dyskinesia,PCD)的一种,约占PCD的50%[1-2]。Kartagener综合征通常以慢性鼻窦炎、支气管扩张、内脏转位三联征为主要临床表现,该病临床罕见,发病率约为1/40 000,占支气管扩张症的1%、内脏反位性疾病的20%[3-4]。因发病率低、早期症状不典型、临床医师认识不足等诸多因素致其易误诊、漏诊、误治、预后不良。本研究总结了上海市肺科医院2004年1月至2017年12月住院诊断为Kartagener综合征患者的临床资料,探讨Kartagener综合征的临床特点,以提高对该病的认识。
对象与方法
1 研究对象 回顾性分析2004年1月至2017年12月上海市肺科医院确诊的Kartagener综合征且资料完整的住院病例。采用门诊结合电话和信件随访患者。最后访视时间为2018年4月30日。最终共有41例患者纳入本研究。本研究经我院伦理审查委员会批准,均征得患者知情同意。
2 研究方法 收集41例患者的一般资料、临床症状、胸部和鼻窦的影像学、痰液病原微生物学、肺功能、支气管镜等检查资料以及治疗转归。总结其临床特点,分析其诊治方法。观察指标包括:①一般资料:收集患者的年龄、性别、发病年龄、婚育史、家族史、合并症;②收集患者的咳嗽、咳痰、喘息、咯血、发热、胸痛、脓涕、听力下降、打鼾等临床症状,并记录症状出现的时间;记录患者入院查体的体征;③收集患者的心电图及腹部彩超检查结果;④患者的影像学资料按以下方式收集:用胸部CT定位患者的病灶部位,并记录病变类型,包括:支气管囊状及柱状扩张,管壁明显增厚,扩张肺纹理增粗,小结节影和树芽征存在与否[5]。用鼻窦CT记录其病灶部位及病变类型,包括:窦腔内黏膜增厚、软组织肿胀、窦腔内积液等;⑤呼吸道病原微生物学检查:有效的痰液病原学检查需具有涂片中白细胞>25/低倍视野且上皮细胞<10/低倍视野视为合格;支气管吸取物送检物视为合格呼吸道病原学检查;⑥肺功能检查:均在我院肺功能室完成,符合中华医学会呼吸病分会的肺功能检查标准[6]。检查结果中当一秒率(FEV1/FVC)< 70%判断为阻塞性肺通气功能障碍。弥散量(DLCO)<预计值的80%则判断为弥散功能障碍。动脉血气分析均在患者静息状态下未吸氧至少15 min后进行;⑦支气管镜检查:部分患者入院后局部麻醉下行支气管镜检查,术中观察支气管黏膜情况并进行气道廓清,收集支气管肺泡灌洗液行微生物检查;⑧治疗:记录患者住院期间及出院后大环内酯类药物、止咳化痰药物、支气管舒张药物以及吸入性糖皮质激素等药物的种类和剂量以及疗程。
结 果
1 一般资料 41例Kartagener综合征的患者,男21例,女20例,年龄17~59岁,平均诊断年龄(42.7±12.5)岁,首次发病的年龄范围1~25岁,平均发病年龄(13.9±6.5)岁,并且随着年龄的增大而临床症状逐渐加重。生育史:不育不孕史2例(4.9%),近亲结婚史3例(7.3%)。有Kartagener综合征家族史3例(7.3%)。
2 临床表现 41例均有慢性鼻窦炎病史。咳嗽(36/41)和咳痰(33/41)是Kartagener综合征患者的最常见的始发症状。此外还可出现发热、胸闷、胸痛、咯血、流脓涕、听力下降、打鼾等。确诊时患者的症状仍以咳嗽(39/41)、咳痰(37/41)、胸闷(31/41)、发热(18/41)、咯血(17/41)为主要表现。35例肺部可闻及湿罗音,多位于下叶,部位较固定,13例可闻及哮鸣音。20例有杵状指。
3 实验室检查 所有患者均行血常规、C反应蛋白、血沉检查,其中白细胞增高29例、C反应蛋白增高者23例,血沉增高者30例。所有患者均行心电图及腹部彩超检查,心电图均提示右位心,彩超均提示全内脏反位。
4 影像学特点 所有患者均行胸片、胸部CT及鼻窦检查(如图1~3)。41例胸部CT均见柱状支气管扩张,其中11例伴有囊状支扩,6例伴有肺不张。30例表现为双侧支扩,2例为单纯右上叶支扩,余9例则累及单侧中叶和/或下叶。下叶(36/41)和左舌段或右中叶(31/41)为最常见的受累部位,胸部CT表现为双肺纹理增粗,支气管呈囊柱状扩张,管壁明显增厚,呈印戒征或粘液栓形成,部分伴有小结节影或树芽征。9例患者有经CT证实的慢性鼻窦炎病史,未行鼻窦CT检查。余32例行鼻窦CT检查,均见上颌窦腔内黏膜增厚及窦腔内积液,其中18例合并筛窦炎,12例合并蝶窦炎,6例合并额窦炎。

图1 患者,女性,29岁,胸片提示右位心,两肺中下野为主的支气管扩张、小斑片阴影
5 支气管镜检查 41例患者中行支气管检查者24例,镜下主要表现为左右支气管呈镜像反位,支气管管腔黏膜充血肿胀,管腔内见黄绿色或白色粘性分泌物,部分见粘液栓(如图4)。支气管镜检查时常规使用生理盐水行气道廓清,收集肺泡灌洗液行微生物检查。

图2 同一患者的胸部CT,双肺支气管管腔扩张、多发树芽征改变、内脏反位。
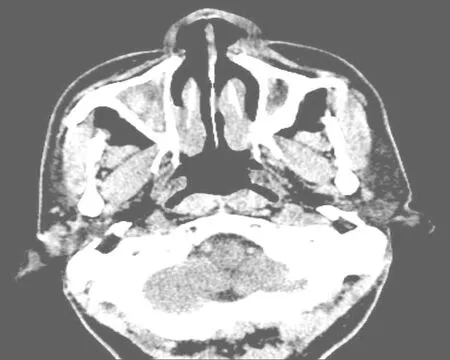
图3 同一患者的鼻窦CT,可见双侧以上颌窦为主的慢性鼻窦炎

图4 同一患者的支气管镜检查,可见支气管呈镜像改变,黏膜充血肿胀,管腔内白色痰液附壁
6 呼吸道病原微生物学检查 41例患者均行痰培养,其中阴性8例,铜绿假单胞菌18例(粘液型10例)、流感嗜血杆菌6例、肺炎克雷伯菌4例、鲍曼不动杆菌3例、非结核分枝杆菌3例、金黄色葡萄球菌2例、肺炎链球菌1例。24例患者同时行支气管肺泡灌洗液培养,阳性13例,其中铜绿假单胞菌9例(黏液型6例)、肺炎克雷伯菌3例、非结核分枝杆菌2例。
7 肺功能特点 所有患者均在静息时行动脉血气分析,11例患者血氧分压在正常范围,8例患者出现呼吸衰竭,余22例均存在不同程度的缺氧。血氧分压平均为(70.8±15.6) mmHg (1mmHg=0.133 kPa)。41例患者中,29例行肺通气功能检查,其中24例患者同时完成了弥散功能检查。5例患者肺功能完全正常;混合性通气功能障碍9例,阻塞性通气功能障碍10例,限制性通气功能障碍5例;弥散功能障碍9例。
8 治疗及转归 41例患者在住院期间均给予静脉抗生素、舒张气道止咳化痰等药物治疗,其中24例经支气管镜行气道廓清治疗,经治疗后患者症状缓解出院。出院后所有患者长期口服止咳、化痰药物。存在阻塞性通气功能障碍的患者应用β2受体激动剂、抗胆碱能药物、甲基嘌呤类药物的一种或联合,3例支气管舒张试验阳性者则吸入糖皮质激素。8例患者采用了小剂量大环内酯类药物长期口服治疗,如阿奇霉素 250 mg/d,疗程3~12个月。本组患者随访时间4个月至13年,5例患者因肺部感染加重反复住院,均为首次住院痰培养查见铜绿假单胞菌者且耐药者,其他患者病情相对稳定。
讨 论
Kartagener综合征是一种罕见的先天性常染色体隐性遗传病,临床表现为支气管扩张、内脏转位伴或不伴鼻窦炎,发病原因尚不明确,为PCD的特殊类型[7]。迄今为止,已有30多个基因的突变被报道与PCD发病密切相关[8],其中DNAI1和DNAH5突变可造成纤毛外动力臂缺陷,DNAI1突变致病患者约占10%[9],DNAH5突变致病患者约占28%[10];因此,DNAI1和DNAH5是最常见的基因突变类型[11]。Kartagener综合征的发病年龄在10~29岁,95%的病例发生在15岁以前,其发病率无显著的性别差异,但有家族遗传倾向,近亲结婚发病率高达20%~30%[12]。本组患者发病年龄1~25岁,平均13.9岁,男∶女为21∶20,这与文献报道一致。但本组资料仅有3例患者有近亲结婚史或Kartagener综合征家族史,这提示临床医生,无相关家族史亦不能排除该病的可能。
Kartagener综合征的典型临床表现包括支气管扩张、鼻窦炎、内脏转位,这些特征均与纤毛运动异常有关。纤毛广泛分布于人体的呼吸道上皮、耳咽管、脑室管膜、输卵管等处,其功能障碍可引起黏液清除功能异常,黏液分泌物和细菌潴留,导致长期、反复感染和慢性炎症改变,从而出现鼻窦炎、中耳炎、支气管炎和支气管扩张等[13]。输卵管上皮异常可导致不孕或异位妊娠,男性精子鞭毛功能异常则致不育,故本病常合并不孕或不育;此外,在胚胎发育过程中,如结纤毛异常,使内脏的定位旋转变为随机旋转,可出现右位心或内脏反位。内脏反位分为胸腹部内脏反位和胸或腹部内脏反位两种,后者常合并多脾或无脾及心血管异常[14],本组资料所有患者均为胸腹部全内脏反位。
本组资料中,90%以上的患者在首次入院时有咳嗽、咳黄脓痰的症状,75%的患者伴有胸闷、呼吸困难,约40%的患者伴有发热、不同程度的咯血、杵状指,查体两下肺可闻及湿啰音,这些临床表现均提示支气管扩张症可能,结合所有患者合并有慢性鼻窦炎,我们不难想到Kartagener综合征。本组患者的心电图均提示右位心,彩超均证实腹部脏器反位。胸部CT,尤其是高分辨率CT是目前诊断支气管扩张的最佳检查,它能显示支气管扩张的特征和部位。本组41例患者行胸部CT检查,均发现右位心及典型的支气管扩张,扩张部位以下肺及中叶或舌段为主。Kartagener综合征分完全型和不完全型2种,同时具备上述三联征的属完全型,只具备支气管扩张和内脏转位的属不完全型,右位心为其诊断的必备条件[15]。本组患者均具备慢性鼻窦炎、支气管扩张、内脏转位三联征,可临床诊断为Kartagener综合征,且为完全型。作为一种特殊的PCD,该病的诊断方法较多[16],可通过糖精实验、鼻呼出气一氧化氮水平测定来间接评估纤毛功能,亦可通过显微镜分析或高速数字视频成像来直接评估纤毛功能,还可通过透射电镜、荧光标记抗体来观察纤毛超微结构。目前,电镜下纤毛超微结构异常是Kartagener综合征诊断的“金标准”,但约30%的患者纤毛超微结构正常[2,16]。因此,随着遗传学诊断技术的进步,二代测序Panel和WES的应用,基因检测在诊断中发挥了重要作用[8]。限于我院的实验室条件,本组患者均未行鼻呼出气一氧化氮水平测定及黏膜活检标本电镜检查。
目前尚无能使纤毛功能恢复的药物,因此Kartagener综合征的治疗目的是防止病情恶化、减慢病情发展。急性期主要采用排痰、化痰、体位引流、支气管镜气道廓清、止血对症以及根据药敏试验选择敏感抗生素治疗。本组患者提示铜绿假单胞菌、流感嗜血杆菌、肺炎克雷伯菌是该病最常见的病原体,故临床上可根据上述病原体选择合理抗生素治疗。对于发作频繁的患者,暂不推荐长期口服抗生素治疗,但长期吸入某些抗生素可明显获益,如妥布霉素、氨曲南等。本组患者经积极抗感染、止咳化痰、支气管镜气道廓清、改善肺功能以及对症支持治疗,症状均改善,病情好转出院。缓解期应加强营养支持、提高机体免疫力,可适当使用免疫调节剂。大环内酯类抗生素不仅具有抗感染,还有抗炎和免疫调节作用。文献报告,长期小剂量阿奇霉素能明显减少PCD患者呼吸道中的铜绿假单胞菌数量,减少患者的急性发作,可延缓早期患者的疾病进展。本组有8例患者行小剂量阿奇霉素长期治疗,其急性发作次数明显低于未服用阿奇霉素者,均取得满意疗效,期待欧洲的临床研究大数据进一步证实。本病预后一般较好,但长期反复呼吸道感染可使病情加重,损害肺功能,最终引起呼吸衰竭、肺心病等。对于终末期患者,肺移植是有效的治疗方法,国内外学者证实Kartagener综合征患者移植后肺功能明显改善、生活质量提高。
总之,Kartagener综合征是一种罕见疾病。幼年起病、反复下呼吸道感染,合并慢性鼻窦炎、内脏反位的支气管扩张症患者需考虑该病。根据典型临床表现,其临床诊断并不困难,但会存在一定误诊、漏诊的可能,还应加强对电镜检查的重视,必要时基因测序进行精准分子诊断。早期诊断、及时治疗可改善患者预后、提高生活质量、延长寿命。

