全腹腔镜下经腹经膈肌胸腹联合治疗Ⅱ型食管胃结合部腺癌的临床体会
杨红美,邹贵军,金慧玉,张朝军
(中国人民解放军总医院第六医学中心,北京,100048)
近年,食管胃结合部腺癌越来越受到重视,甚至将其归为特殊类型肿瘤。食管胃结合部腺癌是指肿瘤中心处于食管-胃解剖交界上下5 cm以内的腺癌,并跨越或接触食管胃结合部。食管胃结合部腺癌常采用Siewert分型,分为Siewert Ⅰ、Ⅱ、Ⅲ,其中Siewert Ⅱ型是指肿瘤中心位于食管胃结合部以上1 cm至食管胃结合部以下2 cm,并累及食管胃结合部[1]。目前,手术仍是治疗食管胃结合部腺癌的首选[2],但其存在较大争议,不同学科在手术入路、切除范围、淋巴结清扫范围、吻合方式方面差异较大[3-4]。以往,食管胃结合部腺癌多采用胸腹联合途径[5-6],手术创伤大,术后并发症多[7],随着腹腔镜技术在胃肿瘤手术中的不断成熟[8-9],经验丰富的术者也尝试在腹腔镜下游离下段食管,手术创伤大大减少,但术后并发症并未明显减少,尤其食管空肠吻合口漏的发生未明显降低,因此,为减少手术创伤、术后并发症,我科尝试在全腹腔镜下经腹经膈肌胸腹联合治疗Ⅱ型食管胃结合部腺癌,近期疗效满意,现将体会报道如下。
1 资料与方法
1.1 临床资料 2015年1月1日至2018年6月1日在解放军总医院第六医学中心行全腹腔镜下经腹经膈肌胸腹联合治疗Ⅱ型食管胃结合部腺癌的患者54例,其中男31例,女23例,49~83岁,平均(66±2.8)岁,术前影像学cTNM分期Ⅱ期21例,Ш期33例。纳入标准:(1)术前胃镜检查并取病理,结果为腺癌;(2)上消化道造影、腹部增强CT、胃镜检查提示肿瘤中心位于食管胃结合部以上1 cm至食管胃结合部以下2 cm,并累及食管胃结合部,术中腹腔镜联合胃镜进一步定位肿瘤上缘,术中冰冻病理确保切缘阴性;(3)胸腹部CT提示无肝脏、肺脏等远处转移;(4)术前讨论经科室两位以上高级职称医师初步评估,可行全腹腔镜下经腹经膈肌胸腹联合胃癌D2根治术+食管空肠π型吻合术;(5)围手术期测定相关指标并准确记录,术后半年复查胃镜等,随访时间≥6个月。
1.2 手术方法 患者取分腿位,脐上1 cm处穿刺10 mm Trocar为观察孔,分别于左、右腋前线肋缘下2 cm处穿刺12 mm、5 mm Trocar,左、右锁骨中线于平脐及脐上2 cm处穿刺5 mm、12 mm Trocar。术者立于患者左侧,第一助手立于右侧。建立CO2气腹,悬吊肝脏,显露食管裂孔部位,行全腹腔镜胃癌根治术[1,10],先按照第6、7、8a、8p、12a、5、3、1、19组顺序清扫右侧淋巴结,常规于幽门下2 cm切断十二指肠,然后按照第4d、4sb、11p、11d、10、4sa、2、20组顺序清扫左侧淋巴结,超声刀切开左侧膈肌3~5 cm,打开左侧胸腔(图1),清扫食管下段周围组织淋巴结(第110组),并游离下段食管5~7 cm,术中胃镜定位肿瘤上缘并经腹腔标记,标记处上方约2 cm处打开食管,留备吻合用。距Treitz韧带约25 cm处用超声刀分离肠系膜约8 cm(注意保证小肠血供),切开对系膜肠壁,置入腔内直线切割闭合器,上提小肠至下纵隔,将吻合器另一臂置入食管内,直视下于左侧胸腔内行食管-空肠侧侧吻合(图2),关闭共同开口后(图3),用3-0倒刺线加固吻合口。距胃肠吻合口约40 cm处远端空肠及近端空肠系膜对侧缘各开一小孔,置入直线切割吻合器行空肠-空肠侧侧吻合,关闭共同开口,完成消化道重建[9,11]。距空肠-空肠吻合口远端约15 cm处置入空肠营养管,固定于腹膜后,由腹壁引出并固定。分别于左、右纵隔放置双腔引流管一根,经肝下、脾窝引出并固定。妥善止血,扩大脐上切口,取出标本。
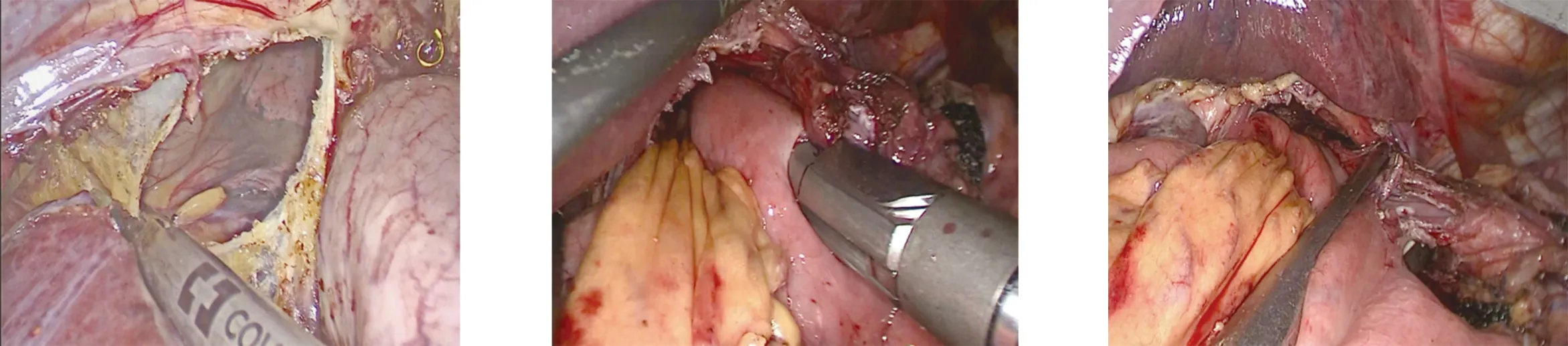
图1 打开左侧膈肌、左侧胸腔 图2 直线切割闭合器行食管-空肠侧侧吻合 图3 直线切割闭合器关闭共同开口
1.3 观察指标 记录淋巴结清扫时间、消化道重建时间、术中失血量、术后住院时间、淋巴结清扫总数、第110组淋巴结数量、术后并发症及随访情况。
2 结 果
54例均顺利完成手术,无死亡病例。本组淋巴结清扫时间平均(105.91±2.92)min,消化道重建时间(70.00±3.13)min,术中失血量(80±20)mL,术后平均住院(9±2)d,淋巴结清扫总数平均(35.5±5.5)枚,第110组淋巴结数量(3.5±1.5)枚,术后第1天下床活动并经空肠营养管入糖水500 mL,第2天开始进肠内营养乳剂500 mL,此后每日增加500 mL,直至2 000 mL,无吻合口出血、肠梗阻发生。2例患者出现食管-空肠吻合口漏,经上消化道造影及胃镜检查提示瘘口直径<0.5 cm,保守治疗后痊愈。术后病理示切缘无肿瘤残留。术后随访≥6个月,无吻合口复发、狭窄、出血等。
3 讨 论
食管胃结合部肿瘤因其解剖位置的特殊性,手术难度较大,围手术期并发症多,常迫使临床医生采用姑息治疗,使部分患者病情进展从而丧失手术机会。全腹腔镜下经腹经膈肌胸腹联合治疗全程在腹腔镜监视下行淋巴结清扫、消化道重建,具有明显优势。
与传统胸腹联合、腹腔镜下不经腹经膈肌治疗Ⅱ型食管胃结合部腺癌相比,其优点为:(1)避免开胸,创伤小,患者疼痛不适明显减轻,不会因疼痛而影响呼吸,从而减少了肺部感染的几率。(2)切开左侧膈肌,进入胸腔,增加了食管下段淋巴结清扫的空间,清扫彻底,可游离足够的食管长度,达到足够的肿瘤切缘、R0切除,降低了吻合口肿瘤残留的可能性,同时亦减少了前方心脏与后方胸主动脉的损伤。(3)全腹腔镜下食管空肠吻合方法较多,此入路为消化道重建提供了很大的操作空间,其中π型食管空肠侧侧吻合在左侧胸腔内实施,简化了腹腔镜操作,降低了消化道重建难度,直视下检查吻合情况,并加固,吻合更加牢靠[12],减少了吻合口狭窄、吻合口漏的发生,扩大的食管裂孔也减少了食管空肠吻合口的张力。(4)下纵隔左、右侧分别放置双腔冲洗管,在食管空肠吻合口一旦发生漏时,可有效提高保守治疗的成功率,同时术后可有效引流左侧胸腔内的积液,进一步降低了肺部感染、气胸、纵隔感染的几率。(5)全腹腔镜的视野较广,使操作更加精细化,减少了心脏、胸主动脉等其他副损伤的发生。(6)脐部小切口减少了疼痛,更加美观。(7)对于无法耐受胸腹联合途径的体弱、心肺功能差的老年患者尤其适合[13-14]。
全胃切除手术中放置空肠营养管的优点:(1)术后第1天开始经空肠营养管进食,早期进食比较符合人体正常的生理活动,有效维持正常消化道组织形态结构与生理功能,减少了相关并发症的发生,有效改善了患者围手术期营养状态,同时节省了费用。(2)保守治疗吻合口漏时,可提供长期、有效、安全的营养支持,缩短瘘的愈合时间。(3)可为全胃切除术后进食较差的患者提供临时营养支持,为后续治疗提供保障。(4)极少发生肠梗阻、肠瘘等并发症;两周后无需使用时,可直接拔除,较为方便、安全。
我们体会:(1)此术式采用先清扫胃小弯、后清扫胃大弯、左右隔肌汇合、先右后左的顺序清扫淋巴结,视野开阔,对助手的配合要求较低,淋巴结清扫彻底,出血发生率低。打开膈肌、左侧胸腔扩大了淋巴结的清扫空间,降低了下段食管周围淋巴结清扫难度。消化道重建时,采用π型食管空肠侧侧吻合简化了腹腔镜下的操作,此术式的优化,整体降低了根治手术的难度,提高了根治程度,更容易普及推广。(2)消化道重建时,术者先于患者左侧在小肠、食管内置入直线切割闭合器,行食管-空肠吻合,直视下观察吻合情况及有无肿瘤残余,然后换位于患者右侧,肿瘤上缘系一粗线,助手牵于此线用力下拉食管,术者直视下用直线切割闭合器关闭共同开口,再间断或连续缝合加固吻合口。(3)食管内置入直线切割闭合器时,可以胃管作引导,避免进入假道,损伤食管,导致吻合失败。(4)术中冰冻病理切缘如提示阳性,可切除此吻合口,行Overlap吻合或圆形吻合。
完全腹腔镜下打开左侧膈肌、左侧胸腔,可游离下段食管约7 cm,在淋巴结清扫方面,对于Siewert Ⅰ型患者仍适用。然而,在消化道重建方面,部分患者因小肠系膜短、血供相对差,采用π型食管空肠侧侧吻合时,可能存在一定张力,此时可采用Overlap方式解决。因此,对于食管胃结合部腺癌而言,可采用此术式进行淋巴结清扫,在消化道重建时,可酌情采用π型或Overlap术式[15]。本研究中,为准确汇报此术式的实际效果,我们仅统计Siewert Ⅱ型食管胃结合部腺癌的病例。其在Siewert Ⅰ型患者的应用效果,会在后期进行单独统计汇报。在后续的临床研究中,除了进行与传统胸腹联合、腹腔镜下不经腹经膈肌治疗Ⅱ型食管胃结合部腺癌术式的对比前瞻性研究外,我们还会尝试双镜联合进一步改善Siewert Ⅰ型食管胃结合部腺癌手术的困境。
综上所述,完全腹腔镜下经腹经膈肌胸腹联合治疗Ⅱ型食管胃结合部腺癌是安全、可行的,可明显缩短年轻外科医生的学习曲线,值得推广应用。

