容量目标通气联合肺泡表面活性物质治疗新生儿呼吸窘迫综合征的疗效分析
张利
(资阳市第一人民医院 儿科,四川 资阳 641300)
新生儿呼吸窘迫综合征(neonatal respiratory distress syndrome,NRDS)是新生儿出生后不久出现的进行性呼吸困难和呼吸衰竭,肺泡表面活性物质及机械通气是治疗该病的常用手段[1-2]。容量目标通气是一种新型的机械通气模式,在满足患儿肺通气量的同时自动调节压力,避免在充气过程中发生损伤[3-4]。本研究在肺泡表面活性物质替代治疗的同时将容量目标通气模式联合用于患儿的治疗,探讨其对患儿病情优化的作用,为后续机械通气模式的选择提供参考。
1 资料与方法
1.1 一般资料
选取2014年1月—2017年3月资阳市第一人民医院收治的NRDS患儿42例作为研究对象,参照随机数表法将入组患儿分为对照组和研究组,各21例。纳入标准:①符合临床NRDS诊断标准[5];②入组前未接受其他治疗;③合并先天性心脏病、先天性肾积水及先天性脑积水等;④家属签署知情同意书。排除标准:①合并新生儿溶血等严重疾患;②合并肺泡表面活性物质等药物过敏;③中途退出治疗、数据获取不完整及有数据脱落。本研究及后续研究计划获本院伦理委员会批准。两组患儿的性别、出生胎龄、出生体重分布差异无统计学意义(P>0.05),具有可比性。见表1。

表1 两组患儿一般资料 (n =21)
1.2 方法
患儿均接受保温、营养支持、补液及预防感染等常规治疗。对照组患儿在常规治疗基础上加入外源性肺泡表面活性物质替代治疗,研究组患儿在对照组基础上加入容量目标通气联合治疗,具体如下:设置呼吸机模式A/C+Vc,吸入氧浓度30%~80%、潮气量4~6 ml/kg、压力上限30 cm H2O、呼吸频率40~50次/min,呼气末正压5 cm H2O。根据患儿实际情况实时调节上述参数。
1.3 观察指标
检测两组患儿治疗前、治疗1周后的动脉血血气,包括动脉血氧分压(arterial partial pressure of oxygen,PaO2)、二氧化碳分压(arterial partial pressure of CO2,PaCO2)、氧指数(oxygenation index,OI)、血氧饱和度(blood oxygen saturation,SpO2)。同一时间点获取两组患儿的外周血标本,抗凝离心处理后留取上层血清,采用酶联免疫吸附法检测其中Th1细胞因子干扰素γ(Interferon-γ,IFN-γ)、Th2细胞因子白细胞介素-4(Interleukin-4,IL-4)的含量,并计算IFN-γ/IL-4比值;检测心肌损伤标志物肌钙蛋白Ⅰ(Troponin I,cTnI)、肌酸激酶同工酶(creatine kinase isoenzyme,CK-MB)及乳酸脱氢酶(lactate dehydrogenase,LDH)的含量。
1.4 统计学方法
数据分析采用SPSS 20.0统计软件,计量资料以均数±标准差(±s)表示,比较用t检验;计数资料以构成比表示,比较用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗前后PaO2、PaCO2、OI及SpO2比较
两组治疗前后PaO2、PaCO2、OI及SpO2比较,差异有统计学意义(P<0.05),研究组治疗前后PaO2、OI及SpO2的差值高于对照组,PaCO2的差值低于对照组。见表2。
2.2 两组治疗前后血清IFN-γ、IL-4及IFN-γ/IL-4比较
两组治疗前后血清IFN-γ、IL-4及IFN-γ/IL-4的差值比较,差异有统计学意义(P<0.05),研究组治疗前后IFN-γ、IFN-γ/IL-4的差值低于对照组,而IL-4的差值高于对照组。见表3。
2.3 两组治疗前后血清cTnI、CK-MB及LDH比较
两组治疗前后血清cTnI、CK-MB及LDH比较,差 异有统计学意义(P<0.05),研究组治疗前后cTnI、CK-MB及LDH的差值均低于对照组。见表4。
表2 两组治疗前后PaO2、PaCO2、OI及SpO2比较 (n =21,±s)
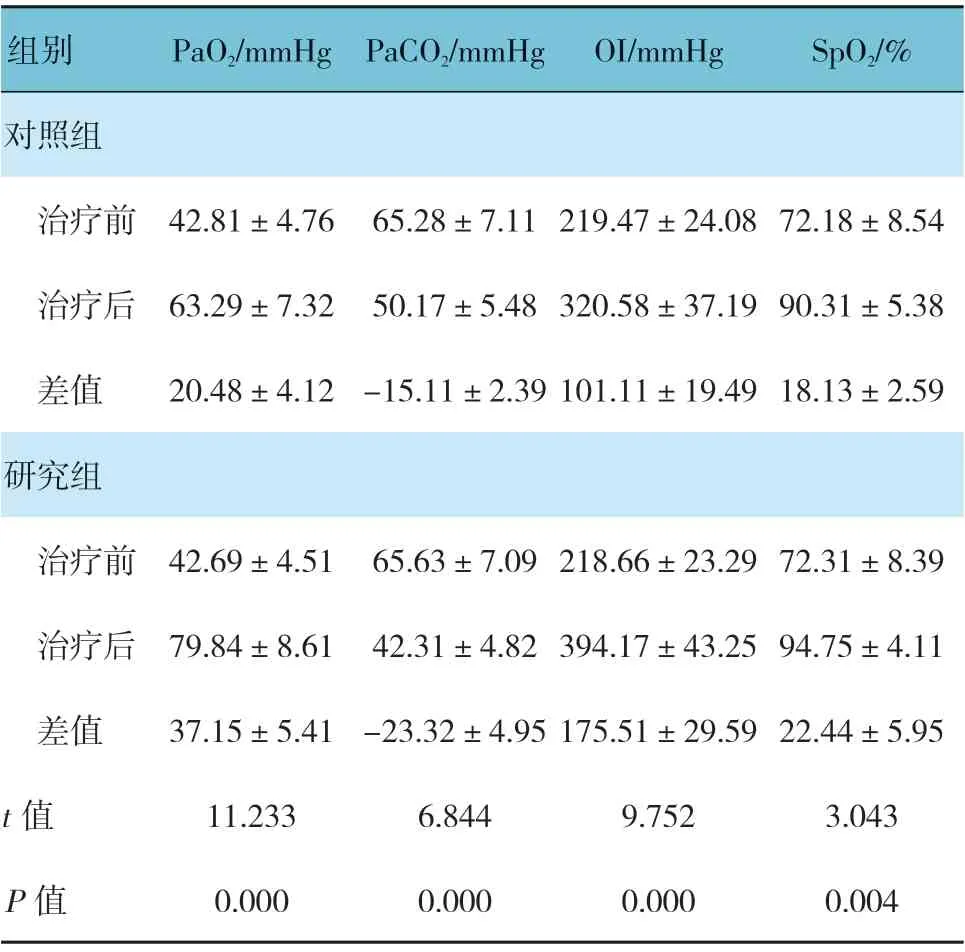
表2 两组治疗前后PaO2、PaCO2、OI及SpO2比较 (n =21,±s)
组别PaO2/mmHgPaCO2/mmHgOI/mmHgSpO2/%对照组 治疗前42.81±4.7665.28±7.11219.47±24.0872.18±8.54 治疗后63.29±7.3250.17±5.48320.58±37.1990.31±5.38 差值20.48±4.12-15.11±2.39101.11±19.4918.13±2.59研究组 治疗前42.69±4.5165.63±7.09218.66±23.2972.31±8.39 治疗后79.84±8.6142.31±4.82394.17±43.2594.75±4.11 差值37.15±5.41-23.32±4.95175.51±29.5922.44±5.95 t值11.2336.8449.7523.043 P值0.0000.0000.0000.004
表3 两组治疗前后血清IFN-γ、IL-4及IFN-γ/IL-4比较 (n =21,±s)

表3 两组治疗前后血清IFN-γ、IL-4及IFN-γ/IL-4比较 (n =21,±s)
组别IFN-γ/(pg/ml)IL-4/(pg/ml)IFN-γ/IL-4对照组 治疗前274.18±30.58104.38±12.732.31±0.29 治疗后137.84±15.19141.62±15.390.97±0.15 差值-136.34±25.8537.24±6.42-1.34±0.21研究组 治疗前273.39±29.74103.95±13.182.29±0.25 治疗后84.51±9.22178.61±20.450.56±0.08 差值-188.88±35.8274.66±10.39-1.73±0.31 t值5.45114.0404.773 P值0.0000.0000.000
表4 两组治疗前后血清cTnI、CK-MB及LDH比较 (n =21,±s)

表4 两组治疗前后血清cTnI、CK-MB及LDH比较 (n =21,±s)
组别cTnI/(μg/L)CK-MB/(u/L)LDH/(u/L)对照组 治疗前19.48±2.1124.18±2.79279.47±30.41 治疗后15.23±1.7117.34±1.88213.58±24.21 差值-4.25±0.62-6.84±0.94-65.88±9.12研究组 治疗前19.53±2.0724.31±2.68279.51±32.75 治疗后11.04±1.3811.06±1.53147.09±16.23 差值-8.49±1.15-13.25±1.85-132.42±20.32 t值14.87214.15613.692 P值0.0000.0000.000
3 讨论
NRDS的发生基于内源性肺泡表面活性物质缺乏,导致患儿肺泡表面张力增加,无法进行有效血气交换,从而发生低氧血症。在外源性肺泡表面活性物质替代治疗基础上,恰当的呼吸支持可进一步优化NRDS病情。传统压力通气模式已经在诸多研究中被证实可增加患儿肺泡通气量并提升血氧饱和度,但也有不少案例显示随通气时长增加患儿可出现呼吸机相关肺损伤,甚至最终导致肺泡通气量转折性下降。容量目标通气是一种通过容量目标压力模式实现通气支持的方式,其可实时感知患儿胸廓及肺顺应性,确保通气量不会超出既定的呼气末压力上限,同时又能最大程度增加肺通气[6-8]。本研究将传统压力控制通气模式、容量目标通气分别联合外源性肺泡表面物质用于NRDS患儿的治疗,探讨不同通气模式辅助治疗下患儿病情的变化情况,以期选出更为理想的通气模式用于后续同类疾病的治疗。
NRDS患儿肺泡进行性萎陷导致肺泡通气量不足,血氧交换减少,患儿体内二氧化碳蓄积、氧含量减少,最终导致呼吸衰竭发生[9]。动脉血气检测是判断NRDS病情的最直观手段[10]。本研究首先比较两组患儿的动脉血气差异,与治疗前比较,两组患儿治疗1周后PaO2、OI及SpO2均提高,而PaCO2降低;进一步与对照组比较,研究组治疗1周后PaO2、OI、SpO2提高,PaCO2降低,说明容量目标通气模式联合外源性肺泡表面活性物质治疗可更为有效地优化NRDS患儿的通气功能,缓解病情,宏观证实了该治疗方式的有效性。
炎症与NRDS的发生密切相关,随患儿病情进展、全身炎症反应加剧。Th1/Th2细胞参与NRDS患儿的炎症进程,Th1细胞分泌IFN-γ等促炎介质,在多种炎症性疾病中其表达量增加[11-12];Th2细胞分泌IL-4等抗炎因子,可促进抗体产生并介导机体体液免疫,其表达被抑制,减弱机体抗炎系统功能[13]。本研究检测两组患儿的Th1/Th2细胞因子含量,与治疗前比较,两组患儿治疗1周后血清IFN-γ、IFN-γ/IL-4降低,IL-4增加;进一步与对照组比较,研究组患儿治疗1周后血清IFN-γ、IFN-γ/IL-4较低,IL-4较高,证实容量目标通气联合外源性肺泡表面活性物质治疗可更为有效地均衡Th1及Th2细胞功能,抑制NRDS患儿的全身炎症反应,这也是其改善NRDS患儿整体病情的重要机制之一。
NRDS病情持续加重可出现全身重要器官缺氧性损伤,其中心肌细胞对缺氧的敏感性最高,依据持续缺氧后早期出现心肌细胞功能损伤,是判断患儿心肌损伤存在与否及严重程度的客观方式[14-15]。cTnI、CK-MB及LDH均是临床应用最多的心肌损伤标志物[16-17]。本研究比较两组患儿血清中上述因子含量的差异,与治疗前比较,两组患儿治疗1周后血清cTnI、CK-MB及LDH的含量降低;进一步与对照组比较,研究组患者治疗1周后血清cTnI、CK-MB及LDH的含量较低。证实NRDS患儿接受容量目标通气联合外源性肺泡表面活性物质治疗可有效保护心肌细胞功能,避免心脏损伤发生。
综上所述,NRDS患儿在外源性肺泡表面活性物质治疗的同时选择容量目标通气模式进行辅助通气,相较于传统压力控制通气模式,可更为有效地优化患儿通气功能并减轻全身炎症反应,保护心肌细胞,值得在日后临床实践中推广应用。

