新型酰腙类荧光探针的合成及其对Al(Ⅲ)的传感性质
龙昭现,李晓红,江光奇,2*
(1.贵州大学 化学与化工学院,贵州 贵阳 550025;2.贵州大学 精细化工研究开发中心 绿色农药和农业生物工程教育部重点实验室,贵州 贵阳 550025)
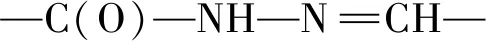
1 实验部分
1.1 仪器与试剂
Bio-Rad型傅立叶红外光谱仪(德国布鲁克公司),KBr压片;JEOL ECX 500 MHz核磁共振仪(日本电子公司),核磁测定以四甲基硅烷(TMS)为内标,二甲基亚砜(DMSO)-D6为溶剂;UV-1800 紫外分光光度计(日本岛津公司);Cary Eclipse荧光分光光度计(美国瓦里安公司);Agilent LC/MSD型质谱仪(美国安捷伦公司)。
1,2,4,5-四溴甲基苯、异烟肼、烟酸酰肼、2,4-二羟基苯甲醛(阿拉丁化学试剂公司),其它试剂均为市售分析纯,金属离子水溶液由相应金属离子的硝酸盐或氯化物配制,实验用水为二次蒸馏水。
1.2 探针1及2的合成
在250 mL圆底烧瓶中加入2.25 g(4.7 mmol)的1,2,4,5-四溴甲基苯、2.76 g(20 mmol)的2,4-二羟基苯甲醛和2.1 g(20 mmol)的碳酸氢钾及100 mL丙酮,加热回流7 d,固体产物使用N,N-二甲基甲酰胺(DMF)重结晶两次后得到产物1,产率为54.6%。产物1的IR(KBr/cm-1):3 448 s,3 090 s,2 852 vs,1 642 vs,1 503 vs,1 430 vs,1 376 vs,1 290 vs,1 226 vs,998 vs,834 vs,798 vs;1H NMR(500 MHz,DMSO-D6)δ:11.03(s,4H,—OH),9.98(s,4H,—CHO),7.69(s,2H,Ar—H),7.61(d,4H,Ar—H),6.63(s,4H,Ar—H),6.56(d,4H,Ar—H),5.32(s,8H,—O—CH2)。
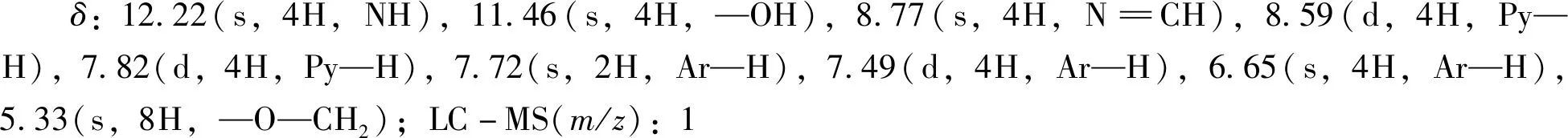
1.3 溶液配制与光谱测定
准确称取0.115 5 g的探针1或2于10 mL容量瓶中,用DMSO溶解后定容,得到1.0×10-2mol/L的储备液;金属离子储备液的浓度均为1.0×10-2mol/L。分别在10 mL的容量瓶中加入探针1或2的储备液10 μL,再加入金属离子储备液50 μL,用DMSO-H2O(7∶3,体积比)定容,探针的浓度为1.0×10-5mol/L,金属离子的浓度为5.0×10-5mol/L。溶液在室温下放置4 h后进行荧光测定,测定的激发波长分别为385 nm和381 nm,激发/发射狭缝为5 nm/5 nm,电压分别为550 V和600 V。
2 结果与讨论
2.1 探针与Al3+的紫外光谱
在DMSO-H2O(7∶3,体积比)体系中测定了Al3+对探针紫外吸收光谱的影响,如图2所示,探针1和2分别在337 nm和333 nm处有一个最大吸收峰,随着Al3+浓度(0~4.0×10-5mol/L)逐渐增加,该两处的吸收峰强度逐渐减弱,并分别在390 nm和383 nm处出现了新的峰,且分别在361 nm和356 nm处出现了等吸收点,表明探针1和2与Al3+生成了稳定的配合物[13-14]。
2.2 探针与Al3+的荧光光谱
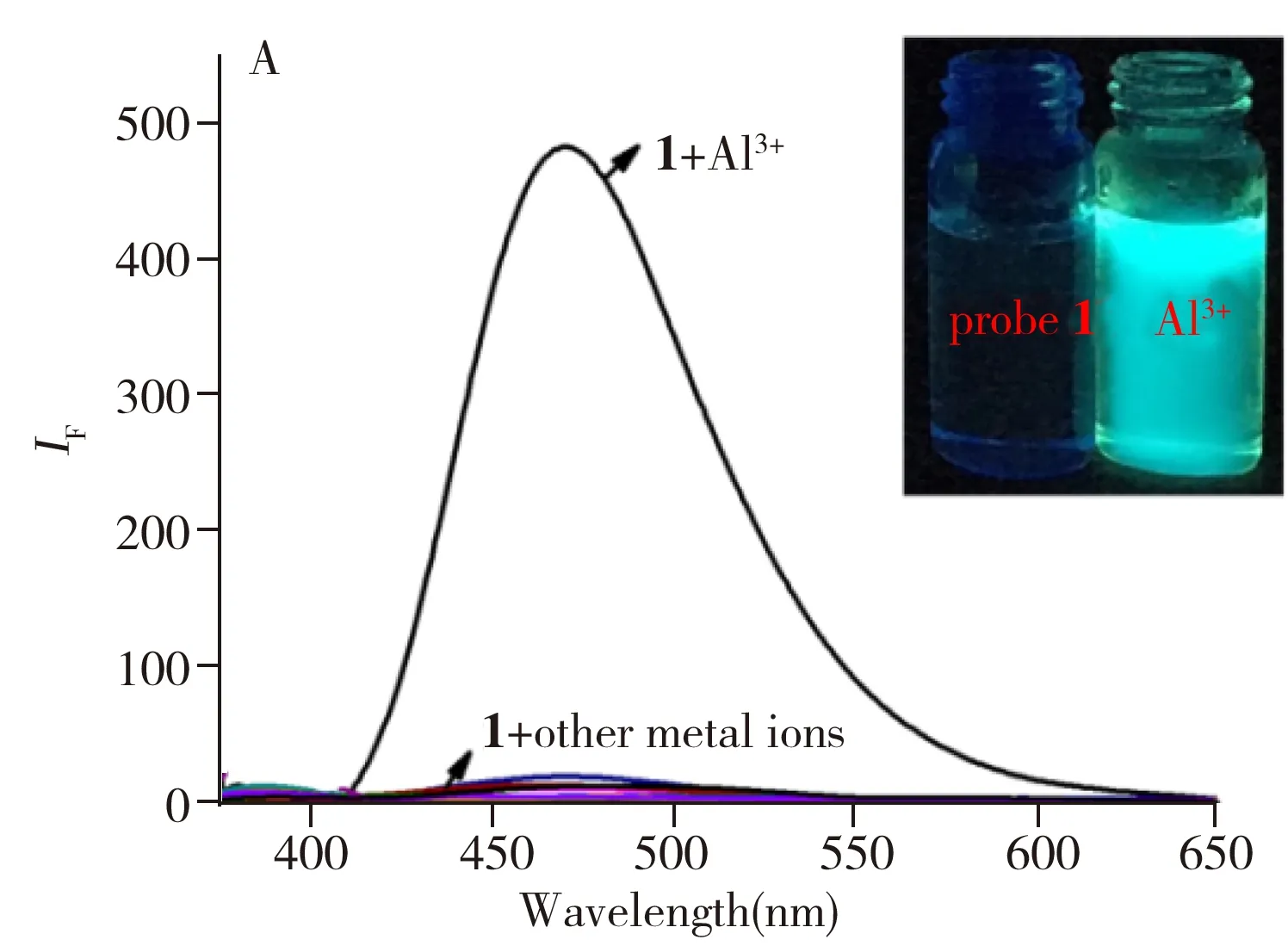
在探针1和2(1.0×10-5mol/L)的溶液中分别加入5.0×10-5mol/L的Zn2+、Cr3+、Cd2+、Co2+、Al3+、Mn2+、Fe3+、Ca2+、Ni2+、Cu2+、Pb2+、Hg2+、K+、Mg2+金属离子溶液,发现两者分别在478 nm和460 nm对Al3+有明显的荧光增强现象,分别出现了肉眼可识别的草绿色和蓝紫色荧光,而上述其它金属离子的荧光增强不显著,如图3所示。
考察了Al3+浓度对体系荧光强度的影响,当Al3+的浓度达到探针浓度的两倍时,体系的荧光强度基本不变,说明探针1和2与Al3+的配位达到了饱和,配位比为1∶2。体系的荧光强度(y)与Al3+浓度(x)在2~18 μmol/L范围内呈良好的线性关系,线性回归方程分别为y=18.478x+28.241(r2=0.987 1)和y=27.946x+12.247(r2=0.985 5)。根据3σ/K方法(σ为空白液的标准方差,K为斜率)计算出探针1和2对Al3+的检出限分别为9.58×10-8mol/L和6.52×10-8mol/L[15]。
2.3 探针与Al3+的配位比及结合常数
根据Job's法,保持体系总浓度不变,逐渐改变探针1和2与Al3+的浓度比,测定体系的荧光强度,以[探针]/[探针+Al3+]为横坐标,分别以385 nm和381 nm处的荧光强度为纵坐标,得到探针与Al3+的Job's曲线图,两条曲线均在0.33左右的位置出现了拐点,说明探针1和2与Al3+的配位比为1∶2。另外根据Benesi-Hildebrand方程[16],以Al3+浓度的倒数为横坐标(x),1/(IF-IF0)为纵坐标(y),线性拟合后的方程分别为y=1.789×10-7x+9.661×10-4(r2=0.997 3)和y=2.044×10-7x-6.419×10-4(r2=0.991 8),可以计算出探针1和2与Al3+的结合常数分别为5.42×103L/mol和3.14×103L/mol。
2.4 竞争离子选择性实验
为了进一步研究其它金属离子共存时对探针1、2检测Al3+的干扰,进行了竞争离子选择性实验。实验发现,Zn2+、Cr3+、Cd2+、Mn2+、Fe3+、Ca2+、Pb2+、Hg2+、K+、Mg2+对探针检测Al3+没有明显的干扰,而Ni2+和Co2+会使荧光强度稍微减弱。但自来水、河水实际水样中一般不含Ni2+和Co2+,因此,Ni2+和Co2+对探针检测水中Al3+无影响。
2.5 探针与Al3+的配位模式及传感机理

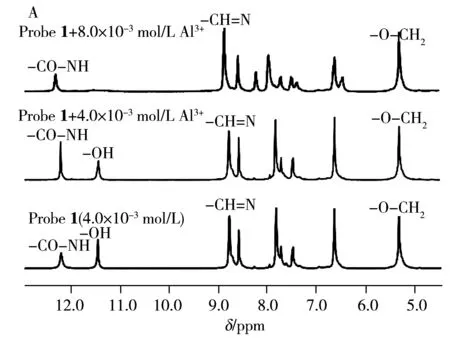

2.6 实际水样中Al3+离子的测定
为了考察探针1和2的在实际水样中的应用,取贵阳市花溪区花溪河水和花溪自来水厂的自来水进行了Al3+的回收率实验。水样未经任何前处理,按体积比(1∶19)与探针1或2的DMSO溶液(1.0×10-5mol/L)混合。向两种实际水样中加入10 μmol/L的Al3+,通过测定体系的荧光强度,计算得出Al3+的含量,实验结果如表1所示。Al3+的实测结果与理论加入量能较好地吻合,相对标准偏差较小。因此,探针1和2可应用于实际水样中一定浓度范围内Al3+的检测。

图5 探针1和2对Al3+的荧光传感机理Fig.5 Sensing mechanism of probes 1 and 2 to Al3+
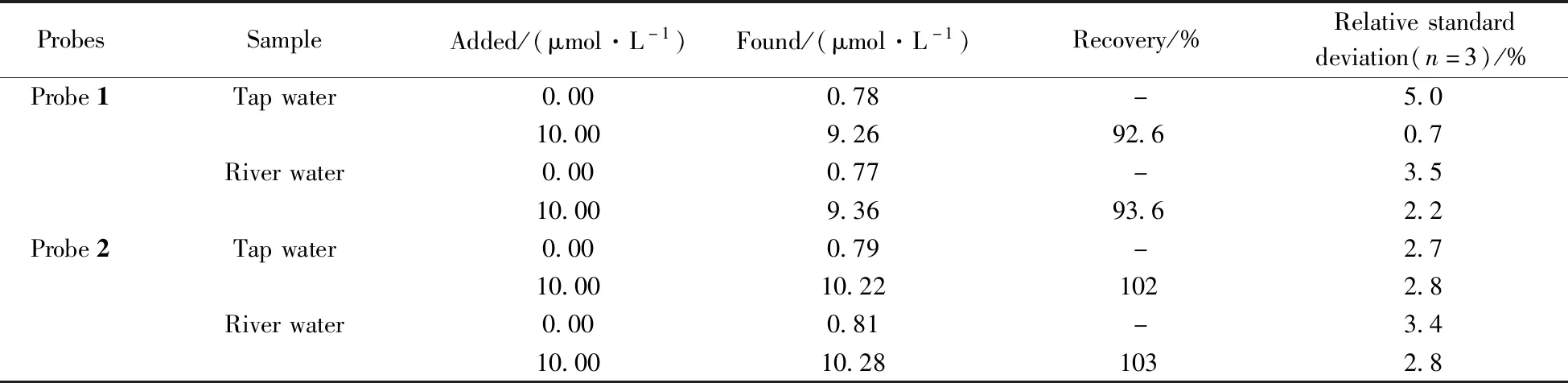
ProbesSampleAdded/(μmol·L-1)Found/(μmol·L-1)Recovery/%Relativestandarddeviation(n=3)/%Probe1Tapwater0.000.78-5.010.009.2692.60.7Riverwater0.000.77-3.510.009.3693.62.2Probe2Tapwater0.000.79-2.710.0010.221022.8Riverwater0.000.81-3.410.0010.281032.8
3 结 论
本文合成了两个新型酰腙类荧光探针1和2。利用紫外可见光谱法、荧光光谱法、核磁共振波谱法和质谱等方法研究了两者对Al3+的选择识别作用,实验结果表明探针1和2与Al3+络合比为1∶2,两者对Al3+的检出限达到了10-8mol/L水平,远低于世界卫生组织饮用水的标准(7.4 μmol/L)[19]。此外,探针1和2可直接用于河水和自来水中Al3+的检测,具有一定的实用价值。

