PVP与PKP手术治疗Genant 3级骨质疏松性椎体压缩骨折:术后延迟性椎体高度丢失的比较
李青松,章玉冰,陶学顺,李勇
(安徽省第二人民医院骨三科,安徽 合肥 230031)
骨质疏松症是一种全身性骨骼疾病,患者骨量减少,微结构恶化,导致脆性骨折的风险增加,尤以骨质疏松性椎体压缩骨折 (osteoporotic vertebral compression fractures,OVCF)多见[1]。自 Galibert等人于1987年报道经皮椎体成形术(Percutaneous vertebroplasty,PVP)以来,经皮骨水泥强化技术已广泛应用于OVCF和脊柱肿瘤等疾病的治疗中,取得了显著疗效[2]。经皮椎体后凸成形术(Percutaneous kyphoplasty,PKP)是PVP基础上的改良技术,利用球囊扩张作用以恢复压缩椎体的高度。多项系统回顾分析表明,上述两种术式均可减轻疼痛、改善功能和生活质量,且并未增加意外骨折、感染、脊髓压迫、呼吸衰竭和死亡率等不良事件[3]。关于PVP与PKP技术在严重塌陷OVCF(Genant半定量分级为3级,椎体高度丢失>40%)的临床表现,既往文献多偏重于骨水泥渗漏和伤椎矫正度的比较;而在随访期间的延迟性椎体高度丢失方面,目前尚罕见相关对比研究。为此,本研究于2015年9月~2017年9月进行了一项分组对比研究,分别行PVP/PKP手术治疗严重塌陷的OVCF患者共46例,以探讨两种术式的疗效、并发症,以及术后随访期间的延迟性椎体高度丢失情况。
1 资料与方法
1.1 样本选择
本研究得到了我院医学伦理委员会的审查批准,经过严格筛选和患者提供书面知情同意后,于2015年9月~2017年9月纳入46例Genant半定量分级为3级的OVCF患者。入选标准如下:①年龄65岁以上;②腰痛时间<3周;③自测视觉模拟评分(Visual analogue scale,VAS)疼痛评分至少7分(范围0~10分);④胸腰椎单节段骨折 (T10-L2);⑤基于Genant半定量分级,均为3级,椎体塌陷 >40%;⑥临床及影像学资料完整。排除标准:①高能外伤后骨折;②既往有脊柱融合史;③椎体骨折块压迫椎管;④脊柱恶性肿瘤,急性感染,神经系统并发症;⑤骨折椎数量>1个;⑥存在骨水泥增强的禁忌证,如凝血病、对水泥或造影剂过敏或全身感染。
1.2 手术方法
在对PVP和PKP技术的相关知识进行了充分讲解后,由患者选择自己的手术方式。局部麻醉下,患者俯卧,术中使用脉搏血氧仪和血压监测仪监测,经皮穿刺和骨水泥填充过程均在X线透视监视下进行。骨水泥材料为:聚甲基丙烯酸甲酯(PMMA)。两种术式均采用双侧经椎弓根入路,PVP技术:术中透视确认穿刺针抵达理想位置后,将调制成牙膏状的骨水泥缓缓注入伤椎内部,直至填充理想或有骨水泥渗漏迹象时,立即停止注射。PKP技术:待穿刺针到达椎体前1/3处,更换工作套管,用骨钻在椎体内建立一工作通道,在通道里置入扩张球囊,撑开球囊,将塌陷的椎体充分膨胀、矫正满意后,移除球囊,缓缓注入调制成牙膏状的PMMA骨水泥。
1.3 观察指标
临床指标:采用双能X线骨密度仪测定患者骨密度;临床记录术前、术后3 d、术后1、3、6和12个月的VAS评分、Oswestry功能障碍指数(oswestry disability index,ODI)。影像学指标:分别于统一时间点,摄取所有患者站立侧位脊柱X线片,测量前1/3、中1/3和后1/3处的椎体高度,椎体相对高度=最小高度/邻近椎体高度的平均值×100%;采用Cobb法测定T10与L2之间的节段后凸角。安全性指标:记录治疗过程中发生的不良事件。
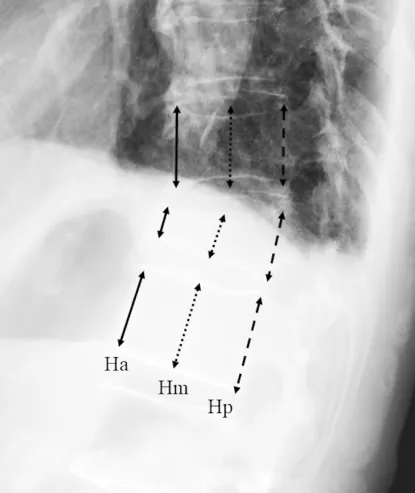
图1 椎体高度测量
1.4 统计学分析
使用Mannw-Hitney U检验比较两组的体重指数、骨密度值、椎体高度、VAS评分和ODI评分等数据;在每组中,使用重复测量t检验比较每个时间点的参数;使用x2检验和Fisher精确检验比较两组间的并发症发生率。以P<0.05为差异有统计学意义。
2 结果
2.1 基线资料比较
本研究共纳入46例严重塌陷的OVCF患者,其中27例接受PVP治疗,19例接受PKP治疗。两组基线数据进行处理,差异均无统计学意义(表1),有可比价值。
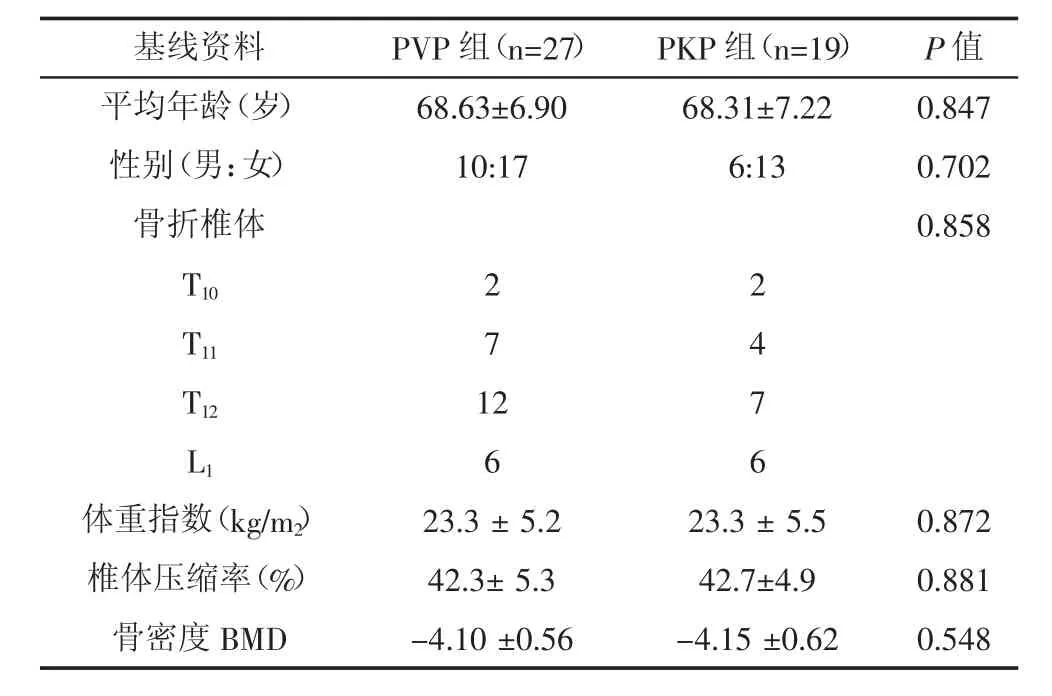
表1 两组严重塌陷OVCF患者的基线资料比较
2.2 临床疗效比较
两组术后疼痛(以VAS评分表示)和功能障碍(以ODI评分表示)均有改善,如图2-3所示,VAS评分和ODI指数均随时间而显著降低(P<0.05)。但组间比较,无论在任何时间点,PVP和PKP组之间的VAS评分或ODI指数均无显著性差异(P>0.05)。

图2 两组患者手术前后的VAS评分比较
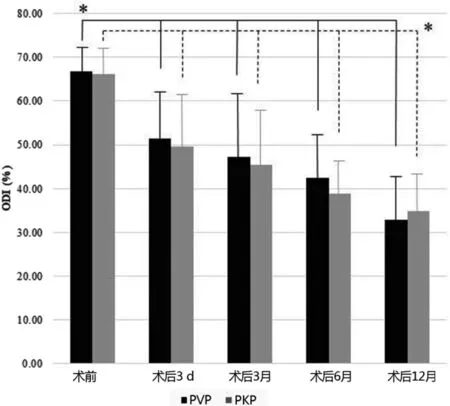
图3 两组患者手术前后的OD指数比较
2.3 影像学指标比较
椎体矫正方面,PKP组术后3 d的椎体相对高度显著优于PVP组 [(79.5±5.6)%vs(70.2±4.6)%,P<0.001]。两组随访期间均出现延迟性椎体高度丢失,且以PKP组的椎体高度丢失更为明显。随访6个月内,PKP组的椎体高度值仍显著大于PVP组(P<0.05),但术后12个月时,两组椎体相对高度已变得相对接近 [PKP组为 (70.2±6.3)%,PVP组为 (67.0±5.2)%,P=0.075]。两组数据变化见图4。
两组术后的节段性后凸角度均有明显改善(均为P<0.05),而随访期间均有延迟性丢失现象,但组间比较,PKP和PVP的差异无统计学意义(P=0.377)两组数据变化见图5。
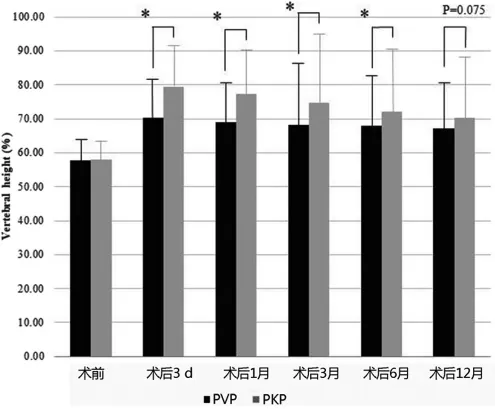
图4 两组手术前后的相对椎体高度(%)比较
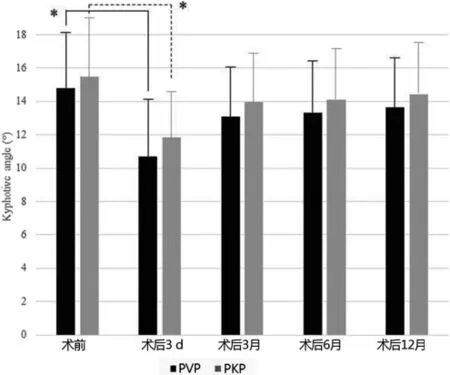
图5 两组手术前后的节段性后凸角比较
2.4 并发症分析
PVP组1例女性患者在术中出现短暂的一过性血压降低现象,而后自行恢复。术后X线检查发现,PVP组10例和PKP组5例患者发生骨水泥渗漏。15例骨水泥渗漏患者中,1例发生椎管内渗漏,5例发生椎间盘内渗漏,9例为椎管外渗漏。上述15例患者均未出现明显症状,未予特殊处理。随访期间,PVP组6例、PKP组4例发生邻近椎体骨折;其中,PVP组3例、PKP组1例,均为3个月内出现新发骨折。上述10例患者均接受止痛和支具等保守治疗后获得痊愈。两组患者的上述并发症比较,差异均无统计学意义(P>0.05)。
3 讨论
OVCF的治疗目标是通过缓解疼痛和改善功能障碍以恢复生活质量。与保守治疗相比,PVP与PKP技术均可快速减轻疼痛[4],改善功能障碍。然而,这两种术式在有效性、安全性和经济适用性方面如何取舍,目前仍然存在争议。
本研究表明,此两种术式均可恢复椎体高度,在术后初期(3 d),使用球囊扩张的PKP手术明显优于PVP。但是随着时间的推移,我们观察到46例患者椎体高度均出现延迟性丢失现象,且PKP组的高度丢失更为显著(图4)。在1年的随访中,两组之间的椎体高度差异已变得微不足道 (P=0.075)。我们认为,在没有伤椎再发骨折的情况下,由于骨硬度的降低,可出现边缘性骨坏死和骨水泥收缩,从而导致术后高度丢失这一现象[5]。PKP是通过球囊扩张以恢复伤椎高度,这一过程使得松质骨更为紧致,可能影响了骨水泥在骨小梁中间的渗透、交互耦合过程,因而术后X线片上骨水泥以边缘光滑的团块状分布最为常见;而在PVP术后,由于骨小梁并未被进一步破坏,通常可见骨水泥与骨小梁的交互耦合现象[6]。Togawa等人[7]的动物研究表明,PKP术中的球囊扩张可压缩周边的骨小梁,使得骨水泥与骨小梁的交互耦合百分比较低。研究认为,骨小梁-骨水泥界面的交互耦合,有助于载荷在伤椎的上、下终板间顺利传递。Kim等[8]在尸体OVCF模型中也显示,PKP样本的压缩刚度要低于PVP样本,导致其在循环加载过程中出现明显的渐进椎体高度丢失。上述学者的研究,亦证实了本文结论。我们认为,PKP术后的延迟性椎体高度丢失现象,可能是由于术后骨小梁-骨水泥界面未能产生良好的交互耦合,在生物力学载荷的反复加载影响下,导致骨水泥周围骨小梁吸收有关。
在本研究中,两组患者疗效无显著差异。两组患者术后VAS评分均立即下降,随访时VAS评分仍较低。Zhao等[9]报道中,PKP的止痛效果表现明显优于PVP。但Chen等[10]和Gu等[1]则报道了PVP和PKP在术后早期和术后12个月的VAS评分和ODI指数比较,并未见显著差异,其结论与本文相同。骨水泥渗漏和术后再发邻近椎体骨折,是此类手术最常见的并发症。前人研究一致认为,PVP在骨水泥渗漏方面,较PKP技术更为严重[1,11]。本研究中,PVP术后渗漏率为 37.04%(10/27),PKP 术后为 26.32%(5/19),虽然PVP的渗漏率更高,但组间差异并不显著(P=0.445),这可能与样本量较少有关。本研究中,所有10例再发骨折患者均接受了成功的保守治疗,由于样本数偏少,我们无法报告严重并发症的重要数据。尽管PVP和PKP是微创手术,也可能会发生严重并发症,包括感染、休克、截瘫和肺栓塞等。但据临床报道,上述不良事件的发生率非常低[12],本研究并未发生上述并发症案例。
本研究存在一定的局限性,包括患者数量偏少,缺乏随机化分组,且没有长期结果。此外,一些影响骨水泥强化效果的因素并没有考虑,如骨水泥粘度和体积等,这些因素对骨水泥渗漏和填充效果均有所影响。而其他临床情况,如骨坏死,则需通过组织学分析来研究。

