镍锰酸锂正极材料及其适配性电解液研究最新进展
李 旺,周 兰,刘佳丽
(上海电气集团股份有限公司中央研究院,上海200070)
2015年5月8日国务院发布《中国制造2025》,将新能源汽车作为重点领域推动发展,明确提出继续支持电动汽车发展,提升动力电池核心技术的工程化和产业化能力,推动自主品牌新能源汽车同国际先进水平接轨。据统计,2016年中国汽车产销突破2 800万辆,新能源汽车产销量超过50万辆,累计推广量超过100万辆,全球占比均超过50%,市场认可度大幅提高。2017年4月25日工业和信息化部、国家发展改革委、科技部联合印发《汽车产业中长期发展规划》的通知明确提出:到2020年,中国新能源汽车年产销达到200万辆,动力电池单体比能量达到300 W·h/kg以上,系统比能量力争达到260 W·h/kg、成本降至 1 元/(W·h)以下;到 2025 年,新能源汽车占汽车产销20%以上,动力电池系统比能量达到350 W·h/kg。
为满足上述要求,开发出具有高能量密度、低成本的正负极材料以及适配性的电解液是当下研究的热点。 在众多锂电池正极材料中,LiNi0.5Mn1.5O4材料[1-3]以其高电压(4.7 V,vs.Li/Li+)、高能量密度(达650 W·h/kg)、资源丰富且价格低廉而受到广泛关注,是下一代高能量密度动力电池正极材料的主要研究方向。然而,LiNi0.5Mn1.5O4材料在长期充放电循环过程中,Mn从电极材料中溶解,破坏了电极材料的结构,导致电池性能恶化。离子掺杂[4-7]、表面包覆[8-10]、复合方法[11]是改善 LiNi0.5Mn1.5O4材料电化学性能的有效途径。同时,开发出与之相适应的高电压电解液,提高LiNi0.5Mn1.5O4电极与电解液的界面稳定性[12],也是提升 LiNi0.5Mn1.5O4电池性能的重要方法。
1 镍锰酸锂正极材料
1.1 离子掺杂
通过 Mn、Ni、Li、O 位掺杂,影响 LiNi0.5Mn1.5O4材料晶体参数,可以提高材料的电导率,抑制电极与电解液的反应,改善Mn的溶解现象,提高材料的倍率与循环性能。
1)阳离子掺杂。Sun等[13]通过低温溶液燃烧法制备了 Cu2+掺杂的 LiNi0.5Mn1.5-xCuxO4(x=0、0.03、0.05、0.10、0.15)材料。 Cu2+进入晶体中占据 Mn4+位,使得晶体参数增大,有利于Li+扩散。Cu2+的加入没有引起新的物相生成,随着Cu2+含量增多,材料排列的有序性增强,其循环性能得到显著提高;同时随着Cu2+含量增多,材料的一次颗粒减小,其倍率性能得到提升,10C倍率循环100次,x=0.05材料的容量保持率为98.0%,纯 LiNi0.5Mn1.5O4材料容量保持率仅为85.5%(见图 1)。

图1 LiNi0.5Mn1.5-xCuxO4的SEM照片(a~e)及其25℃条件下10C倍率循环性能图(f)
Wu 等[14]采用固相法制备了 Ce4+掺杂的 Fd3m空间 结 构 的 LiCexNi0.5-xMn1.5O4(x=0、0.005、0.01、0.02)材料。Ce4+进入LiNi0.5Mn1.5O4晶体结构中占据Ni2+的位置,由于电荷补偿作用,部分Mn4+转化成Mn3+使得晶体参数增大。Ce4+的掺杂可以有效地抑制LixNi1-xO杂质相的产生,降低Li+与过渡金属离子的混乱度,增加了Ni/Mn的无序排列程度,但是Ce4+掺杂量较多时(x=0.02)会出现CeO2相。x=0.005时10C/0.2C倍率放电为94.82%,1C倍率循环100次容量保持率为94.51%;纯LiNi0.5Mn1.5O4材料10C/0.2C倍率放电为82.18%,1C倍率循环100次容量保持率为89.24%。李渊等[15]以Cr为掺杂剂,蔗糖、葡萄糖、柠檬酸为碳源,采用高温固相法制备出LiCr0.2Ni0.4Mn1.4O4材料。Cr的添加既取代Mn位同时也占据Ni位,碳源起到均匀分散前驱体和抑制烧结过程中晶粒过度生长的作用。研究结果表明,采用柠檬酸为碳源制备的LiCr0.2Ni0.4Mn1.4O4材料具有最好的电化学性能,0.5C倍率充电1C倍率放电,放电比容量为149 mA·h/g,循环100次容量保持率为98%。Wang等[16]采用固相法合成了Na+掺杂的Li0.95Na0.05Ni0.5Mn1.5O4材料(LNMO-Na),Na+进入材料晶体中占据Li的8a位置,迫使等量的Li+占据八面体的16d位置,致使晶体的结构稳定性变差。Na+的掺杂抑制了LixNi1-xO杂质相的生成,增加了Ni/Mn的无序排列程度,减小了一次粒子颗粒尺寸,降低了电荷的传递阻抗,提升了材料的倍率性能。图2为LNMO-Na和LNMO在不同倍率下的倍率性能。由图2可以得出,0.2C~10C不同放电倍率下,LNMONa材料的放电倍率性能优于纯LNMO材料。

图2 LNMO-Na和LNMO在不同倍率下的倍率性能
2)阴离子掺杂。Luo 等[17]采用 NH4F 和商业化的LiNi0.5Mn1.5O4为原材料,通过一步加热法制备出不同温度条件下合成的F-掺杂的LiNi0.5Mn1.5O4材料。F-占据O2-的位置,随着合成温度的升高,F-掺杂的LiNi0.5Mn1.5O4材料的晶格参数呈曾大趋势,比表面积呈下降趋势。当合成温度高于700℃时,材料的空间结构由有序的P4332构型向无序的Fd3m转化。当合成温度为400℃时,F-掺杂的LiNi0.5Mn1.5O4材料展现出较好的倍率性能与循环性能,F-在LiNi0.5Mn1.5O4表面富集,抑制了电极与电解液的反应,形成了薄且均匀的保护膜,同时也提高了电极的热稳定性。400℃时F-掺杂的LiNi0.5Mn1.5O4材料,5C倍率循环150次容量保持率为85.8%,产生的SEI膜分布均匀,厚度约为5 nm;而纯LiNi0.5Mn1.5O4材料5C倍率循环150次容量保持率小于20%,产生的SEI膜分布不均,厚度约为10 nm(见图3)。

图3 纯LNMO材料(a)、400℃制备的F-掺杂的LNMO材料(b)5C倍率循环150次TEM照片
1.2 表面包覆
表面包覆层可以抑制电极与电解液的相互作用,缓解HF对电极材料的侵蚀,降低Mn溶解现象,有利于提升材料的循环性能。常见的包覆物主要有金属氧化物、非金属氧化物、无机盐等。

图4 LNMO-T材料SEM照片(a)、高分辨率TEM照片(b)
1)金属氧化物包覆。 Jung等[18]采用湿化学法制备了 RuO2包覆的LiNi0.5Mn1.5O4材料,RuO2包覆量为 0.57%(质量分数)的 LiNi0.5Mn1.5O4材料(Ru2)具有最优的电化学性能,其电子电导率为0.27 S/cm。Ru2材料具有较高的电子电导率,提升了材料的倍率性能,当Super P(炭黑)添加量仅为1%(质量分数)时,1C倍率放电比容量为 100 mA·h/g,纯LiNi0.5Mn1.5O4材料1C倍率放电比容量几乎可以忽略。当活性物质担载量为5 mg/cm2时,Ru2材料0.5C倍率循环148次容量保持率为101.9%,纯LiNi0.5Mn1.5O4材料0.5C倍率循环148次容量保持率仅有90.9%。Tao等[19]采用固相合成法制备出LiNi0.5Mn1.5O4材料,将合成的LiNi0.5Mn1.5O4材料与钛酸四丁酯以物质的量比为10∶1混合,利用湿化学法制备出纳米二氧化钛包覆的LiNi0.5Mn1.5O4材料(LNMO-T)。 LNMO-T 材料表面光滑(见图 4),一次颗粒主要分布在300~500 nm,纳米二氧化钛包覆层分布均匀,包覆层厚度约为2 nm。纳米二氧化钛包覆层抑制了电极与电解液的相互作用,从而减少了Mn的溶解,提升了电极材料的循环性能。2C倍率循环500次LNMO-T电极容量保持率为88.5%,而纯LiNi0.5Mn1.5O4电极1C倍率循环500次,容量保持率为33%。
2)非金属氧化物包覆。Fan等[20]采用商业化的气相二氧化硅与镍锰酸锂材料作用,制备了不同质量分数二氧化硅包覆的镍锰酸锂材料。二氧化硅包覆层可以有效地消耗电解液中的HF,减少LiF在电极表面的沉积,有利于电极性能的提升。随着二氧化硅包覆量增加,循环后材料的容量保持率逐渐增大,高温(55℃)0.5C倍率循环100次,纯镍锰酸锂材料容量保持率为59%,采用0.5%、1%、3%气相二氧化硅包覆后容量保持率分别为69%、86%、87%。
3)无机盐包覆。 Mou 等[21]首先采用溶胶-凝胶法合成了LiNi0.5Mn1.5O4材料,将合成的LiNi0.5Mn1.5O4材料与La(NO3)3·6H2O、Fe(NO3)3·9H2O 通过湿化学法混合,制备出不同LaFeO3质量分数包覆的LiNi0.5Mn1.5O4材料。LaFeO3的引入没有严重地影响LiNi0.5Mn1.5O4材料的晶体结构,随着LaFeO3包覆量增加,晶格参数呈曾大趋势,有利于Li+嵌入与脱嵌。LaFeO3包覆在LiNi0.5Mn1.5O4材料表面,形成了有效的保护层,抑制了HF对电极材料的侵蚀,缓解了Mn的溶解现象,提高了材料的倍率性能和循环性能。高温(55℃)1C倍率循环100次,2%LaFeO3包覆的LiNi0.5Mn1.5O4材料容量保持率为93.29%,纯LiNi0.5Mn1.5O4材料为69.9%。10C倍率放电,2%LaFeO3包覆的LiNi0.5Mn1.5O4材料比容量为99.6 mA·h/g,纯LiNi0.5Mn1.5O4材料为 76.4 mA·h/g。 马腾飞等[22]首先通过高温固相法合成了形貌规则的尖晶石型LiNi0.5Mn1.5O4材料,水热条件下在其表面生长LiCoPO4纳米颗粒包覆层。适量的LiCoPO4包覆层不仅可以诱导LiNi0.5Mn1.5O4表面生成适量的Mn3+以提高材料的电导率和锂离子扩散速率,同时阻碍了Mn3+与电解液的直接接触,减缓了歧化反应及Mn2+的溶出。实验结果表明,5%LiCoPO4(质量分数)包覆的LiNi0.5Mn1.5O4材料具有最优的电化学性能,0.5C倍率充放电循环100次容量保持率为98.5%,20C倍率放电比容量为130 mA·h/g。
1.3 复合方法
通过离子掺杂与表面包覆相结合,可以有效地提高材料的电导率,抑制电极与电解液的相互作用,增强电极的稳定性。Xu等[23]采用碳酸盐共沉淀法合成出 F-掺杂的 LiNi0.5Mn1.5O4-xFx(x=0、0.02),然后通过与CH3COOLi和 Si(OC2H5)4反应,在 LiNi0.5Mn1.5O3.98F0.02材料表面形成Li4SiO4包覆层,最终制备出F-掺杂的Li4SiO4包覆的空心多孔结构的镍锰酸锂材料。空心多孔结构有利于电极与电解液的接触,有利于材料电化学性能的发挥;F-掺杂占据O2-位置,增强了镍锰酸锂材料的结构稳定性;Li4SiO4包覆层抑制了电极与电解液的反应,同时Li4SiO4为Li+提供三维传输网络,是良好的Li+导体,降低了电极阻抗,进一步提高了电极性能。2%Li4SiO4(质量分数)包覆的LiNi0.5Mn1.5O3.98F0.02材料具有较好的电化学性能,高温(55℃)5C充放电循环100次后容量保持率为94.2%,而纯LiNi0.5Mn1.5O4材料仅为54.9%。
2 高电压电解液
随着高电压正极材料研究的逐步深入,与之相匹配的高电压电解液的研究受到广泛关注。传统的碳酸酯基电解液在4.5 V以上会发生分解,导致电池性能迅速恶化,使得高电位的正极材料的应用受到阻碍。通过引入成膜添加剂、改变锂盐的种类或浓度、调整主溶剂的种类及比例等方法,可以提高电解液的耐高压性能,推动高电压材料电池体系的商业化进展。
1)成膜添加剂的影响。在传统的碳酸酯基溶剂电解液中,加入成膜添加剂可以优先碳酸酯基溶剂氧化分解,形成稳定的SEI膜,抑制电极与电解液的进一步反应,增强电极的稳定性。Chen等[24]采用1 mol/L的LiPF6-EC(碳酸乙烯酯)/DEC(碳酸二乙酯)/DMC(碳酸二甲酯)(3∶5∶2,体积比)为基础电解液(STD),选用 TMB(硼酸三甲酯)、TEB(硼酸三乙酯)为成膜添加剂,来研究其对镍锰酸锂半电池的影响。充电过程中TMB与TEB优先氧化分解,产生薄且稳定的保护膜覆盖在电极表面,有效地抑制了碳酸基类电解液与电极材料的分解,提高了半电池的循环性能。当TMB与TEB添加量均为2%(质量分数)时,展现出较好的循环稳定性。1C倍率循环600次,基础电解液半电池容量保持率为23.4%,添加2%TMB的半电池容量保持率为85.3%,添加2%TEB的半电池容量保持率为72.6%。将循环后的半电池拆开,取出对电极测试Mn、Ni含量,添加2%TMB的对电极Mn、Ni含量最少,而基础电解液对电极 Mn、Ni含量最高(见图 5)。任春燕等[25]以 1 mol/L的LiPF6-EC(碳酸乙烯酯)/DEC(碳酸二乙酯)/EMC(碳酸甲乙酯)(1∶1∶1,体积比)为基础电解液,选用DMNB(1,2-二甲基-4-硝基苯)为正极成膜添加剂,研究其对镍锰酸锂半电池的影响。DMNB优先于电解液主溶剂发生氧化反应,在正极表面形成稳定的SEI膜,增强了电极的稳定性。研究结果表明,DMNB添加量为0.2%(质量分数)时,具有较好的电化学效果,室温循环100次容量保持率为97.2%,而基础电解液仅为93.1%。
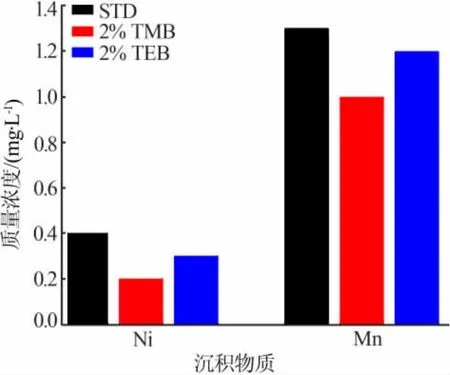
图5 在STD、TMB、TEB电解液中循环后锂片电极上Ni和Mn的沉积含量
2)锂盐的影响。锂盐是电解液的重要组成部分,调整锂盐浓度以及探索不同新型锂盐如LiODFB(二氟草酸硼酸锂)、LiBOB(双乙二酸硼酸锂)、LiTFSI(双三氟甲基磺酰亚胺锂)等对电解液的影响,也是电解液研究的重点方向。Drozhzhin等[26]以LiBF4为锂盐、PC(碳酸丙烯酯)为溶剂,制备了0.83、1.66、2.49 mol/L 3种不同锂盐浓度的电解液。随着锂盐浓度的增加,镍锰酸锂半电池的库伦效率逐渐增大,每个循环间的容量损失减少。在不同锂盐浓度的电解液循环后,电极表面组成成分没有明显不同,将在2.49 mol/L的高浓度锂盐电解液中形成SEI膜的电极放在0.83 mol/L的低浓度锂盐电解液中测试,并未明显改变0.83 mol/L低浓度锂盐半电池的电化学性能,表明电化学稳定性是由电解液的组成决定的,而不是CEI界面性质。
3)溶剂的影响。采用耐高压性更强的溶剂代替碳酸酯基溶剂是实际可行的办法,如氟代溶剂、腈类有机溶剂、砜类有机溶剂等,是目前研究集中的领域。 Zhao 等[27]为改善 0.7 mol/L 的 LiDFOB(二氟草酸硼酸锂)-EC (碳酸乙烯酯)/EMC (碳酸甲乙酯)/ADN(己二腈)(49∶49∶2,体积比)电解液放电容量差、ADN在低电位易分解的现象,引入了含硫的溶剂如ES(亚硫酸乙烯酯)、DMS(亚硫酸二甲酯)、SL(环丁砜)。通过对镍锰酸锂半电池和MCMB(中间相炭微球)半电池的电化学性能测试分析,得出0.7 mol/L的 LiDFOB-EMC/ES/ADN(49∶49∶2,体积比)电解液与 0.7 mol/L 的 LiDFOB-EMC/SL/ADN (65.3∶32.7∶2,体积比)电解液适用于5 V高电压锂离子电池体系。ES/SL与ADN及LiDFOB存在协同效应,缓解了上述问题。
3 结语
随着电动汽车的应用与普及的广泛深入,续航里程成为制约其发展的重要问题。开发高能量密度、低成本的动力电池迫在眉睫。镍锰酸锂高电压正极材料,资源储量丰富,成本低、易于产业化,已取得长足的发展。但是,可商业化的5 V高电压电解液的发展相对滞后,其是制约高电压电池体系应用的主要问题。

