鸦胆子药渣的化学成分研究
罗应, 申海艳, 张敏, 谭华欣, 文红波, 申清香
鸦胆子药渣的化学成分研究
罗应a, 申海艳b*, 张敏a, 谭华欣a, 文红波a, 申清香c
(南华大学, a. 衡阳医学院生物化学与分子生物学教研室; b. 病原生物学研究所, 湖南省分子靶标新药研究协同创新中心; c. 第二附属医院妇产科,湖南 衡阳 421001)
为了解鸦胆子()药渣的化学成分,从中分离得到了10个化合物,经波谱分析分别鉴定为对羟基苯甲酸(1)、对羟基苯甲醛(2)、3,4-二羟基苯甲酸(3)、3,4-二羟基苯甲醛(4)、松柏醛 (5)、芥子醛 (6)、3-吲哚甲醛 (7)、3-吲哚甲酸 (8)、-谷甾醇 (9)和鸦胆苦醇 (10)。其中化合物4~6、8为首次从鸦胆子分离得到。
鸦胆子;药渣;化学成分
鸦胆子[(L.) Merr]是苦木科(Sinaroubaceae)鸦胆子属植物,主要分布于我国的广东、广西等华南热带亚热带地区。全世界鸦胆子属植物有6种,均不同程度地作为民间用药,具有多种药理活性[1]。我国有2种,为鸦胆子和柔毛鸦胆子(),其中鸦胆子的种子称为鸦胆子,作中药。据中华本草记载,鸦胆子具有良好的清热解毒、杀虫、截疟、止痢等功效,主要用于治疗热毒血痢、冷痢、疟疾、鸡眼、疣等[2]。现代药理活性研究表明,鸦胆子有抗炎、拒食、抗疟、抗病毒、抗阿米巴、抗溃疡、抗肿瘤、降血糖和除草等多方面的作用[3–4]。鸦胆子含有丰富的化学成分,主要包括苦木内酯类、三萜类、生物碱类、黄酮类、脂肪酸类等化合物[5–7]。中药鸦胆子提取鸦胆子油后,产生的药渣主要作为畜禽饲料添加剂使用,但药渣中尚存在大量活性较高的化学成分,未能充分发挥鸦胆子的药用价值,造成这一中药资源利用不充分[8]。为了进一步促进和开发利用鸦胆子,本课题组对鸦胆子药渣的化学成分进行了系统研究,从中分离纯化了10个化合物(图1)。
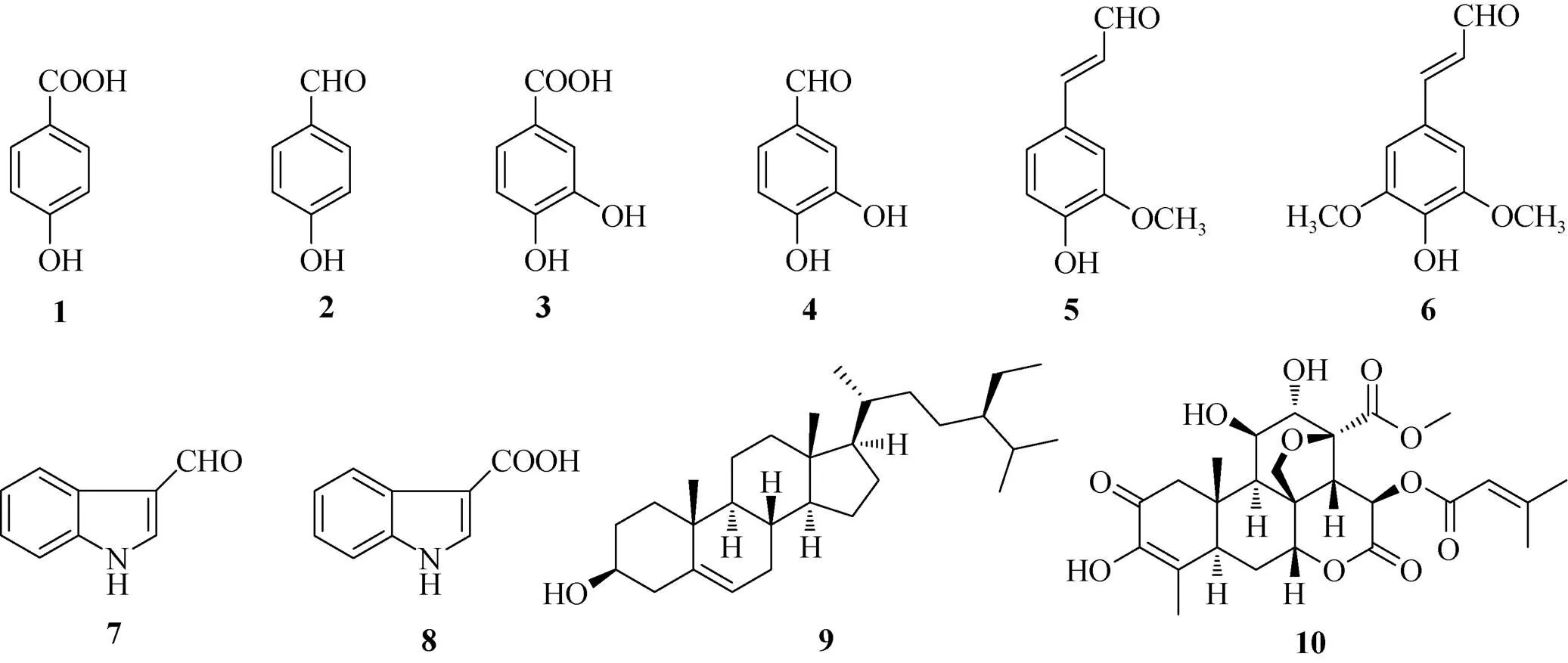
图1 化合物1~10的结构
1 材料和方法
1.1 仪器和材料
Bruker DRX-500型超导核磁共振仪(TMS为内标,瑞士Bruker公司);API 2000质谱仪(美国Applied Biosystems公司)。CCA-1110循环式冷却箱、N-1000旋转蒸发仪和SB-1000电热恒温水浴锅(日本东京理化公司)。正相柱层析硅胶(80~100、200~300目,青岛海洋化工有限公司);反相柱层析硅胶(YMC ODS-A,50m,日本YMC公司);薄层层析硅胶板(HFGF254,山东烟台江友硅胶开发有限公司); Sepha- dex LH-20 (Amersham Biosciences公司)。DMSO、甲醇(分析纯,天津富宇试剂公司);氘代试剂(Sigma公司)。显色方法为紫外荧光显色(254 nm)、碘蒸气显色以及喷洒硫酸-乙醇溶液(10∶90,)加热显色。
鸦胆子药材采自广西省百色市,经南华大学郑兴教授鉴定为苦木科鸦胆子属植物鸦胆子[(L.) Merr]的果实,标本保存于南华大学代谢病药物研究实验室。鸦胆子经广东省佛山市中南药化厂提取鸦胆子油后得鸦胆子药渣。
1.2 提取和分离
鸦胆子药渣(16 kg)用85%的乙醇浸提3次,每次3 d,提取液经旋转蒸发仪减压浓缩后得乙醇浸膏。把浸膏溶于热水中,依次用二氯甲烷和正丁醇萃取,减压浓缩后得二氯甲烷萃取物(900 g)、正丁醇萃取物(300 g)和水部分。二氯甲烷萃取物(900 g)经正相硅胶柱层析(200~300目),以氯仿-甲醇(100∶0~0∶100)梯度洗脱,洗脱液经TLC薄层层析检测,合并主点相同的流分,共得到15个组分(C1~C15)。C3(30 g)经减压柱(200~300目)色谱分离,依次用石油醚-乙酸乙酯(100∶0~0∶100)梯度洗脱,得到10个亚组分(C3-1~C3-10)。C3-5(6.0 g)依次通过正相硅胶柱层析分离纯化,以氯仿-甲醇(90∶10~0∶100)为流动相梯度洗脱、Sephadex LH-20凝胶柱以甲醇洗脱和多次正相硅胶层析柱(200~300目)分离纯化,以氯仿-甲醇(50∶1)或石油醚-乙酸乙酯(20∶1)洗脱,得到化合物1 (5.0 mg)、3 (2.5 mg)、4 (1.5 mg)和9 (8.2 mg)。C6(18 g)经减压柱 (200~300目)色谱分离,依次用氯仿-甲醇(100∶0~0∶100)梯度洗脱,得到8个亚组分(C6-1~C6-8)。C6-4(8.0 g)经正相硅胶层析柱(200~300目)分离纯化,以氯仿-甲醇(50∶1)恒定梯度洗脱,再经Sephadex LH-20凝胶柱以氯仿/甲醇(1∶4)洗脱,得到化合物5 (8.0 mg)、7 (12.0 mg)、8 (5.5 mg)和10 (100 mg)。C6-5(1.0 g)经Sephadex LH-20凝胶柱以甲醇洗脱,得到化合物2 (3.2 mg)和6 (4.5 mg)。
1.3 结构鉴定
化合物1 白色针状结晶;ESI-MS: 161 [M + Na]+, 137 [M − H]–, 分子式为C7H6O3;1H NMR (500 MHz, CD3OD):7.89 (2H, d,= 8.7 Hz, H-2,6), 6.83 (2H, d,= 8.7 Hz, H-3,5);13C NMR (125 MHz, CD3OD):123.3 (C-1), 133.6 (C-2,6), 116.7 (C-3,5), 164.0 (C-4), 170.7 (COOH, C-7)。波谱数据与文献[9]报道的一致,确定该化合物为对羟基苯甲酸。
化合物2 白色针状结晶;ESI-MS: 145 [M + Na]+, 121 [M − H]–, 分子式为C7H6O2;1H NMR(500 MHz, CD3OD):9.74 (1H, s, CHO), 7.75 (2H, d,= 8.6 Hz, H-2,6), 6.89 (2H, d,= 8.6 Hz, H-3,5);13C NMR (125 MHz, CD3OD):127.6 (C-1), 130.7 (C-2,6), 114.1 (C-3,5), 162.4 (C-4), 190.1 (CHO, C- 7)。波谱数据与文献[10]报道的一致,确定该化合物为对羟基苯甲醛。
化合物3 白色结晶;ESI-MS: 177 [M + Na]+, 153 [M − H]−, 分子式为C7H6O4;1H NMR (500 MHz, CD3OD):7.37 (1H, d,= 2.1 Hz, H-2), 7.35 (1H, dd,= 8.0, 2.1 Hz, H-6), 6.73 (1H, d,= 8.0 Hz, H-5);13C NMR (125 MHz, CD3OD):123.9 (C-1), 117.8 (C-2), 151.5 (C-3), 146.1 (C-4), 113.7 (C-5), 115.8 (C-6), 170.2 (COOH)。波谱数据与文献[10]报道的一致,确定该化合物为3,4-二羟基苯甲酸。
化合物4 白色结晶;ESI-MS: 161 [M + Na]+, 137 [M − H]−, 分子式为C7H6O3;1H NMR (500 MHz, CD3OD):9.56 (1H, s, CHO), 7.20 (1H, dd,= 7.9, 1.9 Hz, H-6), 7.18 (1H, d,= 1.9 Hz, H-2), 6.80 (1H, d,= 7.9 Hz, H-5);13C NMR (125 MHz, CD3OD):131.5 (C-1), 117.0 (C-2), 147.9 (C-3), 154.5 (C-4), 116.1 (C-5), 127.3 (C-6), 194.0 (CHO, C- 7)。波谱数据与文献[10]报道的一致,确定该化合物为3,4-二羟基苯甲醛。
化合物5 淡黄色油状;ESI-MS: 201 [M + Na]+, 177 [M − H]−, 分子式为C10H10O3。1H NMR (CDCl3, 500 MHz):9.62 (1H, d,= 7.7 Hz, H-9), 7.37 (1H, d,= 15.8 Hz, H-7), 7.13 (1H, dd,= 8.2, 1.9 Hz, H-6), 7.10 (1H, d,= 1.9 Hz, H-2), 7.04 (1H, d,= 8.2 Hz, H-5), 6.93 (1H, dd,= 15.8, 7.7 Hz, H- 8), 3.92 (3H, s, 3-OCH3);13C NMR (CDCl3, 125 MHz):126.7 (C-1), 109.5 (C-2), 147.0 (C-3), 149.0 (C-4), 115.0 (C-5), 124.0 (C-6), 153.0 (C-7), 126.5 (C-8), 193.5 (C-9), 56.0 (3-OCH3)。波谱数据与文献[11]报道的一致,确定该化合物为松柏醛。
化合物6 黄色油状物;ESI-MSz: 231 [M + Na]+, 207 [M − H]−, 分子式为C11H12O4。1H NMR (500 MHz, CDCl3):9.60 (1H, d,= 7.7 Hz, H-9), 7.33 (1H, d,= 15.8 Hz, H-7), 6.77 (2H, s, H-2, 6), 6.56 (1H, dd,= 15.8, 7.7 Hz, H-8), 3.88 (6H, s, OCH3);13C NMR (125 MHz, CDCl3):123.4 (C-1), 103.5 (C-2, 6), 145.2 (C-3, 5), 136.0 (C-4), 151.1 (C-7), 124.6 (C-8), 191.3 (C-9), 54.3 (OCH3)。波谱数据与文献[12]报道的一致,确定该化合物为芥子醛。
化合物7 黄色粉末;ESI-MS: 168 [M + Na]+, 144 [M − H]−, 分子式为C9H7NO;1H NMR (500 MHz, CD3OD):9.95 (1H, s, 3-CHO), 8.22 (1H, d,= 7.8 Hz, H-4), 8.15 (1H, s, H-2), 7.54 (1H, d,= 8.0 Hz, H-7), 7.31 (2H, m, H-5 and H-6);13C NMR (125 MHz, CD3OD):139.3 (C-2), 118.5 (C-3), 124.6 (C-3a), 121.4 (C-4), 123.2 (C-5), 124.3 (C-6), 113.6 (C-7), 137.8 (C-7a), 185.9 (CHO)。波谱数据与文献[13]报道的一致,确定该化合物为3-吲哚甲醛。
化合物8 无定形粉末;ESI-MS: 184 [M + Na]+, 160 [M − H]−, 分子式为C9H7NO2;1H NMR (500 MHz, CD3OD):7.94 (1H, m, H-4), 7.82 (1H, s, H-2), 7.31 (1H, m, H-7), 7.06 (2H, m, H-5, H-6);13C NMR (125 MHz, CD3OD):133.3 (C-2), 109.8 (C-3), 127.6 (C-3a), 122.1 (C-4), 122.3 (C-5), 123.6 (C-6), 112.9 (C-7), 138.2 (C-7a), 169.4 (COOH)。波谱数据与文献[14]报道的一致,确定该化合物为3-吲哚甲酸。
化合物9 白色结晶;ESI-MS: 437 [M + Na]+, 413 [M − H]−, 分子式为C29H50O;1H NMR (500 MHz, CD3OD):5.34 (1H, brs, H-6), 3.52 (1H, m, H-3), 1.01 (3H, s, 19-CH3), 0.93 (3H, d,= 6.5 Hz, 21-CH3), 0.84, 0.82, 0.79 (3×3H, overlap, 26, 27, 29-CH3), 0.68 (3H, s, 18-CH3);13C NMR (125 MHz, CD3OD):37.1 (C-1), 31.2 (C-2), 70.8 (C-3), 42.5 (C-4), 141.3 (C-5), 121.4 (C-6), 31.2 (C-7), 31.5 (C-8), 50.5 (C-9), 36.3 (C-10), 21.1 (C-11), 39.9 (C-12), 42.1 (C-13), 56.2 (C-14), 24.3 (C-15), 28.5 (C-16), 56.3 (C-17), 12.9 (C-18), 19.7 (C-19), 36.3 (C-20), 18.9 (C-21), 33.8 (C-22), 26.6 (C-23), 45.3 (C-24), 29.6 (C-25), 19.8 (C-26), 19.3 (C-27), 23.4(C-28), 12.0 (C-29)。波谱数据与文献[15]报道的一致,确定该化合物为-谷甾醇。
化合物10 白色无定形粉末;ESI-MS: 543 [M + Na]+, 519 [M − H], 分子式为C26H32O11;1H NMR (500 MHz, DMSO):7.85 (1H, s, 3-OH), 5.95 (1H, m, H-15), 5.67 (1H, s, H-2′), 4.98 (1H, s, H- 1′′′), 4.89 (1H, d,= 4.8 Hz, 11-OH), 4.55 (1H, d,= 7.2 Hz, H-17a), 4.14 (1H, d,= 4.0 Hz, H-12), 4.04 (1H, t,= 4.3 Hz, H-11), 3.68 (3H, m, 21-OCH3), 3.65 (1H, m, H-17b), 3.32 (1H, m, 12-OH), 2.95 (1H, d,= 13.0 Hz, H-5), 2.69 (2H, q,= 2.7 Hz, H-1), 2.21 (1H, d,= 4.1 Hz, H-9), 2.16 (3H, d,= 0.9 Hz, 4′-CH3), 2.13 (1H, m, H-6a), 1.95 (3H, d,= 0.9 Hz, 5′-CH3), 1.79~1.73 (4H, overlap, H-6b, 18-CH3), 1.29 (3H, s, 4′-CH3);13C NMR (125 MHz, DMSO):48.7 (C-1), 192.7 (C-2), 144.2 (C-3), 128.3 (C-4), 41.0 (C- 5), 28.6 (C-6), 82.5 (C-7), 40.5 (C-8), 39.8 (C-9), 44.7 (C-10), 71.3 (C-11), 74.5 (C-12), 81.2 (C-13), 48.5 (C-14), 67.2 (C-15), 167.2 (C-16), 72.2 (C-17), 13.1 (18-CH3), 15.0 (19-CH3), 169.9 (C-20), 52.0 (21- OCH3), 164.1 (C-1′), 114.8 (C-2′), 158.1 (C-3′), 26.8 (4′-CH3), 19.9 (5′-CH3)。波谱数据与文献[16]报道的一致,确定该化合物为鸦胆苦醇。
2 结果和讨论
应用硅胶柱层析、葡聚糖凝胶柱层析等色谱层析分离手段,从鸦胆子药渣中分离得到10个化合物,经波谱分析,分别鉴定为:对羟基苯甲酸 (1)、对羟基苯甲醛 (2)、3,4-二羟基苯甲酸(3)、3,4-二羟基苯甲醛 (4)、松柏醛 (5)、芥子醛 (6)、3-吲哚甲醛 (7)、3-吲哚甲酸 (8)、-谷甾醇 (9)和鸦胆苦醇 (10)。化合物4~6、8为首次从鸦胆子分离得到,化合物2~8为首次从鸦胆子药渣中分离得到。
据报道,鸦胆苦醇(10)具有杀虫止痢、抗疟、抗肿瘤、抗炎等功效,但其毒性较大,溶解度小,因而,许多研究者将其作为先导化合物,进行结构改造,合成具有高效、低毒的苦木内酯类衍生物[17]。鸦胆苦醇(10)还可作为化疗药增效剂,能使癌细胞增敏,提高化疗药物的疗效,减轻化学耐药性,能增加很多癌细胞对顺铂或者其他化疗药物的敏感性[18]。本研究进一步丰富了鸦胆子药渣的化学物质基础,对于促进鸦胆子资源更有效的开发利用具有重要的意义。
[1] LIU J H, JIN H Z, ZHANG W D, et al. Chemical constituents of plants from the genus[J]. Chem Biodiv, 2009, 6(1): 57–70. doi: 10. 1002/cbdv.200700409.
[2] Editor of Chinese Material Medica, State Administration of Traditional Medicine of China. Chinese Material Medica [M]. Shanghai: Shanghai Science and Technology Press, 1999: 7. 国家中医药管理局《中华本草》编委会. 中华本草 [M]. 上海: 上海科学技术出版, 1999: 7.
[3] SU Z W, HUANG H J, LI J L, et al. Chemical composition and cytotoxic activities of petroleum ether fruit extract of fruits of(Simarubaceae) [J]. Trop J Pharm Res, 2013, 12(5): 735–742.
[4] CHUMKAEW P, SRISAWAT T. Phytochemical and antimalarial screening ofplant extracts [J]. J Chem Pharm Res, 2014, 6(12): 253–256.
[5] GUO Z, VANGAPANDU S, SINDELAR R W, et al. Biologically active quassinoids and their chemistry: potential leads for drug design [J]. Curr Med Chem, 2005, 12(2): 173–190.
[6] CHUMKAEW P, PECHWANG J, SRISAWAT T. Two new antimalarial quassinoid derivatives from the stems of[J]. J Nat Med, 2017, 71(3): 570–573. doi: 10.1007/ s11418-017-1089-2.
[7] ZHAO L J, LI C, ZHANG Y, et al. Phytochemical and biological activities of an anticancer plant medicine:[J]. Anti- cancer Agent Me, 2014, 14(3): 440–458. doi: 10.2174/1871520611313 6660336.
[8] WANG Q. Studies on chemical constituents from the dregs of[D]. Guangzhou: Guangdong Pharmaceutical University, 2016. 王群. 中药鸦胆子药渣的化学成分研究 [D]. 广州: 广东药科大学, 2016.
[9] ZHANG Y J, NIE H, ZHOU D X, et al. Chemical constituents of[J]. Chin Trad Herb Drugs, 2017, 48(11): 2172– 2176. doi: 10.7501/j.issn.0253-2670.2017.11.003.张艳军, 聂辉, 周德雄, 等. 桂野桐化学成分的研究[J]. 中草药, 2017, 48(11): 2172–2176. doi: 10.7501/j.issn.0253-2670.2017.11.003.
[10] ZHANG D, LIU W G, YANG L, et al. Chemical constituents of sterile fronds of[J]. Chin Pharm J, 2013, 48(8): 587–589.张东, 刘为广, 杨岚, 等. 紫萁营养叶中化学成分的研究 [J]. 中国药学杂志, 2013, 48(8): 587–589.
[11] DING L F, WANG H Y, WANG K, et al. Chemical constituents from[J]. Chin Trad Herb Drugs, 2017, 48(4): 639–643. doi: 10.7501/j.issn.0253-2670.2017.04.004.丁林芬, 王海垠, 王扣, 等. 福建柏化学成分研究 [J]. 中草药, 2017, 48(4): 639–643. doi: 10.7501/j.issn.0253-2670.2017.04.004.
[12] CAO Y G, ZHENG X K, QI M, et al. Phenolic constituents from fruit ofvar.[J]. Chin Trad Herb Drugs, 2017, 48(22): 4615–4619. doi: 10.7501/j.issn.0253-2670.2017.22.004.曹彦刚, 郑晓珂, 齐曼, 等. 水栀子中酚性成分研究 [J]. 中草药, 2017, 48(22): 4615–4619. doi: 10.7501/j.issn.0253-2670.2017.22.004.
[13] WANG C, YANG Y, MEI Z N, et al. Cytotoxic compounds from[J]. Chem Nat Compd, 2013, 49(4): 699–701. doi: 10.1007/s10600-013-0711-0.
[14] ZHANG Y, CHEN Q, LIU L L, et al. Isolation and identification of chemical constituents from(Linn.) Cavan. (I) [J]. J Shenyang Pharm Univ, 2013, 30(5): 335–341. doi: 10.14066/j.cnki. cn21-1349/r.2013.05.004.张祎, 陈秋, 刘丽丽, 等. 维药蜀葵花化学成分的分离与结构鉴定 (I) [J]. 沈阳药科大学学报, 2013, 30(5): 335–341. doi: 10.14066/j. cnki.cn21-1349/r.2013.05.004.
[15] LI A F, SUN A L, LIU R M, et al. Chemical constituents ofpeels [J]. J Chin Med Mat, 2014, 37(3): 428–431. 李爱峰, 孙爱玲, 柳仁民, 等. 栝楼果皮化学成分研究 [J]. 中药材, 2014, 37(3): 428–431.
[16] HARIGAYA Y, KONDA Y, IGUCHI M, et al. Spectroscopic studies of brusatol [J]. J Nat Prod, 2004, 52(4): 740–748. doi: 10.1021/np5006 4a012.
[17] NOORSHAHIDA A, WONG T W, CHOO C Y. Hypoglycemic effect of quassinoids from(L.) Merr (Simaroubaceae) seeds [J]. J Ethnopharmacol, 2009, 124(3): 586–591. doi: 10.1016/j.jep.2009.04.058.
[18] REN D M, VILLENEUVE N F, JIANG T, et al. Brusatol enhances the efficacy of chemotherapy by inhibiting the Nrf2-mediated defense mechanism [J]. Proc Natl Acad Sci USA, 2011, 108(4): 1433–1438. doi: 10.1073/pnas.1014275108.
Chemical Constituents from the Dregs of
LUO Yinga, SHEN Hai-yanb*, ZHANG Mina, TAN Hua-xina, WEN Hong-boa, SHEN Qing-xiangc
(a. Department of Biochemistry and Molecular Biology, Hengyang Medical College; b. Institute of Pathogenic Biology, Hunan Province Cooperative innovation Center for Molecular Target New Drug Study; c. Department of Gynaecology and Obstetrics, the Second Affiliated Hospital, University of South China,Hengyang 421001, Hunan, China)
In order to understand the chemical constituents of dregs of, ten compounds were isolated and purified by column chromatography. On the basis of spectral data, their structures were identified as-hydroxybenzoic acid (1),-hydroxy-benzaldehyde (2), 3,4-dihydroxybenzoic acid (3), 3,4-dihydroxy- benzaldehyde (4),coniferaldehyde (5), sinapaldehyde (6), 1H-indole-3-carbaldehyde (7), 1H-indole-3-carboxylic acid (8),-sitosterol (9), and brusatol (10).Compounds 4-6 and 8 were obtained fromfor the first time.
; Dregs; Chemical constituents
10.11926/jtsb.3984
2018-08-15
2018-09-18
湖南省自然科学基金项目(2018JJ3433);湖南省教育厅科学研究项目(17C1399);湖南省卫生计生委科研计划课题项目(C2017016);湖南省分子靶标新药研究协同创新中心开放基金项目(0223-0002-0002000-55)资助
This work was supported by the Natural Science Foundation of Hunan Province (Grant No. 2018JJ3433), the Project for Science Research of the Department of Science Education in Hunan Province (Grant No. 17C1399), the Planning Project for Science Research of Health and Family Planning Commission of Hunan Province (Grant No. C2017016), and the Open Fund of Cooperative Innovation Center for Molecular Target New Drug Study in Hunan Province (Grant No. 0223-0002-0002000-55).
罗应(1985~ ),男,讲师,研究方向为天然药物化学。E-mail: 15100026@usc.edu.cn
通信作者 Corresponding author.E-mail: haiyanshen2013@163.com

