分化型甲状腺癌远处转移131I 治疗后疾病进展的影响因素
武新宇,李博,闫新慧,李夏黎,高永举*,樊锐太
1.河南省人民医院核医学科,河南郑州 450003;2.郑州大学人民医院核医学科,河南郑州 450003;3.郑州大学第一附属医院放射治疗科,河南郑州 450003;*通讯作者 高永举 gyongju@163.com;樊锐太 fanruitai@hotmail.com
远处转移是分化型甲状腺癌(differentiated thyroid cancer,DTC)的主要致死因素,但大部分患者疾病进展相对缓慢,长期生存率较高,其疾病特异性生存率(disease-specific survival,DSS)可达23.0%~37.5%,需要长期随访观察[1]。随访观察过程中疾病进展大多提示预后不良。本研究回顾性分析 115例 DTC 远处转移患者131I 治疗后的临床资料及随诊结果,通过分析随诊患者疾病无进展生存期(progression-free survival,PFS)筛选影响疾病进展的因素,为尽早选择最优治疗方案提供参考。
1 资料与方法
1.1 研究对象 回顾性分析 2008年8月—2016年6月于河南省人民医院核医学科行131I 治疗的DTC 术后远处转移患者。纳入标准:①131I 治疗后全身显像(131I post-treatment whole body scan,Rx-WBS)或断层显像(SPECT/CT)提示DTC 远处转移;②病理证实的DTC 远处转移病灶;③其他影像学检查(X 线、CT、MRI、PET/CT)考虑转移性病变,伴甲状腺球蛋白异常增高。符合上述1 项即诊断为远处转移。患者未随诊及资料不全者予以排除。最终纳入115例患者,其中男36例,女79例;年龄18~89 岁,平均(50.92±19.68)岁;单纯肺转移63例,单纯骨转移18例,单纯肝转移 2例,合并 2个及以上器官转移32例。
1.2 治疗方法
1.2.1131I 治疗 按照131I 治疗操作规范进行,口服131I 5.55~9.25 GBq/次,131I 疗程间评估为治愈或疾病进展患者及清灶治疗后Rx-WBS 显像病灶不摄取131I患者不再继续治疗。本组中98例转移灶给予2 次及以上131I 治疗,累积剂量9.25~49.95 GBq,平均剂量(23.13±8.45)GBq。131I 治疗间期行促甲状腺激素(thyroid stimulating hormone,TSH)抑制治疗(TSH<0.1 μIU/ml);17例转移灶不摄取131I(经 1~2 次131I 治疗)患者行TSH 抑制治疗。
1.2.2 Rx-WBS 及 SPECT/CT 显像 患者治疗后第 5 天行131I 全身及SPECT/CT(感兴趣区)断层+CT 显像。采用双探头扫描仪(GE infniavc hawkey4 或Discovery NM/CT670)。
1.2.3 实验室检查 治疗后6个月及每次131I 治疗前1 d 分别检测患者血清甲状腺球蛋白(Tg)与抗甲状腺球蛋白抗体(TgAb),采用电化学发光法,严格按说明书操作,试剂由罗氏公司提供,仪器采用Cobas E602 型全自动电化学分析仪,血清Tg 正常参考值范围 3.5~77 ng/ml。TgAb 测定采用贝克曼 UniCelDxI 800 化学发光免疫分析仪,TgAb 正常参考值范围0~4 IU/ml。分析比较均为同等条件下进行。
1.3 疾病进展评价标准 Rx-SPECT/CT 显像或其他影像学检查以转移灶治疗后最大病灶最长直径和为基础。转移灶最长直径和增大≥20%,或出现新发病灶,或血清抑制状态Tg 水平上升(增高≥25%)判定为疾病进展[2]。骨转移灶通过测量转移灶的软组织肿块大小获得;合并多处转移病灶大小以最大转移灶直径为标准;转移灶摄取与不摄取131I 同时存在时,归为不摄取131I。
1.4 疾病进展影响因素分析 影响因素包括患者年龄(≥45 岁及<45 岁),病理学类型(乳头状癌、滤泡癌),是否合并淋巴结转移,转移灶部位(单纯肺、其他),转移灶大小(≥1 cm 及<1 cm),转移灶是否摄取131I[3]。
1.5 统计学方法 采用SPSS 17.0 软件,应用Kaplan-Meier 绘制疾病无进展生存曲线,对疾病进展影响的单因素分析应用log-rank检验;单因素分析有统计学意义的因素纳入多因素 Cox 比例风险回归分析。P<0.05 表示差异有统计学意义。
2 结果
2.1 随访结果 本组患者平均随访(4.5±3.8)年,中位随访时间为 3.5年。随访期间疾病进展 37例(32.17%)。其中死亡11例,7例死亡与甲状腺癌有关。7例死亡患者中,4例因肺转移肿块增大致呼吸衰竭,2例因脑转移灶进展,1例因骨转移致病理骨折并发感染。见图1、2。
2.2 影响疾病无进展生存率单因素分析结果 患者年龄、转移灶部位、转移灶大小及转移是否摄取131I在进展与无进展患者间差异有统计学意义(P<0.05)。见表1、图3。
2.3 影响DTC 远处转移灶进展因素分析 将患者年龄、转移灶部位、转移灶大小及转移灶是否摄取131I等 4 项因素纳入 Cox 多因素风险回归分析。结果表明,患者转移灶部位及131I 摄取情况与DTC患者远处转移疾病进展有关。合并肺外转移及转移灶不摄取131I患者疾病进展比例更高。见表2。
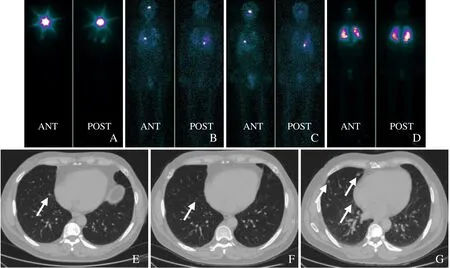
图1 男,51 岁,甲状腺两叶滤泡癌术后,先后服用131I 治疗4 次,分别为5.55 GBq、5.55 GBq、5.55 GBq、7.40 GBq,累积剂量24.05 GBq,箭示肺转移病灶。A:第1 次Rx-WBS图像:①残留甲状腺显影,②双肺摄取131I 增高灶,考虑肺转移;B、C:第2、3 次Rx-WBS图像:①残留甲状腺清除完全,②双肺摄取131I 增高灶,对比好转(131I 浓集程度减低);D:第4 次Rx-WBS图像:双肺摄取131I 增高灶,对比进展(病灶增多,131I 浓集程度增高);E:右下肺前基底段(近斜裂)结节影;F:右下肺结节明显缩小;G:双肺多发结节影,对比增大、增多
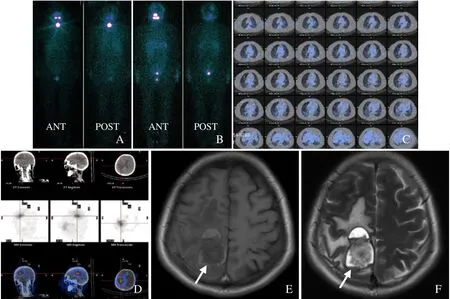
图2 女,56 岁,甲状腺两叶乳头状癌131I 治疗2 次,分别为5.55 GBq 和5.55 GBq;累积剂量11.1 GBq,箭示转移病灶。A、C:第1 次131I 治疗后,Rx-WBS+肺部SPECT/CT图像:①残留甲状腺显影,②双肺结节影,未见明显131I 摄取,考虑PTC 肺转移(血清Tg 228.4 ng/ml);B、D:第2 次Rx-WBS+脑部SPECT/CT图像:①残留甲状腺清除完全,②右侧顶叶不规则低密度影,伴水肿,摄取131I 增高灶,考虑PTC 脑转移(对比新发改变,131I 浓集);E、F:MRI 平扫,右侧顶叶占位,呈长T1、稍长T2 信号,周边见短T1 长T2 信号

图3 各影响因素对疾病无进展生存率曲线比较。A:转移灶大小;B:转移灶部位;C:年龄;D:转移是否摄取131I
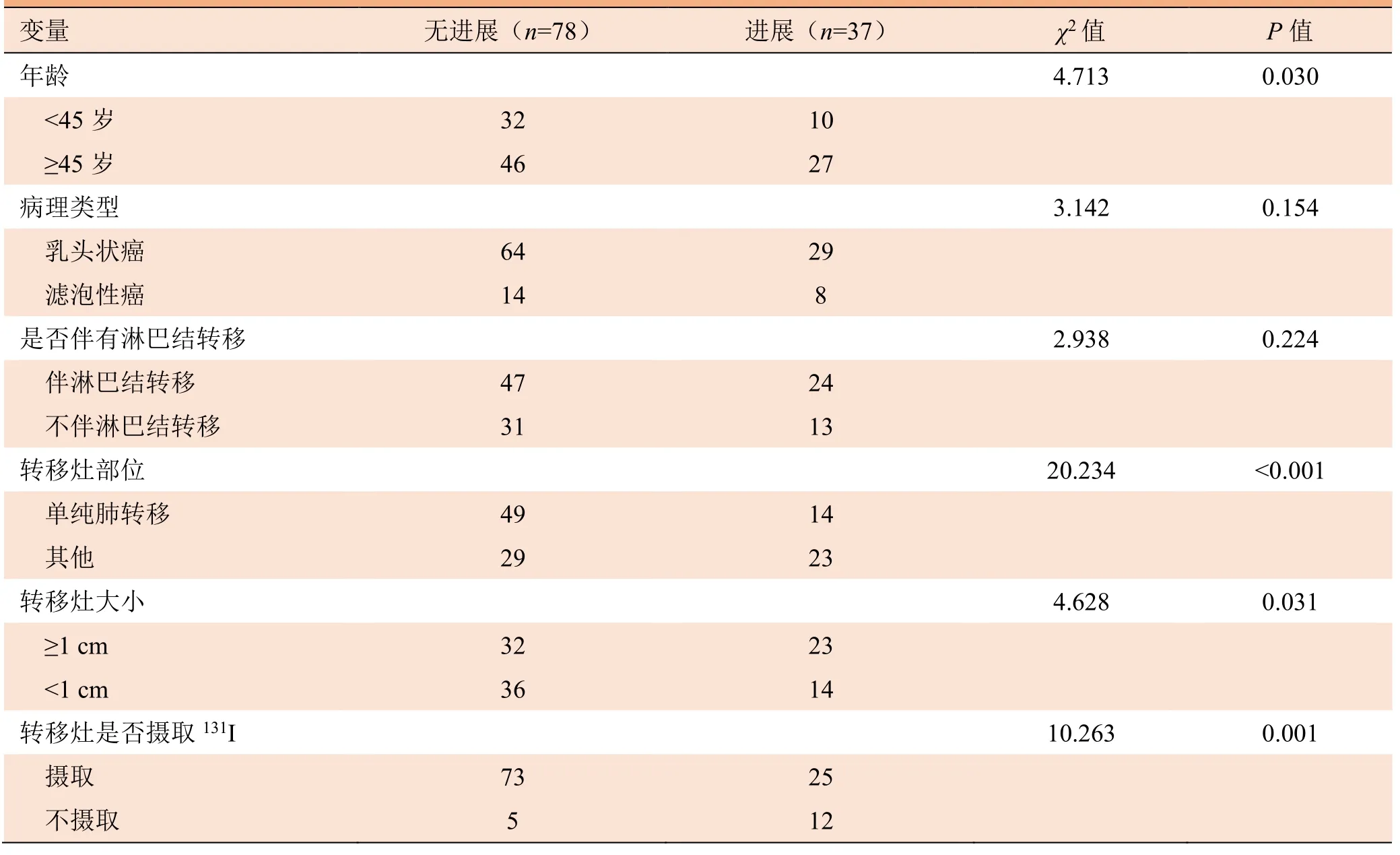
表1 115例DTC 伴远处转移患者不同进展情况单因素分析(例)

表2 Cox 模型筛选危险因素及参数估计
3 讨论
131I 治疗 DTC 转移灶的疗效及影响因素有较多报道。研究显示,疗效与病灶摄取131I 程度、131I 在病灶中的滞留时间直接相关;病灶大小、转移部位及患者年龄也是影响疗效的因素[3]。DTC 远处转移患者需要接受长期 TSH 抑制治疗并定期随诊。随诊过程中患者出现疾病进展,需要调整治疗方案。本研究以转移灶治疗后最小值为观察起点,疾病进展作为终点事件,即观察疾病无进展生存期,探讨疾病进展的影响因素。
本组患者平均随访(4.5±3.8)年,中位随访时间为3.5年。随访期间疾病进展37例(32.17%)。98例转移灶摄取131I患者接受131I 治疗+左甲状腺素钠片抑制治疗,25例随诊过程中发现疾病进展;17例转移灶不摄取131I患者行左甲状腺素钠片抑制治疗,随诊观察期间12例疾病进展。37例进展患者中,10例患者131I 治疗过程中评估好转(包括1例治愈患者),随诊观察期间证实病灶进展,提示高危患者即使治疗后提示好转也应注意随诊监控。随诊观察37例疾病进展患者中,7例病灶增大,但血清 Tg 水平未见明显改变,其中5例合并TgAb 增高,考虑TgAb 对Tg 测量的干扰;另外2例考虑可能Tg 构象改变或Tg释放到血液机制障碍有关[4];4例患者Tg 水平明显升高,病灶大小变化不明显(其中1例骨转移影像学未见明显病灶,摄取131I 增高),考虑Tg 水平变化与肿瘤大小变化并不完全一致[5]。本研究疾病进展比例较既往研究结果偏低,可能与本研究随访观察时间较短,或与病理类型为低分化甲状腺癌患者纳入较少有关[6-7]。
本研究针对 DTC 远处转移患者年龄、病理学类型、131I Rx-WBS 显像是否合并淋巴结转移、转移灶部位、转移灶大小、转移灶是否摄取131I 等6 项可能影响疾病无进展生存期的临床特征进行单因素分析,log-rank检验分析结果表明患者年龄、转移灶部位、转移灶大小及转移灶是否摄取131I 的无进展生存率差异有统计学意义。DTC 伴远处转移患者年龄越小、单纯肺转移、转移灶越小及转移灶摄取131I 的疾病无进展生存期长,预后较好。
针对上述 4 项因素进行 Cox 多因素风险回归分析,排除了单因素分析结果中患者年龄及转移灶大小因素,提示转移灶部位及转移灶是否摄取131I 是DTC患者远处转移的疾病进展独立影响因素。既往有研究表明患者年龄及肿瘤大小是疾病预后的重要因素,患者年龄大、转移灶体积大,则患者预后差[6,8]。既往研究多以患者死亡作为终点事件,本研究以疾病进展作为终点事件,故造成结论的差异。
单纯肺转移是影响疾病进展的独立因素。本研究大部分远处转移患者发生肺转移(82.61%),其中单纯肺转移63例。Cox 多因素风险回归提示相对于单纯肺转移患者,DTC 伴肺外转移降低了患者疾病无进展生存期,增加了疾病进展相对危险度。既往研究表明,DTC 肺转移患者较其他部位转移患者治疗效果好,主要考虑肺部转移灶对131I 的辐射敏感性较其他部位(如骨骼)转移灶更高[9]。肺转移摄取131I患者进行多次131I 治疗可以获得疾病缓解及无进展生存。尽管肺转移灶摄取131I 比例(83.16%)低于骨转移灶(95.56%),但单纯肺转移患者可以获得更长的疾病无进展生存期,进一步提示转移部位是影响疾病进展的重要因素。
转移灶是否摄取131I 是影响疾病无进展生存率的独立因素。本研究17例患者转移灶未见明显131I 摄取,接受 TSH 抑制治疗,随诊观察该组 12例患者(70.58%)发现疾病进展;98例转移灶摄取131I,按照诊疗规范行131I 多次治疗。25例(25.51%)随诊过程中发现疾病进展。Cox 多因素风险回归分析提示DTC 远处转移灶摄取131I 可以增加患者疾病无进展生存期,降低疾病进展相对危险度,提示转移灶摄取131I 的患者预后较好,但较Haq 等[10]报道的远处转移灶不摄碘是患者不良预后的独立预测因素(HR=10.44)值偏低,可能原因是该研究主要分析DTC 远处转移的生存率,而本研究分析疾病无进展生存率。转移灶摄取131I 是分化型甲状腺癌的特性之一,转移灶不摄取131I 大多提示肿瘤失分化或分化较差,疾病恶性程度较高,疾病进展较快。
本组患者随诊观察中死亡 11例,4例与甲状腺疾病无关,其中2例(均接受多次131I 治疗)死于其他肿瘤(胰腺癌、肺癌各1例),2例死于其他原因。既往研究提示131I 治疗可能增加继发肿瘤的风险,且与131I 应用剂量有关[11]。本研究纳入患者继发肿瘤病例数较少,随访时间相对较短,131I 治疗与继发肿瘤是否有关尚需进一步研究。
总之,DTC 伴远处转移患者经过规范的治疗,多数可获得较长的疾病无进展生存期,但应坚持随访监控;DTC 伴远处转移患者转移灶部位及转移摄取131I情况是影响患者疾病进展的独立因素。随着对分化型甲状腺癌分子病理学研究(如 BRAFV600E 突变、RET/PTC 重排)的深入,越来越多的治疗靶点被发现,与之对应的分子靶向药物开始进入临床试验阶段,从而为治疗提供了新的思路[12]。

