严重创伤性脑损伤后凝血功能障碍与预后的关系
常盼盼,刘畅,崇巍
(中国医科大学附属第一医院 1.神经外科;2.急诊科,沈阳 110001)
凝血功能障碍在创伤性脑损伤 (traumatic brain injury,TBI) 患者中发生率约为30%,且患者预后不佳,TBI并发凝血功能障碍时死亡率高达50%[1-2]。虽然大部分创伤 (头部创伤除外) 相关的凝血功能障碍认为与大面积组织损伤、失血性休克、组织灌注程度以及液体复苏对血液的稀释有关[3-5],但TBI患者大量失血及大面积损伤的情况并不常见,而且复苏时的液体量也严格控制,这提示TBI相关凝血功能障碍发生的机制更加复杂特殊。TBI相关凝血功能障碍的发生机制尚存在争议,目前较多研究[6-7]认为TBI相关凝血功能障碍发生的原因可能是由于脑组织损伤后导致大量组织因子释放激活了血小板以及凝血相关分子,进而导致凝血功能障碍。
目前,国内外大部分创伤指南均未针对TBI相关凝血功能障碍做出明确指导。输入血液制品 (血小板、新鲜冰冻血浆及冷沉淀等) 是目前应用相对较广的治疗策略[7],但入液量过大可能引起TBI患者液体负荷量过大,并增加了输血相关并发症的发生风险[8]。还有一些处于研究阶段的新型治疗方案,如利用抗凝血酶Ⅲ[9]、低分子量肝素[10]、凝血因子Ⅶa[11]以及前列环素[12]等来作为TBI的药物治疗策略,但这些药物的治疗效果均未经大样本临床研究证实。另外,部分TBI患者的凝血指标在创伤初期仅表现轻度异常,易被忽略,但患者却预后不良[13],因此TBI发生后尽早纠正凝血功能障碍,对预测并改善患者预后有很大价值。
国内外学者[1,14]对TBI后的凝血情况进行了较多研究,但对严重创伤性脑损伤 (severe traumatic brain injury,sTBI) 后早期凝血功能异常与患者预后的研究却较少。有研究[15]报道格拉斯哥昏迷评分(Glasgow Coma Scale,GCS) <8或损伤严重程度评分(injury severity score,ISS) ≥16及中线移位是无其他部位明显损伤的TBI患者发生凝血功能障碍的独立危险因素,提示对于sTBI患者,凝血功能障碍发生可能会更加显著及持久。本研究分析我院58例sTBI患者的临床资料,旨在阐明sTBI后凝血功能障碍与预后的关系。
1 材料与方法
1.1 研究对象
回顾性分析2013年11至2014年11月我院急诊神经外科收治的经CT证实的58例sTBI患者 (无其他部位严重创伤) 的临床资料。年龄12~88岁,其中男41例、女17例。纳入标准:患者入院时GCS<9且头部简明损伤评分 (abbreviated injury scale,AIS) ≥3且除头部以外其他部位AIS<3;排除使用过抗凝药物、肝衰竭和无院内凝血化验指标的患者。
1.2 预测因素和预后判断
记录患者年龄、性别、入院时GCS和瞳孔对光反射情况、首次头CT是否有中线移位以及首次血小板计数 (blood platelet count,PLT)、凝血酶原时间 (prothrombin time,PT)、活化部分凝血活酶时间 (activated partial thromboplastin time,APTT)、纤维蛋白原 (fibrinogen,Fg)、血糖。CT检查在入院后即刻进行,中线移位判定:中线移位>5 mm;实验室检查与CT检查同时或随后进行,血液样本为静脉血。凝血功能障碍:APTT>40 s和 (或) PT>15 s和(或) PLT<120×109/L[16],根据有无凝血功能障碍将患者分为凝血功能障碍组与无凝血功能障碍组。
根据患者离院时按格拉斯哥预后评分 (Glasgow Outcome Scale,GOS) 分为预后良好组 (GOS 3~5) 和预后不良组 (GOS 1~2)。
1.3 统计学分析
采用SPSS 19.0统计软件分析,符合正态分布的计量资料以表示,组间比较采用t检验;非正态分布的计量资料以中位数 (四分位数间距) 表示,组间比较采用非参数秩和检验;计数资料以频数(构成比) 表示,组间比较采用χ2检验。上述单因素分析以P< 0.15为有统计学意义。将上述单因素分析得出有显著差异的因素进行多因素logistic回归分析,以P< 0.10为有统计学意义,进一步对多因素分析得出的独立危险因素绘制受试者工作特征 (receiver operating characteristic,ROC)曲线,并计算曲线下面积、截断值、灵敏度及特异度。
2 结果
2.1 单因素分析结果
58例中预后不良组27例 (46.6%),预后良好组31例 (53.4%);凝血功能障碍组18例 (31.0%),无凝血功能障碍组40例 (69.0%)。总死亡率24.1%,凝血功能障碍发生率31.0%,并发凝血功能障碍患者的死亡率为33.3%。单因素分析结果显示,与预后良好组比较,预后不良组瞳孔反射异常率、中线移位发生率、血糖、PT、APTT均明显升高 (均P< 0.05);PLT、GCS、Fg均明显降低 (均P< 0.05),见表1。凝血功能障碍组与无凝血功能障碍组GCS比较无统计学差异[6 (5~8)和7 (5.25~8),P=0.618]。
2.2 多因素logistic回归分析结果
对单因素分析有统计学意义的因素进行多因素logistic回归分析,结果显示,瞳孔反射是否正常、中线是否移位、血糖、GCS、PT、APTT为预后不良的独立危险因素,见表2。
2.3 绘制ROC曲线
对logistic回归多因素分析中的独立危险因素(血糖、GCS、PT、APTT) 绘制ROC曲线,结果显示,ROC曲线形态及曲线下面积证实PT、APTT对预测sTBI的预后有一定的临床意义,见表3、图1。
3 讨论
TBI相关凝血功能障碍发生机制尚不完全明确,可能是由于以下原因导致: (1) 患者受脑外伤本身较为严重[17]; (2) TBI后的二次损伤[18]; (3) 凝血功能异常导致进展性出血性损伤[19]; (4) 微血管血栓形成[20]。TBI后脑组织释放大量组织因子,激活血小板以及凝血因子使外源性凝血途径启动[7],从而使机体处于高凝状态,导致微循环血栓形成并可进一步激发纤溶亢进,最终导致弥散性血管内凝血(disseminated intravascular coagulation,DIC)[21]。 此外,也有研究[22]认为TBI可能会合并缺氧、酸中毒、细菌感染或休克,这会导致血管内皮细胞受损,激活内源性凝血途径及血小板凝集,进而出现凝血功能障碍。凝血功能障碍可在TBI后1 h内发生,与不良预后相关[23]。另外有研究[24]报道sTBI患者中凝血功能障碍的发生率>60%。因此及时检测以及早期纠正TBI后凝血功能障碍临床意义重大。
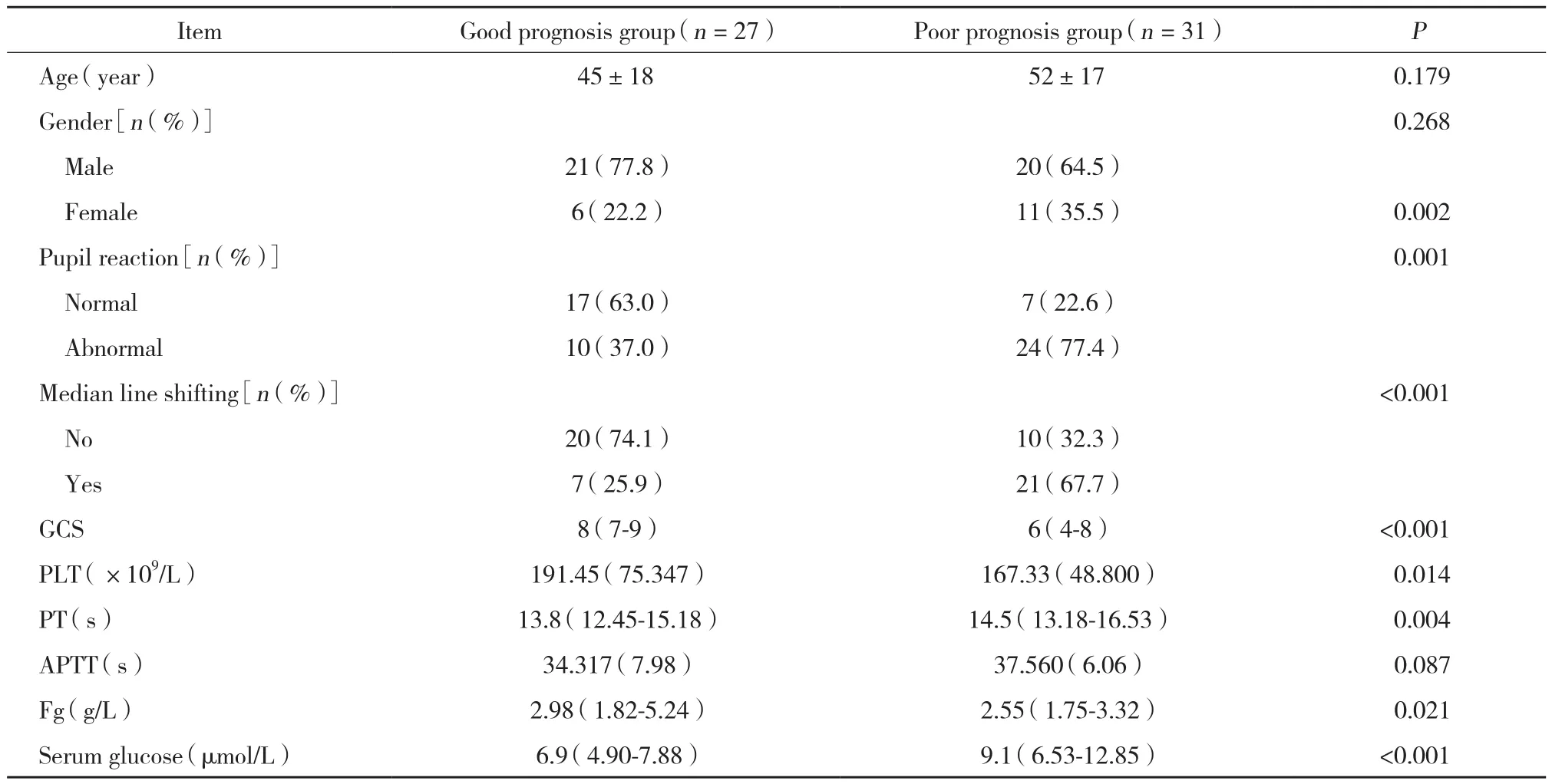
表1 预后良好组与预后不良组各项临床指标单因素分析比较Tab.1 Univariate analysis between the good and poor prognosis groups
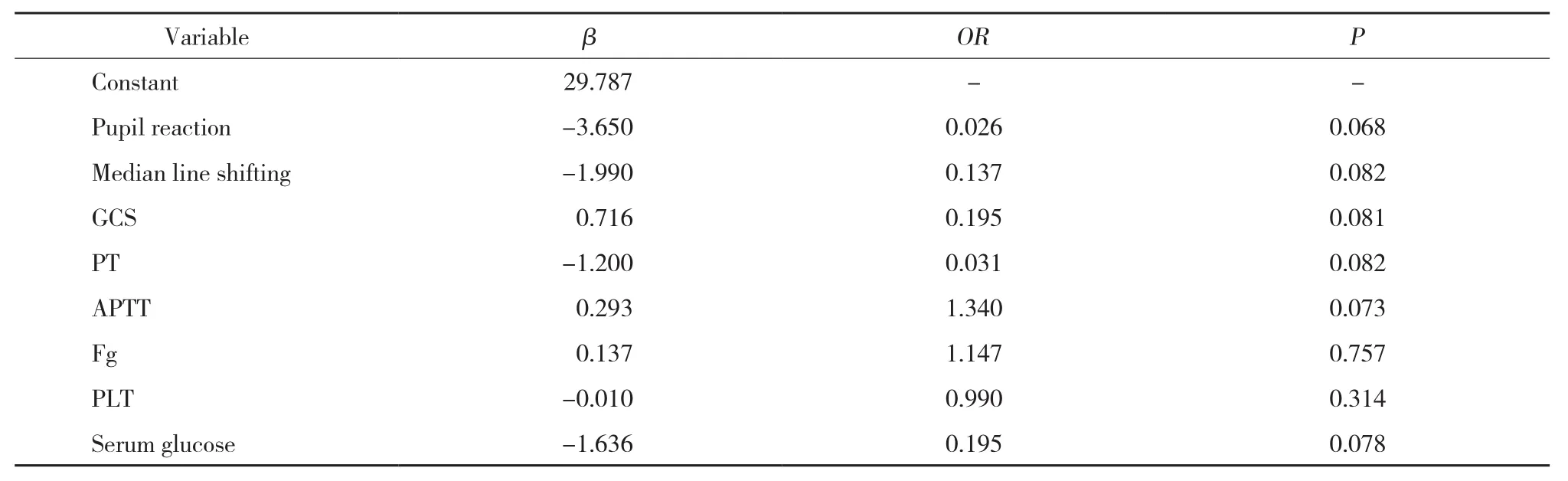
表2 预后不良患者危险因素多因素logistic回归分析结果Tab.2 Multivariate logistic regression analysis of the poor prognosis of sTBI group
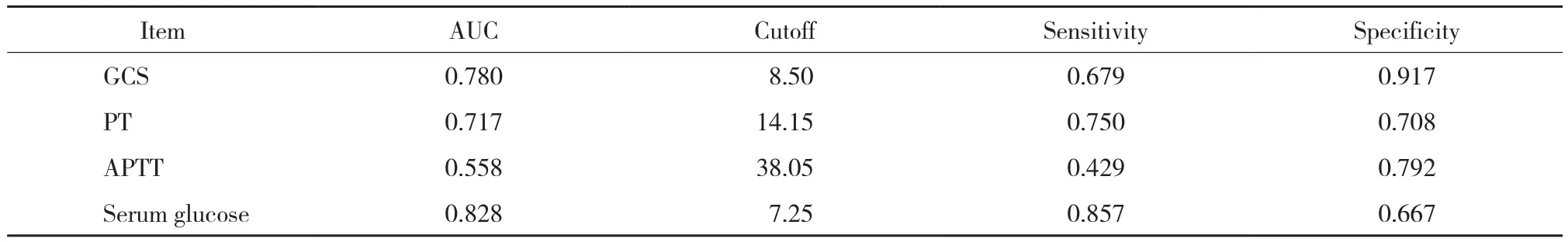
表3 各指标ROC曲线下面积、截断值、灵敏度及特异度Tab.3 The area under the ROC curve,cutoff,sensitivity,and specificity of GCS,PT,APTT and serum glucose

图1 sTBI患者的年龄、血糖、GCS及PT的ROC分析Fig.1 ROC curve analysis for evaluating the prognostic accuracy of age,serum glucose,GCS,and PT in sTBI patients
本研究结果显示,58例sTBI患者凝血功能障碍的发生率为31.03%,这与EPSTEIN等[1]和HARBANGI等[2]的研究结果一致。并发凝血功能障碍患者的死亡率为33.33%,低于以往研究[1-2]结果,考虑其原因可能是本研究的终点为患者离院时,故可能漏掉离院后死亡的患者。另外,本研究显示首诊瞳孔反射异常、中线移位、血糖升高以及GCS评分是本组患者预后不良的独立危险因素,与以往研究结果一致。入院时GCS评分一直是评估TBI患者预后的简单有效指标[25];sTBI患者颅内往往伴有严重的水肿或者即发的颅内血肿,这可能是瞳孔反射异常、中线移位成为独立危险因素的重要原因;而血糖升高早已认为是TBI患者预后不良的危险因素[26]。
此外,与预后良好组比较,预后不良组的PT、APTT明显升高,PLT、Fg明显降低,但PLT和Fg并不是本研究患者预后不良的独立危险因素。过去研究[21]发现sTBI患者并发血小板减少及凝血功能障碍的风险较高,并与患者预后不良有相关性。TBI后凝血功能障碍既包括高凝状态也包括低凝状态[2],这提示Fg在TBI发生后是波动的。虽然本研究均在患者入院后立即采集血液样本,但每个患者从受伤到入院的时间是不可控的,这可能是导致Fg在本研究中不是独立危险因素的原因。虽然TBI可能影响血小板的功能,但除PLT之外,评价其功能的因素还有很多,如血小板活化因子 (platelet activating factor,PAF)、 Fg、纤维蛋白降解产物、血管性血友病因子 (von Willebrand factor,VWF) 等[27],这可能是导致PLT在本研究中不是独立危险因素的原因。
本研究中PT、APTT是sTBI患者预后不良的独立危险因素,且PT的曲线下面积要明显高于APTT。MURRAY等[28]研究也发现PT是TBI预后的独立危险因素。目前认为TBI相关凝血功能障碍发生的机制主要可能是TBI后脑组织释放大量组织因子,从而激活了外源性凝血途径,最终导致凝血功能障碍[2]。有研究发现凝血因子Ⅶ在TBI相关凝血功能障碍中起重要作用[29],而凝血因子Ⅶ主要调节外源性凝血途径。PT反映外源性凝血途径功能,本研究的结果与上述观点一致。
凝血功能障碍组与无凝血功能障碍组入院时GCS比较无统计学差异 (P> 0.05),IVES等[30]研究结果也表明凝血功能障碍的发生与TBI的严重程度无关,但与患者预后相关,进一步支持了TBI相关凝血功能障碍可能是患者预后不良的独立危险因素。
本研究存在一些局限性: (1) 样本量较小,可能会导致本研究的敏感度及阳性预测值下降以及一些有意义的指标可能没有统计学意义。 (2) 本研究为回顾性研究,只能在一定程度上反映sTBI相关凝血功能障碍与预后不良的相关性,要进一步验证两者是否有因果关系以及制定更加科学合理的干预措施,还需进行前瞻性研究。
综上所述,sTBI后凝血功能障碍发生率较高,且与患者预后不良有关。PT、APTT可以较好辅助评估sTBI患者的预后。密切检测凝血指标对早期发现及纠正sTBI后凝血功能障碍有重要意义,对改善、预测sTBI患者预后也有积极的作用。

