血清FGF-23、sKL检测对持续非卧床腹膜透析患者心脏瓣膜钙化的预测价值
周麟,李向东,赵明
(西安交通大学医学院附属三二〇一医院,西安723000)
终末期肾脏疾病患者长期存在钙、磷以及血脂等代谢异常,其中高磷血症诱发的心脏瓣膜钙化是终末期肾脏疾病患者较严重的并发症之一[1]。心脏瓣膜钙化是导致患者心功能不全、心内膜炎、血栓等心血管事件的独立危险因素。研究显示,39%~50%的终末期肾脏疾病患者因心血管事件而死亡[2,3]。早期预测终末期肾脏疾病患者心脏瓣膜钙化,对改善预后,提高患者生存率具有重要意义。血清成纤维生长因子23(FGF-23)是新近发现的由骨组织合成并分泌的激素,属FGF19亚家族成员,介导了血磷及维生素D的代谢过程[4,5]。可溶性klotho蛋白(sKL)是由klotho基因编码,在甲状旁腺、肾脏、大脑脉络膜表皮细胞广泛表达的单向跨膜蛋白,参与了高磷血症、高钙血症的发病过程[6,7]。关于血清FGF-23、sKL在持续非卧床腹膜透析(CAPD)患者发病过程中的作用,目前研究较少。本研究通过检测血清FGF-23、sKL水平,探讨其在预测CAPD患者发生心脏瓣膜钙化中的价值。
1 资料与方法
1.1 临床资料 选择2016年3月~2017年9月本院收治的终末期肾脏疾病患者109例,均采用腹膜透析液(钙浓度1.25 mmol/L,购于百特公司)进行透析,3~4次/d。纳入标准:CAPD>3个月且病情稳定;预计生存时间超过6个月;入组前1个月内未接受免疫抑制剂、激素类药物治疗。排除标准:孕产妇及哺乳期;心脏功能不全;肝脏功能障碍;急性腹膜炎、原发性骨代谢疾病、严重营养不良等;急慢性感染性疾病或自身免疫性疾病;恶性肿瘤。随访6个月,患者经心脏超声检查诊断为心脏瓣膜钙化51例(瓣膜钙化组)、心脏瓣膜正常58例(瓣膜正常组)。心脏瓣膜钙化标准[8,9]:在二尖瓣与左室后壁间处或在房室交接处有点状或团块状的回声增强,瓣膜厚度>3 mm,即为二尖瓣瓣膜钙化;主动脉瓣瓣膜有点状或团块状回声增强,瓣膜厚度>3 mm,即主动脉瓣瓣膜钙化。二者均为心脏瓣膜钙化。同期选取30例体检健康者作为对照组。本研究获得医院伦理委员会批准,患者及家属签署知情同意书。
1.2 血液生化指标检测 采用全自动生化分析仪检测空腹血糖、血磷、碱性磷酸酶(ALP)、血钙、胆固醇(TC)、高密度脂蛋白(HDL)、低密度脂蛋白(LDL)、甘油三酯(TG)、血清肌酐(SCr)、血清尿素氮(BUN),同时计算总尿素清除指数(Kt/V)、校正钙。
1.3 血清FGF-23、sKL水平检测 采集患者入院次日清晨空腹肘静脉血3 mL及对照组体检当日空腹肘静脉血3 mL,2 000 r/min离心20 min,留取上清液,保存于-80 ℃环境下留待检测。血清标本在室温环境下复融后采用酶联免疫吸附法检测FGF-23、sKL水平。试剂盒由美国Millipore公司提供,操作严格按照试剂盒说明进行。

2 结果
2.1 三组一般资料比较 瓣膜钙化组男29例,女22例;年龄39~67(45.92±11.57)岁;原发病为慢性肾小球肾炎23例,高血压肾病12例,多囊肾9例,其他7例;有高血压病史9例,糖尿病史9例;透析龄(49.24±12.33)个月。瓣膜正常组男35例,女23例;年龄41~73(47.71±10.36)岁;原发病为慢性肾小球肾炎28例,高血压肾病15例,多囊肾6例,其他9例;有高血压病史13例,糖尿病史8例;透析龄(42.38±13.03)个月。对照组男19例,女11例;年龄38~70(45.64±12.23)岁;有高血压病史6例,糖尿病史4例。瓣膜钙化组、瓣膜正常组透析龄比较差异有统计学意义(P<0.05);三组性别、年龄、病史比较差异无统计学意义(P均>0.05)。
2.2 三组血液生化指标比较 三组血磷、ALP、血钙、SCr、Kt/V比较差异有统计学意义(P均<0.05);瓣膜钙化组、瓣膜正常组血磷、ALP、血钙、SCr水平高于对照组(P均<0.05),Kt/V低于对照组(P<0.05);瓣膜钙化组透析龄、血磷、ALP、血钙、SCr水平高于瓣膜正常组(P均<0.05),Kt/V低于瓣膜正常组(P<0.05)。见表1。
表1 三组血液生化指标比较
注:与对照组比较,*P<0.05;与瓣膜正常组比较,#P<0.05。
2.3 三组血清FGF-23、sKL水平比较 瓣膜钙化组血清FGF-23、sKL水平分别为(5 038.22±639.45)、(186.57±65.24)pg/mL,瓣膜正常组分别为(1 652.87±550.90)、(621.04±82.96)pg/mL,对照组分别为(639.72±410.02)、(1 286.55±75.60)pg/mL。三组血清FGF-23、sKL水平比较差异有统计学意义(P<0.05)。与对照组比较,瓣膜钙化组和瓣膜正常组血清FGF-23水平高,血清sKL水平低(P均<0.05);与瓣膜正常组比较,瓣膜钙化组血清FGF-23水平高,血清sKL水平低(P均<0.05)。
2.4 CAPD患者心脏瓣膜钙化的影响因素 以心脏瓣膜是否钙化作为因变量,表1中有统计学意义的变量为自变量进行多因素逐步Logistic回归分析(α入=0.05,α出=0.10),结果显示,血磷、血清FGF-23水平升高是CAPD患者心脏瓣膜钙化的独立危险因素(OR分别为1.995、2.328,P均<0.05),血清sKL水平升高是CAPD患者心脏瓣膜钙化的保护因素(OR=0.742,P均<0.05)。见表2。
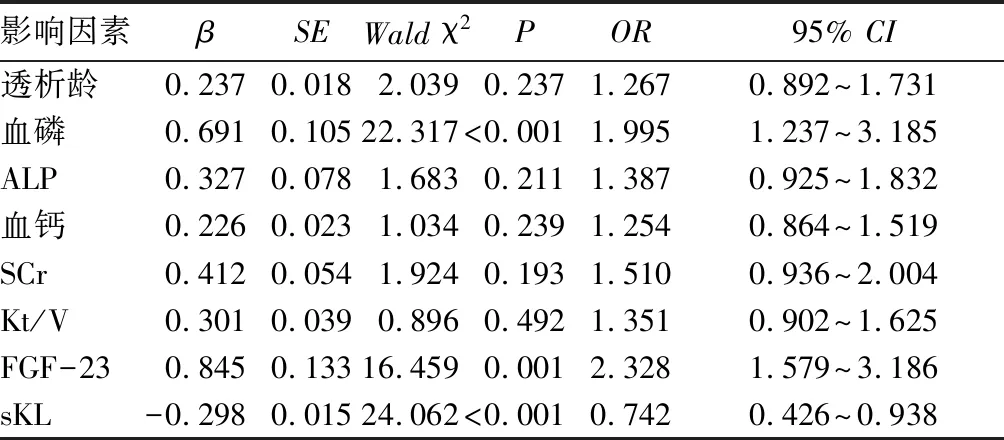
表2 CAPD患者心脏瓣膜钙化影响因素的Logistic回归分析
2.5 血清FGF-23、sKL对CAPD患者发生心脏瓣膜钙化的预测价值 绘制ROC曲线,FGF-23预测心脏瓣膜钙化的曲线下面积(AUC)为0.844,95%CI:0.763~0.926,最佳截断值为2 538.67 pg/mL,灵敏度、特异度分别为0.80、0.89,准确度为0.83;sKL预测心脏瓣膜钙化的AUC为0.814,95%CI:0.728~0.900,最佳截断值为254.79 pg/mL,灵敏度、特异度分别为0.76、0.85,准确度为0.79;FGF-22联合sKL预测心脏瓣膜钙化的AUC为0.941,95%CI:0.893~0.988,灵敏度、特异度分别为0.89、0.92,准确度为0.92。
3 讨论
心脏瓣膜钙化在终末期肾脏疾病患者中的发病率约为50%,是终末期肾脏疾病的常见并发症,也是导致患者心血管事件高发及死亡率高的主要因素[10]。找到终末期肾脏疾病患者发生心脏病瓣膜钙化的影响因素,对制订针对性干预措施以降低心血管事件发生率和改善预后具有重要意义。肾脏疾病患者在透析过程中易出现矿物质代谢紊乱,其中钙、磷平衡破坏是引起患者心脏瓣膜钙化的始动因素[11,12]:正常人体中,通过肠道吸收、肾脏排泄及重吸收等生理过程,血磷在细胞内外保持动态平衡。终末期肾脏疾病患者,肾小球滤过率明显下降以及损伤的肾间质减少了激素作用的靶点,最终导致高磷血症,血磷升高使血管壁以及心脏瓣膜的矿物质沉积,进而诱发心脏瓣膜钙化。
FGF-23是在人体肾脏中发挥磷酸盐平衡调节作用的激素,终末期肾脏疾病患者血磷升高时,FGF-23代偿性合成及分泌增加以减少肾脏对磷酸盐的重吸收,同时还通过减少维生素D含量而减少肠道对磷的吸收。由于FGF-23相对分子质量较大,在肾脏中不易被透析清除。当终末期肾脏疾病患者肾功能丧失时,患者血液中FGF-23水平明显升高[13]。Olauson等[14]研究发现,小鼠衰老模型中FGF-23对心血管具有毒性作用,高水平FGF-23与血管钙化密切相关。乔青等[15]证实高水平FGF-23是腹膜透析患者心脏瓣膜钙化的危险因素。Klotho蛋白是分布于肾脏近曲小管细胞膜上的衰老因子,血清中sKL主要来源于模型klotho蛋白胞外段脱落。研究显示,低水平sKL使肾脏中磷排泄障碍,进而导致机体血磷水平升高而诱发心脏瓣膜钙化[16,17]。Gutierrez等[18]认为sKL蛋白通过改善内皮细胞功能以及增加一氧化氮合成来降低血压,进而抑制血管钙化来保护血管。
本研究结果显示,终末期肾脏疾病患者血磷、ALP、血钙、SCr水平高于体检健康者,Kt/V低于体检健康者。提示肾脏疾病患者存在不同程度肾功能障碍和矿物质平衡。进一步分析发现,瓣膜钙化组血磷、ALP、血钙、SCr、FGF-23、透析龄高于瓣膜正常组,且Kt/V、sKL水平低于瓣膜正常组。说明瓣膜钙化患者血磷、血钙水平更高,肾功能损伤更严重,透析时间更长,并且FGF-23、sKL水平更高。上述结果提示血磷、FGF-23、sKL等指标可能参与了心脏瓣膜钙化。采用多因素Logistic回归校正混杂因素后,血磷、FGF-23是CAPD患者心脏瓣膜钙化独立危险因素,其中血磷每升高1 mmol/L,心脏瓣膜钙化发生风险增加1.995倍。推测其原因可能为肾脏疾病患者血磷升高,使血管平滑肌细胞释放更多的Ⅲ型钠依赖磷转运蛋白1,并引起血管平滑肌细胞发生骨样改变,细胞外基质钙化,最终导致心脏瓣膜钙化[19]。FGF-23每升高1 pg/mL,心脏瓣膜钙化发生的风险增加2.328倍。研究显示,1,25(OH)2D3能缓解血管钙化,其活性受到抑制则会加速血管钙化;FGF-23水平升高,抑制了Cyp27b1基因的表达,以致25(OH)D3转化为活性1,25(OH)2D3。同时,FGF-23促进了Cyp24基因的表达,进而导致1,25(OH)2D3活性被抑制[20]。sKL是终末期肾脏疾病患者心脏瓣膜钙化的保护因素,其水平每升高1 pg/mL,心脏瓣膜钙化风险减少25.8%。sKL水平升高可促进远端肾小管内钙的重吸收以及近端肾小管内磷酸盐尿的产生,最终使血管平滑肌细胞中磷摄取减少。
本研究结果还显示,FGF-23联合sKL预测CAPD患者发生心脏瓣膜钙化的价值较高。AUC高于FGF-23、sKL单独检测。提示CAPD患者血清FGF-23、sKL可作为临床预测心脏瓣膜发生风险的重要生化标记物。
综上所述,血清FGF-23水平升高、sKL水平降低与CAPD患者心脏瓣膜发生钙化密切相关;二者早期联合检测有助于预测CAPD患者心脏瓣膜钙化的发生风险。本研究尚存在不足,对FGF-23、sKL预测CAPD患者心脏瓣膜钙化的机制研究不足,下一步将开展队列研究深入探讨两项指标在CAPD患者心脏瓣膜钙化发生过程中的机制。

