曲妥珠单抗联合PC 单周化疗方案治疗HER2 阳性晚期乳腺癌患者的临床研究
王艳
(河南省郑州市第三人民医院肿瘤内科 郑州450000)
乳腺癌为女性常见恶性肿瘤,发生于乳腺腺上皮组织,早期无明显症状,但中晚期乳腺癌细胞连接松散,可能出现脱落,癌细胞可随淋巴液或血液向全身转移,危及生命。有报道指出[1],20%~30%乳腺癌存在人表皮生长因子受体2(HER2)基因的过度表达。HER2 具有酪氨酸激酶活性,可激活细胞下游信号通路传导,调节细胞分化、生长、增殖、凋亡,可作为乳腺癌治疗的靶点。曲妥珠单抗可选择性作用于HER2 胞外Ⅳ区,抑制肿瘤细胞增殖,激活细胞毒反应,发挥抗癌作用。本研究以我院HER2 阳性晚期乳腺癌患者为对象,予以曲妥珠单抗联合PC 单周化疗方案治疗,观察其治疗效果。现报道如下:
1 资料与方法
1.1 一般资料 选取2014 年3 月~2017 年3 月我院收治的64 例HER2 阳性晚期乳腺癌患者为研究对象,采用随机数字表法分为对照组与观察组,每组32 例。观察组年龄37~72 岁,平均(54.62±7.62)岁;临床分期:Ⅲb 期8 例,Ⅳ期24 例;病理类型:导管癌30 例,小叶癌2 例。对照组年龄38~71 岁,平均(54.46±7.31)岁;临床分期:Ⅲb 期9 例,Ⅳ期23例;病理类型:导管癌29 例,小叶癌3 例。两组一般资料比较,均无显著性差异(P>0.05),具有可比性。本研究经我院医学伦理委员会审核批准。
1.2 入选标准 纳入标准:符合《中国抗癌协会乳腺癌诊治指南与规范(2015 版)》诊断标准[2];化学染色法检测HER2 阳性;经病理学检查确诊;KPS 评分≤70 分;心电图、血常规、肝肾功能正常;预计生存时间>3 个月;患者及其家属均知晓参与本研究,并自愿签署知情同意书。排除标准:合并其他恶性肿瘤者;合并其他类型乳腺癌者;存在癌细胞远处转移者;存在血液系统疾病或恶病质者;对研究所用药物过敏者。
1.3 治疗方法
1.3.1 对照组 予以PC 单周化疗方案治疗,第1天、第8 天、第15 天,静滴紫杉醇注射液(国药准字H20084032)80 mg/m2+5%葡萄糖溶液250 ml,静滴卡铂(国药准字H37022012)AUC5+5%葡萄糖溶液250 ml,21 d 为1 个周期,共4 个化疗周期,每个周期间隔7 d。化疗前,予地塞米松及止吐药物。化疗期间,进行保肝、护胃治疗。
1.3.2 观察组 在对照组基础上予以曲妥珠单抗(国药准字J20180073)单周方案治疗,首次负荷静滴4 mg/kg,静滴时间>90 min,之后每次2 mg/kg,1次/d 周,治疗12 周。两组均随访1 年。
1.4 观察指标 比较两组治疗效果、治疗前后血清糖类抗原125(CA125)、癌胚抗原(CEA)水平、B 淋巴细胞瘤-2 基因(Bcl-2)、Bcl-2-Associated X 的蛋白质(Bax)表达水平。
1.5 检测方法 抽取空腹静脉血3 ml,离心10 min取血清,3 000 r/min,采用放射免疫法测定CA125、CEA 水平,试剂盒购自上海酶联生物科技有限公司,按照说明书操作。用穿刺针采集肿瘤组织标本,制备细胞悬液,提取RNA,采用PCR 基因扩增仪以RT-PCR 法扩增B 淋巴细胞瘤-2 基因(Bcl-2)、Bcl-2-Associated X 的蛋白质(Bax),获取凝胶图像,定量分析,测得Bax、Bcl-2 基因表达水平。
1.6 疗效判定标准 参照实体瘤疗效评价标准(RECIST1.1)进行疗效判定[3]:病灶基本消失,维持时间≤4 周,为完全缓解(CR);基线病灶最长径总和缩小≥30%,维持时间≤4 周,为部分缓解(PR);基线病灶最长径总和增大<20%或缩小<30%,为稳定(SD);基线病灶最长径总和增大≥20%或出现新病灶,为进展(PD)。有效率=(完全缓解+部分缓解)/总例数×100%。
1.7 统计学分析 采用SPSS 22.0 统计学软件处理数据,计量资料以(x±s)表示,行t 检验,计数资料用%表示,行χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 两组临床疗效比较 观察组治疗有效率明显高于对照组,P<0.05。见表1。
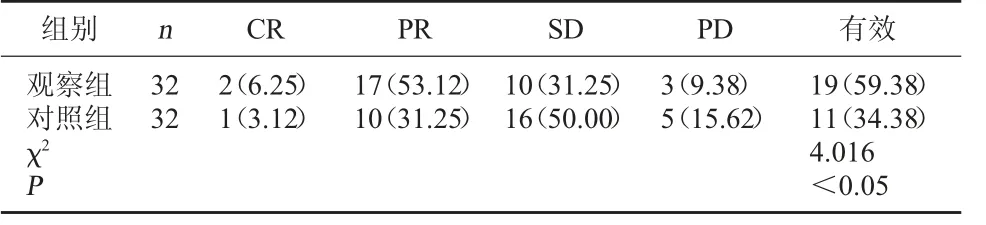
表1 两组临床疗效比较[例(%)]
2.2 治疗前后两组血清CA125、CEA 水平比较治疗前,两组血清CA125、CEA 水平比较,均无显著性差异(P>0.05);治疗后,观察组血清CA125、CEA水平均明显低于对照组,P<0.05。见表2。
表2 治疗前后两组血清CA125、CEA 水平比较

表2 治疗前后两组血清CA125、CEA 水平比较
时间 组别 n CA125(U/ml) CEA(ng/ml)治疗前 观察组3236.83±4.7614.60±2.19对照组3237.08±4.4114.33±2.02 t 0.2180.513 P>0.05>0.05治疗后 观察组3213.72±2.034.41±0.82对照组3219.55±2.697.64±1.18 t 9.78612.716 P<0.05<0.05
2.3 治疗前后两组Bax、Bcl-2 基因表达水平比较治疗前,两组Bax、Bcl-2 基因表达水平比较,均无显著性差异(P>0.05);治疗后,观察组Bax 表达水平明显高于对照组,Bcl-2 表达水平明显低于对照组,P<0.05。见表3。
表3 治疗前后两组Bax、Bcl-2 基因表达水平比较

表3 治疗前后两组Bax、Bcl-2 基因表达水平比较
组别 n 治疗前B ax治疗后 治疗前 Bc l-2治疗后观察组320.37±0.080.95±0.142.23±0.340.87±0.14对照组320.34±0.060.76±0.102.36±0.371.50±0.25 t 1.6976.2471.46412.438 P>0.05<0.05>0.05<0.05
3 讨论
PC 化疗方案是治疗晚期乳腺癌的常用方法。紫杉醇为抗微管细胞毒药物,可促进微管蛋白聚合,阻止其解聚,稳定微管,进而抑制微管网动态重组。此外,紫杉醇还会影响微管“束”排列,阻碍肿瘤细胞分裂。而卡铂为周期非特异性抗肿瘤药,可促使DNA链交叉联结,抑制癌细胞。紫杉醇与卡铂联用,可发挥协同作用,增强抗癌效果。陈海等[4]研究发现,紫杉醇联合卡铂治疗局部晚期乳腺癌,能减少复发及转移,有利于改善预后。
但对于HER2 阳性晚期乳腺癌患者,仅采用PC化疗方案,疗效不甚理想,原因可能在于HER2 的过度表达会抑制肿瘤细胞凋亡,加快其增殖,增强肿瘤侵袭性。因此,可以HER2 为靶点治疗HER2 阳性晚期乳腺癌。权利丰[5]研究发现,曲妥珠单抗联合紫杉醇新辅助化疗治疗HER2 阳性晚期局部晚期乳腺癌,可提高治疗效果,且复发率低。曲妥珠单抗为人源化单克隆抗体,能特异性作用于HER2 细胞外部位,与HER2 绑定,调控细胞信号传导,促使细胞内HER2 蛋白降解,杀伤肿瘤细胞[6]。此外,曲妥珠单抗可降低血管生长因子活性,抑制血管新生,并能增强细胞毒作用。曲妥珠单抗对肿瘤细胞有高度亲和性、靶向性,对非靶细胞杀伤较小。张国淳等[7]对曲妥珠单抗辅助治疗HER2 阳性乳腺癌进行回顾性生存分析发现,曲妥珠单抗辅助治疗能提高HER2 阳性乳腺癌患者长期生存率。本研究结果显示,观察组治疗有效率明显高于对照组,P<0.05。提示曲妥珠单抗联合PC 单周化疗方案治疗HER2 阳性晚期乳腺癌患者,能提高治疗效果。
肿瘤标志物为恶性肿瘤细胞异常物质,与恶性肿瘤发生发展密切相关。乳腺癌患者血清CA125 水平明显高于正常水平。CEA 为广谱性肿瘤标志物,在乳腺癌、结肠癌、肺癌等多种恶性肿瘤组织中均可检出。本研究结果显示,治疗后,观察组血清CA125、CEA 水平均明显低于对照组,P<0.05。表明曲妥珠单抗联合PC 单周化疗方案治疗HER2 阳性晚期乳腺癌患者,能有效控制肿瘤进展。正常细胞会由基因控制自主死亡,而恶性肿瘤细胞凋亡失控,主要与其相关基因表达异常有关。黄春军等[8]研究显示,注射用曲妥珠单抗用于局部晚期乳腺癌治疗,可上调Bax 基因表达水平,下调Bcl-2 基因表达水平。Bcl-2 为凋亡抑制基因,Bcl-2 过度表达会抑制细胞凋亡。而Bax 属于促凋亡基因,可与Bcl-2 蛋白结合,形成异源二聚体,干扰Bcl-2 抑制凋亡作用。本研究结果显示,治疗后,观察组Bax 表达水平明显高于对照组,Bcl-2 表达水平明显低于对照组,P<0.05。可见曲妥珠单抗应用于HER2 阳性晚期乳腺癌治疗,能调节Bcl-2、Bax 基因表达,加快肿瘤细胞凋亡。综上所述,曲妥珠单抗联合PC 单周化疗方案治疗HER2 阳性晚期乳腺癌患者,能提高治疗效果,调节Bcl-2、Bax 基因表达,加快肿瘤细胞凋亡,控制肿瘤进展。

