香蕉皮改性材料对废水中二价Cd离子的吸附特性与机理
平 巍,吴 彦,杨春霞,辛 倩,王 翔, 李 灵,张 敏,蒋昕辰,刘 利
香蕉皮改性材料对废水中二价Cd离子的吸附特性与机理
平 巍,吴 彦※,杨春霞,辛 倩,王 翔, 李 灵,张 敏,蒋昕辰,刘 利
(重庆三峡学院环境与化学工程学院,三峡库区水环境演变与污染防治重庆高校市级重点试验室,重庆 404100)
为探究农业生物质制备绿色吸附材料处理含Cd2+废水方法,以香蕉皮为原料,制备改性吸附材料。采用单因素试验,优化了改性工艺条件。通过静态吸附试验,结合等温模型和吸附动力学模型探讨了其对Cd2+吸附过程。利用比表面及孔径分析(brunner-emmet-teller)、扫描电镜(scanning electron microscope)、能谱仪(energy disperse spectroscopy)、元素分析仪、傅里叶变换红外光谱(Fourier transform infrared spectroscopy)等手段对改性前后材料的表面形态和结构进行表征,并分析了改性和吸附过程的机理。结果表明:改性较佳工艺条件为NaOH浓度为0.25 mol/L,改性时间为30 min。在此条件下香蕉皮改性后,对水中Cd2+的理论饱和吸附量由37.61 mg/g提高到87.15 mg/g,平衡时间由60 min缩短到45 min。吸附符合Langmuir等温模型(2=0.998)和准二级动力学模型(2=0.999)。改性后的香蕉皮对水中Cd2+的吸附以离子交换吸附为主。研究结果可为木质纤维素生物质改性制备绿色吸附材料处理含重金属废水提供理论依据。
生物质;重金属;吸附;改性;香蕉皮;Cd2+
0 引 言
镉(Cd)是一种重金属污染物,因其容易在生物体内富集[1]、毒性大[2-3],不能生物降解等特点,对人体健康威胁较大[4-5]。目前中国Cd污染形势严峻,覆盖11个省份25个地区[6],含镉废水的处理技术,亟待突破。吸附法被认为是去除环境重金属较为经济有效的方法[7]。目前,利用农林固体废弃物制备吸附材料,广泛应用于含重金属废水处理[8-10]。其中化学改性制备天然吸附剂,制备方法简单、成本低,产品具有可降解性和可再生性,具有独特的优势[11-12]。Munusamy等[13]以柠檬皮为原料,通过碱和草酸化学改性的柠檬皮纤维对Cu、Pb、Zn、Ni、Cd等众多离子都具有较高的吸附量;齐亚凤等[14]以甘蔗渣为原料,通过均苯四甲酸二酐(pyromellitic dianhydride, PMDA)乙二酸四乙酸二酐(tetraacetic anhydride oxalate, EDTAD)改性,对Cu2+和Zn2+的吸附量分别达到60.21 mg/g和33.45 mg/g;毛娜[15]以橘子皮为原料,通过氢氧化钾、乙醇和氯化钙进行皂化处理,对Zn2+的最大吸附量可达92 mg/g。
大量研究表明不同原料采用不同的改性方法得到材料,其吸附能力差别甚大[16]。香蕉皮中含有大量纤维素、半纤维素、木质素等膳食纤维,而且果胶和低聚糖含量丰富[17],较高的羟基基团含量[18-19]使得香蕉皮本身具有一定的吸附潜力。张才零等[20]在其研究中发现,香蕉皮对水中的Cd2+具备一定的吸附能力。Shang等[18]在其研究中发现,香蕉皮通过丁二酸酐改性之后,对水中的油类有较好的吸附性能;胡巧开等[21]研究发现,香蕉皮通过乙酸和乙醇浸泡改性后,能有效去除水中的Cr2O72–。郑文钊等[22]利用乙醇和乙酸改性香蕉皮,得到的材料对水中的Pb2+的最大吸附量为6.87mg/L。前期研究[23-25]发现,采用NaOH溶液对香蕉皮进行改性,能够有效提高其对氨氮和重金属离子的吸附能力,是一种较为可行的改性方法。但未对针对各类重金属吸附优化改性工艺条件,且改性机理尚不明确。
本文以香蕉皮为原料,通过NaOH改性制备吸附材料,吸附去除水中的Cd2+,通过单因素试验优化了改性工艺条件,在此基础上进一步研究了pH值、投加量、初始浓度和吸附时间对吸附过程的影响效果,并通过等温模型、动力学研究结合仪器表征探究了改性过程及其吸附Cd2+机理,以期为木质纤维素生物质改性制备绿色吸附材料处理含重金属废水提供参考。
1 材料与方法
1.1 试验材料
香蕉皮改性方法:市售香蕉取皮,用去离子水反复冲洗,于恒温干燥箱中(103±3)℃烘至恒质量,研磨成粉末,过筛(粒径0.18~0.25 mm),放入干燥器备用。称取10 g干香蕉皮粉末,放入2 L烧杯中,加入1 000 mL一定浓度的NaOH溶液,恒温水浴振荡器上以(25±2)℃恒温震荡一段时间后,抽滤,并用去离子水反复冲洗抽滤,直到滤液pH值为7且滤液无色透明,将获得的固体粉末(103±3)℃烘干即制得香蕉皮改性吸附材料。
为优化改性工艺,以Cd2+去除率为参指标,采用单因素试验讨论了改性剂浓度和改性时间2个条件对改性效果的影响,并找出较佳改性工艺条件。试验条件设置如下:
1)改性剂浓度的影响:固液比设置为10 g/L(称取10 g原香蕉皮加入1 L改性剂溶液),改性时间60 min,NaOH浓度因素水平设置为:0.05、0.1、0.15、0.2、0.25、0.3、0.4、0.5 mol/L。
2)改性时间的影响:固液比设置为10 g/L,改性剂浓度设置为0.25 mol/L,改性剂时间因素水平设置为:10、15、20、25、30、35、40、45、50、60 min。
材料的表征方法:材料的比表面积(brunner-emmet- teller)及孔径分布采用比表面及孔径分析仪(NOVA2000e,美国康塔仪器公司)测定;材料C、H的含量采用元素分析仪(EA3000,意大利欧维特公司)测定;材料表面形态采用扫描电子显微镜(JSM-7800F,日本电子株式会社)测定;材料表面元素组成采用能谱仪(Zeiss Supra 5,德国卡尔蔡司股份公司)测定;材料官能团结构采用傅里叶变换红外光谱仪(Nicolet 6700,美国尼高力仪器公司)进行KBr压片法测定。
1.2 吸附试验
量取50 mL的Cd2+溶液于250 mL锥形瓶中,用 0.2 mol/L的HCl和NaOH调节pH值,加入改性香蕉皮(粒径范围0.15~0.18 mm),然后置于恒温摇床(25± 1)℃中振荡,空白试验采用去离子水加入改性香蕉皮在同条件下振荡。达到试验设定的吸附时间后,用0.25m的水系滤膜进行过滤,收集滤液采用原子吸收分光光度计(AA7000,日本岛津公司)测定滤液中Cd2+的浓度。每次吸附试验重复3次,取均值,试验条件设置如下:
1)改性工艺的优化:Cd2+质量浓度100 mg/L,pH值为6±0.05,吸附时间为120 min。
2)吸附剂投加量影响试验:Cd2+质量浓度100 mg/L,pH值为6±0.05,吸附时间为120 min,吸附剂投加量因素水平设定为:1.2、1.6、2、3、4、6、8、12 g/L。
3)pH值影响试验:设定Cd2+浓度100 mg/L,吸附剂投加量为4 g/L,吸附时间为120 min(通过预试验确定)。考虑Cd2+在pH值>7的溶液中会发生水解,因此pH值因素水平为:3~7,梯度为0.5。
4)吸附等温拟合试验:pH值为6±0.05,吸附剂投加量4 g/L,吸附时间60 min(通过预试验确定),Cd2+浓度水平设定为:10、15、20、30,…,1 000 mg/L。
5)吸附动力学拟合试验:Cd2+浓度1 000 mg/L,pH值为6±0.05,投加量设定为4 g/L,因素水平设定为:1、2、5、10、15、20,…,120 min。
为探讨材料吸附性能的变化,试验过程中采用未改性的香蕉皮粉末作为对照,对照试验的方法和条件设置同上。
1.3 效果评价方法
吸附量的计算参照公式(1),去除率计算参照公式(2):


式中为去除率,%;q为吸附量,mg/g;0为吸附前Cd2+质量浓度,mg/L;为吸附后滤液Cd2+质量浓度,mg/L;为水样体积,L;为吸附剂投加量,g。
1.4 分析模型
1.4.1 等温模型
为了更好地探讨吸附行为,分别用Langmuir、Freundlich、Temkin和Dubinin-Radushkevich(D-R)等温吸附模型对试验结果拟合。
1)Langmuir假定吸附质以单分子层的形式均匀地被吸附在吸附剂的表面上,最后达到稳定值,即最大吸附量q[26-27]。

通过k的值可计算吸附平衡常数。
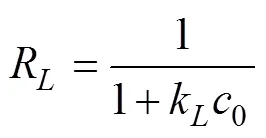
式中q为理论饱和吸附量,mg/g;k为 Langmuir吸附平衡常数,L/mg;R为吸附反应平衡常数,无量纲。
2)Freundlich模型通常能够模拟不均匀表面吸附剂的吸附行为,其吸附中心的吸附热呈指数下降[27-28]。

式中k为与吸附剂的吸附能力有关的常数,(mg/g)×(L/mg),是与吸附强度有关的常数,无量纲。
3)Temkin模型中,吸附质在吸附剂表面的吸附热随覆盖度的增大而线性降低[28-29]。

式中为Temkin方程平衡结合常数,mg/L;是与吸附热有关的系数,无量纲。
4)Dubinin-Radushkevich(D-R)等温模型
D-R模型能估算吸附自由能,并判断吸附过程的类型[28-29]。
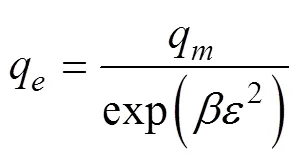


式中是D-R方程系数,mol2/J2;是Polanyi吸附势,J/mol;为理想气体常数,8.314 J/(mol·K);为绝对温度,K;为吸附自由能,J/mol。
1.4.2 动力学模型
吸附动力学是用吸附量随吸附时间的变化关系揭示吸附过程中的传质和反应规律。本研究采用以下4种动力学模型对改性香蕉皮吸附Cd2+吸附动力学数据进行拟合。
1)一级动力学模型用于描述边界扩散控制的单层吸附,基于假定吸附受扩散步骤的控制,吸附速率与平衡吸附量呈线性关系[27,30]。
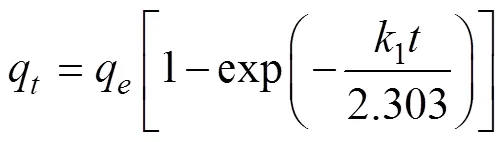
式中q为时刻的吸附量,mg/g;为吸附时间,min;1为一级吸附速率常数,min–1;
2)准二级动力学模型通常用于描述包括液膜扩散、表面吸附和孔内扩散的整个吸附过程,能够全面反映吸附过程的动力学机制[31-33]。
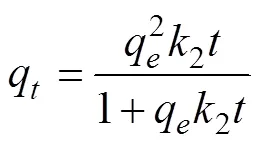
式中2为二级吸附速率常数,g/(mg·min)。
3)Elovich模型用于描述由反应速率和扩散因子综合调控的非均相扩散过程[32,34]。
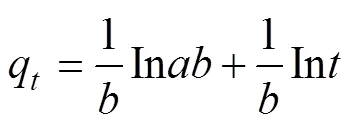
式中(g/(mg·min))、(g/mg)为Elovich方程常数,分别表示吸附速率及解吸常数。
4)粒子扩散模型用于描述孔内扩散为主导的吸附过程。用来判断其是否为吸附速率控制步骤[22,35]。
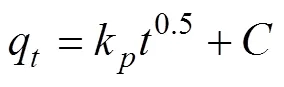
式中k为扩散速率常数,mg/(g·min0.5),为边界层常数,越大说明边界层对吸附的影响越大。
2 结果与分析
2.1 改性条件对去除率的影响
图1a为改性剂的浓度对材料去除Cd2+性能的影响,由图可知,当浓度从0.05提高至0.25 mol/L,去除率由67.45%升高至87.76%,进一步提高改性剂浓度,则去除率开始下降,这是因为NaOH能够有效溶解香蕉皮内的胶质[36],NaOH浓度较低时,这些胶质的去除不完全,改性不彻底;而浓度过高,则会破坏香蕉皮材料骨架,可能导致微观结构坍塌,因此,0.25 mol/L为较适宜的改性剂浓度。图1b为改性时间对材料去除Cd2+性能的影响,在改性时间为0~30 min范围内,延长改性时间对Cd2+的去除率有积极的作用,Cd2+去除率由72.30%升高至87.83%,然而,继续延长改性时间,则对Cd2+去除率影响不大,NaOH溶液随香蕉皮内的多糖、果胶等物质的浸出需要一定的反应时间[36],改性时间太短,反应还未完全发生,改性效果受限;而30 min后,改性反应基本完成,继续延长时间,对材料的影响甚微。因此,30 min是较为适宜的改性时间。
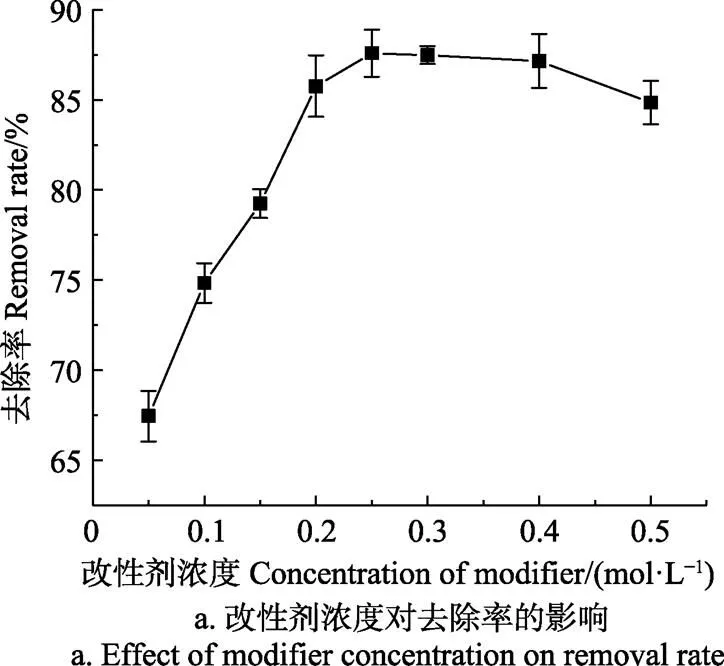
注:图a中Cd2+质量浓度为100 mg·L–1,改性固液比为10 g·L–1,改性时间为60 min。
Note: Concentration of Cd2+is 100 mg·L–1,modified solid-liquid ratio is 10 g·L–1, modification time is 60 min in Fig.a;

注:图b中Cd2+质量浓度为100 mg·L–1,改性剂浓度为0.25 mol·L–1,改性固液比为10 g·L–1
2.2 吸附材料投加量对去除率的影响
如图2所示,改性前后的香蕉皮对水中Cd2+的去除率均随着投加量的提高而升高。当吸附材料投加量从 1.2 g/L提高至4 g/L,改性前后的香蕉皮去除率分别由32.53%、63.3%上升至65.78%、86.8%。而吸附量则分别从27.11 、52.72 mg/L下降至16.45 、21.7 mg/L。进一步提高吸附剂投加量,2种材料对Cd2+去除率提升缓慢,而吸附量进一步降低。Ajmal等[35]研究稻壳对Cd2+的吸附也发现了类似规律。这可以解释为:溶液中可供吸附的点位随着投加量增加而增多,因此能够吸附去除更多的Cd2+。同时,也使得部分吸附点位空闲,因此单位吸附量下降[37]。对比2种材料对Cd2+的去除效果可以看出,改性后香蕉皮对Cd2+的去除效果显著增强(<0.05)。
2.3 pH值对去除率的影响
由图3可以看出,2种材料对Cd2+的吸附均随pH值的增大而增大。在pH值3~5范围内,无论改性前后的香蕉皮对Cd2+的去除率均低于50%,随着pH值的升高,去除率缓慢提升,说明吸附过程在酸性条件下明显受到抑制,这与郑文钊等[22]的研究结论是一致的。在低pH值条件下,吸附剂表面会带正电,同时材料中部分矿物质,如K+、Ca2+等离子在酸性条件下,释放到溶液中,和Cd2+存在强烈的竞争吸附,从而影响吸附效果[33]。随着pH值的进一步升高,去除率迅速提高,当pH值为6时,去除率达到87.71%。这是因为随着pH值的提高,H+的浓度下降,同时材料内可溶性矿物质释放量较少,产生的吸附竞争较弱[32]。另外,在较高的pH值条件下,改性吸附剂中一些极性官能团开始电离,也可能会参与到吸附过程中,通过-COOH和-OH对Cd2+进行离子交换机制或者H键作用发生吸附[25]。另外,由图3可知,改性前后的香蕉皮,在吸附达到平衡后,其pH值均高于初始pH值,推断一方面是因为材料本身的缓冲作用,另一方面是因为水中的Cd2+和吸附剂表面的K+、Ca2+、Na+等碱性粒子发生了交换的缘故。当pH值大于7,Cd2+开始水解沉淀,故试验不再针对更高的pH值作讨论。对比可发现,在试验pH值范围内,改性后的香蕉皮对Cd2+的去除能力均显著高于改性前(<0.05),表明改性方法对pH值具有较好的适应性。

注:Cd2+浓度为100 mg·L–1,pH值为6±0.05,吸附时间为120 min

注:Cd2+浓度为100 mg·L–1,吸附剂投加量为4 g·L–1,吸附时间为120 min
2.4 吸附等温模型分析
如图4所示,改性前后的香蕉皮对Cd2+的吸附量均随着Cd2+浓度的增加而提高。对于未改性的香蕉皮,在初始浓度10~300 mg/L(对应平衡浓度0.44~164.94 mg/L)范围内,Cd2+的吸附量呈线性增长趋势,吸附量从2.39迅速提高到33.76 mg/g。随着浓度的增加,吸附量提高趋势逐渐平缓,在400~1 000 mg/L(对应平衡浓度260.23~851.08 mg/L)范围内,Cd2+的吸附量仅从34.93提高到37.23 mg/g。改性后,在初始浓度为10~600 mg/L(对应平衡浓度0~306.13 mg/L)范围内,吸附量从2.32提高到79.96 mg/g,在初始浓度700~ 1 000 mg/L(对应平衡浓度384.18~676.06 mg/L)范围内,吸附量仅提高4.03 mg/g。这可以解释为当Cd2+浓度较低时,材料具有足够的吸附点位,而随着浓度的提高,这些吸附点位逐渐被吸附质占据,吸附趋于饱和。在初始浓度为1 000 mg/L时,改性前后的香蕉皮对Cd2+的吸附量分别为37.23、84.96 mg/g,因此,改性后的香蕉皮对Cd2+的吸附量显著提高(<0.05),而且适用的浓度范围更宽。
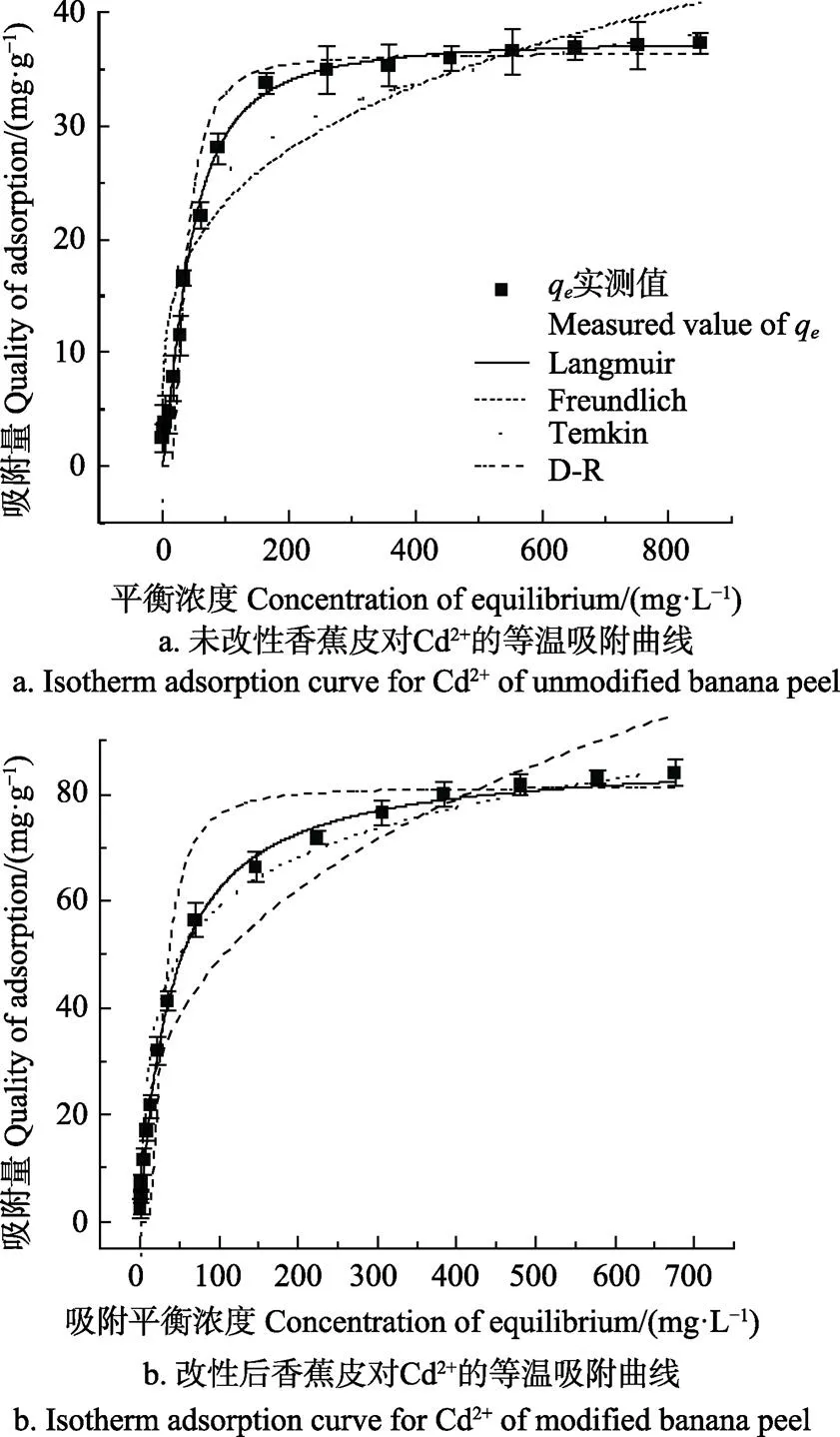
注:pH值为6±0.05,吸附剂投加量为4 g·L–1,吸附时间为120 min
对试验数据进行等温拟合,结果如图4和表1所示。Langmuir等温模型对2种材料的决定系数均大于0.99,且拟合的饱和吸附量与试验吸附量接近,这说明Langmuir等温模型均能较好地描述吸附机理,意味着吸附过程以单分子层吸附为主导[38],这与刘恒博等[39]研究改性小麦秸秆吸附Cd2+的结论类似。通过拟合参数k计算无量纲平衡常数R,未改性香蕉皮对Cd2+的R在0.18~0.96范围内,而改性后的香蕉皮的R在0.04~0.80范围内。通常,R的值在0~1之间,说明无论改性与否,香蕉皮对Cd2+的吸附均为有益吸附。

表1 吸附等温拟合参数
注:q是理论饱和吸附量;k是Langmuir吸附平衡常数;k为与吸附剂的吸附容量有关的Freundlich常数;是与吸附强度有关的 Freundlich 模型常数;为Temkin平衡结合常数;是 Temkin 方程与吸附热有关的系数;是吸附自由能;2为决定系数。
Note:qis the theoretical saturated adsorption;kis Langmuir adsorption equilibrium constant;kis the Freundlich constant related to the adsorptive capacity of adsorbents;is the Freundlich model constant related to the adsorptive strength;is the Temkin equilibrium binding constant;is the coefficient of the Temkin equation relating to the adsorption heat;is the adsorption free energy;2is coefficient of determination.
从Freundlich等温模型拟合结果看,改性香蕉皮对Cd2+的吸附1/值均小于0.5。表明吸附易于发生[30]。而改性后的香蕉皮的k值为9.837,高于未改性的香蕉皮,说明,香蕉皮改性后对Cd2+有更高的分配系数,即吸附能力更强[32]。Temkin模型对改性后的香蕉皮拟合值和值均高于未改性香蕉皮,表明香蕉皮改性后对Cd2+有更强的吸附势[38]。D-R模型中,改性前后的香蕉皮对Cd2+的吸附自由能分别为0.055、0.069 kJ/mol,平均吸附能在8~16 kJ/mol代表吸附过程为化学吸附,低于8 kJ/mol为物理吸附[32-33],因此,2种材料对Cd2+的吸附均为物理吸附,分子间作用力起到了重要作用。
2.5 吸附时间影响及动力学过程分析
如图5,改性前后的香蕉皮对Cd2+的吸附随时间变化趋势总体呈一致性,即先快后慢的趋势,这说明吸附过程严格受吸附材料的活性点位数量的控制[40-41]。即吸附前期吸附材料空闲活性点位数量多,因此吸附推动力很大。随着吸附时间的延长,水中Cd2+浓度逐渐减小,吸附材料表面的空闲活性点位变少,吸附传质推动力迅速减小,吸附速率逐渐下降并最终趋于饱和。改性前后2种材料分别在60 和45 min达到了吸附平衡。对应的吸附量分别为36.38和83.69 mg/g,这说明香蕉皮改性后,无论是吸附速率还是吸附量,都得到了强化。为进一步探讨改性前后的香蕉皮对水中Cd2+的吸附过程,分别用一级动力学模型、准二级动力学模型、Elovich模型和粒子扩散模型对试验数据拟合,结果图5和表2。由结果可知,香蕉皮改性前后对Cd2+的吸附准二级动力学决定系数更高,且准二级动力学模型拟合的平衡吸附量(未改性38.526 mg/g,改性85.957 mg/g)与试验值(未改性37.07 mg/g,改性84.56 mg/g)更接近,说明准二级动力学模型比一级动力学模型能更好地拟合两种材料对水中Cd2+吸附过程,这表明改性前后的香蕉皮对Cd2+的吸附为物理-化学复合过程[30]。从Elovich模型拟合结果分析,改性后香蕉皮的值明显高于改性前,值正好相反,说明改性后香蕉皮的吸附速率更快,解吸速率更低[34],因此,改性后的香蕉皮对Cd2+的吸附速率高于改性前,同时暗示了香蕉皮改性后,对Cd2+有更高的亲和力和更高的吸附势,这与Freundlich等温模型拟合结果一致。从粒子扩散模型拟合结果分析,改性后值(28.241 kJ/mol)大于未改性(11.259 kJ/mol),说明改性后的香蕉皮对Cd2+的吸附受边界层影响更大,更倾向于表面吸附[42-44]。
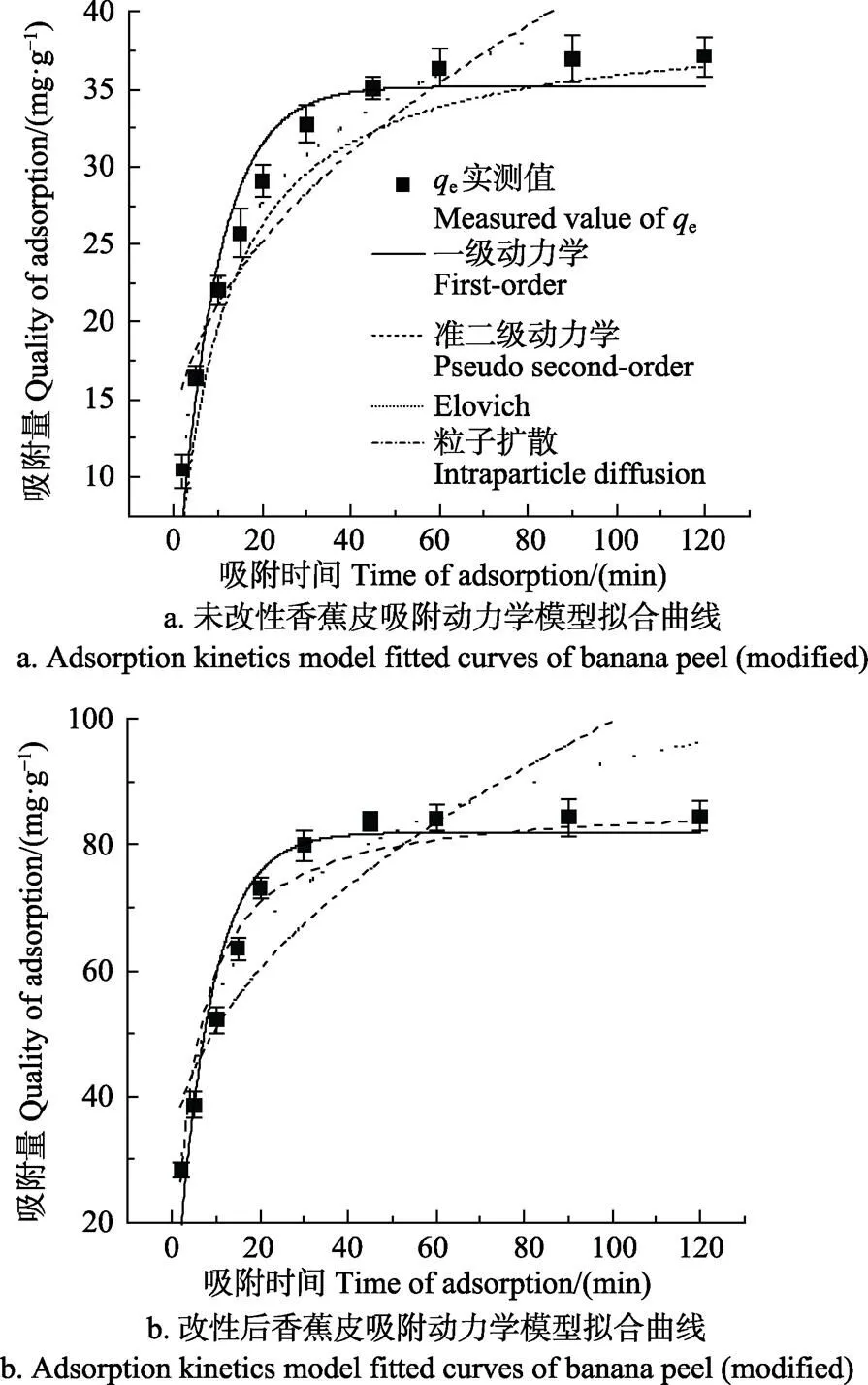
注:Cd2+浓度为100 mg·L–1,pH值为6±0.05,吸附剂投加量为4 g·L–1
2.6 讨 论
2.6.1 改性过程即吸附机理探讨
未改性和改性后的香蕉皮表面形态结构如图6所示。可以发现,香蕉皮经改性后,其表面的褶皱变得更突出,表面异构化程度明显提高。这是因为NaOH对香蕉皮内的果胶和多糖类物质具有强烈的溶解浸出作用[36],改性后香蕉皮表面覆盖和空隙内填充的胶质成分被去除,疏松的骨架结构开放外露,有利于离子扩散进入材料内部而被吸附。香蕉皮改性前后的比表面积和孔径分布如表3所示。由表3可以看出,对比改性前,改性后的香蕉皮BET比表面积、总孔容分别增加了108倍和3.6倍。其中,微孔容、介孔容和大孔容分别增加了35.3倍、3.48倍和2.7倍,微孔孔容大幅提高,对比表面积具有很大的贡献,并使得平均孔径下降。同时,应该指出,改性后的香蕉皮比表面积仍远小于活性炭[45]和生物炭[6,32-33],暗示了改性香蕉皮的吸附性能并不完全依赖其比表面积。
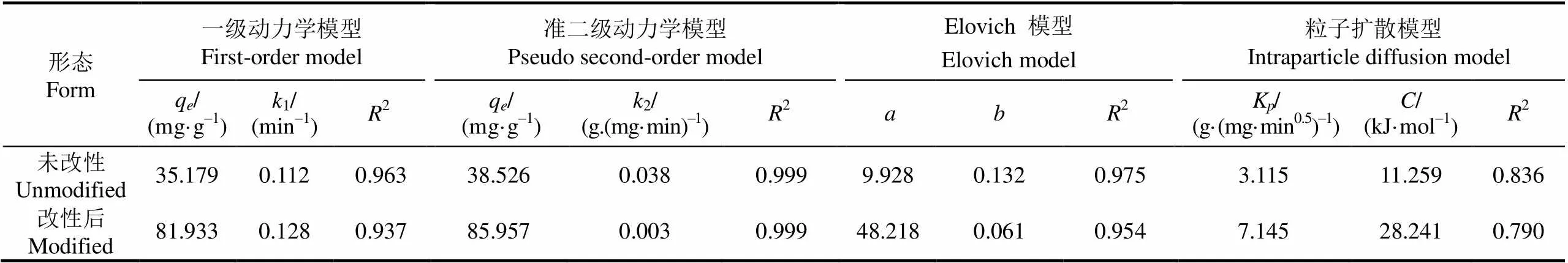
表2 吸附动力学拟合参数
注:q为吸附量;1为一级吸附速率常数;2为二级吸附速率常数;为 Elovich方程常数;K是颗粒内扩散速率常数;是边界层常数。
Note:qis the quantity of adsorption;1is first order adsorption rate constant;2is pseudo second-order adsorption rate constant;are Elovich equation constant;Kis intraparticle diffusion rate constant;is boundary layer constant.

图6 香蕉皮改性前后表面形态(× 2 000)

表3 香蕉皮改性前后比表面积及孔径分析
香蕉皮改性前后及改性香蕉皮吸附Cd2+后的表面元素组成见表4。对比改性前后香蕉皮的元素组成可知,改性后,C的相对含量提高,H和O的相对含量降低,这使得材料的H/C由0.158降低到0.102,而O/C比由0.731降低至0.469。H/C值降低,表明香蕉皮改性后芳香性增强,结构变得更稳强[46],而O/C值降低说明改性后材料极性下降[47]。这些改变有利于材料在水中保持稳定的形态,有利于Cd2+的吸附。另一方面,改性后,K相对含量降低了4.38个百分点,而Na的相对含量从0增加至1.55%,推测在改性过程中,NaOH电离出的Na+进入了材料内部,取代了香蕉皮中的K和部分游离H。从离子交换的角度分析,Na+的交换势低于K+和H+[48],因此,该过程有利于Cd2+通过离子交换被材料吸附。而吸附Cd2+后,未改性香蕉皮和改性后的香蕉皮Cd2+相对含量分别从0增加至3.65%,和8.03%,证实Cd2+确实被两种材料吸附,也表明改性后的香蕉皮对Cd2+的吸附能力有所提高。此外,未改性的香蕉皮在吸附Cd2+后,K含量从4.9%降低到2.93%,同时H/C由0.158降低到0.141,这可以解释为吸附过程中,Cd2+与香蕉皮中的K和H发生了交换作用。而改性后的香蕉皮在吸附Cd2+后,K和Na的相对含量均降至0,这说明在吸附过程,材料中的K、Na等金属元素中与Cd2+发生了离子交换,同时,H/C比和O/C变化幅度不大,说明其他元素成分变化不大,暗示了离子交换是吸附的主要方式。对比可知,未改性的香蕉皮K元素交换不彻底,这是因为改性前,大量多糖物质和可溶性纤维覆盖在材料表面,阻碍了Cd2+与材料充分接触。而改性后的香蕉皮,在去除表面覆盖物后,内部结构开放外露,使得离子交换彻底完成,因此,改性有利于香蕉皮对Cd2+的吸附。

表4 未改性和改性后香蕉皮吸附Cd2+前后元素组成分析
图7是未改性和改性后的香蕉皮分别在吸附Cd2+前后的傅里叶变换红外光谱(Fourier transform infrared spectroscopy, FT-IR)。对比改性前后香蕉皮的FT-IR图谱,均含有O-H(3 320cm–1)、C-H (2 910 cm–1)、C=O (1 600 cm–1)、C-C(1 390 cm–1)、C-O(1 020 cm–1)[49]。香蕉皮改性后,3 320 cm–1的峰有所减弱,这是因为一方面,部分含O-H的成分在改性过程中被溶出,这与材料在改性前后O/C比变小推断一致。另一方面,材料表面部分缔合O-H的H被Na取代导致材料O-H含量降低;此外,改性后,2 910 cm–1处C-H伸缩振动增强,说明改性后材料C-H相对含量增加;1 600 cm–1处的峰形发生了明显的变化,是因为Na+与C=C键提供的 π电子形成了基团结构导致的;1 020 cm–1处的峰明显增强,这说明部分C-O中的氧原子与Na结合成键。未改性香蕉皮在吸附Cd2+后,O-H基峰明显减弱,表明O-H被Cd2+占据,说明O-H与Cd2+发生配体交换作用,郭文娟等[50]在研究生物炭吸附Cd2+时发现了同样的现象;1 600 cm–1处的峰型变化,说明C=C键提供的π电子与Cd2+结合生成了新的结构,即发生了阳离子―π键作用[6,33]。1 020 cm–1处吸收峰明显增强,说明C-O基团中的氧原子参与成键,在吸附过程中与Cd2+发生了配位。而改性后的香蕉皮在吸附Cd2+后,峰位置和峰形变化均不明显,说明吸附前后官能团无明显变化,由此推断材料中的Na、K等元素与Cd2+发生的离子交换是其吸附的主要途径,这与之前吸附前后材料的元素组成变化得到的结论是一致的。离子交换的本质是吸附剂表面带负电荷基团与溶液中带正电荷的重金属离子之间的静电作用[51],而阳离子―π键作用中也存在静电力。静电作用主要是由库仑力引起的,吸附能较低,偏向物理吸附作用[37],这与香蕉皮吸附Cd2+的(表1)值较低相符。

图7 未改性和改性后的香蕉皮吸附Cd2+前后傅里叶变换红外光谱
基于试验数据和表征结果,可以推断香蕉皮改性前后的变化及其对水中Cd2+的吸附机理,如图8所示。香蕉皮中含有大量的纤维,富含各类活性基团,在改性前具备对Cd2+一定的吸附潜力。然而香蕉皮表面被大量多糖、果胶等物质覆盖,导致在吸附过程中,Cd2+很难扩散进入材料内部。改性后,香蕉皮表面及空隙内填充的多糖和果胶被NaOH溶液溶出,留下结构疏松且富含大量活性基团的纤维骨架,有利于Cd2+扩散进入材料空隙内部充分吸附。同时,通过改性,材料中引入了离子交换势很小的Na,因此对Cd2+的亲和提高。
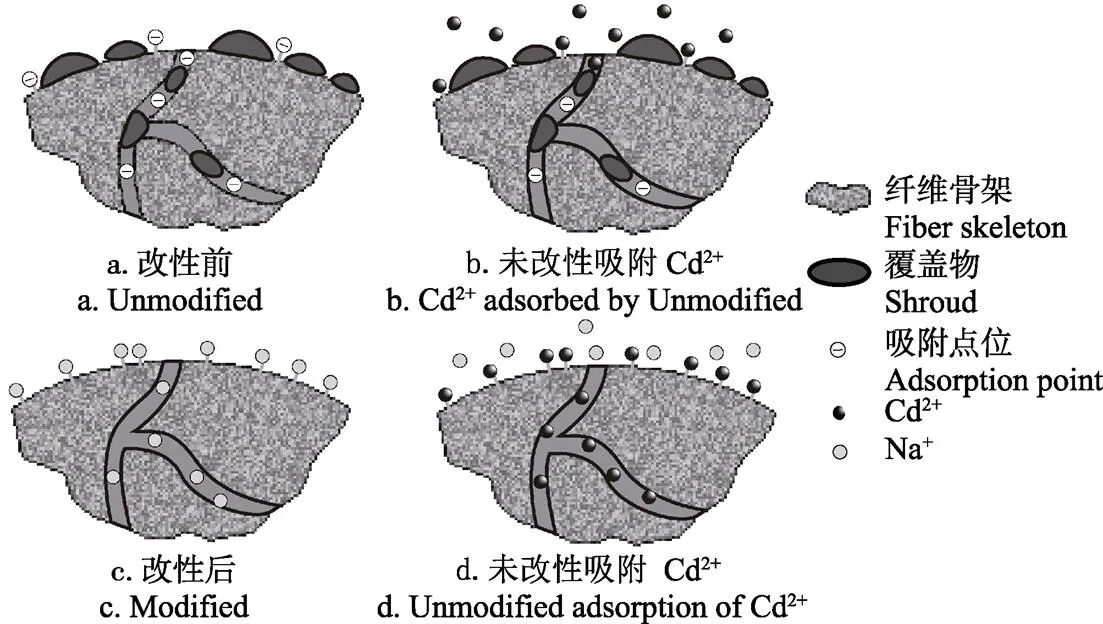
图8 香蕉皮改性过程及对Cd2+的吸附机理
2.6.2 改性香蕉皮对Cd2+的吸附性能及应用
如表5,对比发现,各类吸附材料对Cd2+的吸附差异较大,本研究采用NaOH改性香蕉皮对Cd2+的吸附量高于一般生物炭和改性生物质材料。达到吸附平衡的时间仅略长于棉花秸秆生物炭和改性小麦壳,由此可见,改性香蕉皮对Cd2+的吸附在能够在较短的时间内即可达到较高的吸附量,即在平衡时间和吸附量2个方面都具有一定优势。鉴于改性香蕉皮为粉末状,可作为一次性的吸附材料,用作水体修复等领域,此外,朱中原[36]在其研究中表明,NaOH浸泡的香蕉皮实质上是一种水不溶性膳食性纤维,在医药领域有应用的潜力。后续可以对材料的成型进行进一步研究,提高工程应用的价值。

表5 不同生物质吸附材料对Cd2+吸附性能比较
3 结 论
1)NaOH改性香蕉皮能够提高对水中Cd2+的吸附性能,其较优改性工艺条件为NaOH浓度0.25 mol/L、改性时间30 min。在此工艺条件下对香蕉皮改性后,其对Cd2+的吸附达到平衡的时间由60 min缩短到45 min,饱和吸附量由37.61 mg/g提高到87.15 mg/g。
2)改性前后的香蕉皮对水中Cd2+吸附符合Langmuir等温模型,动力学模型符合准二级动力学模型,说明两种材料吸附Cd2+为单分子层吸附,吸附过程属于物理-化学复合过程。
3)香蕉皮改性后表面的胶质覆盖物被去除,使得吸附点位完全暴露出来,且引入了大量Na,这是其吸附Cd2+性能提升的主要原因。
[1] 鲁雪梅,熊鹰,张广之. 树脂在重金属水处理中的应用[J]. 北京大学学报(自然科学版),2012,48(6):1030-1038.Lu Xuemei, Xiong Ying, Zhang Guangzhi. Application of resins on the treatment of waters polluted by heavy metals[J]. Acta Scientiarum Naturalium Universitatis Pekinensis, 2012, 48(6): 1030-1038. (in Chinese with English abstract)
[2] 郭卉,虞敏达,何小松,等. 南方典型农田区浅层地下水污染特征[J]. 环境科学,2016,37(12):4680-4689.Guo Hui, Yu Minda, He Xiaosong, et al. Pollution characteristics analysis in shallow groundwater of typical farmland area, southern China[J]. Environmental Science, 2016, 37(12): 4680-4689. (in Chinese with English abstract)
[3] Islam M S, Ahmed M K, Raknuzzaman M, et al. Heavy metal pollution in surface water and sediment: A preliminary assessment of an urban river in a developing country[J]. Ecological Indicators, 2015, 48(48): 282-291.
[4] 何昱轩,张黎明,郭飞飞,等. 硅基吸附剂处理含镉废水的研究进展[J]. 化工进展,2018,37(2):724-736.He Yuxuan, Zhang Liming, Guo Feifei, et al. Advances in cadmium removal from wastewater by silica-based materials[J]. Chemical Industry and Engineering Progress, 2018, 37(2): 724-736. (in Chinese with English abstract)
[5] Shah M T, Ara J, Muhammad S, et al. Health risk assessment via surface water and sub-surface water consumption in the mafic and ultramafic terrain, Mohmand agency, northern Pakistan[J]. Journal of Geochemical Exploration, 2012, 118: 60-67.
[6] 王震宇,刘国成,Monica Xing,等. 不同热解温度生物炭对Cd(Ⅱ)的吸附特性[J]. 环境科学,2014,35(12):4735-4744.Wang Zhenyu, Liu Guocheng, Monica Xing, et al. Adsorption of Cd(Ⅱ) varies with biochars derived at different pyrolysis temperatures[J]. Environmental Science, 2014, 35(12): 4735-4744. (in Chinese with English abstract)
[7] Zhu Q, Wu J, Wang L, et al. Adsorption characteristics of Pb2+onto wine lees-derived biochar[J]. Bull Environ Contam Toxicol, 2016, 97(2): 294-299.
[8] Xu X, Cao X, Zhao L, et al. Removal of Cu, Zn, and Cd from aqueous solutions by the dairy manure-derived biochar[J]. Environmental Science & Pollution Research International, 2013, 20(1): 358-368.
[9] 柳琴,郝林林,郑彤,等. 改性木屑对水中Cr(Ⅵ)的吸附性能[J]. 环境工程学报,2015,9(3): 1021-1026.Liu Qin, Hao Linlin, Zheng Tong, et al. Adsorptive performance of chromium(Ⅵ) by modified sawdust[J]. Chinese Journal of Environmental Engineering, 2015, 9(3): 1021-1026. (in Chinese with English abstract)
[10] Jin H M, Hanif M U, Capareda S, et al. Copper(II) removal potential from aqueous solution by pyrolysis biochar derived from anaerobically digested algae-dairy-manure and effect of KOH activation[J]. Journal of Environmental Chemical Engineering, 2016, 4(1): 365-372.
[11] Qu J, Meng X, Jiang X, et al. Enhanced removal of Cd(II) from water using sulfur-functionalized rice husk: Characterization, adsorptive performance and mechanism exploration[J]. Journal of Cleaner Production, 2018, 183(10): 880-886.
[12] 许芳,张利平,程先忠,等. 改性桑树叶吸附材料对废水中Cd(Ⅱ)的吸附性能研究[J]. 岩矿测试,2016,35(1):62-68.Xu Fang, Zhang Liping, Cheng Xianzhong, et al. Study on biosorption performance of Cd(Ⅱ) in waste water by modified mulberry leaves[J]. Rock and Mineral Analysis, 2016, 35(1): 62-68. (in Chinese with English abstract)
[13] Munusamy T A, Lai Y L, Lin L C, et a1. Cellulose based native and surface modified fruit pee is for the adsorption of heavy metal ions from aqueous solution: langrnuir adsorption isotherms[J]. Journal of Chemical and Engineering Data, 2010, 55(3): 1186-1192.
[14] 齐亚凤,何正艳,余军霞,等. 改性甘蔗渣对Cu2+和Zn2+的吸附机理[J]. 环境工程学报,2013,7(2):585-590. Qi Yafeng, He Zhengyan, Yu Junxia, et al. Adsorption mechanism for Cu2+and Zn2+by modified bagasse[J]. Chinese Journal of Environmental Engineering, 2013, 7(2): 585-590. (in Chinese with English abstract)
[15] 毛娜. 改性橘子皮对水中金属离子的吸附[J]. 广州化工,2014,42(22):108-110. Mao Na, The adsorption capacity of zinc and iron of water by modified orange peel[J]. Guangzhou Chemical Industry, 2014, 42(22): 108-110. (in Chinese with English abstract)
[16] 李思,章宇飞,张金辉,等. 改性材料吸附处理重金属废水的研究进展[J]. 当代化工,2013,42(8):1093-1096. Li Si, Zhang Yufei, Zhang Jinhui, et al. Research progress in adsorption treatment of heavy metal wastewater by modified materials[J]. Contemporary Chemical Industry, 2013, 42(8): 1093-1096. (in Chinese with English abstract)
[17] Khawas P, Deka S C. Comparative nutritional, functional, morphological, and diffractogram study on culinary banana peel at various stages of development[J]. International Journal of Food Properties, 2016, 19(12): 2832-2853.
[18] Shang W, Sheng Z, Shen Y, et al. Study on oil absorbency of succinic anhydride modified banana cellulose in ionic liquid[J]. Carbohydrate Polymers, 2016, 141(5): 135-142.
[19] 刘志江,李檬,肖惠宁,等. 改性纤维素的制备及分光光度法对Cu2+吸附研究[J]. 影像科学与光化学,2017,35(3):274-280. Liu Zhijiang, Li Meng, Xiao Huining, et al. Novel amino modified cellulose for copper(Ⅱ) adsorption via spectrophotometry[J] Imaging Science and Photochemistry, 2017, 35(3): 274-280. (in Chinese with English abstract)
[20] 张才灵,罗楠,智霞,等. 香蕉皮和香蕉叶对重金属Cd2+离子的吸附性能研究[J]. 广州化工,2013,41(14),52-55. Zhang Cailing, Luo Nan, Zhi Xia, et al. Absorption behavior for heavy metal Cd2+cations of banana peels and banana leaves[J]. Guangzhou Chemical Industry, 2013, 41(14): 52-55. (in Chinese with English abstract)
[21] 胡巧开,余中山. 改性香蕉皮吸附剂对六价铬的吸附[J]. 工业用水与废水,2012,43(5):67-70.Hu Qiaokai, Yu Zhongshan. Adsorption of Cr(VI) by modified banana peel[J]. Industrial Water & Wasterwater, 2012, 43(5): 67-70. (in Chinese with English abstract)
[22] 郑文钊,胡巧开,陈芳,等. 改性香蕉皮对Pb2+的吸附研究[J]. 离子交换与吸附,2013,29(5):440-448. Zheng Wenzhao, Hu Qiaokai, Chen Fang, et al. Adsorption of Pb2+by modified banana peels[J]. Ion Exchange and Adsorption, 2013, 29(5): 440-448. (in Chinese with English abstract)
[23] 董建丰. 香蕉皮改性吸附剂的制备及其吸附性能研究[D]. 重庆:重庆大学,2015. Dong Jianfeng. Study on Preparation and Adsorption Capability of the Modified Banana Peel Adsorbent[D]. Chongqing: Chongqing University, 2015. (in Chinese with English abstract)
[24] 平巍,李波,董建丰,等. 生物质改性吸附材料的制备工艺优化及对氨氮的吸附特性[J]. 农业环境科学学报,2017,36(12):2521-2526. Ping Wei, Li Bo, Dong Jianfeng, et al. Optimization of preparation technology for biomass-modified adsorption material and its adsorption properties for ammonia nitrogen[J]. Journal of Agro-Environment Science, 2017, 36(12): 2521-2526. (in Chinese with English abstract)
[25] 董建丰,平巍,张六一,等. 香蕉皮改性吸附剂对氨氮吸附特性[J]. 环境工程学报,2016,10(4):1807-1812. Dong Jianfeng, Ping Wei, Zhang Liuyi, et al. Adsorption characteristics of banana peel modified adsorbent[J]. Chinese Journal of Environmental Engineering, 2016, 10(4): 1807-1812. (in Chinese with English abstract)
[26] Demi̇Ral H, GündüzoğLu G. Removal of nitrate from aqueous solutions by activated carbon prepared from sugar beet bagasse[J]. Bioresource Technology, 2010, 101(6): 1675-1680.
[27] Fang C, Zhang T, Li P, et al. Application of magnesium modified corn biochar for phosphorus removal and recovery from swine wastewater[J]. International Journal of Environmental Research & Public Health, 2014, 11(9): 9217-9237.
[28] BalarakD, Mostafapour F, AzarpiraH.Temkin and dubinin- radushkevich isotherms studies of equilibrium sorption of ampicilin unto montmorillonite nanoparticles[J]. Journal of Pharmaceutical Research Internationa, 2017, 20(2): 1-9.
[29] Dada A O, Olalekan A P, Olatunya A M, et al. Langmuir, freundlich, temkin and dubinin-radushkevich isotherms studies of equilibrium sorption of Zn2+unto phosphoric acid modified rice husk[J].IOSR Journal of Applied Chemistry, 2012, 3(1): 38-45.
[30] Lagergren S. About the theory of so-called adsorption of solution substances[J]. Kungliga Svenska Vetenskapsakademiens Handlinger, 1898, 24(4): 1-39.
[31] 常春,刘天琪,廉菲,等. 不同热解条件下制备的秸秆炭对铜离子的吸附动力学[J]. 环境化学,2016,35(5):1042-1049. Chang Chun, Liu Tianqi, Lian Fei, et al. Adsorption kinetics of copper ion on straw biochars prepared under different pyrolysis condition[J]. Environmental Chemistry, 2016, 35(5): 1042-1049. (in Chinese with English abstract)
[32] 张连科,刘心宇,王维大,等. 油料作物秸秆生物炭对水体中铅离子的吸附特性与机制[J]. 农业工程学报,2018,34(7):218-226. Zhang Lianke, Liu Xinyu, Wang Weida, et al. Characteristics and mechanism of lead adsorption from aqueous solutions by oil crops straw-derived biochar[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2018, 34(7): 218-226. (in Chinese with English abstract)
[33] 王彤彤,马江波,曲东,等. 两种木材生物炭对铜离子的吸附特性及其机制[J]. 环境科学,2017,38(5):2161-2171. Wang Tongtong, Ma Jiangbo, Qu Dong, et al. Characteristics and mechanism of copper adsorption from aqueous solutions on biochar produced from sawdust and apple branch[J]. Environmental Science, 2017, 38(5): 2161-2171. (in Chinese with English abstract)
[34] Peers A M. Elovich adsorption kinetics and the heterogeneous surface[J]. Journal of Catalysis, 1965, 4(4): 499-503.
[35] Ajmal M, Rao R A, Anwar S, et al. Adsorption studies on rice husk: Removal and recovery of Cd(II) from wastewater[J]. Bioresource Technology, 2003, 86(2): 147-149.
[36] 朱中原. 香蕉皮中水不溶性膳食纤维提取工艺研究[J]. 食品工程,2012(3):29-31. Zhu Zhongyuan. Study on extraction of soluble dietary fiber in banana peel[J]. Food Engineering, 2012(3): 29-31. (in Chinese with English abstract)
[37] 陈雷,韩杨,席北斗,等. 粉煤灰提铝中间产物合成4A分子筛对氨氮的吸附行为研究[J]. 环境科学学报,2018,38(3):993-1000. Chen Lei, Han Yang, Xi Beidou, et al. Adsorption of ammonium with 4A zeolite synthesized by using byproducts duringalumina extraction from fly ash[J]. Acta Scientiae Circumstantiae, 2018, 38(3): 993-1000. (in Chinese with English abstract)
[38] 罗来盛,周美华. 微波活化制备加拿大一枝黄花活性炭及对Cd(Ⅱ)的吸附[J]. 环境工程学报,2012,6(5):1543-1547. Luo Laisheng, Zhou Meihua. Adsorption of Cd(Ⅱ) ions onto activated carbon prepared from solidago canadensis by means of microwave activated[J]. Chinese Journal of Enviromental Engineering, 2012, 6(5): 1543-1547. (in Chinese with English abstract)
[39] 刘恒博,徐宝月,李明明,等. 改性小麦秸秆对水中Cd2+吸附的研究[J]. 水处理技术,2013,39(4):15-19. Liu Hengbo, Xu Baoyue, Li Mingming, et al. Adsorption of aquatic cadmium(II) by modified wheat straw[J]. Technology of Water Treatment, 2013, 39(4): 15-19. (in Chinese with English abstract)
[40] Belayachi A, Bestani B, Bendraoua A, et al. The influence of surface functionalization of activated carbon on dyes and metal ion removal from aqueous media[J]. Desalination & Water Treatment, 2016, 57(37) :17557–17569
[41] Ho Y S, Mckay G. Pseudo-second order model for sorption processes[J]. Process Biochemistry, 1999, 34(5): 451-465.
[42] Li N, Bai R, Liu C. Enhanced and selective adsorption of mercury ions on chitosan beads grafted with polyacrylamide via surface-initiated atom transfer radical polymerization[J]. Langmuir the Acs Journal of Surfaces & Colloids, 2005, 21(25): 11780.
[43] Cruz C C V, Costa A C A D, Luna A S. Kinetic modeling and equilibrium studies during cadmium biosorption by dead Sargassum, sp. biomass[J]. Bioresource Technology, 2004, 91(3): 249-257.
[44] Weber W, Morris J. Proceeding of International Conference on water pollution symposium[M]. Oxford: Pergamon Press, 1962.
[45] Hasegawa G. Monolithic electrode for electric double-layer capacitors based on macro/meso/microporous S-containing activated carbon with high surface area[J]. Journal of Materials Chemistry, 2011, 21(7): 2060-2063.
[46] 简敏菲,高凯芳,余厚平. 不同裂解温度对水稻秸秆制备生物炭及其特性的影响[J]. 环境科学学报,2016,36(5):1757-1765. Jian Minfei, Gao Kaifang, Yu Houping. Effects of different pyrolysis temperatures on rice straw preparation of bio-char and its characteristics[J]. Acta Scientiae Circumstantiae, 2016, 36(5): 1757-1765.(in Chinese with English abstract)
[47] Singh B, Singh B P, Cowie A L. Characterisation and evaluation of biochars for their application as a soil amendment[J]. Australian Journal of Soil Research, 2010, 48(6/7): 516-525
[48] 袁俊生,杨永春. 钠型斜发沸石在K+-Na+-NH4+和K+-Na+-Ca2+水溶液体系中的离子交换平衡[J]. 离子交换与吸附,2008,24(6):496-503. Yuan Junsheng, Yang Yongchun. Ion exchange equilibria between clinoptilolite and aqueous solutions of K+-Na+-Ca2+and K+-Na+-NH4+[J]. Ion Exchange and Adsorption, 2008, 24(6): 496-503. (in Chinese with English abstract)
[49] 丁文川,杜勇,曾晓岚,等. 富磷污泥生物炭去除水中 Pb(Ⅱ)的特性研究[J]. 环境化学,2012,31(9):1375-1380. Ding Wenchuan, Du Yong, Zeng Xiaolan, et al. Aqueous solution Pb(Ⅱ) removal by biochar derived from phosphorusrich excess sludge[J]. Environmental Chenistry, 2012, 31(9): 1375-1380. (in Chinese with English abstract)
[50] 郭文娟,梁学峰,林大松,等. 土壤重金属钝化修复剂生物炭对镉的吸附特性研究[J]. 环境科学,2013,34(9):3716-3721. Guo Wenjuan, Liang Xuefeng, Lin Dasong, et al. Adsorption of Cd2+on biochar from aqueous solution[J]. Environmental Science, 2013, 34(9): 3716-3721.
[51] 李力,陆宇超,刘娅,等. 玉米秸秆生物炭对Cd(Ⅱ)的吸附机理研究[J]. 农业环境科学学报,2012,31(11):2277-2283. Li Li, Lu Yuchao, Liu Ya, et al. Adsorption mechanisms of Cd(Ⅱ) on biochars derived from corn straw[J]. Journal of Agro-Environment Science, 2012, 31(11): 2277-2283.
[52] Xu X, Cao X, Zhao L, et al. Removal of Cu, Zn, and Cd from aqueous solutions by the dairy manure-derived biochar[J]. Environmental Science & Pollution Research, 2013, 20(1): 358-368.
[53] 林芳芳,易筱筠,党志,等. 改性花生壳对水中Cd2+和Pb2+的吸附研究[J]. 农业环境科学学报,2011,30(7):1404-1408. Lin Fangfang, Yi Xiaoyun, Dang Zhi, et al. Adsorption of Cd2+and Pb2+from Aqueous Solution by Modified Peanut Shells[J]. Journal of Agro-Environment Science, 2011, 30(7): 1404-1408. (in Chinese with English abstract)
[54] 郭学益,肖彩梅,梁莎,等. 改性柿子粉吸附剂对Cd2+的吸附性能[J]. 中南大学学报(自然科学版),2012,43(2): 9-14. Guo Xueyi, Xiao Caimei, Liang Sha, et al. Adsorption of Cd2+by chemically modified persimmon powder[J]. Journal of Central South University(Science and Technology), 2012, 43(2): 9-14. (in Chinese with English abstract)
[55] 梁东旭,罗春燕,周鑫,等. 改性小麦壳对水溶液中Cd2+的吸附研究[J]. 农业环境科学学报,2015,34(12):2364-2371. Liang Dongxu, Luo Chunyan, Zhou Xin, et al. Adsorption of Cd2+from aqueous solution by modified wheat chaff[J]. Journal of Agro-Environment Science, 2015, 34(12): 2364-2371. (in Chinese with English abstract)
Properties and mechanism of Cd(II) adsorption from waste water by modified banana peel
Ping Wei, Wu Yan※, Yang Chunxia, Xin Qian, Wang Xiang, Li Ling, Zhang Min, Jiang Xinchen, Liu Li
(404100
In order to explore the method of preparing green adsorption material from agricultural biomass to treat waste-water containing Cd2+, the banana peel was modified by NaOH to adsorb Cd2+. The condition of modification and adsorption process were discussed through static adsorption experiment combined with isotherm (involve Langmuir, Freundlich, Temkin and D-R) and kinetics models (involve First-order, Pseudo Second-order, Elovich and Intraparticle diffusion). The surface structure and properties were characterized by using Brunauer-Emmett-Teller (BET) surface area and pore size analysis, scanning electron microscope (SEM), energy dispersive spectrometer (EDS), element analyzer (EA) and Fourier transform infrared spectrometer (FTIR), which were used to explore the mechanism of modification and adsorption. The results of optimized modification conditions showed that NaOH was 0.25 mol/L, modification time was 30 min. Static adsorption experiment showed that adsorption capacity of modified banana peel reached 87.15 mg/g and the Equilibrium time reached 45 min. The results showed that under the same conditions, the dosage of 4 g/L and the pH value of 6 were better than those of unmodified banana peel (adsorption capacity = 37.61 mg/g, equilibrium time = 60 min). BET specific surface area and pore size analysis confirmed that the specific surface area and total pore volume increased 108 times and 3.6 times respectively after modification. Scanning electron microscopy showed that the surface became uneven and wrinkled after modification. The changes mentioned above were conducive for Cd2+to enter the interior of the material along through diffusion,thus contacting and reacting fully with adsorbent. According to the change of element composition, the H/C ratio of the modified banana peel decreased from 0.158 to 0.102, while the K content decreased by 4.38 percentage points, while the Na content increased by 1.55 percentage points after the modification, indicating the exchange reaction between K and Na.Furthermore, FTIR denoted active functional groups such as O-H (3 320 cm–1), C-H (2 910 cm–1), C=O (1 600 cm–1), C-C (1 390 cm–1), C-O (1 020 cm–1) were found on the surfaces of banana peel whether modified or not, indicated good adsorption potential for Cd2+. The results showed that the isothermal adsorption and adsorption kinetics of banana peel under different modification conditions were described by Langmuir isotherm model and pseudo-second order model, respectively. The results showed that Cd2+ions were adsorbed by unmodified and modified banana peel through a single layer membrane, and the mechanism of Cd2+was complex interaction of physical and chemical factors. Freundlich, D-R isotherm model and Elovich kinetic fitting results showed that banana peel had a strong affinity for Cd2+and the adsorption capacity was enhanced after modification. Combined with characterization and model analysis, it was concluded that the adsorptive mechanism of raw banana for Cd2+was multiple, including ion exchange/ligand exchange, cation-π and electrostatic interaction, while the adsorptive mechanism of modified banana peel for Cd2+was ion exchange. The results showed that NaOH modified banana peel had good adsorbability for Cd2+in aqueous solution. This conclusion will provide an important theoretical basis for the preparation of environmental friendly adsorbents from lignocellulose biomass to remove heavy metals from polluted water.
biomass; heavy metals; adsorption; modification; banana peel; Cd2+
2018-08-19
2019-04-07
国家自然科学基金项目(31670467);重庆市教委科学技术研究项目(KJ1401023)
平 巍,讲师,主要从事水处理技术、固体废物资源化研究。Email:1510069@qq.com
吴 彦,讲师,博士,主要从事固体废物资源化技术研究。Email:wuyan19850827@hotmail.com
10.11975/j.issn.1002-6819.2019.08.032
X712
A
1002-6819(2019)-08-0269-11
平 巍,吴 彦,杨春霞,辛 倩,王 翔,李 灵,张 敏,蒋昕辰,刘 利.香蕉皮改性材料对废水中二价Cd离子的吸附特性与机理[J]. 农业工程学报,2019,35(8):269-279. doi:10.11975/j.issn.1002-6819.2019.08.032 http://www.tcsae.org
Ping Wei, Wu Yan, Yang Chunxia, Xin Qian, Wang Xiang, Li Ling, Zhang Min, Jiang Xinchen, Liu Li.Properties and mechanism of Cd(II) adsorption from waste water by modified banana peel[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2019, 35(8): 269-279. (in Chinese with English abstract) doi:10.11975/j.issn.1002-6819.2019.08.032 http://www.tcsae.org

