鞘内吗啡泵植入治疗顽固性癌痛
李富波,龚格格,任长和,欧册华
(西南医科大学附属医院疼痛科,四川泸州 646000)
随着肿瘤发病率增高,癌痛患者的数量逐年增加,尤其是中晚期癌性疼痛。癌痛多数是慢性疼痛,部分癌痛患者虽经长期规范治疗但疼痛仍没有得到理想的控制,最终发展成为难治性或顽固性癌痛[1]。顽固性癌痛对患者生理、心理情感、认知和社会成分都是一种痛苦的体验。持续、有效的消除疼痛,可明显提高患者生活质量,延长生存时间[1]。对于鞘内输注药物控制癌痛的文献不多,现将本科收治的病例总结如下。
1 资料与方法
1.1 一般资料
收集2016年1月至2018年9月就诊于西南医科大学附属医院经病理确诊的晚期恶性肿瘤8例。其中男性3例,女性5例,年龄35~59岁,平均年龄(49.62±3.04)岁,病程(6.1±3.5)月,随访时间(5.5±1.2)月。1例直肠癌,2例宫颈癌,1例肺癌,1例脂肪肉瘤,1例胰腺癌,1例肝癌,1例膀胱癌。排除禁忌症,经三阶梯治疗疼痛控制不佳的晚期恶性肿瘤患者。本临床研究得到医院药事委员会、医务部、伦理委员会批准,全部患者均签署知情同意书。
1.2 方法
患者入手术室后,常规心电监护,建立静脉通路。左侧卧位,标记穿刺位置为L3-4间隙,标记囊袋放置位置为右下腹部及导管到达位置T10椎体。常规消毒手术区域,用1%利多卡因局麻腰穿点、囊袋放置位置及导管位置。用17 G穿刺针做后正中线旁1 cm穿刺,有黄韧带突破感后继续穿刺,拔除针心;见透明脑脊液流出。放置鞘内导管,C臂投影显示到达T10(根据疼痛节段定位)后(如图1~2),拔除导管钢芯,接注射器回抽见脑脊液流出通畅。于右下腹部做竖形切口约4 cm,钝性分离至浅肌膜层,制作约4×5 cm囊袋。建立皮下隧道,连接导管与输注港,置入制作囊袋。消毒皮肤,逐层缝合皮肤。蝶形针(德国贝朗)穿刺皮肤输液港,连接通畅。

图1 C臂透视下穿刺部位导丝、到达目标位
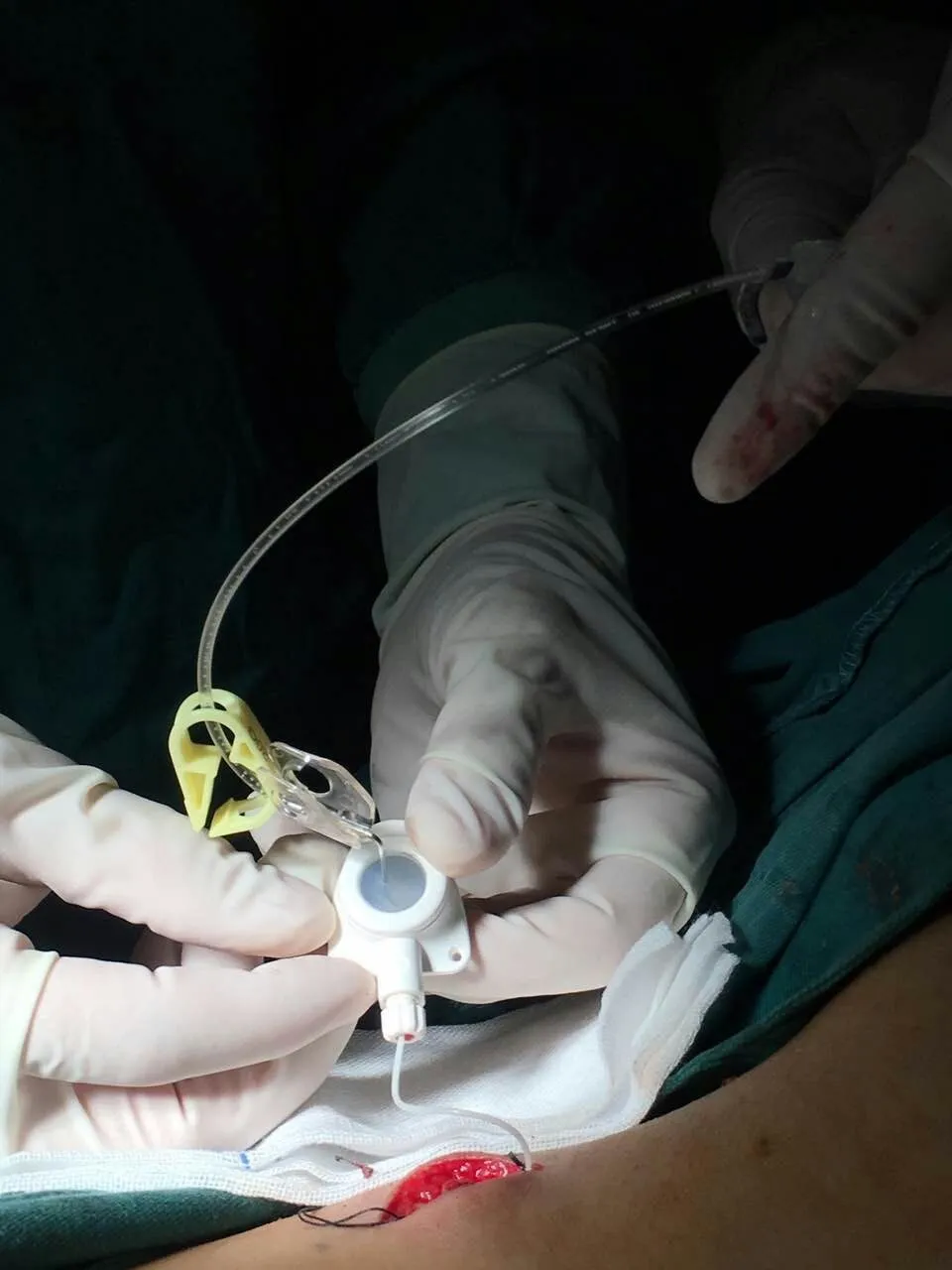
图2 鞘内植入输注系统(德国贝朗)
1.3 观察指标
通过调阅电子病历系统、电话微信随访,记录术前VAS评分、术前阿片药物的剂量、术后(1 d、1周、1月、2月、3月)VAS评分、术后并发症、鞘内吗啡日用量。采用VAS加权计算方法评价疼痛缓解情况,优效为疼痛基本消失,VAS评分降低幅度>75%,良效为VAS评分降低幅度在51%~75%,有效为疼痛VAS评分降低幅度在26%~50%,差效为VAS评分降低幅度≤25%。有效率=(优效+良效+有效)/总例数×100%。
1.4 统计分析
统计软件采用SPSS 17.0进行对比分析;计量资料采用均数±标准差(±s)表示。
2 结 果
2.1 术后疗效
所有患者在鞘内给药后疼痛开始明显减轻,术后1 d有7例优效、1例良效,术后1周8例均优效,有效率100%。
2.2VAS评分及并发症
鞘内输注系统能将顽固性癌痛控制于轻度疼痛,术前VAS评分9.38 ± 0.51(n=8);术后1 d 2.71± 0.75(n=8);术后1周1.86 ± 0.9(n=8);术后1月1.71 ± 0.75(n=7);术后2月1.92 ± 0.51(n=7);术后3月1.65 ± 0.72(n=7),如图3。术后出现并发症为蝶形针脱落1例、输液港周围积液1例、恶心呕吐1例、蝶形针周围形成窦道1例,未出现导管阻塞、导管尖端肉芽肿、迂曲、椎管内出血、感染及尿储留等。
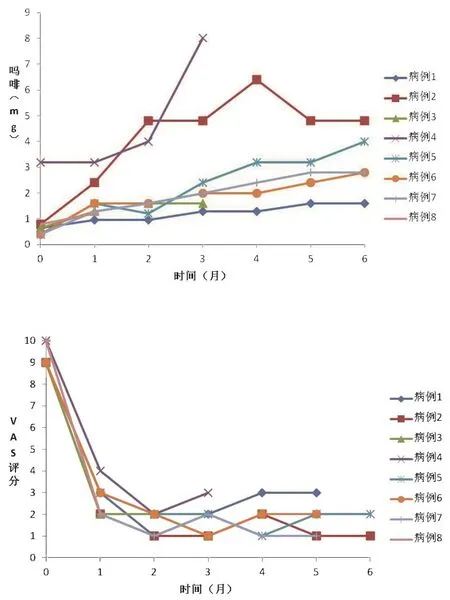
图3VAS评分-时间(月)
2.3 鞘内吗啡用药量
1例患者于术后半个月死亡;2例患者于术后3个月死亡。随着疾病进展,鞘内吗啡日用量逐渐增大,术后吗啡日用量1.11 ± 1.12 mg(n=8),术后1月1.72± 0.75 mg(n=7),术后2月2.27± 1.53 mg(n=7),术后3月3.35 ± 2.64 mg(n=7),术后4月3.31 ±2.61 mg(n=5),术后5月3.13 ± 1.16 mg(n=5),术后6月3.34±1.53 mg(n=5)。其中1例脂肪肉瘤鞘内吗啡泵术后未进行抗癌治疗,1例宫颈癌术后4月重新开始抗癌治疗,吗啡日用量明显增加;其余4例仍同时进行抗癌综合治疗,鞘内吗啡日用量逐渐缓慢增大,如图4。
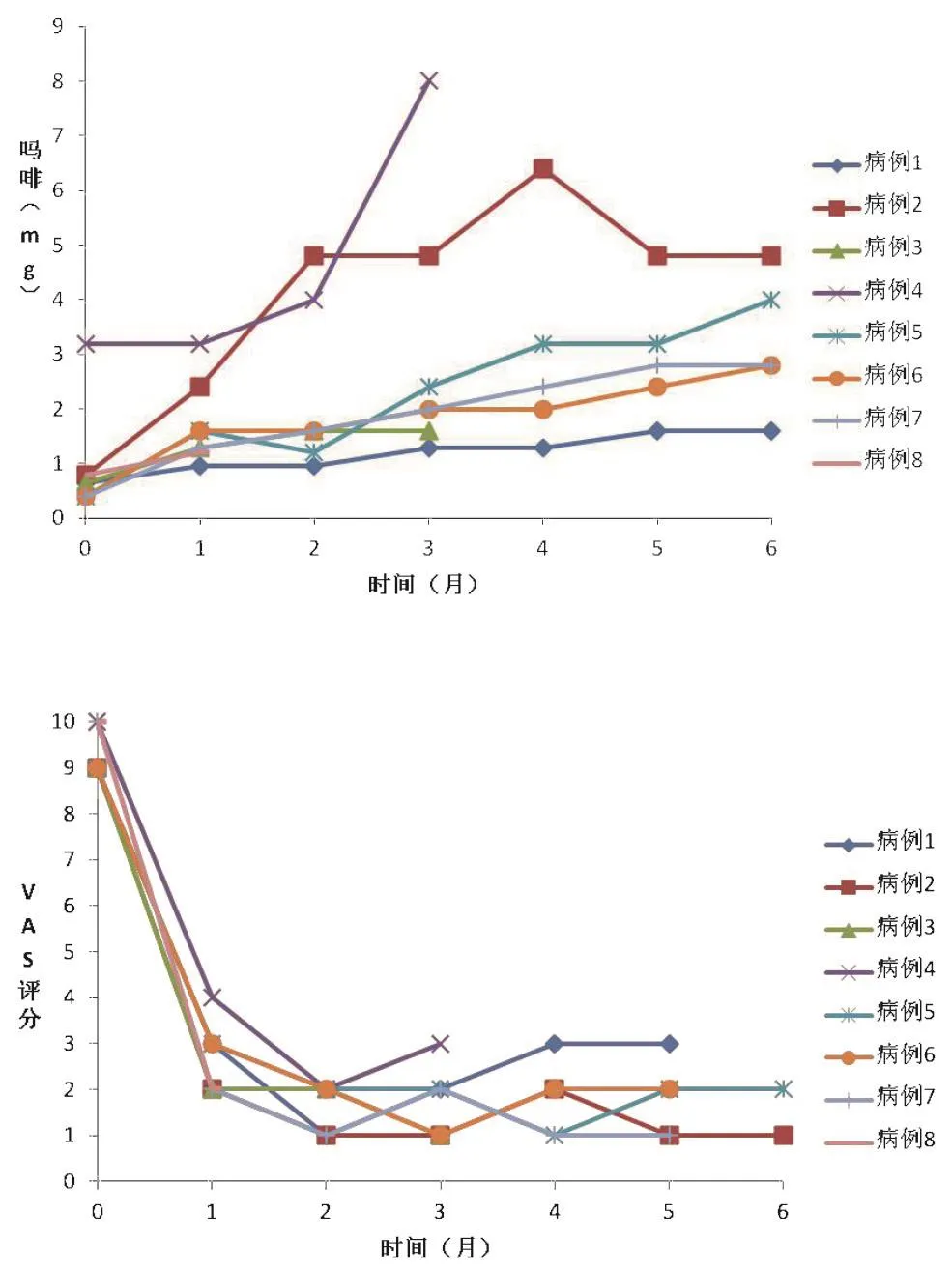
图4 鞘内吗啡日用量(mg)-时间(月)
3 讨论
癌痛是肿瘤患者最常见的症状之一,晚期癌症患者中有70%~90%会经历疼痛,其中30%~45%为严重疼痛,而有25%的患者带着剧烈疼痛的折磨离世[2]。全球癌症的发病率正以年3%~5%的速度逐年递增,癌痛病人的数量也逐年上升[3]。基于癌痛发病率逐年上升、对患者个人及家庭影响大,如何控制癌痛,提高肿瘤患者的生活质量成为临床研究的重要方向。
世界卫生组织(World Health Organization,WHO)在1986年提出的简单有效的三阶梯止痛方法,得到公认。三阶梯止痛时,非甾体类止痛药随着剂量的逐渐增加,会出现“天花板效应”,且许多患者易出现严重的恶心、呕吐、胃粘膜病变等不良反应[4];而阿片类药物长时间、高剂量应用时,会导致耐药、成瘾以及便秘等不良反应增加[5]。NCCN癌痛指南中指出,当口服及其他途径用药效果欠佳时,推荐采用椎管内麻醉技术如硬膜外自控镇痛及蛛网膜下腔自控镇痛[6-8]。
黄明等[9]研究显示治疗后1 d、14 d,1月、3 月疼痛缓解总有效率分别为88.9%、88.9%、100%、100%,未发生手术相关性并发症及吗啡不良反应。吗啡是顽固性癌痛的常用药物,通过椎管内给药可直接作用于阿片受体结合位点,所需的有效镇痛剂量较小,作用时间持久且不良反应较轻[10-12],还可抑制肿瘤细胞的增殖[13]。国外研究显示[14-15]鞘内给予吗啡能够直接作用于大脑及脊髓中的阿片受体,阻止阿片受体与P物质的结合从而产生镇痛作用,且对神经正常功能没有影响。
8例患者在术前均使用传统的镇痛方法:口服盐酸吗啡缓释片、盐酸曲马多缓释胶囊、盐酸羟考酮缓释片以及芬太尼透皮贴剂等控制,通过阿片类药物剂量换算系数表[16],术前口服吗啡日用量分别为192、240、192、960、245、230、330和432 mg。与术后鞘内输注吗啡日剂量比较,是有统计学差异(P=0.00)。宋莉等[17]研究发现,对于顽固性癌痛患者,用传统镇痛方法时,吗啡日均剂量:282.9±95.5 mg/d,和本研究相似;俞良等[18]研究也发现:使用鞘内吗啡泵后吗啡的日均消耗量(3.60±3.25)mg明显低于传统镇痛方法的吗啡日均消耗量(397.50±304.66)mg。
目前国内关于该类研究尚无大样本前瞻性数据,多为小样本、自身前后比较观察性研究。传统镇痛疗法无创,患者接受程度高,使用方便,但是由于吗啡日均消耗量较多,副作用也明显增高。鞘内输注系统属于有创治疗,需要专业人员指导,但吗啡日均消耗量相对较小,副作用小。通过随访观察,本研究总结其优点如下:①患者用药量明显减少,鞘内用药只需小剂量吗啡,本研究中鞘内吗啡日用量最大8 mg(如图2),并未到达文献报道的16 mg大剂量[19];②由于鞘内输注的药物直接作用于中枢,患者出现爆发痛时PCA可立即解救,比口服或肌肉注射起效时间明显缩短;③吗啡泵是持续给药,血药浓度稳定,波动小,一般不会出现血药浓度峰,由于其用药量很小,不易产生成瘾性;④由于鞘内用药量少,不良反应明显减少,1例在术后出现恶心、呕吐,给予卧床休息及补液后好转;1例患者严重低白蛋白血症,术后输液港周围出现积液,给予换药、引流、加压包扎、补充白蛋白后愈合。部分患者置入吗啡泵之前口服用药剂量较大,突然停药会造成反跳现象或者疼痛加重,所以不建议植入吗啡泵后直接停药,而是循序渐进地减少口服药物,直至停药,这样才能更好地控制疼痛[7]。
鞘内吗啡输注系统植入后,在其整体管理中,需注重以下几点:首先加强院外随访,定期与患者家属沟通,了解注药泵工作情况,可及时发现问题并处理,保证患者长时间有效镇痛、预防并发症发生。其次做好家庭护理教育,向患者及家属普及镇痛泵的相关知识,心理疏导,避免病态悲观反应出现[20],并准备一定量的口服镇痛药物,确保在没有医务人员的情况下,可自行简单的处理突发情况,比如疼痛加重或爆发痛。术后继续抗肿瘤治疗,可减缓癌痛的发展及鞘内吗啡日耗量。
本研究不足之处:①样本量小,统计可能存在偏差,后续研究中继续加大样本量;②随访时间短,加强随访为后续生存分析提供依据。
4 结论
鞘内小剂量吗啡可将顽固性癌痛控制于轻度疼痛;随着疾病进展,鞘内吗啡日用量逐渐增加;使用鞘内吗啡泵恶心、便秘等不良反应减少。

