瑞舒伐他汀钙合成中Wittig反应的烯烃杂质的合成及其核磁共振二维谱解析
刘霞 龚杰 陈斌 张桂菊 张惠芝 谢永居
摘 要 瑞舒伐他汀钙是一种调脂药物,在通过Wittig反应合成其中间体R1的过程中会产生烯烃杂质。本研究通过多聚甲醛合成此烯烃杂质,并用核磁共振氢谱(1H-NMR)、核磁共振碳谱(13C-NMR)和核磁共振二维相关谱DEPT135、HSQC、HMBC对合成的烯烃杂质进行结构归属解析。
关键词 瑞舒伐他汀钙 烯烃杂质 Wittig反应 核磁共振二维谱解析
中图分类号:O657.61; R914.5 文献标志码:A 文章编号:1006-1533(2019)09-0067-04
Synthesis of olefin impurity from Wittig reaction in rosuvastatin calcium synthesis and the analysis of its two-dimensional nuclear magnetic resonance spectrum
LIU Xia*, GONG Jie, CHEN Bin, ZHANG Guiju, ZHANG Huizhi, XIE Yongju**(Jiangxi Fushine Pharmaceutical Co., Ltd., Jiangxi Jingdezhen 333000, China)
ABSTRACT Rosuvastatin calcium is a lipid-lowering drug. The olefin impurity from the Wittig reaction in the synthesis of intermediate R1 was synthesized by paraformaldehyde and its structure attribution was analyzed by 1H-NMR, 13C-NMR, DEPT135, HSQC, and HMBC.
KEY WORDS rosuvastatin calcium; olefin impurity; Wittig reaction; 2D-NMR analysis
瑞舒伐他汀鈣是一种调脂药物,自2002年11月在荷兰首先获得批准后,现已在世界上60多个国家上市。瑞舒伐他汀钙具有强力的3-羟基-3-甲基戊二酰辅酶A还原酶抑制活性,其降低低密度脂蛋白胆固醇水平、升高高密度脂蛋白胆固醇水平的作用优于已上市的其他他汀类药物,耐受性和安全性均好,被誉为“超级他汀类药物”[1]。目前,在瑞舒伐他汀钙的合成过程中一般都有通过Wittig反应合成中间体R1的步骤(图1上部),此反应中会产生烯烃副产物,产生原因为D5的醇解反应产物D6中残剩有甲醇,甲醇在D7的合成过程中被氧化成甲醛,甲醛参与Wittig反应产生了烯烃杂质(图1下部)。有文献[2]报告了此烯烃杂质的合成方法,我们对该合成方法作了改进[3],但对此烯烃杂质的核磁共振信号归属还未进行研究。本研究通过多聚甲醛合成此烯烃杂质,并用核磁共振一维谱和二维相关谱对合成的烯烃杂质进行结构归属解析。
1 仪器与试剂
1.1 仪器
Bruker 400 MHz核磁共振波谱仪(德国Bruker公司);UTP-313电子天平(上海花潮电器有限公司)。
1.2 试剂
Z8.2(江苏阿尔法药业有限公司);二甲基亚砜、多聚甲醛、碳酸钾、甲苯、甲醇、氘代氯仿(均国药集团化学试剂有限公司)。
2 实验方法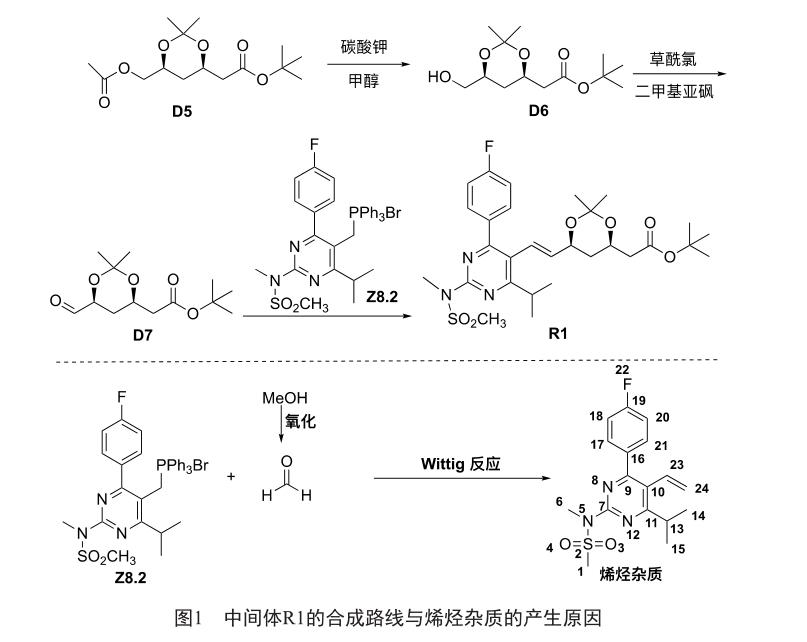
烯烃杂质的核磁共振波谱均用Bruker 400 MHz核磁共振波谱仪检测,其中1H-NMR检测的观测频率为400MHz,13C-NMR检测的观测频率为100 MHz。核磁共振实验采用5 mm直径的核磁管,其一维、二维实验均于控温下进行。烯烃杂质的纯度用安捷伦1260液相色谱仪检测,质谱用Waters Xevo G2-XS Tof质谱仪检测,红外光谱用岛津IRAffinity-1红外光谱仪检测。
3 烯烃杂质的合成
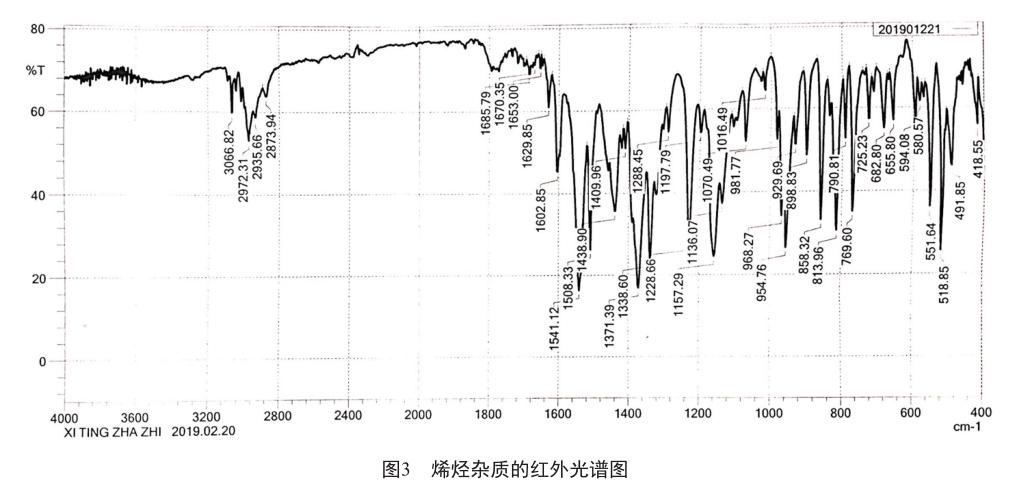
在500 L四口烧瓶中依次加入二甲基亚砜 50 ml、Z8.2 10.0 g、多聚甲醛0.9 g、碳酸钾20.8 g,搅拌、升温, 70 ℃下保温反应30 min,然后降温至30 ~ 40 ℃,加入甲苯100 ml,搅拌、过滤。滤液中加入水100 ml,搅拌10 min后分液,有机相用水100 ml分2次洗涤,45 ℃下减压蒸馏至干,甲醇重结晶、过滤、烘干,即得烯烃杂质,收率为88.6%,纯度为99.2%,质谱检测显示分子量为350([M+1]+)(图2)。烯烃杂质的红外光谱谱带(单位:cm-1)为3 066、2 972、2 873、1 670、1 602、1 508、1 438、1 371、1 338、1 157、968(图3),显示与烯烃、苯环、甲基、烯烃、磺酰胺等基团相吻合。
4 烯烃杂质的核磁共振波谱解析
以氘代氯仿为溶剂,进行烯烃杂质的核磁共振波谱检测。
1H-NMR谱图(图4)显示,烯烃杂质分子中有多组质子信号,共含20个质子,部分活泼质子未出峰。δ7.26是溶剂的质子信号。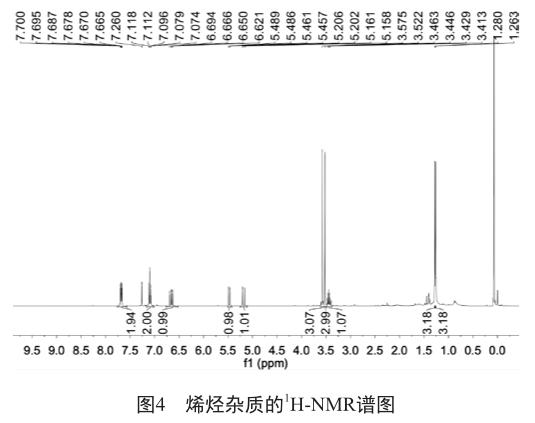
13C-NMR谱图(图5)显示,烯烃杂质分子中有多组碳信号,共含17个碳,部分等同性碳在同一位置出峰。
DEPT135谱图(图6)显示,烯烃杂质分子中有1组仲碳、7组叔碳或伯碳,其余为季碳。依据HSQC谱图(图7)可以确认各组碳与氢的连接关系。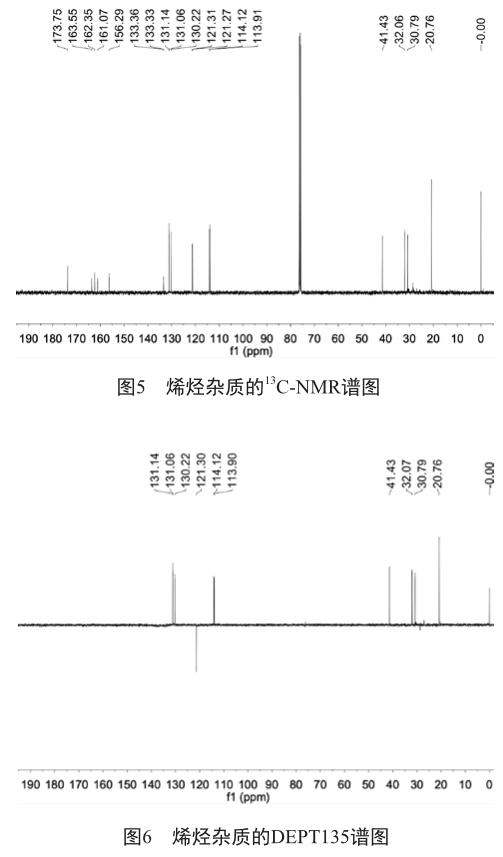
DEPT135谱图显示,δ 121.30为仲碳,对应为C24,对应的HSQC谱图中,δ 5.18(dd, 1H)/δ 5.47(dd, 1H)归属为H24。根据脂肪族普通甲基的出峰规律,δ 1.26(s, 3H)/δ 1.28(s, 3H)归属为H14/H15,对应的HSQC谱图中,δ 20.76归属为C14/C15。
在HMBC谱图(图8)中,C14/C15与δ 3.40 ~ 3.48(m, 1H)有相关,因此δ 3.40 ~ 3.48(m, 1H)归属为H13,对应的HSQC谱图中,δ 30.79归属为C13。
在HMBC谱图中,δ 173.75与H13/H14/H15均有相关,因此δ 173.75归属为C11;δ 121.27与H13有相关,因此δ 121.27归属为C10;C24与δ 6.62 ~ 6.69(m, 1H)有相关,结合烯烃的出峰规律,δ 6.62 ~ 6.69(m, 1H)归属为H23,对应的HSQC谱图中,δ 130.22归属为C23。
在HMBC谱图中,与H23有相关的碳信号包括C10、C11和δ 162.35,因此δ 162.35归属为C9。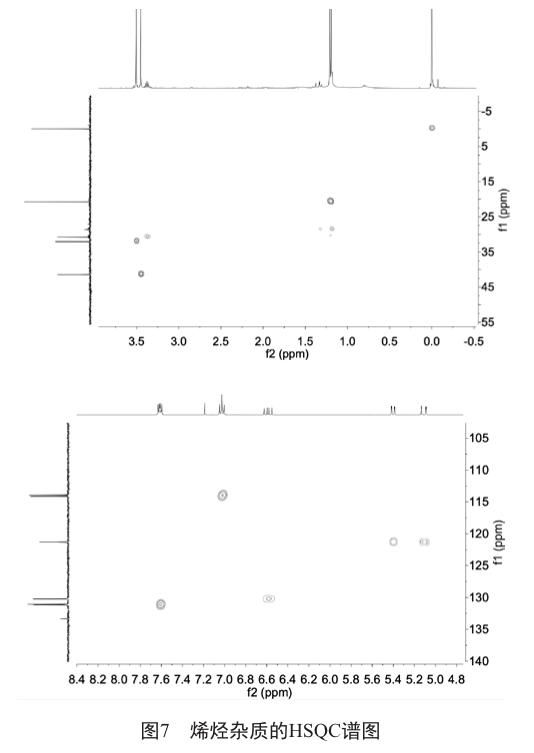

在1H-NMR谱图中,δ 3.52、δ 3.58均为单峰,且均含3个质子,因此归属为H1或者H6。此外,在HMBC谱图中,δ 156.29与H1或者H6有相关,因此δ 156.29归属为C7,δ 3.58(s, 3H)归属为H6,δ 3.52(s, 3H)归属为H1,对应的HSQC谱图中,δ 41.43归属为C1,δ 32.06归属为C6。
在13C-NMR谱图中,根据氟苯的出峰规律,结合氟对相连的碳原子的裂分规律,δ 162.31(J=248 Hz)归属为C19。结合对称性,在1H-NMR谱图中,δ 7.07 ~ 7.12(m, 2H)和δ 7.67 ~ 7.70(m, 2H)归属为H18/H20或者H17/H21。再结合氟原子的电负性性质,δ 7.67 ~ 7.70(m, 2H)归属为H17/H21,δ 7.07 ~ 7.12(m, 2H)归属为H18/H20,对应的HSQC谱图中,δ 114.02(J=21 Hz)归属为C18/C20,δ 131.10(J=8 Hz)归屬为C17/C21。在DEPT135谱图中,δ 133.35(J=3 Hz)为季碳,归属为C16。
至此,烯烃杂质的1H-NMR和13C-NMR谱图解析完毕,结构归属结果归纳见表1和表2。
5 结语
本研究通过多聚甲醛合成烯烃杂质,并用1H-NMR、13C-NMR以及核磁共振二维相关谱DEPT135、HSQC、HMBC对合成的烯烃杂质进行了结构归属解析。
参考文献
[1] Carswell CI, Plosker GL, Jarvis B. Rosuvastatin [J]. Drugs, 2002, 62(14): 2075-2085.
[2] Mallela SPS, Nandi S, Nangi GBS, et al. Process for preparing pyrimidine propenaldehyde: US, 8394956B2 [P]. 2013-12-03.
[3] 谢永居, 龚杰, 张桂菊, 等. 一种瑞舒伐他汀钙中间体杂质的制备方法: 中国, 201510423435.1 [P]. 2015-12-16.

