pH对玉米胚芽蛋白Pickering乳液稳定性及流变学性质的影响
张 会,任 健
(1.齐齐哈尔大学 食品与生物工程学院,黑龙江 齐齐哈尔 161006; 2.农产品加工黑龙江省普通高校重点实验室,黑龙江 齐齐哈尔 161006)
现代食品工业越来越注重食品对人类营养及健康改善的功能,大量生物活性成分被广泛应用于各类食品体系。但这类物质中的大多数生物可利用度均较低。特别是各种疏水性生物活性物质,包括脂溶性维生素、多不饱和脂肪酸、类胡萝卜素和疏水性植物多酚,如何在食品中有效添加并保持其稳定性是目前食品工业的一大技术难题。构建食物蛋白胶体粒子是功能因子稳定性及生物效价的一个重要途径[1]。
我国是玉米生产消费大国,玉米胚芽资源丰富。目前主要以玉米胚芽为原料制备玉米胚芽油,而脱脂后含有优质天然植物蛋白的玉米胚芽粕大多被用作饲料,消化吸收率较低,造成了一定的环境污染和资源浪费,并没有发挥其潜在的经济价值[2]。因此,可将玉米胚芽粕作为原料提取玉米胚芽蛋白,实现资源再利用。玉米胚芽蛋白具有良好的功能性质,既含有亲水性基团又含有疏水性基团,具有两亲性质,为其作为Pickering乳液稳定剂奠定基础。目前国内外关于Pickering乳液的研究主要集中在醇溶蛋白[3],而关于玉米胚芽蛋白Pickering乳液的研究较少。
本文以玉米胚芽蛋白为原料,利用高压均质法制备玉米胚芽蛋白Pickering乳液,主要研究了pH对玉米胚芽蛋白Pickering乳液粒径、电位、稳定性及流变性的影响,为开发新型活性载体物质提供理论参考。
1 材料与方法
1.1 实验材料
玉米胚芽饼:黑龙江龙凤玉米开发有限公司;大豆油:益海嘉里食品营销有限公司;尼罗蓝、尼罗红。
GYB40-10S型高压均质机;T25型乳化分散机;Kinexus pro+型高级旋转流变仪:英国Malvern公司;TCS SP8激光共聚焦显微镜。
1.2 实验方法
1.2.1 玉米胚芽蛋白的提取
用粉碎机将玉米胚芽饼粉碎,过100目筛,得到较细颗粒玉米胚芽粉,采用石油醚浸提方法将玉米胚芽粉脱脂,采用碱提酸沉法提取玉米胚芽蛋白,NaOH浓度为0.08 mol/L,酸沉pH 为4.7,然后对其进行水洗、中和、冷冻干燥,得玉米胚芽蛋白[4]。
1.2.2 玉米胚芽蛋白Pickering乳液的制备
配制玉米胚芽蛋白分散液。将3 g玉米胚芽蛋白溶于240 mL蒸馏水中,磁力搅拌2 h,充分溶胀后,次日分别逐滴加入60 mL 的大豆油,经乳化分散机(20 000 r/min)分散2 min,用1 mol/L的HCl或NaOH调其pH,得到pH分别为3、5、7、9、11的粗乳液。用高压均质机将此粗乳液均质处理3次,压力设定为40 MPa[5]。
1.2.3 乳液的微结构表征
取1 mL乳液样品,加入20 μL 0.02%的尼罗红、20 μL 0.1%的尼罗蓝,混合均匀,染色1 min,用胶头滴管取1滴在20 mm的玻底培养皿中,利用激光共聚焦显微镜观察乳液微结构,激发波长为488 nm和633 nm[6]。
1.2.4 乳液粒径电位的测定
采用 Zetasizer Nano ZS测定新制备的玉米胚芽蛋白Pickering乳液的Zeta电位和粒径。取适量乳液,用去离子水稀释,然后进行Zeta电位和粒径测定[7]。
1.2.5 乳液离心稳定性及贮藏稳定性的测定
分别取不同pH的玉米胚芽蛋白Pickering乳液4 mL装入5 mL离心管中,10 000 r/min下离心2 min,测定其乳析指数的变化。分别取不同pH的玉米胚芽蛋白Pickering乳液5 mL装入10 mL透明玻璃瓶中,观察刚均质后的乳液及贮藏1、3、7 d时乳液乳析指数的变化,分析贮藏时间对Pickering乳液稳定性的影响,实验做3次平行。
1.2.6 表观黏度的测定
乳液表观黏度通过马尔文流变仪进行测定。将乳液样品分别置于平行板之间,选用PU60 mm的模具平板,设置间距为1 mm,剪切速率0.1~100 s-1,25℃下平衡5 min,然后开始测定玉米胚芽蛋白Pickering乳液表观黏度的变化。
2 结果与讨论
2.1 乳液的微结构
利用激光共聚焦显微镜(CLSM)观察乳液液滴的微结构,1%蛋白乳液,油相比例为20%,pH为5,采用尼罗红和尼罗蓝分别对蛋白与油相进行染色,染色后油相为绿色,蛋白为红色,测定结果如图1所示。
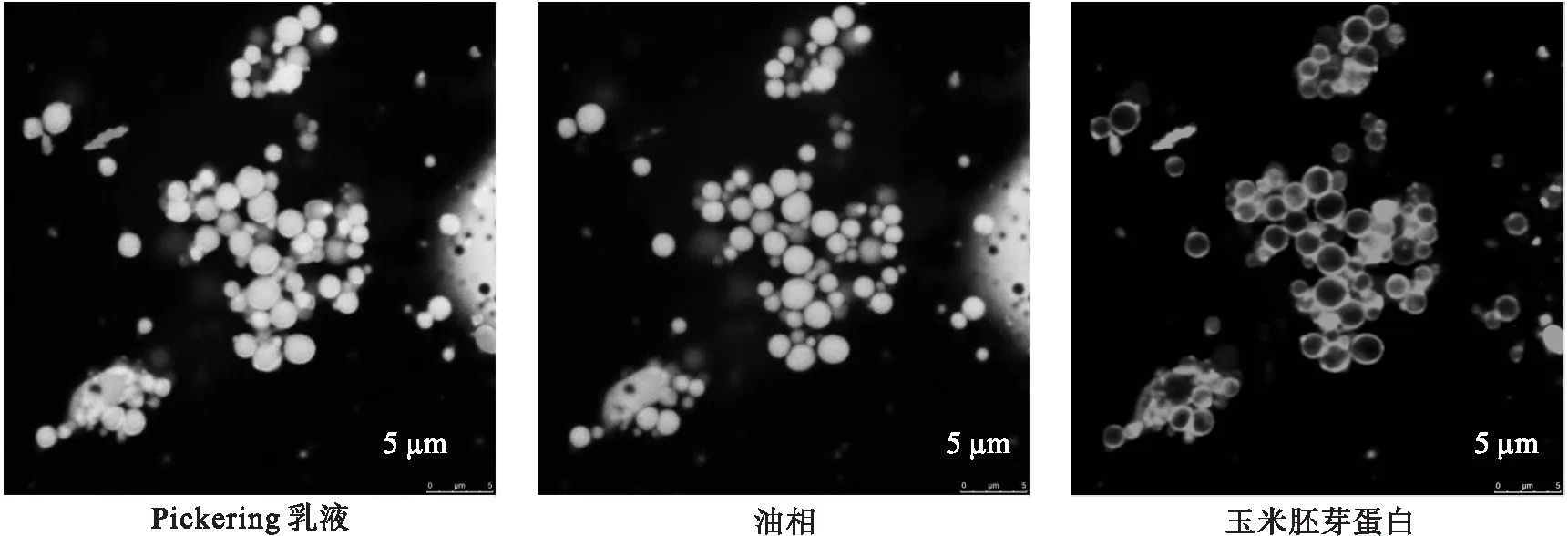
图1 玉米胚芽蛋白Pickering乳液CLSM图像
由图1可以看到,红色的玉米胚芽蛋白包裹着绿色的油滴,说明该乳液是蛋白颗粒稳定的水包油型 Pickering乳液[8]。
2.2 乳液粒径
pH对乳液粒径的影响如图2所示。
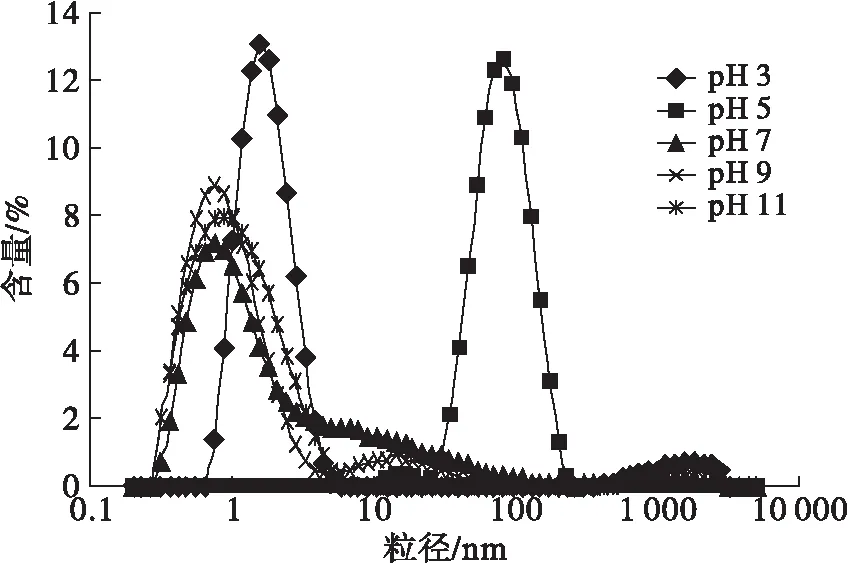
图2 pH对玉米胚芽蛋白Pickering乳液粒径的影响
由图2可知,pH为3、5、7、9、11时乳液的平均粒径分别为1.689、71.05、1.422、0.955 3、0.943 1 nm,随着pH的增加,乳液的粒径先增大后减小,pH为5时乳液粒径最大,pH 5接近玉米胚芽蛋白等电点,等电点时液滴表面的静电荷几乎为0,液滴之间的静电斥力小,易于发生聚集[9],导致玉米胚芽蛋白Pickering乳液的平均粒径增大,乳液不稳定。随着pH继续增大,蛋白包裹的液滴表面静电荷量增大,液滴之间的静电斥力增大,能使液滴之间保持平衡而不发生聚集,所以pH为11时乳液粒径最小,乳液的稳定性好。
2.3 乳液电位
pH对乳液电位的影响如图3所示。
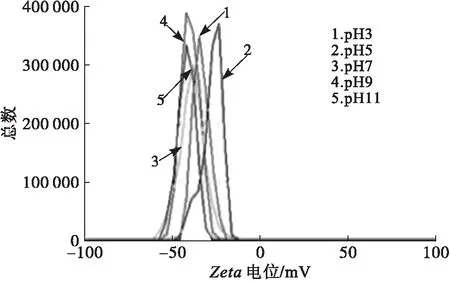
图3 pH对玉米胚芽蛋白Pickering乳液电位的影响
由图3可知,pH为3、5、7、9、11时乳液的电位分别为-33.3、-26.6、-38.6、-39.5、-41.7 mV,随着pH的增大,乳液电位绝对值呈现先减小后增大的趋势。pH 5时乳液电位绝对值最小,因为pH 5接近玉米胚芽蛋白等电点,颗粒表面电荷达到最小,乳液电位绝对值变小。颗粒的带电变化与玉米胚芽蛋白中氨基和羧基之间的电离平衡有关,溶液整体带电性影响乳液的稳定性,乳液中颗粒间电荷的相互排斥作用小,易发生聚集,难以维持稳定的结构,乳液不稳定[10]。反之,pH 11时乳液电位绝对值最大,为乳液中的颗粒间提供了相对较强的电荷排斥作用,颗粒不易聚集,乳液较为稳定[11]。
2.4 乳液的表观黏度
pH对乳液表观黏度的影响如图4所示。
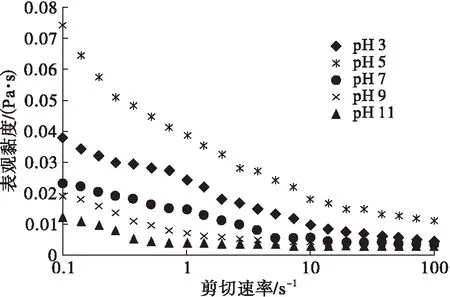
图4 pH对玉米胚芽蛋白Pickering乳液表观黏度的影响
由图4可知,在剪切速率0.1~100 s-1的范围内玉米胚芽蛋白Pickering乳液的表观黏度随剪切速率的增大而下降,即发生了剪切稀释现象,分析原因可能是由于絮凝态的油滴在剪切过程中互相分离的缘故[12]。随着pH的增加,表观黏度先增大后减小,pH 5时表观黏度最大,这可能是因为粒径较大的缘故,根据托克斯定律[13],pH 5时在蛋白质等电点附近,蛋白质分子表面电荷几乎为0,分子间的相互排斥力减弱,颗粒极易碰撞、凝聚,聚合物溶液中的聚合物分子具有缠绕着的环状和长分子链,所有这些物质在静止时将保持内部的不规则次序,因为具有相当高的内部阻力阻碍流动,表现出较高的黏度,反之,pH 11时蛋白溶解度高,颗粒间静电斥力大,乳液粒径小,分散性好,则表观黏度较小[14]。
2.5 乳液稳定性
2.5.1 离心稳定性
pH对乳液离心稳定性的影响如图5所示。

图5 pH对玉米胚芽蛋白Pickering乳液
由于离心时所产生的离心力,使乳液液滴汇聚,从而加快乳液的乳析分层过程。离心后,下层为水层,上层为颗粒包裹的致密乳化层,乳析指数能反映乳液的稳定性。由图5可知,pH 5时乳液乳析指数在75%左右,并出现破乳现象[15],pH 3时乳液发生轻微分层,但无破乳现象,其他pH下的乳液没有明显的分层现象,乳液离心稳定性较好。
2.5.2 贮藏稳定性
pH对玉米胚芽蛋白Pickering乳液贮藏稳定性的影响如图6所示。通过观察乳化层在贮藏过程中发生的变化,判断乳液的贮藏稳定性,如果乳液不分层,不出现乳析现象,则说明乳液稳定性良好,如果乳液层不断变化,并伴有溢油、破乳等现象,则乳液的稳定性不佳[15]。在贮藏过程中由于重力的作用,乳液中的水层在下方,富含油脂的乳液在上方。
由图6a可知:新鲜制备的5种乳液均未出现分层现象,pH 5的乳液贮藏1 d(见图6b)后出现分层,乳析指数在15%左右,贮藏3 d(见图6c)后乳液中的水层界面高度增加并且变清晰,其他pH的乳液3 d内均未出现分层,乳液较稳定;贮藏7 d时pH 5的乳液乳析指数达到约20%,pH为7和9的乳液出现分层现象,且乳析指数为pH 5>pH 7>pH 9,pH为3的乳液底部也出现不明显的分层现象,由此可见pH为11时,乳液贮藏稳定性最好。分析原因可能是pH 5的乳液接近蛋白质等电点,颗粒表面电荷几乎为0,电荷排斥力小,液滴聚集,乳液絮凝分层,pH越大,粒子间电荷排斥力越大,分散性越好,乳液越稳定[16]。

注:a.新鲜制备的乳液;b.贮藏1 d的乳液;c.贮藏3 d的乳液;d.贮藏7 d的乳液。
图6 pH对玉米胚芽蛋白Pickering乳液贮藏稳定性的影响
3 结 论
采用高压均质的方法制备不同pH的玉米胚芽蛋白Pickering乳液,乳液类型为水包油型;随着pH的增大,乳液粒径先增大后减小,电位绝对值先减小后增大;随着剪切速率的增大,乳液表观黏度逐渐减小,呈剪切稀释现象;pH为11时乳液离心稳定性、贮藏稳定性最佳。

