2019年高考化学《考试大纲》分析及考向预测
湖北 文丽娟 杨恩健
2019年高考化学《考试大纲》已经发布,经与2018年高考化学《考试大纲》进行逐字对比,可以发现基本没有变动,考核目标与要求、考试范围与要求均没有什么变化,这也符合《考试大纲》修订原则的一贯特征。在新一轮高考改革到来之前,将以平稳过渡的方式进入新改革。
一、2019年高考化学命题基本方向
2018年6月8日高考结束当天,教育部考试中心推出《2018年高考各科试题评析》。文章评述2018年高考各科试题,很好地体现了“立德树人、服务选才、引导教学”的核心功能,特别突出“立德树人”和“素质教育”为首要功能。化学试题的要求:贯彻改革要求,推动素质教育;展现成果,突出贡献,发挥学科育人功能;情境真实,应用导向,聚焦学科核心素养;形式多样,数据详实,测评学科关键能力;依据大纲,回归教材,考查学科必备知识。
高考化学考试内容改革:基础性,注重对学科基础知识和基本方法的考查;综合性,不断加强模块的综合,探索学科间的综合;应用性,加强与社会、生产、生活实际的联系,考查应用能力;创新性,加强探索设计型创新思维能力的考查、自主学习创新思维能力。
2019年的高考化学命题会保持稳定性和一定的发展性,考查的主干知识、核心能力以及题型基本没有变化,结合《考试大纲》和近几年高考命题的特点及变化趋向,现对2019年高考进行合理预测。
二、高考化学试题预测
1.立德树人、服务选拔、素养导向考查
在不同情景下利用知识和技能完成任务、应变能力,学科观念、学科视野,体现实践能力和创新精神;运用知识能力:独立思考、分析问题和解决问题、交流合作,适应社会发展;在知识积累、能力提升和素质养成的过程中,逐步形成正确的核心价值观。命题注重考查中学化学的基础知识,突出对中学化学主干知识的考查,引导中学化学教学注重形成完整的学科体系。
预测2019年高考化学试题,就选择题而言,融合多个模块内容考查综合性,每一题一个主题思想,每个选项则围绕主题涉及不同知识内容或同一知识点的不同认识角度,有效考查学生对主干知识的深度理解能力及其对于学科体系的掌握程度,进而考查思维的深刻性、独特性与敏捷性,体现对学科素养的考查。就非选择题部分而言,每一道题都力争以一个完善的整体出现,不再是知识零散的堆积。尽量展示一个完整的工业过程、完备的研究方法、系统的实验设计,使学生感受一个完整的知识体系,以及各个阶段处理的目的,培养学生看问题、解决问题的系统性和完整性。体现化学知识的应用,体现科学研究的一般规律。
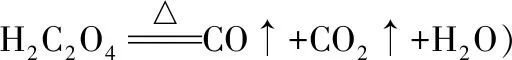

下列说法不正确的是
( )
A.第①步操作要微热溶解,其原因是适当加快溶解速率并减少H2C2O4的分解
C.步骤③所用的洗涤剂最合适的是冷水
D.步骤②固体K2CO3需适量,防止KHC2O4被消耗
【答案】C
【解析】本题是考查化学工艺流程,尽量展现一个完整的工艺流程,培养学生看待问题的整体意识。A选项,草酸受热易分解,故A正确;B选项,CuO和KHC2O4反应生成二草酸合铜(Ⅱ)酸钾晶体和水,故B正确;C选项,根据题中所给信息,二草酸合铜(Ⅱ)酸钾微溶于冷水,可溶于热水,微溶于酒精,根据流程,③得到的是滤液,因此所用的洗涤剂应为热水,故C错误;D选项,步骤②K2CO3需适量,原因是K2CO3可以与KHC2O4反应生成K2C2O4,故D正确。
2.注重实验,侧重方法,体现学科特点

①加强了对基础实验操作和现象等过程的考查
【例2】用下列实验装置进行相应实验,能达到实验目的的是(夹持装置未画出)
( )
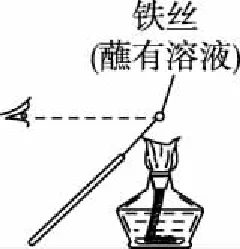
甲

乙
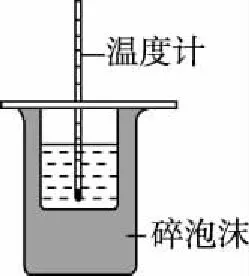
丙
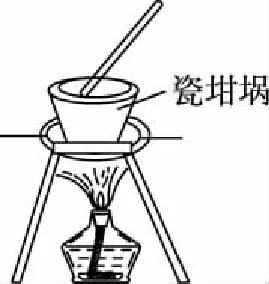
丁
A.用装置甲检验NaCl溶液中是否有K+
B.用装置乙验证牺牲阳极的阴极保护法
C.用装置丙进行中和热的测定
D.用装置丁加热熔融Na2CO3固体
【答案】B
【解析】观察K元素的焰色反应需要透过蓝色的钴玻璃,由图可知,缺少蓝色的钴玻璃,故A错误;Fe为正极,锌为负极,铁被保护,属于牺牲阳极的阴极保护法,故B正确;为了使反应物充分反应,需要环形玻璃搅拌棒,由图可知,缺少环形玻璃搅拌棒,故C错误;瓷坩埚中的二氧化硅与Na2CO3反应,仪器选择不合理,应使用铁坩埚,故D错误;故选B。
②设置新情境考查实验技能的迁移能力
命题素材贴近学生学习体验并适度把教材中实验情境组合或创新,本例题就很好的将教材上对基础实验技能的考查迁移至了考题(氢气还原氧化铜实验原理的迁移、实验安全操作原理的迁移、Fe3+检验的迁移、中和滴定终点判断的迁移),学生若能在解题过程中看出教材的原型,知识的迁移能力会逐渐提升。
【例3】(2018年·全国卷Ⅱ·28,改编)K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题:
(1)将FeC2O4和H2O2依次加入到K2C2O4溶液中,微热搅拌至溶液呈亮绿色,并有红褐色沉淀生成,过滤后将滤液重结晶制备K3[Fe(C2O4)3]·3H2O,请写出制备方程式:____________________。

(3)某小组为探究三草酸合铁酸钾的热分解产物,按如图所示装置进行实验。

①通入氮气的目的是________________。
②证明分解产物中有CO2和CO的现象是________________。
③样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________。
(4)测定三草酸合铁酸钾中铁的含量。
①称量mg样品于锥形瓶中,溶解后加稀H2SO4酸化,用cmol·L-1KMnO4溶液滴定至终点。滴定终点的现象是________________。
②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液VmL。该晶体中铁的质量分数的表达式为____________________。


(3)①隔绝空气、使反应产生的气体全部进入后续装置
②B中澄清石灰水变浑浊,E中黑色固体变红且F中出现白色沉淀 ③取少许固体粉末于试管中,加稀硫酸溶解,滴入1~2滴KSCN溶液,溶液变红色,证明含有Fe2O3

命题通过设计新颖的实验情境,要求考生根据实验目的,以问题为导向,将基础实验知识、基本操作技能和研究方法与新情境相结合,自主选择仪器、药品,设计实验步骤、推测实验现象、处理实验数据、归纳总结得出结论等,在较高层次考查“证据推理与模型认知”“科学探究与创新意识”等学科素养。
【例4】某同学在实验室实验时的记录如下:
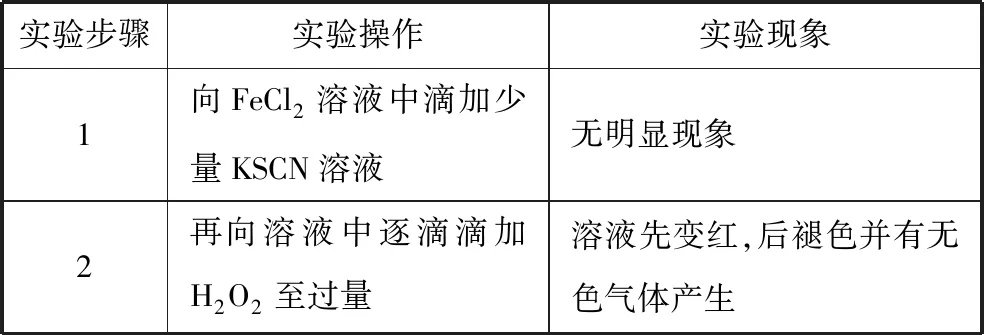
实验步骤实验操作实验现象1向FeCl2溶液中滴加少量KSCN溶液无明显现象2再向溶液中逐滴滴加H2O2至过量溶液先变红,后褪色并有无色气体产生
现对产生现象的原因进行了探究。
[提出假设]
假设一:产生的气体是O2
假设二:产生的气体是N2、SO2、CO2等气体
(1)H2O2与FeCl2酸性溶液反应的离子方程式:____________________。
[实验设计]课题小组设计如图实验装置验证假设二气体成分。
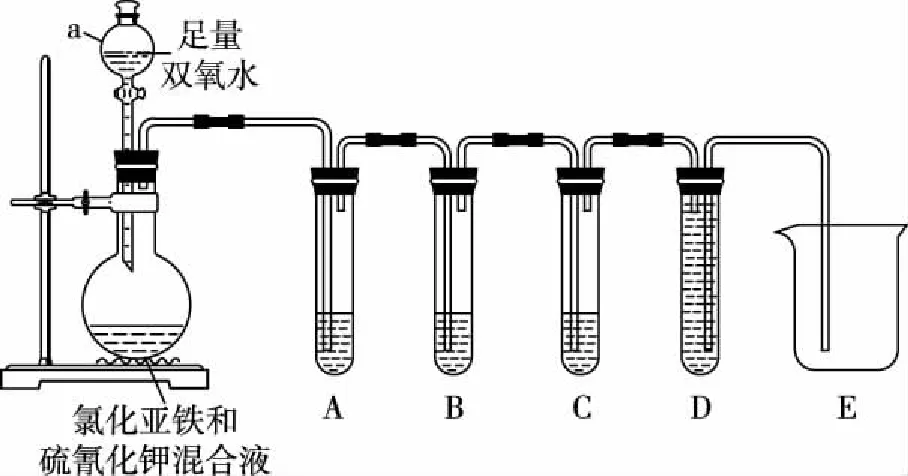
所用试剂:H2O2溶液、FeCl2溶液、KSCN溶液、品红溶液、KMnO4(H+)溶液、Ca(OH)2溶液、NaOH溶液、蒸馏水。
回答下列问题:
(2)仪器a的名称是________。
(3)A、B、C、D试管中的试剂分别是________、________、________、________。
(4)气体中含有CO2的现象是________________。
;
气体中含有N2的现象是________________。
(5)还原性的强弱顺序:Fe2+________(填“>”或“<”)SCN-,理由是________________。
【答案】

(2)分液漏斗
(3)品红溶液、KMnO4(H+)溶液、Ca(OH)2溶液、NaOH溶液
(4)B中的酸性KMnO4溶液变浅,而C中Ca(OH)2溶液变溶液浑浊 D中NaOH溶液排入到F中
(5)> 向FeCl2和KSCN混合溶液中滴加少量H2O2至过量,溶液先变红,说明H2O2优先氧化Fe2+


3.关注与化学相关的社会热点和科技前沿
从试题素材、考核知识点以及情景设置等角度,着力引导学生关注我国社会、经济和科学技术的发展,弘扬社会主义核心价值观。通过挖掘历史文献和顶级科研论文寻找合适资料,以中国古代科技文明、我国科学家最新研究成果编制试题,体现中国传统科技文化对人类发展和社会进步的贡献,引导学生热爱化学,为国奉献。减缓因陌生感带来的难度增加,探究相关物质的结构性质制法很有必要。2018年全国卷Ⅰ部分题目取材背景:

题号题型取材背景7选择题新能源汽车电池金属的回收11选择题CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除27实验题在医药、橡胶、印染、食品等方面应用广泛的焦亚硫酸钠(Na2S2O5)的制备28反应原理综合题在含能材料、医药等工业中得到广泛应用的一种新型的绿色硝化技术(采用N2O5为硝化剂)35物质结构与性质(选做题)以金属Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能36有机化学基础(选做题)高分子膨胀剂的合成
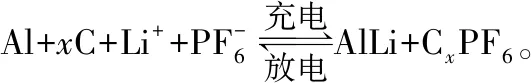
( )

C.充电时,两个电极增加的质量相等
【答案】D

【例6】2018年11月在法国凡尔赛召开的国际计量大会第26次会议将阿伏加德罗常数的定义修改为“1摩尔包含6.022 140 76×1023个基本单元,这一常数被称为阿伏加德罗常数,单位mol-1”。基于这一定义,阿伏加德罗常数的不确定度被消除了,新定义将于2019年5月20日正式生效。NA为阿伏加德罗常数的值,下列说法错误的是
( )
A.22.4 L(标准状况)氖气含有的电子数为10NA
B.0.4 mol NH3与0.6 mol O2在催化剂作用下充分反应,得到NO的分子数为0.4NA
C.27 g Al中加入足量1 mol/L的NaOH溶液,转移电子数为3NA
D.一定条件下,水蒸气通过Na2O2使其增重2 g时,反应中转移的电子数为NA
【答案】B
【解析】A.Ne为单原子气体,质子数为10,电子数为10,标况下22.4 L气体的物质的量为1 mol,故其所含电子数为10NA,故A正确;B.氨气的催化氧化为可逆反应,氨气不可能完全反应,所以生成的NO的分子数小于0.4NA,故B错误;C.27 g Al为1 mol,与NaOH充分反应生成NaAlO2,转移电子数为3NA,故C正确;D.水蒸气与Na2O2的反应,生成NaOH和O2,固体增加的重量可看成是H2O中“H2”的质量,增重2 g,参加反应的H2O为1 mol,转移电子数是NA,故D正确。
4.重用图表,巧设情境,考查化学素养
化学是信息、能源、材料、生命和环保等科学的重要基础,化学与生活、生产、科技等领域息息相关。试卷体现了“以化学知识及真实问题为依托,着力考查化学学习能力”的指导思想,许多试题的情境源于社会生活和科技前沿等热点问题,引导学生认识化学与人类社会和谐发展之间的关系,体现学科价值;体现学以致用;注重考查实践能力、创新意识和“科学精神与社会责任”的化学素养。
关注《考试大纲》中保留或新增的题型示例的图表信息,信息图文符号丰富、陌生情境下信息获取能力和分析解决能力。所谓无图不成题,图表类信息在近几年高考试题中出现的越来越频繁,涉及分值不断加大,对能力要求越来越高。
【例7】炭黑是雾霾中重要的颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是
( )

A.氧分子的活化包括O—O键的断裂和C—O键的生成
B.每活化一个氧分子放出0.29 eV的能量
C.水可以使氧分子活化反应的活化能降低0.42 eV
D.炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
【答案】C
【解析】本题从化学反应势能图的角度考查化学反应活性中间体和催化剂的催化过程。由图可知,炭黑和氧气在生成活化氧的过程中,活性中间体有C—O键的生成,生成活化氧时有O—O键断裂,故A正确;反应物的相对能量为0,活化氧的相对能量为-0.29 eV,所以每活化一个氧分子放出0.29 eV的能量,故B正确;有水参与时(虚线)活化能从0.75 eV降低为0.57 eV,降低值为0.18 eV,故C错误;题中信息可以理解成:O2+炭黑→炭黑-2[O]([O]表示活化氧),活化氧可以快速氧化二氧化硫,发生反应:2SO2+炭黑-2[O]→2SO3+炭黑,所以炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂,故D正确。
5.突出概念、原理的深度理解和应用,注重能力考查
高考命题的出发点是知识,但落脚点是考查获取知识、鉴别知识的能力和运用知识分析解决实际问题的能力,知识是作为考查能力的载体。试题命制首先确定要考查的能力,然后以实际问题为素材,确定考查的主干知识体系,在此基础上设置问题情景和设问方式。设问要体现认识、分析和解决实际问题的思维过程、态度、观点和方法,关注对学生综合科学素养的考查。
【例8】废旧光盘金属层中的少量Ag,某科研小组采用如下方案进行回收(金属层中其他金属含量过低,对实验的影响可忽略)。



(1)“氧化”阶段需在80℃条件下进行,最适宜的加热方式为____________________。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为____________________;HNO3也能氧化Ag,从反应产物的角度分析,以HNO3代替NaClO的缺点是____________________。
(3)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并________________。
(4)从“过滤Ⅱ”后的滤液中获取单质Ag的过程中,在加入2 mol·L-1水合肼溶液后,后续还需选用的试剂有________(①1 mol·L-1H2SO4、②10%氨水、③1 mol·L-1NaOH溶液,填序号)。反应完全后获取纯净的单质银再进行的实验操作过程简述为________________________________。
【答案】(1)水浴加热

(3)将洗涤后的滤液合并入过滤Ⅱ的滤液中
(4)① 过滤、洗涤、干燥


