水绵发酵产乙醇工艺构建及条件优化
田育青,张 秀,朱 密,何军良,周 旋
(1.武汉工程大学化学与环境工程学院,湖北 武汉 430205;2.华中科技大学环境科学与工程学院,湖北 武汉 430074)
《2018中国环境状况公报》指出,我国地表水的主要污染指标为氨氮、总磷、挥发酚、有机物等,此类污染物质能刺激浮游藻类大量繁殖,使得水体呈现富营养化特征[1]。近年来,将藻类修复技术应用于处理污染水体得到了广泛的关注[2],如张聪[3]将水绵用于去除城市污水处理厂二级处理出水中氮、磷、COD等污染物,使出水达到了一级A标准;雷国元[4]研究了水绵与团集刚毛藻去除氮、磷等污染物的效率,并探究了水绵抑制微型藻类生物生长的性能与机制,指出将大型丝状绿藻用于处理富营养化的自然水体是可行的。大型丝状绿藻的主要成分—碳水化合物最多可达藻干重的70%[5],由于其生物量巨大以及富含碳水化合物,能够产生的乙醇量是木材的4倍,干草的5倍[6]。蒋媛媛[7]采用铜藻发酵产乙醇,以原料计算乙醇的得率可达到11%;刘茂玲[8]分别用螺旋藻、蓝藻以及水葫芦发酵产乙醇,乙醇的得率可分别到达7.6%、35.1%、5.1%。乙醇具有清洁无污染、燃烧值高、可再生等优点,被公认为是常规化石燃料的理想替代品[9]。目前,国内外对藻类产乙醇的研究较多,但是与水绵的相关研究较少[10]。因此,构建水绵发酵产乙醇的工艺并对工艺参数进行优化,打通水绵治理污染水体的“最后一公里”,拓宽生物乙醇的原料来源,可为我国藻类制备乙醇提供新思路与技术基础,具有重要的意义。
1 材料与方法
1.1 试验材料
1.1.1 水绵干燥样
武汉东湖湖泊水环境质量为Ⅳ类,轻度富营养化,主要超标项目为总磷和化学需氧量[11]。试验所用水绵取自武汉东湖(2018年2~3月份),将其冲洗后晒干,粉碎过筛并保存。
1.1.2 主要试剂
主要试剂有:浓硫酸(98%,分析纯,武汉志远天合化工有限公司);纤维素酶(活度为10万u/g,和氏璧生物科技有限公司);酿酒酵母菌(南宁广龙工贸有限责任公司)。
1.1.3 主要溶液
(1) 水绵稀酸预处理混合物:配制总体积为600 mL,量取18 mL的98%浓硫酸稀释后,向锥形瓶中加入20 g的水绵干燥样,在100℃的条件下,搅拌2 h。
(2) 酵母活化液:称量10 g淀粉与蒸馏水混合,微沸10 min,待冷却后与5 g酵母粉充分混合,使用1 L容量瓶定容,于30℃封闭遮光48 h后,用于试验。
(3) 发酵辅助营养液:3 g/L蛋白胨,0.25 g/LCaCl2,0.25 g/L MgSO4,2.5 g/L KH2PO4。
1.2 试验装置
为了使水绵中纤维素、淀粉等可发酵的碳水化合物充分参与发酵反应,设计了水绵发酵产乙醇试验装置,详见图1。
试验过程为:首先将经粉碎过筛处理后的水绵干燥样置于预处理罐中,使用稀硫酸处理一段时间;然后将其在预水解罐中使用纤维素酶进行进一步处理,再将预水解后的水绵放置发酵罐中,加入一定量的发酵辅助液与酵母活化液,发酵一段时间后进行固液分离;最后将分离后的固态物质与液体密封保存,产物乙醇主要存在于液体之中。
该试验装置所具备的特点是:稀硫酸在破坏木质纤维结构的同时,可以使小部分的纤维素以及大部分的半纤维素水解成葡萄糖、木糖等可溶性单糖[12-13],并释放热量,这不仅缩短了酶水解的时间,为水解提供了适宜的酸性环境,也降低了酶水解温度控制的能耗;酶水解与发酵过程在分散并行系统中进行,在解决酶解产物(纤维二糖、葡萄糖等)对酶催化产生的抑制作用[14]、水解与发酵过程温度不一致问题的同时[15],有效地降低了发酵过程中温度控制的能耗;除此之外,发酵辅助液体与酵母活化液混合制备,是缩短产乙醇周期的关键技术。
1.3 试验方法
1.3.1 水绵干燥样成分的测定
水绵干燥样的水分按照《食品安全国家标准——食品中水分的测定》(GB 5009.3—2016)中的方法测定;灰分按照《饲料中粗灰分的测定》(GB/T 6438—2007)中的方法测定;粗纤维按照《植物类食品中粗纤维的测定》(GB/T 5009-10—2003)中的方法测定;纤维素和半纤维素按照参考文献[16]中的方法测定;淀粉按照《食品安全国家标准——食品中淀粉的测定》(GB 5009-5—2016)中的方法测定。

图1 水棉发酵产乙醇试验装置示意图Fig.1 Schematic diagram of ethanol production by Spirogyra fermentation
1.3.2 乙醇浓度的测定
产物乙醇浓度按照参考文献[17]中的方法测定。
1.3.3 单因素试验
选取预处理混合物中稀硫酸用量、纤维素酶用量、预水解时间、预水解温度、发酵时间和发酵温度共6个单因素,利用图1装置进行单因素试验。
试验分组设计如下:试验组①预处理混合物(制备见第1.1.3节)的初始pH值分别为3、4、5、6、6.5,纤维素酶用量为2.000 g,预水解时间为50 min,预水解温度为50℃,发酵温度为30℃,发酵时间为12 h;试验组②纤维素酶用量分别为0.250 g、0.500 g、0.750 g、1.000 g、1.500 g、2.000 g,预处理混合物的初始pH值为5左右,其余条件同实验组①;试验组③预水解时间分别为10 min、20 min、30 min、40 min、50 min、60 min、90 min,其余条件同上;试验组④预水解温度分别为40℃、45℃、50℃、55℃、60℃,其余条件同上;试验组⑤发酵温度分别为20℃、30℃、40℃、45℃、50℃,其余条件同上;试验组⑥发酵时间分别为5 h、10 h、15 h、20 h、25 h,其余条件同上。
1.3.4 响应面试验
在单因素试验的基础上,设预水解时间、发酵时间、发酵温度为自变量(原因详见2.2),产物乙醇的浓度为响应值,基于Design-Expert软件,利用响应面中心组合设计法得到各因素水平值(见表1),并采用响应面分析法,得到水绵发酵产乙醇工艺参数的回归模型。

表1 响应面法的各因素水平
1.3.5 水绵发酵产乙醇工艺全过程的优化
在回归模型预测出的最佳试验条件下,进行了放大10倍的产乙醇试验。在发酵过程中,每隔2 h进行一次乙醇浓度的测定,并采用Logistic模型[18][模型数学表达式见式(1)],基于1st Opt软件,对产物乙醇浓度的变化情况进行非线性拟合与优化,以得到能较好地描述水绵发酵产乙醇全过程的分段优化模型。
(1)
式中:p为t时刻乙醇浓度(g/L);p0为t0时刻对应的初始乙醇浓度(g/L);pmax为理论最大产乙醇浓度(g/L);vmax为理论最大乙醇产生速率[g·(L·h)-1];t为发酵时间(h)。
2 结果与分析
2.1 水绵干燥样的成分
水绵干燥样主要成分及其含量的测定结果,见表2。

表2 水绵干燥样主要成分及其含量(%)
注:含量取平均值,测定误差在5%以内。
由表2可知,水绵干燥样中含有67.53%的淀粉、纤维素、半纤维素等碳水化合物,由此可见采用水绵发酵产乙醇具有巨大的潜力。
2.2 单因素试验结果与分析
不同因素对产物乙酵浓度的影响,见图2。
由图2(a)可知,pH值从3.0变化至5.0再至6.5的范围内,产物乙醇浓度(平均值表示,下同)先上升随后下降,这可能是稀硫酸处理水绵干燥样存在着最佳用量。有研究表明,稀硫酸用量低(pH值较高)时,不能有效地处理干燥样,而用量过高(pH较低)时,导致干燥样中有机物质炭化[19]。因此,在后续的响应面试验中,将初始pH值控制在5.0左右,即选定预处理固液混合物中硫酸的含量为3%。

图2 水棉发酵产乙醇工艺中不同因素对产物乙醇浓度的影响Fig.2 Influence of related factors on ethanol concentration
由于纤维素酶成本高阻碍了纤维发酵产乙醇的工业化[20],除了开发廉价且高效的纤维素酶外,根据具体的反应研究纤维素酶的最佳用量也是降低成本的一种重要途径。由图2(b)可见,当纤维素酶用量低于1 g酶/g干燥样时,产物乙醇的浓度随纤维素酶用量的增加几乎呈线性增加;但当纤维素酶用量超过1时,产物乙醇的浓度变化趋于稳定。因此,在后续的响应面试验中将纤维素酶的用量选定为1 g酶/g干燥样。
预水解时间的长短,将会影响纤维素酶的作用效果。由图2(c)可见,预水解时间在0~50 min范围内时,产物乙醇的浓度随预水解时间的增加而增加,当预水解时间超过50 min时,产物乙醇的浓度基本趋于稳定。因此,在后续的响应面试验中将预水解时间的区间设定为40~60 min。
预水解温度能直接影响纤维素酶的活性,从而影响产物乙醇的浓度。但纤维素酶是起协同作用的多组分酶系,所以温度在适当范围变化对多组分酶系的影响较小,可能会使得乙醇产量的变化不显著。由图2(d)可见,在试验温度范围内,产物乙醇的浓度总体变化趋势较为平缓,最佳预水解温度在50℃~55℃范围内。因此,结合考虑预水解的能耗,在后续的响应面试验中将预水解温度选定为50℃左右。
发酵温度能直接影响酵母活性,从而对产物乙醇的浓度产生影响。由图2(e)可见,产物乙醇的浓度随发酵温度的变化较为显著,当发酵温度在40℃左右时,产物乙醇的浓度达到了最高值。因此,在后续的响应面试验中将发酵温度选定为40℃左右。
发酵时间短,会导致发酵不完全,但发酵时间过长,则会增加生产成本。由图2(f)可见,发酵时间少于15 h时,产物乙醇的浓度随发酵时间的增加不断增高,但继续延长发酵时间后,产物乙醇的浓度变化趋于平缓。因此,在后续的响应面试验中选择发酵时间为10~20 h。
2.3 响应面试验结果与分析
按照前述响应面设计方案进行试验,并对试验结果进行多元回归拟合,得到水绵制备乙醇的初步回归拟合模型如下:
Y=-9.37+0.29A+0.29B+0.14C+2.8×10-3AB+3.5×10-4AC+1.95×10-3BC-3.212×10-3A2-0.014B2-1.487×10-3C2
(2)
式中:Y为乙醇浓度(g/L);A为预水解时间(min);B为发酵时间(h);C为发酵温度(℃)。
上述回归拟合模型的决定系数见表3,该回归拟合模型的方差分析结果见表4。

表3 回归拟合模型的决定系数

表4 响应面二次式模型的方差分析结果
由表3和表4可知,初步回归模型的F值为152.12,p值<0.000 1(<0.050 0),“Pred R-Squared”为0.918 6,“Adj R-Squared”为0.988 4,反映信噪比的“Adeq Precision”为38.714(>4)。由此可见,该模型在所选择的因素水平范围内,可较为准确地预测A、B、C三因素交互作用下的产乙醇浓度,且此模型只有0.01%的概率发生幅度改变,即模型是合理的。
2.4 最佳产乙醇条件及其产量分析
根据上述所得到的初步回归模型[(式(2)],基于BBD模块,构建了不同因素与产物乙醇浓度关系的三维响应曲面以及相应的等高线,见图3。
由图3(a)可见,预水解时间与发酵时间对乙醇浓度的影响较为明显,其中在选取的条件范围内,预水解时间的变化对乙醇浓度的影响更大;由图3(b)可见,发酵温度与预水解时间对乙醇浓度的影响较为明显,其中发酵温度对乙醇浓度的影响更大;由图3(c)可见,发酵时间与发酵温度对乙醇浓度的影响较为明显,其中发酵温度对乙醇浓度的影响更大。因此,在研究范围内可以得出:预水解时间、发酵时间和发酵温度三参数之间的交互作用对乙醇浓度的影响较为明显;对乙醇浓度的影响作用按照从大到小的顺序排序为:发酵温度>预水解时间>发酵时间。其中,通过模型预测出的最高产乙醇浓度为5.71 g/L,其条件为预水解时间56 min左右、发酵时间为19 h左右、发酵温度40℃左右。然而在实际情况下,往往将最高乙醇产量与实际生产结合考虑,即可得到“最佳产乙醇条件”概念。通过此模型,得到了最佳产乙醇浓度为5.46 g/L,其条件为预水解时间52 min左右、发酵时间14 h左右、发酵温度40℃左右。“最佳产乙醇浓度”较“最高产乙醇浓度”相差约0.25 g/L(仅占最高产乙醇浓度的4.5%),但可节省大约5 h左右的产乙醇时间,能显著地缩短产乙醇周期。在最佳产乙醇条件下,进行重复试验得到实际产乙醇浓度平均值为5.61 g/L,与模型预测值5.46 g/L相差2.7%(<5%)。因此,该模型预测出的最佳产乙醇条件及其产量是可靠的。
2.5 水绵发酵产乙醇全过程预测
2.5.1 产乙醇全过程的非线性拟合
本文采用Logistic模型对水绵发酵产乙醇全过程进行非线性拟合,模型预测得到的乙醇浓度平均值与乙醇实际浓度平均值及其两者比较的相对误差,见表5。
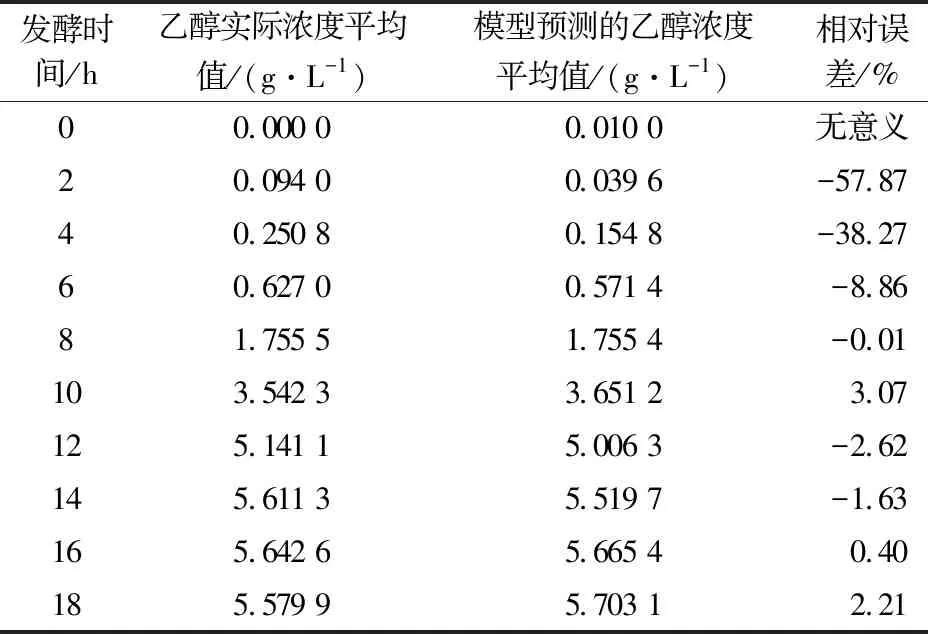
表5 乙醇预测浓度与实际浓度平均值的比较及其相对误差
经计算可知,模型拟合的决定系数R2为0.998 9,表明Logistic模型整体表现出较好的拟合效果。
由表5可知,发酵时间从8 h到18 h,模型的预测浓度与实际浓度的相对误差均小于5%,符合拟合标准,但发酵时间从0 h到8 h,模型的预测浓度与实际浓度的相对误差均大于5%,达不到拟合的标准。因此,须对发酵时间为0 h至8 h的时间段的模型进行进一步优化。

图3 不同因素与产物乙醇浓度关系的三维响应曲面以及相应的等高线Fig.3 Three-dimensional response surface of related factors and product ethanol concentration and the corresponding contour
2.5.2 产乙醇全过程数学模型优化
通过对发酵时间为0 h至8 h时间段的模型进行进一步优化,得到其数学表达式如下:
(3)
式中:p为乙醇浓度(g/L);t为发酵时间(h)。
产乙醇全过程分段模型的拟合效果见图4。

图4 产乙醇全过程分段模型方程的拟合效果Fig.4 Fitting degree of segmented model equation for the whole process of ethanol production
由图4可见,分段拟合后,乙醇浓度预测值与试验实测值的相对误差均小于5%,其中决定系数R2在0 h至8 h、8 h至18 h两个时间段分别为1和0.998 9。因此,使用此分段模型方程对产乙醇的整个周期进行拟合与预测,具有较强的可靠性。通过对式(3)进行分析,可得到最大乙醇浓度为5.715 8 g/L(实际最佳产乙醇浓度为5.61 g/L,两者误差小于5%),最大乙醇产生速率为0.691 9 g/[g/(L·h)]。
3 结论与展望
通过对水绵干燥样成分的测定以及水绵发酵产乙醇工艺的优化,得到以下结论:
(1) 水绵干燥样中约含有67.53%的淀粉、纤维素等可发酵产乙醇的碳水化合物,因此水绵发酵产乙醇具有较大的潜力。
(2) 在所选研究因素的范围内,预水解时间、发酵时间与发酵温度对最终的乙醇得率有显著的影响,这些影响因素之间具有交互关系,并非独自作用。在600 mL的预处理料液混合物(含20 g水绵干燥样、18 mL的98%浓硫酸)、150 mL的酵母活化液与200 mL的发酵辅助营养液组成的1 L发酵体系中,最佳产乙醇条件为:纤维素酶(10万u/g)与水绵干燥样的投加质量比为1∶1、预水解温度50℃、预水解时间50 min、发酵温度40℃、发酵时间14 h。其对实际乙醇生产中,最优工艺参数的选择具有指导意义。
(3) 在优化后的工艺条件下,得出了最大乙醇浓度为5.715 8 g/L,最大乙醇产生速率为0.691 9 g/[g/(L·h)]等重要发酵参数,这些参数对产乙醇全过程的调控具有指导意义。
生物乙醇是当今发展迅速的液体生物质能[21],因其具有清洁无污染、燃烧值高、可再生等优点[22]已被公认为是常规化石燃料的理想替代品[6]。藻类已被列入第三代生物能源,并已被研究者们成功应用于制备生物乙醇等领域,是能源制备领域最有前景的候选原料之一[23]。水绵作为具备发酵产乙醇潜力的藻类之一,具有生长周期短、适应性强、打捞成本低等特点,若能将水绵规模化人工养殖与治理污水同步、水绵产乙醇应用与能源政策相对接,这将在产生巨大环境效益的同时,带来可观的经济效益。

