ZnO包覆LiNi0.5Mn1.5O4正极材料的制备及其电化学性能
巩家旭 戴亚堂 鲁静华 王 伟 蒲琳钰 张 欢
(1. 西南科技大学材料科学与工程学院 四川绵阳 621010; 2. 西南科技大学理学院 四川绵阳 621010)
近年来,随着纯电动汽车和储能设备的快速发展,对锂离子电池性能要求越来越高。然而,由于安全性、储能能力等方面的限制,目前锂离子电池的性能还无法完全满足新能源产品的需求。在对高能量密度的动力电源迫切需求下,正极材料的研究开发受到研究者们的广泛重视[1]。LiNi0.5Mn1.5O4由于生产成本低、循环稳定性优越、较强的环境相容性而备受关注[2],尤其是镍锰酸锂具有4.7 V的高电压平台以及650 Wh/kg的高能量密度,且可提供快速的三维锂离子通道,具有优异的倍率性能[3-4]。然而,4.7 V高工作电压使得电解液分解生成的副反应产物损害正极材料镍锰酸锂,影响结构的稳定性,大幅度降低循环寿命[5];在高温环境下,材料的膨胀应力增大,极大地降低了材料性能[6]。为了提高镍锰酸锂在高电压、高温下的应用性能,可以通过电化学惰性物质对材料进行包覆,从而达到对正极材料的保护作用。通常,金属氧化物被用来做包覆物,如Al2O3[7],ZnO[8],TiO2[9],ZrO2[10]等,其中ZnO因具有相对较高的吉布斯自由能[11],在正极材料基体表面与电解液副反应产生的HF之间的反应速率相对更快,并且在高温下ZnO表现出更好的稳定性。
目前,对正极材料的包覆研究较为广泛,但关于ZnO包覆LiNi0.5Mn1.5O4高温性能研究较少。本文采用共沉淀法制备了锂离子电池正极材料LiNi0.5Mn1.5O4,并通过ZnO对材料进行表面包覆改性。对未包覆的LiNi0.5Mn1.5O4和包覆不同含量ZnO的LiNi0.5Mn1.5O4进行结构表征和电化学室温、高温性能测试。
1 实验部分
1.1 试剂与仪器
试剂:乙酸镍、乙酸锰、乙酸锂、乙酸锌、碳酸氢铵、N-甲基吡咯烷酮(NMP)等试剂均为分析纯,成都科龙化工试剂厂;导电剂Super p,上海汇平化工有限公司;聚偏氟乙烯(PVDF),上海东氟化工科技有限公司;泡沫镍、Celgard-2400型隔膜、锂片均来自郑州景弘新能源科技有限公司。
仪器:透射电子显微分析系统(TEM),Libra-200FE,德国蔡司仪器公司,加速电压15 kV;场发射扫描电子显微镜系统(FESEM),Ultra-55,加速电压为200 kV,德国蔡司仪器公司;X射线衍射仪(XRD),X' Pert Pro,荷兰帕纳科公司,辐射源Cu Kα射线,电压40 kV,电流20 mA,扫描速度5°·min-1,步宽0.02°,扫描范围10°~80°;激光拉曼光谱仪(Raman),InVia,英国雷尼绍公司,Ar离子激光器波长为514.5 nm,曝光时间为30 s,检测范围为200~800 nm-1;电化学工作站,Chi760i,上海辰华仪器有限公司,电化学阻抗图谱分析中频率范围为105~10-2Hz;电池测试仪,BTS-5V/1mA,深圳市新威尔电子有限公司,恒流充放电测试中电压范围为3.5~5 V。
1.2 样品制备
采用共沉淀法制备LiNi0.5Mn1.5O4(简称LNMO)前驱体Mn0.75Ni0.25CO3,按化学计量比Mn∶Ni=3∶1精确称取乙酸锰及乙酸镍,常温下溶于100 mL蒸馏水中搅拌10 min;加入20 mL无水乙醇,在搅拌同时,向溶液中缓慢滴加100 mL碳酸氢铵水溶液(2 moL·L-1),滴加完毕后继续搅拌5 h。对搅拌后的溶液进行离心洗涤,并在80 ℃下通风烘干,得到前驱体Mn0.75Ni0.25CO3。按化学计量比精确称取Mn0.75Ni0.25CO3∶Li=3∶1.03(锂过量3%以弥补高温下损失)的乙酸锂,和前驱体在玛瑙研钵中研磨20 min 后置于马弗炉中,空气气氛中400 ℃下预烧3 h,750 ℃下煅烧12 h,然后以1 ℃/min速率降温,得到LNMO材料。
将制备的LNMO溶于100 mL蒸馏水中,加入10 mL无水乙醇,超声分散10 min;以醋酸锌为锌源,按照ZnO包覆量为1%,1.5%,2.5%将一定量的醋酸锌分别加入LNMO分散液中,室温下搅拌4 h。对搅拌后的溶液离心洗涤,在80 ℃下通风干燥除去溶剂,然后放入马弗炉中400 ℃下煅烧4 h,得到氧化锌包覆的正极材料LNMO,按照包覆量1%,1.5%,2.5%分别记为LNMO@1% ZnO,LNMO@1.5% ZnO,LNMO@2.5% ZnO。
1.3 电极制备和电池组装
以制备的材料为活性物质、PVDF为黏结剂、Super p为导电剂,将三者按质量比8∶1∶1共同加入研钵中研磨均匀后,加入N-甲基吡咯烷酮继续研磨成浆料。将该浆料均匀涂覆在铝箔集流体上(涂层厚度约为200 μm),放入真空干燥箱中在100 ℃下真空干燥10 h。干燥后的极片用辊压机反复滚压3次后用切片机切出直径为14 mm的圆片,以该圆片作为正极,锂片作为负极,Celgard-2400膜为隔膜,1 mol/L的LiPF6/EC+DMS (EC与DMS的体积比为1∶1)溶液为电解液,在氩气气氛的手套箱中组装成CR2016型纽扣电池。
2 结果与讨论
2.1 材料结构与形貌分析
图1为基体LNMO和包覆了1%,1.5%,2.5%ZnO后的XRD图谱。基体LNMO和不同包覆量的LNMO产物的特征衍射峰均与LiNi0.5Mn1.5O4标准卡片(PDF#80-2162)一致,说明所制备的LNMO产物基体均为尖晶石型镍锰酸锂,并都属于Fd3m空间群。所有特征峰高而尖锐,说明产物结晶度较好,但所有样品在(400)晶面附近均有一个微弱的杂质衍射峰(图中以*标注),该杂质相的产生可能是由于镍锰酸锂在高温烧结过程中由于氧缺失导致杂质Li1-xNixO的生成[12]。包覆后的产物衍射峰的位置和强度未发生明显变化,说明包覆对基体LNMO的结构未产生影响。未能检测出ZnO对应的特征衍射峰,可能是由于样品中的包覆物含量较少所导致[13]。
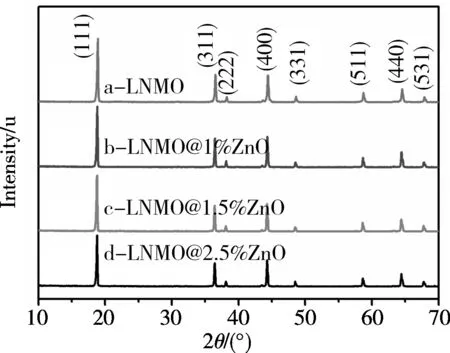
图1 样品的的XRD图谱Fig.1 XRD patterns of samples

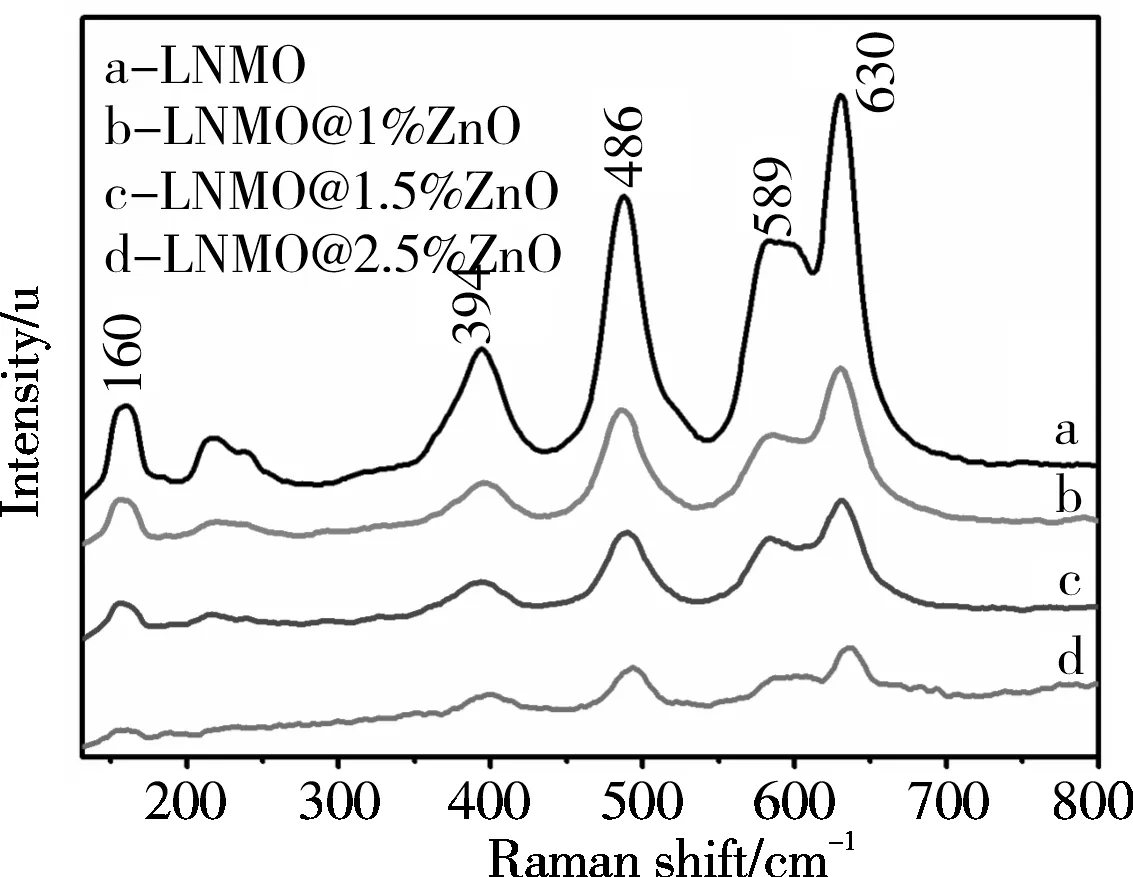
图2 样品的拉曼图谱Fig.2 Raman spectrum of samples
为研究包覆前后材料形貌变化,对包覆前后样品进行扫描电镜分析,并通过能量色散X射线光谱仪及扫描电子显微镜对包覆物ZnO进行定量分析。从图3中可以观察到,未包覆的LMNO材料表面平整,颗粒大多为轮廓清晰的正八面体形状,分布较为均匀,尺寸为微米级。包覆1%,1.5%,2.5% ZnO的LNMO材料,从图中可以观察到,包覆对基体材料的粒径和形状没有影响,但随着包覆量增大,材料表面粗糙度增加并在表面附着大量小颗粒,这些小颗粒可能是部分ZnO团聚形成,也有可能是包覆过程中二次烧结所导致。为进一步证明ZnO包覆成功,对包覆前后的材料进行EDS分析及元素面扫描分析,如图4、图5所示,包覆后不仅检测到LNMO基体元素的X射线特征能量,也检测出了Zn元素的特征能量,含量随包覆量不同依次为1.08%,1.5%,2.49%,符合拟包覆量。从EDS元素面扫描分析可以观察到ZnO均匀分布在LNMO基体表面。由此可得,ZnO对LNMO材料进行了包覆,从而减少材料应用于锂离子电池中与电解液的接触面积,提高应用性能。
2.2 电化学性能测试
图6(a)为未包覆及包覆不同含量ZnO的LNMO在0.1C(1C=147 mAh/g)倍率下的充放电曲线,从图中可以得出,样品在4.7 V左右均出现一个较长的充放电平台,对应于Ni4+/Ni3+和Ni3+/Ni2+两个电化学氧化还原反应。在4.0 V左右出现的较小平台对应于Mn4+/Mn3+电化学氧化还原反应。随包覆量提高至1.5%,在4.7 V左右的平台逐渐变宽,但当包覆量提高至2.5%时,该平台宽度小于包覆量为1.5%时的平台宽度。从表1中也可以得出,随包覆量提高至1.5%,首次充放电比容量均有显著提升,但当包覆量提高至2.5%时,该比容量出现了小幅度降低,这可能是由于包覆量过大对Li+在极片中的脱嵌过程产生阻碍。另外包覆1.5%,2.5% ZnO的LNMO首次充放电效率均高于基体,这可能是包覆后的材料与电解液接触面积减少导致SEI膜的形成程度减少[17],但对于包覆量为1%时该效率降低的原因尚不明确。

图3 样品的FESEM图谱Fig.3 FESEM images of samples

图4 LNMO@1%ZnO, LNMO@2.5% ZnO的EDS图谱Fig.4 EDS images of LNMO@1%ZnO, LNMO@2.5% ZnO

图5 LNMO@1.5% ZnO的元素面扫描图Fig.5 EDS dot map of LNMO@1.5% ZnO
从图6(b)可以得出,在0.1C倍率下充放电循环100次后,包覆的LNMO样品的放电比容量均高于基体容量。从表1中也可以得出,随包覆量提高至1.5%时,放电比容量以及容量保持率均随之提高,表明ZnO对基体的包覆可以有效减少活性物质和电解液的接触面积从而提高样品的容量及循环稳定性能。但随包覆量提高至2.5%时,样品的放电比容量和容量保持率虽高于基体,却相对于包覆1.5% ZnO的样品略有下降,这可能是由于包覆量较多,对Li+到达基体表面的阻碍作用有关[18]。
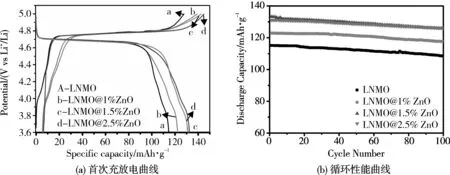
图6 室温下样品的0.1C首次充放电曲线和循环性能曲线Fig.6 The first charge-discharge curves and the cycling performance of samples at 0.1C current rate and room temperature
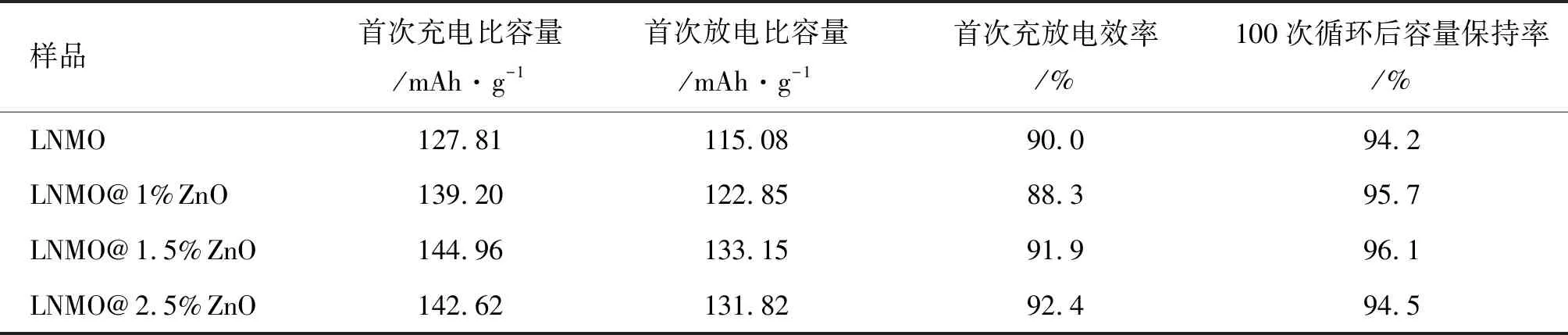
样品首次充电比容量/mAh·g-1首次放电比容量/mAh·g-1首次充放电效率/%100次循环后容量保持率/%LNMO127.81115.0890.094.2LNMO@1%ZnO139.20122.8588.395.7LNMO@1.5%ZnO144.96133.1591.996.1LNMO@2.5%ZnO142.62131.8292.494.5
如图7(a)所示,随充放电电流倍率提高至1C,所有样品的放电比容量均较0.1C倍率下有所降低。在1C倍率下100次循环后基体和包覆1%,1.5%,2.5% ZnO的LNMO放电比容量依次为92.50,97.70,119.58,108.34 mAh/g;容量保持率依次为:85.4%,87.0%,90.1%,86.1%。由此看出ZnO包覆量为1.5%时,在该条件下容量和容量保持率均优于其他样品。因此结合图6可得到结论,在室温下,包覆一定量的ZnO可以提高LNMO的电化学性质,尤其在ZnO包覆量为1.5%时,电化学性能提升最为显著。
图7(b)为55 ℃下样品在1C倍率循环100次的曲线,从图中可以看出,充放电循环100次后LNMO基体和包覆1%,1.5%,2.5% ZnO的LNMO放电比容量依次为40.07,72.01,98.02,90.00 mAh/g;容量保持率依次为:42.9%,68.1%,77.2%,78.4%。样品在高温下的电化学性能均低于常温条件,这是由于高温下电极中的氧化还原反应速率加剧,离子传输速率增快,导致材料的膨胀应力增大,随电化学反应进行材料结构逐渐被破坏[19]。可以看出包覆1.5%的ZnO在高温条件下放电比容量优于其他样品,并且随着ZnO包覆量的提高,样品在高温下的充放电循环稳定性得到显著提高,说明在高温条件下包覆的ZnO对基体依然起到一定程度的保护作用。
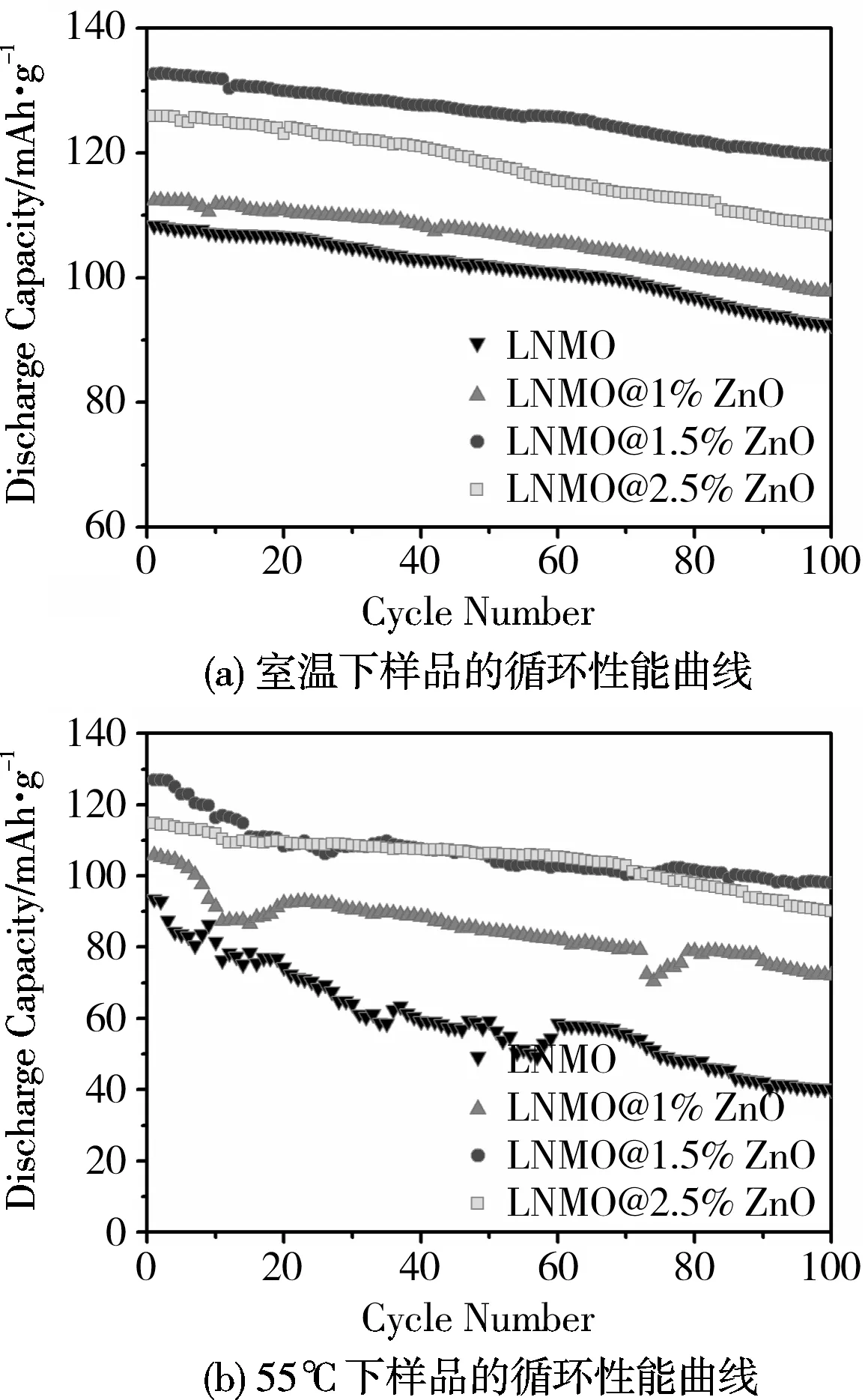
图7 室温和55 ℃下1C倍率的样品循环性能曲线Fig.7 The cycling performance of samples at room temperature and 55 ℃ and 0.1C current rate
图8为基体LNMO及不同ZnO包覆量的LNMO室温下的交流阻抗图谱。图谱高频区的圆弧反映了基体LNMO及包覆后的样品中锂离子在材料表面SEI膜中迁移,与电荷传递电阻及双电层电容有关;低频区的斜线反映了锂离子在活性物质中的扩散[20]。从图中得知,包覆后的LNMO的阻抗相比于基体均有降低,这是由于包覆后,ZnO包覆层降低了LNMO正极材料与电解液的接触程度从而抑制副反应的发生,使得电荷转移电阻明显减小,并提高了材料的结构稳定性。其中,ZnO包覆量为1.5%时材料的阻抗相对较小,电化学性能提升较为显著。

图8 室温下样品的交流阻抗图谱Fig.8 Electrochemical impedance spectroscopy of samples at room temperature
3 结论
本文采用共沉淀方法制备了锂离子电池正极材料LiNi0.5Mn1.5O4,并通过ZnO对其进行表面包覆改性。对未包覆的基体LNMO和包覆不同含量ZnO的LNMO进行结构表征和电化学性能测试,结果如下:(1) ZnO成功包覆在LiNi0.5Mn1.5O4表面,包覆量分别为1%,1.5%,2.5%,且包覆对基体材料的结构没有产生影响。(2) 包覆ZnO后的材料电化学性能明显优于未包覆的基体材料。包覆1.5% ZnO的材料电化学性能提升最为显著,室温0.1C倍率下首次放电比容量为133.15 mAh/g,充放电循环100次后容量保持率为96.1%;在室温1C倍率下首次放电比容量为132.66 mAh/g,充放电循环100次后容量保持率为90.1%;在55 ℃高温1C倍率下首次放电比容量为126.96 mAh/g,充放电循环100次后容量保持率仍能达到77.2%。(3) 交流阻抗测试表明,ZnO包覆在基体LNMO表面能有效减小基体材料与电解液的接触面积,减少材料与电解液的副反应程度,从而保持结构的稳定性,降低电荷转移阻抗,提高材料的电化学性能,尤其在ZnO包覆量为1.5%时材料的阻抗相对较小,电化学性能提升较为显著。

