鸦胆子药渣抗葡聚糖硫酸钠诱导小鼠肠炎作用研究*
高建胜,黄子健,潘碧妍,何国熙,窦耀星,王彤彤,谢友良,陈建南,苏子仁**
(1.广州白云山明兴制药有限公司 广州 510250;2.广州中医药大学中医药数理工程研究院 东莞 523808;3.广州中医药大学第一临床医学院 广州 510405)
溃疡性结肠炎(Ulcerative colitis,UC)是一种非特异性慢性炎症,属于炎症性肠病(Inflammatory bowel disease,IBD)的一种[1]。其临床特征为结肠黏膜的弥漫性浅表炎症[2]。根据其主要表现:急性疼痛,呕吐,体重减轻,腹泻和血便等[3],在中医理论中,UC 被归属于“久痢”、“肠澼”、“便血”[4]。据研究报道,UC 的发病率在世界上呈上升趋势[5],10 年内包括我国在内的部分东南亚国家UC 患病率呈指数增长且增长幅度已翻倍[6]。UC 病程久,复发率高,伴随营养不良、肠道损伤外,还可引起溃疡性结肠炎相关性结直肠癌严重的并发症,对人们的生活质量产生严重的影响[7]。该病病因和发病机制尚未完全明确[8],现代医学认为该病的发生是在遗传、环境、心理等多种因素共同作用下,导致的肠黏膜局部溃疡而发病。目前临床上治疗UC 无特效药物,主要以氨基水杨酸类制剂、免疫抑制剂、抗生素、类固醇激素等[9],上述药物种类和数量虽多,但全部属于化药范畴,疗效欠佳,且长期服用常出现明显的不良反应,使得治疗UC 成为一个困扰临床医生的难题。因此,寻求安全、有效、患者顺应好的药物成为研究UC 领域的热点。近年来,随着天然产物的不断发现,我们将目光转向我国传统中草药疗法。
鸦胆子是苦木科(Simaroubaceae)鸦胆子属植物鸦胆子(Brucea javanica(L.)Merr)的干燥成熟果实,属于常用中药。鸦胆子性寒味苦,归大肠经、肝经,有小毒,具有清热解毒,截疟,止痢的功效,常用于痢疾,疟疾。近年来,研究多集中于鸦胆子的抗肿瘤作用及机制[10-12],鲜有对其治疗痢疾这一传统应用的报道。不断有临床研究表明,口服或者灌肠鸦胆子油及其鸦胆子相关制剂对UC 均具有很好的治疗作用[16-18]。此外,已有研究表明鸦胆子苦醇、鸦胆因D、鸦胆子油乳对DSS 诱导的UC 小鼠模型具有较为良好的治疗作用[13-15]。在鸦胆子油实际生产过程中,石油醚提取鸦胆子油后,会产生大量鸦胆子药渣。根据前期研究,鸦胆子药渣含有鸦胆子苦醇、鸦胆因D 等苦木内酯类成分,但是否具有抗UC 的作用,尚未得到证实。本文拟开展鸦胆子药渣治疗肠炎作用的研究,现将结果报道如下:
1 材料和方法
1.1 实验动物
48 只SPF 级Balb/c 雄性小鼠,体重为20-23 g,购自广东省医学实验动物中心,合格证号:SYXK(2013-0085)。
1.2 试剂与材料
葡聚糖硫酸钠(DSS,分子量:36 000-50 000,加拿大MP 生物医药公司);美沙拉嗪(5-ASA,上海爱的发制药有限公司);TNF-α、IL-1β、IFN-γ酶联免疫反应Elisa 试剂盒(美国ebioscience 公司)。苏木素、伊红购自于广州化学试剂总厂。
鸦胆子药渣提取物:取鸦胆子提油后的药渣2 500 g,粉碎,经100 目筛网过滤得到药渣粉。按照药渣粉:乙醇=1∶3(W/V)的比例加入乙醇。加热回流提取2 次,每次2 h,合并滤液。采用旋转蒸发仪浓缩体积,回收乙醇后浓缩得到浸膏70 g。
1.3 实验动物的分组、造模及取材处理
造模前,将48 只小鼠饲养在光照/黑暗周期为12小时的房间中,保持房间温度(22-24℃)和相对湿度(40-55%)。适应性喂养7 d 后,依表1 随机分为:正常对照组,DSS 组,5-ASA 组,鸦胆子药渣低、中、高剂量组,共6个小组,每组8只。
正常组给予蒸馏水,其余5 组给予3%DSS 水溶液造模,分别装于水壶中供小鼠自由饮用7 d。造模时,正常对照组和DSS 组给予蒸馏水,其余各组小鼠灌胃给予如表1所示相应的药物进行治疗,持续7 d,每日1次。于第8 d 处死小鼠,剖腹取出全结肠,挤出肠道中所含粪便。迅速纵剖结肠并把粪便残留物用生理盐水冲洗去除,并吸除结肠多余生理盐水后测量其长度和重量。取0.5 cm 结肠组织固定于体积分数10%甲醛中,石蜡包埋,4 μm 厚切片以备HE 染色用;剩余部分取1.0 cm分装于离心管中,液氮冻存后转入-80℃冰箱,用于ELISA分析。

表1 小鼠分组及给药剂量
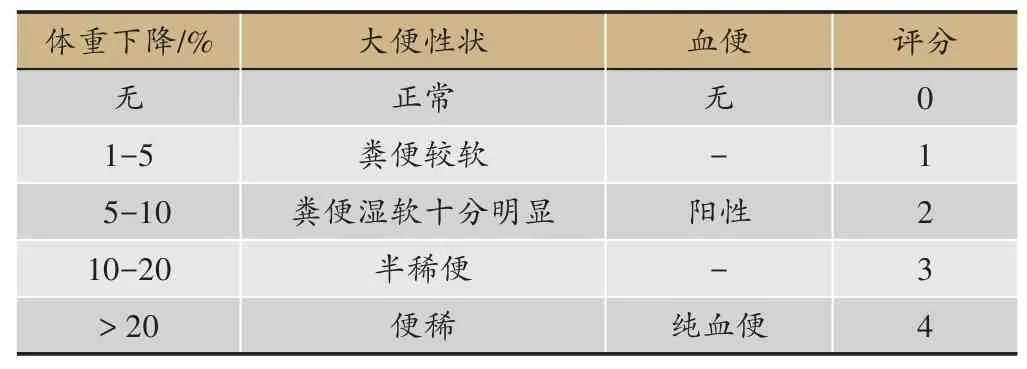
表2 DAI评分方法
1.4 疾病活动指数(Disease activity index,DAI)评估
造模期间,每天观察动物健康状况并记录其一般情况:体重变化、粪便特征、腹泻和直肠出血情况。在实验结束时,DAI 指数由不清楚实验方案的人员按表2标准评分。
1.5 病理切片
将小鼠肠组织制作病理切片后,在显微镜下观察结肠组织的病理变化,并进行结肠炎症和损伤程度组织学病理评分(Histological score),评分由两名病理学家按照下述表3标准进行盲评。
1.6 酶联免疫吸附法(ELISA)测定炎症因子及炎性介质
根据试剂盒说明书加入匀浆介质并制备组织匀浆,离心后取上清液测定TNF-α、IL-1β及IFN-γ含量。
1.7 统计方法
采用GraphPad Prism 7.0 软件进行绘图,采用SPSS 23.0 软件进行统计学分析,数据结果以平均值±标准差表示。各指标组间比较使用单因素方差分析(One-way ANOVA),方差齐时,组内两两多重比较采用LSD 法;方差不齐时,组内两两多重比较采用Dunnett's T3 法。P<0.05 或P<0.01 表示有显著性差异。

表3 组织病理状态评分

图1 小鼠一般活动情况(n=8)
2 实验结果
2.1 小鼠一般活动情况观察
在实验过程中,正常组小鼠毛色光亮,每天饮水摄食正常,排便正常,体质量呈持续上升;造模后小鼠出现活动减少,精神倦怠,出现厌食,体重减轻和水样粪便及肛门部位不同程度的出血等情况。如图1A 所示:模型组第3 d 起,小鼠开始逐渐出现腹泻、黏液便,明显的体重减轻;阳性药组小鼠前4 d 虽保持持续下降趋势,但第五天开始,饮食逐渐增多,体重下降减缓且呈上升趋势,活动增加,大便逐渐恢复正常;鸦胆子药渣提取物各给药组与阳性药组趋势类同,且呈剂量依赖关系;其中,鸦胆子药渣提取物高剂量组小鼠体重增长最为明显。根据实验第8 d 小鼠DAI 指数评分标准进行计算,结果如图1B。模型组的DAI评分显著高于正常对照组(P<0.01)。与模型组比较,阳性药治疗后能够显著降低小鼠DAI分数(P<0.01);鸦胆子药渣提取物各给药组能够不同程度地降低了DSS 诱导的溃疡性结肠炎的DAI评分(P<0.01),并呈剂量依赖关系;其中,鸦胆子药渣提取物高剂量组降低小鼠DAI评分最为显著。
实验第8 d小鼠结肠长度结果如图1B。模型组小鼠结肠长度相比正常对照组明显缩短(P<0.01)。与模型组比较,阳性药治疗后能够显著改善结肠长度的缩短情况(P<0.01);鸦胆子药渣提取物各给药组均能不同程度改善小鼠结肠长度缩短情况(P<0.01),与阳性药组趋势类同,且呈剂量依赖关系;其中,鸦胆子药渣提取物高剂量组改善小鼠结肠长度的缩短最为显著(P<0.01)。综上所述,鸦胆子药渣提取物能够改善DSS 诱导的溃疡性结肠炎小鼠的宏观表现,其中高剂量的鸦胆子药渣提取物对小鼠溃疡性结肠炎改善最为显著。
2.2 DSS诱导的UC模型小鼠的结肠组织结构变化
结肠组织病理切片染色及组织病理学评分,结果见图3。正常对照组小鼠的结肠组织结构完整,腺体排列整齐、无萎缩,黏膜层及结肠黏膜下层无明显的炎细胞浸润。模型组小鼠结肠组织显示有明显的坏死,上皮破损或缺损,黏膜下层可见大量的炎性细胞浸润,同时伴有隐窝增生,其组织病理学评分,显著高于正常对照组(P<0.01)。阳性药组较模型组情况好转,黏膜上皮破损不明显,黏膜层及下层炎症细胞浸润减少,固有层腺体萎缩情况减轻,肌层及浆膜较为完整,改善小鼠结肠组织病理学评分(P<0.01);鸦胆子药渣提取物各给药组与阳性药组趋势类同,均能减轻结肠组织病理变化和改善小鼠结肠组织病理学评分(P<0.01),且呈剂量依赖关系;其中,鸦胆子药渣提取物高剂量组小鼠改善结肠组织病理变化和病理学评分最为明显。

图2 小鼠结肠长度比较(n=8)
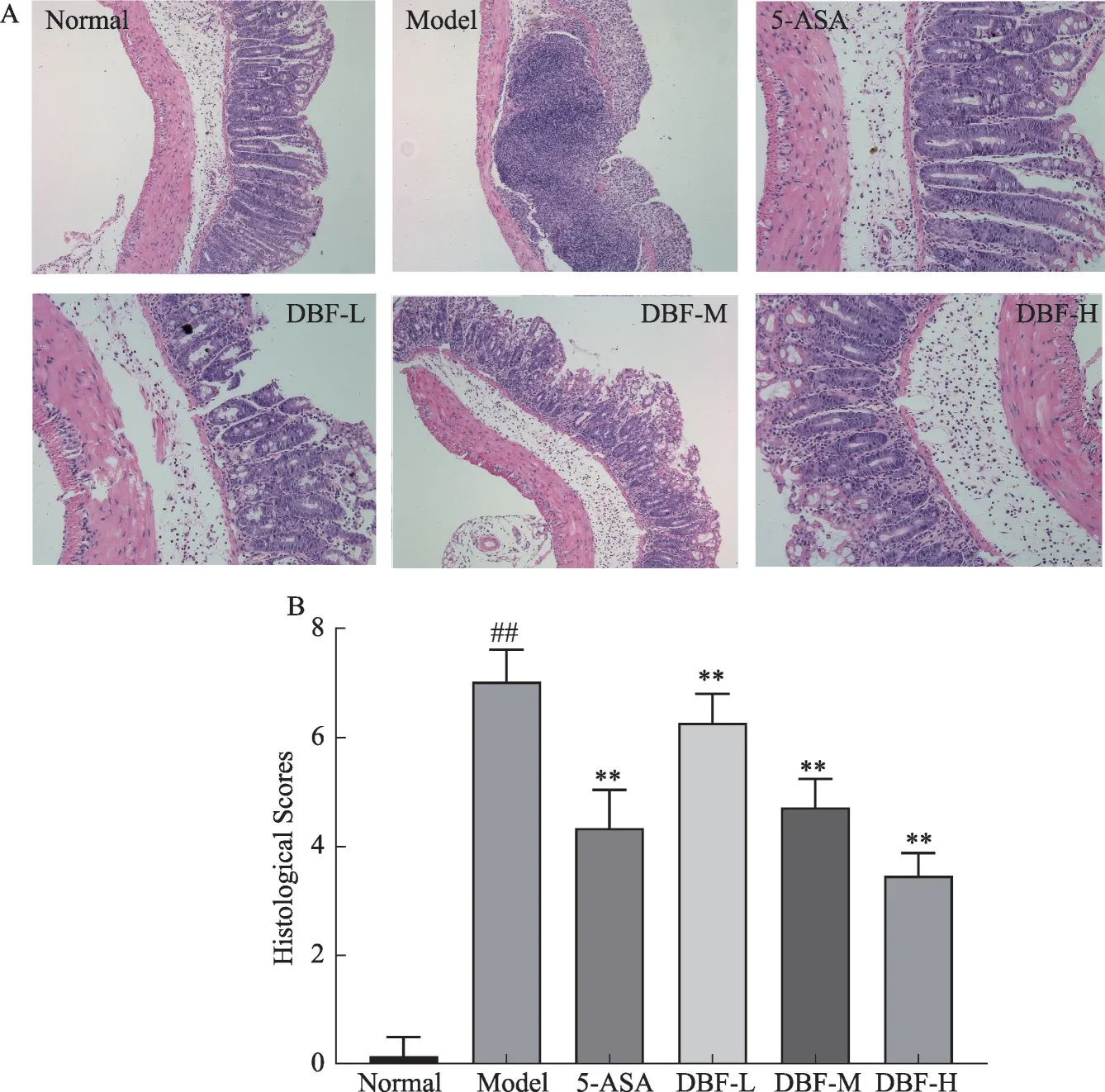
图3 结肠组织结构变化及组织病理学评分(n=8)
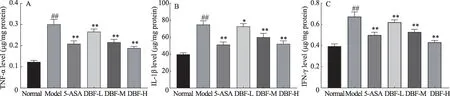
图4 对小鼠结肠组织中免疫炎性细胞因子产生的影响(n=8)
2.3 DSS 诱导的UC 模型小鼠结肠组织中细胞炎症因子的影响
小鼠结肠组织中细胞炎症因子测定结果,见图4。模型组小鼠肠组织中的促炎细胞因子TNF-α、IL-1β、IFN-γ水平均明显高于正常对照组(P<0.01);与模型组比较,阳性药组小鼠肠组织中的促炎细胞因子TNF-α、IL-1β、IFN-γ水平均显著降低(P<0.01);鸦胆子药渣提取物各给药组能够不同程度的降低促炎因子水平(P<0.05,P<0.01),且呈剂量依赖关系;其中,鸦胆子药渣提取物高剂量组降低小鼠肠组织中的促炎细胞因子TNF-α、IL-1β、IFN-γ水平最为明显。
3 讨论
溃疡性结肠炎(UC)是炎症性肠病(Inflammatory bowel disease,IBD)的一种,该病是一种累及胃肠道的慢性炎症性疾病,发病机制尚不明确。其有终生复发倾向,病程迁延,发作与缓解交替,且有癌变倾向,临床表现以持续或反复发作的腹痛、腹泻、粘液血便等症状为主[13]。近年来,UC 的发病率在发展中国家呈指数增长,在发达国家稳定增长。根据UC 所表现出来的临床症状,中医学将其归属于“休息痢”、“肠澼”、“肠风”、“久痢”、“賍毒”、“滞下”等范畴[19]。《医学衷中参西录》中指出:“凡痢之偏于热者用之皆有捷效,而以治下鲜血之痢,泻血水之痢,则尤效”,“凉血解毒,善治热性赤痢,二便因热下血”。目前,临床上治疗UC 常用治疗药物多为氨基酸水杨酸盐、免疫抑制剂、皮质类固醇激素、抗生素等[20],一定程度上可以缓解患者的临床症状,但是不能从根本上完全治愈UC,且伴随不同程度的副作用,是现代医学难治病症之一[21]。因此,寻求安全有效的治疗方案和药物刻不容缓。
鸦胆子是苦木科鸦胆子属植物(Brucea javanica(L.)Merr.)的干燥成熟果实,始载于《本草纲目拾遗》,又名老鸦胆、苦参子等。其味苦,性寒,归大肠、肝经,具有清热解毒、截疟、止痢之功效,外用还可腐蚀赘疣。主治痢疾,疟疾;外治赘疣,鸡眼。鸦胆子用于痢疾治疗由来已久,是民间用于治疗里急后重、腹泻腹痛、赤白脓血便等重要药用植物之一[22]。张锡纯[18]认为“治痢最要药品,其痢之偏热者,当以鸦胆子为最要之药”。已有文献报道,鸦胆子油口服乳液保留灌肠治疗UC 疗效明显[16],除此之外,鸦胆子油乳和鸦胆子成分鸦胆苦醇、鸦胆因D 对DSS 诱导的小鼠溃疡性结肠炎均有明显的治疗作用[13-15]。根据文献我们已知鸦胆子药渣中含有鸦胆子苦醇、鸦胆因D 等苦木内酯类成分[23],因此,我们选用提油后的鸦胆子药渣提取物作为研究对象,探究提油后的鸦胆子药渣对DSS 诱导的小鼠UC是否同样具有明显的治疗作用。
目前,UC 动物模型已成为研究该病病因的有效手段,其中化学试剂DSS诱导的小鼠结肠炎与人类UC临床表现特点相似[24,25],如体重下降、腹泻腹痛、结直肠缩短、直肠出血、以及相应的组织学特性,包括组织多部位的侵蚀、结肠黏膜炎症变化,间或腺窝脓肿等。本实验研究发现,口服给予小鼠不同剂量鸦胆子药渣提取物后,能够不同程度的增加小鼠体重,改善便血及肠组织变化。结合实验动物的DAI 评分(结合体重下降、粪便性状、便血状态三者的变化而得出的评分)和结肠长度变化,能够从宏观变化的角度说明鸦胆子药渣提取物对UC 具有治疗作用。此外,细胞因子是细胞经刺激而合成分泌的一类具有生物活性的小分子蛋白的统称,具有调节免疫应答、介导炎症介质和参与组织修复等功能[26]。现代研究认为各种细胞因子对于肠道免疫系统至关重要。作为细胞间的信号传递分子,长期而持久的分泌失衡可使炎症反应呈现慢性化表现。目前已知与UC 发病密切相关的细胞因子主要有白介素(interleukin,IL)、肿瘤坏死因子(Tumor necrosis factor,TNF)、干扰素(interferon,IFN)等[27-28]。TNF-α作为TNF 的一种亚型,是机体炎症与免疫反应的重要调节因子。TNF-α的过度表达可导致上皮屏障损伤,上皮细胞凋亡,以及结肠上皮细胞分泌趋化因子[29];同时,其作为促炎因子,与抑炎因子间的失衡可导致UC 的发生与发展,在该疾病发病机制中起到核心作用[30]。IL-1β是由活化的固有免疫细胞如巨噬细胞、单核细胞产生的一个经典的促炎性细胞因子,在宿主防御和感染以及炎症病理发展过程中发挥重要作用。IL-1β水平的增加,会引起损害结肠组织的自身免疫过程[31],是UC 发病、发展的重要因素[32]。IFN-γ是由Thl 淋巴细胞和NK 细胞产生的一种二聚体糖蛋白,具有免疫调节活性,是吞噬细胞和中性粒细胞激活物[33]。IFN-γ对伤口的调节作用由TNF-α介导,对伤口修复至关重要[34]。本研究通过实验发现,与正常对照组相比,模型组的TNF-α、IFN-γ、和IL-1β水平增加明显,给与鸦胆子药渣提取物后能显著降低TNF-α、IFN-γ、和IL-1β水平的增加,表明其潜在的抗炎作用。
综上所述,鸦胆子药渣提取物对实验性结肠炎小鼠具有治疗作用,具体体现为能够改善UC 小鼠的体重下降,疾病活动度,改善结肠组织的缩短程度和病理损伤程度。其机制可能是通过降低TNF-α、IFN-γ、和IL-1β表达,进而维持体内促炎症因子平衡,修复局部结肠黏膜功能,恢复肠黏膜屏障保护功能来实现的。实验结果为鸦胆子提油后的药渣用于UC 治疗提供了科学依据。