甲磺酸阿帕替尼联合腹腔灌注顺铂对合并腹腔积液老年晚期卵巢癌患者的临床疗效
任妹
我国卵巢癌发病率居妇科恶性肿瘤第3 位,死亡率在妇科恶性肿瘤排名第一[1],严重威胁着女性健康。发病后早期症状不典型,初诊时约70%患者已属晚期[2]。尽管标准的卵巢肿瘤减灭术辅以铂类为基础的化疗可以使其获得临床缓解,但近90%的患者将面临复发并最终死亡[3,4]。复发导致极少数患者对二线化疗有效,绝大部分患者因缺乏有效的二线以上治疗方案而预后不良。老年患者营养状况及自身素质不佳,同时易合并高血压、冠心病、糖尿病等基础疾病,故而无法耐受高强度化疗,导致治疗有效率低,预后差,因此寻求一条安全、高效的治疗途径显得尤为重要。
自从1971年Folkman[5]提出“实体恶性肿瘤的生长和转移离不开新生血管”这一观点后,与肿瘤血管生成相关的研究层出不穷。在肿瘤血管生成和生长中,血管内皮生长因子(vascular endothelial growth factor,VEGF)或VEGF 受体(VEGF receptor,VEGFR)-2 信号通路扮演着关键角色[6],其本质是一种与内皮细胞具有高亲和力的糖蛋白,可特异性与血管内皮细胞结合并增加血管通透性。
恶性腹腔积液是晚期卵巢癌常见的合并症之一。早些年,有许多研究表明VEGF 在恶性胸腹水形成中起着重要作用,最近有研究显示VEGF 参与恶性腹腔积液的发生发展,腹水中VEGF 水平是腹膜转移的重要预后指标[7]。甲磺酸阿帕替尼是一种新型口服小分子抗血管生成药物,可高度选择性地抑制VEGFR-2 酪氨酸激酶活性,阻断血管内皮生长因子结合后的信号转导,从而有效抑制肿瘤血管生成[8]。研究证实,甲磺酸阿帕替尼在多种实体瘤中均取得了可靠疗效[9]。但其对合并腹腔积液的老年晚期卵巢癌治疗的相关报道甚少,本研究选取合并腹腔积液的老年晚期卵巢癌患者为研究对象,旨在探讨甲磺酸阿帕替尼联合腹腔灌注化疗的有效性和安全性,以期为老年晚期卵巢癌患者治疗提供一条新的途径。
1 材料与方法
1.1 一般资料选取2016年1月~2017年12月在我院就诊的、经病理学检查确诊合并腹腔积液的晚期卵巢癌患者共76 例。随机分为观察组和对照组,各38 例。对照组年龄68~83 岁,平均(75.0±1.5)岁,观察组年龄66~82 岁,平均(74.0±1.3)岁。所有入组患者均符合以下标准:①年龄>60 岁;②经病理学检查证实为卵巢癌,腹水行脱落细胞检查,证实为癌性腹水;③既往接受过至少两种系统化疗后进展或复发的晚期卵巢癌;④无明显化疗及腹腔穿刺禁忌证;⑤非哺乳期或妊娠期妇女;⑥自愿签署知情同意书。两组研究对象的基线资料相比,差异无统计学意义(P>0.05),存在可比性。
1.2 治疗方法对照组:仅行腹腔灌注化疗。具体方法:在B 超定位下患者行腹腔穿刺引流术,腹水引流干净后,予以顺铂40mg 腹腔灌注,每2 周进行1 次,在灌注前,均向腹腔内注射地塞米松5mg,术前予以盐酸昂丹司琼8mg 静脉推注预防性止吐。术后嘱患者每隔30min 转换体位,使化疗药物与腹膜充分接触。
观察组:在对照组的基础上,于腹腔灌注化疗的当天开始口服盐酸阿帕替尼片(商品名:艾坦,江苏恒瑞医药股份有限公司,国药准字H20140103,规格:250mg×10 片/盒),每次500mg,1 次/日,直到患者病情进展或产生不可耐受的副反应。
1.3 评价指标
1.3.1 腹水控制情况 采用WHO 疗效判断标准对腹水疗效进行评定:完全缓解(complete remission,CR):腹水完全消失,持续时间达4 周以上;部分缓解(partial remission,PR):腹水量减少≥50%,持续时间达4 周以上;疾病稳定(stable disease,SD):腹水量减少<50%或腹水量增加<25%,持续时间达4 周以上;疾病进展(progression disease,PD):腹水量增加≥25%。用(CR+PR)/总例数×100%来评价有效率(response rate,RR);用(CR+PR+SD)/总例数×100%来评价疾病控制率(disease control rate,DCR)。
1.3.2 近期疗效(肿瘤控制情况) 每月对患者进行CT 或MRI 检查,采用WHO 实体瘤评价标准对肿瘤控制情况进行评定,评价结果分为CR、PR、SD、PD 四个等级,其中RR=(CR+PR)/ 总例 数×100%,DCR=(CR+PR+SD)/ 总例数×100%。
1.3.3 远期疗效(总生存时间、无进展生存时间) 总生存时间(OS)定义为患者接受治疗到患者死亡或者随访结束的时间;无进展生存时间(PFS)定义为患者接受治疗到病情进展或者患者死亡的时间。
1.3.4 不良反应评估 采用疼痛数字评估法(NRS)评估患者疼痛情况,1~3 分为轻度疼痛;4~6 分为中度疼痛;7~9 分为重度疼痛;10 分为剧痛。本实验仅记录4 分及以上疼痛。
1.4 随访随访截至2019年1月或者患者死亡,中位随访期为12 个月(3~17 个月)。
1.5 统计学分析采用SPSS 19.0 软件对数据进行统计描述和分析。计量资料采用均数±标准差(±s)描述。分类资料采用例数(百分比)描述,组间比较采用Pearsonχ2检验。采用Log-rank 检验比较组间的生存情况。P<0.05 为差异有统计学意义。
2 结果
2.1 两组腹水控制情况比较观察组的有效率和腹水控制率明显高于对照组,差异有统计学意义(P<0.05),见表1。
2.2 两组肿瘤控制情况比较观察组有效率及疾病控制率明显高于对照组,差异有统计学意义(P<0.05),见表2。
2.3 两组中位生存时间及中位无进展生存时间比较Log-Rank 检验结果显示,观察组患者的平均生存时间和中位生存时间均长于对照组,差异有统计学意义(χ2=10.253,P=0.001),见表3。从累积生存概率曲线图也可以看出,观察组的生存概率下降趋势较对照组缓慢,见图1。
观察组患者的平均无进展生存时间和中位无进展生存时间均长于对照组,差异有统计学意义(χ2=16.726,P<0.001),见表4。从累积生存概率曲线图也可以看出,观察组的无进展生存概率下降趋势较对照组缓慢,见图2。
2.4 两组不良反应发生率比较观察组和对照组患者的血压升高、皮肤瘙痒、发热、恶心、呕吐、腹痛、乏力发生率及总体不良反应发生率比较,差异无统计学意义(P>0.05),见表5。
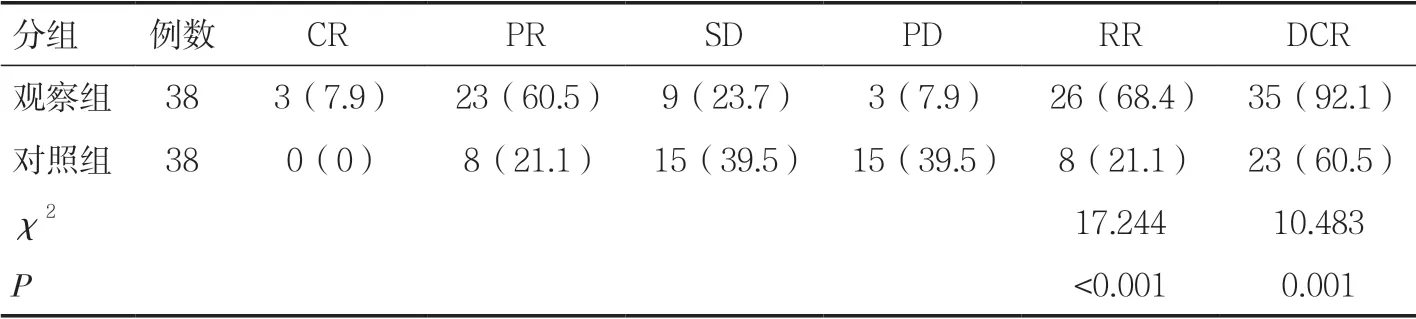
表1 两组患者腹水控制情况比较[n(%)]
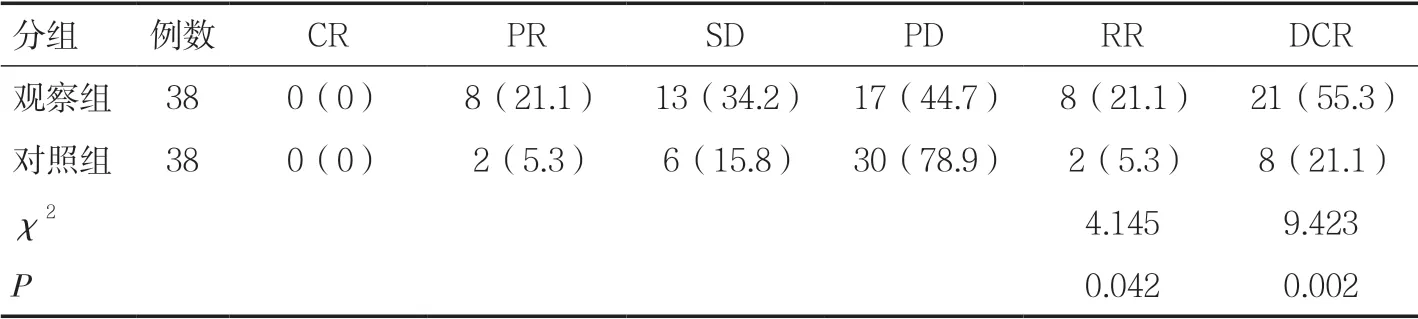
表2 两组患者肿瘤控制情况比较[n(%)]
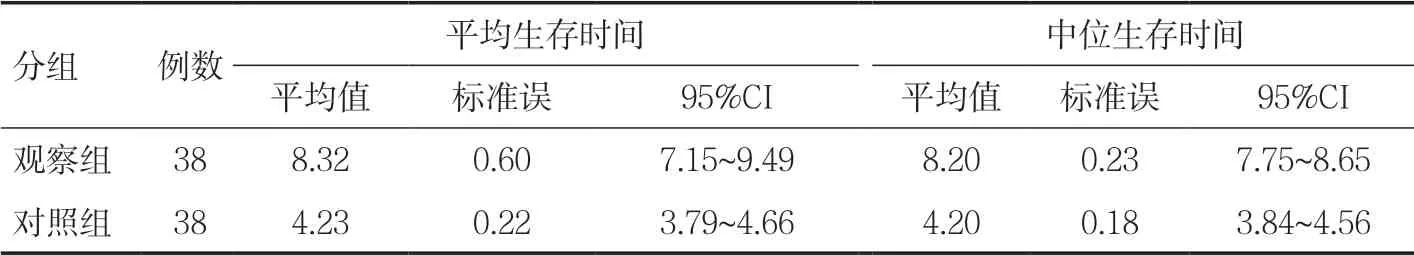
表3 两组患者总生存时间的Log-Rank 检验
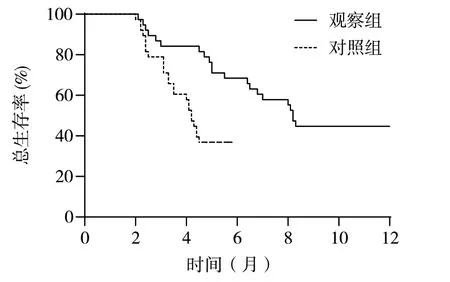
图1 两组患者的总生存时间曲线图
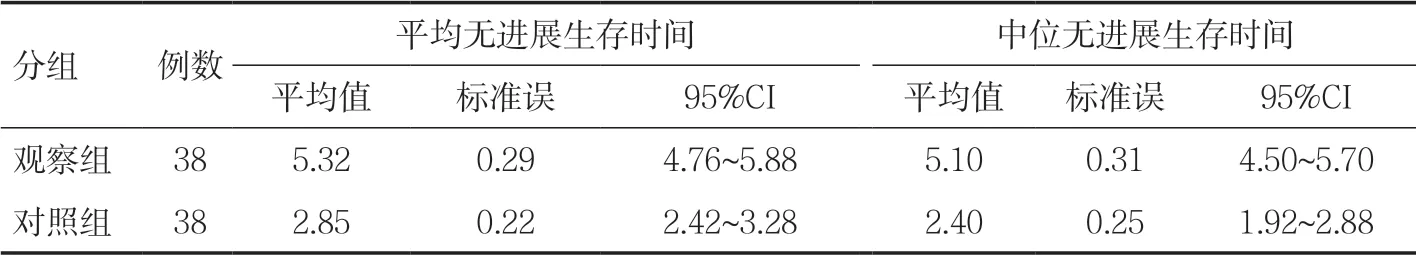
表4 两组患者无进展生存时间的Log-Rank 检验
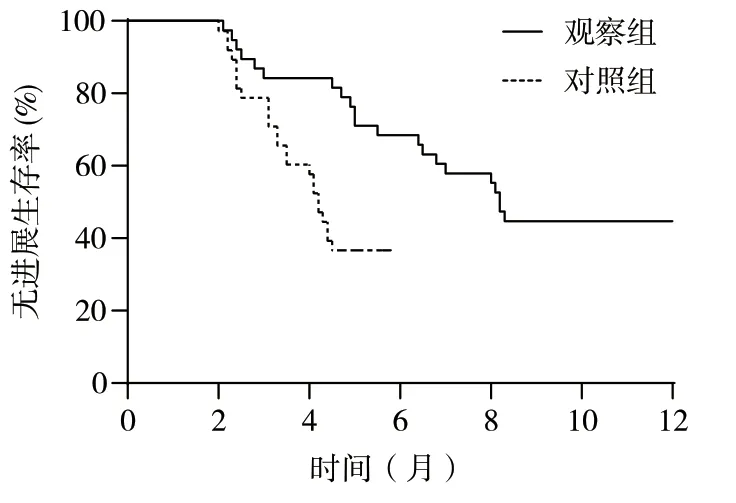
图2 两组患者的无进展生存时间曲线图
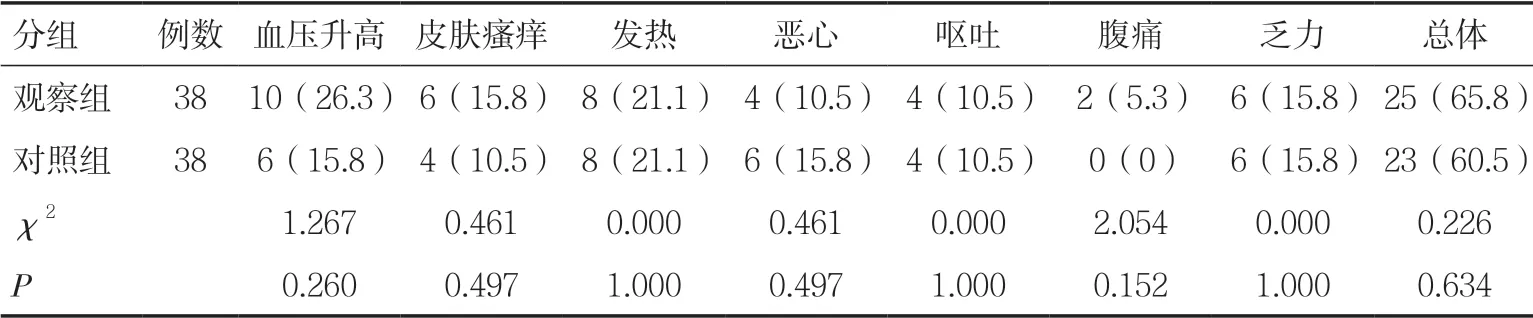
表5 两组患者不良反应发生情况比较[n(%)]
3 讨论
卵巢癌是女性生殖系统常见肿瘤,发病率和死亡率均较高[10],严重威胁女性健康。肿瘤细胞减灭术联合化疗是卵巢癌的重要治疗方式。铂类药物通过细胞毒性作用损伤DNA,同时亦可致线粒体受损从而导致细胞凋亡,是目前卵巢癌的一线化疗药物,疗效确切。顺铂是一种细胞周期非特异性药,在腹腔灌注化疗中,可不通过腹膜屏障,在腹腔局部形成较高的药物浓度,并通过与腹膜的充分接触,清除游离癌细胞,减少局部复发[11]。卵巢癌进展过程中,血供需求迅速上升,因此新生血管形成速度成为影响卵巢癌生长的重要因素。研究发现在所有促血管生成因子中,作用最强的当属VEGF家族[12]。VEGF 通过与VEGFR-2 结合,激活下游信号,诱导内皮细胞生长、迁移及管状形成,从而促进新生血管形成。因此阻断VEGF-VEGFR-2 信号通路可以抑制血管的异常增生[13]。同时VEGF 升高能增加血管通透性,导致患者腹腔积液量不断增加。鉴于此,合并腹腔积液的晚期卵巢癌患者配合抗血管生成的靶向药物可提高疗效。
甲磺酸阿帕替尼是我国自主研发的口服小分子靶向抗血管生成药物,它能选择性地抑制VEGFR-2,从而抑制VEGF 刺激的血管内皮增殖及迁移,并对c-Kit、c-Src 络氨酸激酶产生轻度抑制,从而抑制新生血管生成[8]。研究表明,无论单独使用阿帕替尼还是联合其他细胞毒性药物,均对实体瘤模型如胃癌、肝癌、肺癌有较好疗效,且联合用药效果更佳[14]。
本研究选取既往接受过至少两种系统化疗后进展或复发的合并腹腔积液晚期卵巢癌为研究对象。结果显示,相较于单独使用顺铂腹腔灌注,联合使用甲磺酸阿帕替尼能有效提高腹水控制率(92.1% vs 60.5%,P<0.05)和疾病控制率(55.3% vs 21.1%,P<0.05);联合用药组患者中位OS(8.2月vs 4.2月)及中位PFS(5.1月 vs 2.4月)较对照组明显延长,差异具有统计学意义。
值得注意的是,两组研究对象均为老年患者,年龄大,体质差,因此除疗效外,安全性亦是本研究的关注焦点。结果表明:研究中的用药不良反应主要集中在血压升高、皮肤瘙痒、恶心、呕吐等方面,但反应程度较轻,经过对症支持处理后均能很好改善。观察组中,阿帕替尼使用剂量选择500mg/d,不良反应可控,可耐受,且相较于对照组,总体不良反应仅轻度增加,但不具有统计学差异。
综上所述,在合并腹腔积液的老年卵巢癌患者中,甲磺酸阿帕替尼联合顺铂腹腔灌注化疗显示出较为满意的临床疗效,且药物副反应可控,可耐受,对于老年卵巢癌患者是一项值得推荐的治疗方法。

