前列地尔联合常规治疗对2型糖尿病周围神经病变患者的临床疗效
莫巍,叶圣荣
(浙江台州市中西医结合医院,a 内科,b 中医科,317523)
糖尿病性周围神经病变(DPN)是指2型糖尿病(T2DM)发展到一定阶段导致的周围神经功能异常[1],发病率为60%~90%,多起病隐匿,发展至晚期时具有不可逆的特点,降低患者生活质量[2]。因此,早期有效治疗可改善预后情况,提高神经传导速度,具有重要意义。本研究观察前列地尔联合常规治疗对DPN疗效,分析其对DPN神经传导速度的影响,并从其对血清同型半胱氨酸(Hcy)及超氧化物歧化酶(SOD)、总抗氧化能力(T-AOC)的影响,分析其可能的作用机制。
1 对象与方法
1.1 研究对象 选取2014年10月至2017年10月我科收治的120例DPN患者,根据随机数字表,分为对照组和观察组。对照组男35例,女25例;年龄范围35~75岁,年龄(54.4±4.4)岁;治疗前T2DM病程范围5~15年,病程(10.3±2.8)年;治疗前DPN病程范围1~10年,病程(7.3±2.8)年,其中<5年者27例,≥5年者33例;体质指数(BMI)为(24.7±3.2)kg/m2。观察组男34例,女26例;年龄范围34~75岁,年龄(53.2±4.7)岁;治疗前T2DM病程范围5~15年,病程(10.5±2.6)年;治疗前DPN病程范围1~10年,病程(7.2±2.4)年,其中<5年者25例,≥5年者35例;BMI为(24.8±3.4)kg/m2。两组年龄、性别构成等一般资料比较,差异均无统计学意义(P>0.05)。本研究经我院伦理委员会批准。
1.2 标准
1.2.1 DPN诊断标准[3](1)符合T2DM诊断标准:空腹血糖(FPG)>7.8 mmol/L,餐后2 h血糖(OGTT)>11.1 mmol/L;(2)具有神经病变导致的麻木,感觉障碍等症状和体征;(3)肌电图检查提示神经损伤;(4)温觉、足底感觉等不同程度减弱,敏感性下降,反射消失,神经传导速度减慢。
1.2.2 纳入标准 (1)符合DPN诊断标准;(2)患者签订书面知情同意书。
1.2.3 排除标准 (1)其他类型糖尿病,糖尿病酮症、高渗状态者;(2)已合并严重并发症,如肝肾功能异常、心力衰竭、严重感染等;(3)腰椎病变及脉管炎等原因导致的周围神经病变;(4)过敏体质;既往精神性疾病史或认知障碍患者;(5)足背动脉搏动消失或明显减弱。
1.3 治疗方法 严格控制血糖水平,糖尿病饮食,给予患者糖尿病相关知识宣教;对照组给予500 μg/d甲钴胺肌内注射营养神经;观察组每天同时静脉滴注前列地尔注射液10 μg(北京泰德制药股份有限公司生产)+0.9%氯化钠注射溶液250 mL,治疗30 d。
1.4 疗效评定
1.4.1 疗效评估 (1)显效:症状消失,感觉功能恢复,肌反射正常,神经传导速度增加20%以上;(2)有效:症状好转,肌腱反射改善,神经传导速度增加,但没超过20%;(3)无效:症状及感觉功能无好转,腱反射仍消失,肌电图检查无变化。总有效率=(显效+有效)/每组总人数×100%。
1.4.2 神经电生理指标 检测正中神经与腓总神经的运动神经传导速度(MNCV) 和感觉神经传导速度(SNCV),最终得分为重复测量3次求平均值。
1.4.3 多伦多临床神经病变评分(TCSS)[4](1)神经症状:下肢麻木、疼痛、针刺样感觉、乏力、走路不稳及上肢相似症状,有计1 分,无计0 分,共6 分;(2)神经反射:踝反射及膝反射,双侧分别计分,消失计2 分,减弱计1分,正常计0 分,共8 分;(3)感觉功能:右侧拇趾的痛觉、温度觉、触压觉、振动觉及位置觉,异常计1 分,正常计0 分,共5分;总分为三部分的分数之和,共19分。
1.4.4 血清Hcy及T-AOC 清晨空腹采肘静脉血4 mL,离心。以ELISA法检测血清Hcy。采用黄嘌呤氧化酶法测定SOD,采用Fe3+/Fe2+还原法测定T-AOC。
1.4.5 安全性指标评价 采取多伦多保肢评分(TESS)不良反应量表,观测治疗前后患者血、尿、便常规、肝肾功能、心电图变化。

2 结果
2.1 治疗效果对比 观察组总有效率为85.0%(51/60),高于对照组为71.7%(43/60),P<0.05。见表1。
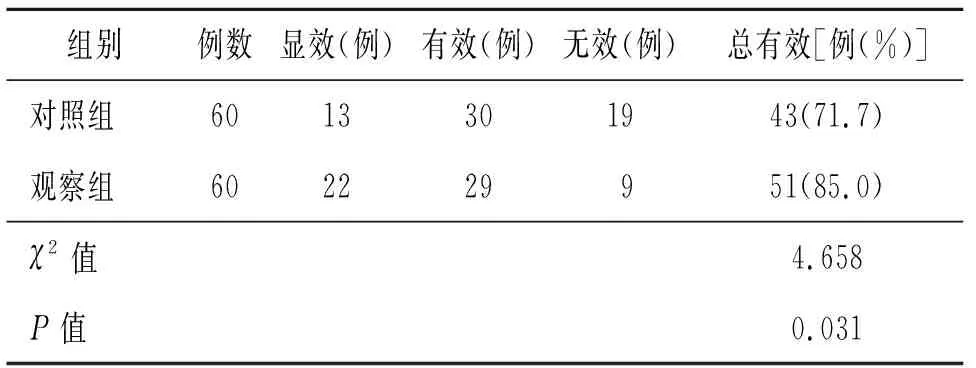
表1 两组治疗效果对比
2.2 神经电生理指标对比 治疗后,观察组正中神经和腓总神经的SNCV分别为(49.9±1.6)m/s和(40.8±2.6)m/s,正中神经和腓总神经的MNCV分别为(45.5±3.4)m/s和(40.3±2.4)m/s,高于治疗前水平和对照组相关指标水平(P<0.05)。见表2。
2.3 TCSS 评分和TESS评分比较 观察组TCSS评分(7.8±0.7)分,低于对照组(11.4±0.5)分,P<0.05;两组TESS评分差异无统计学意义(P>0.05)。见表3。
2.4 血清Hcy及抗氧化能力 治疗后,两组Hcy水平均降低,观察组Hcy(13.9±1.8)μmol/L,低于对照组,P<0.05;两组SOD和TAOC水平升高,观察组分别为(86.8±2.8)nu/mL和(14.5±2.4)u/mL,高于对照组,P<0.05。见表4。

表3 两组患者 TCSS评分和TESS评分比较分)
注:TCSS为多伦多临床神经病变评分;TESS为多伦多保肢评分
3 讨论
近30年我国糖尿病发病率呈逐年上升趋势,成年人患者每年新增近10%,其中2型糖尿病占90%。随着病程的延长,DPN成为常见并发症[5-8]。
前列地尔为血管活性药物,可增加细胞内环磷酸腺苷浓度,发挥扩血管作用,并可有效调节体内脂质代谢,抑制神经髓鞘异常脂肪合成,可阻断神经纤维脱髓鞘得进一步损伤[9]。该药物还可抑制血小板聚集,改善局部组织微循环,发挥促纤溶和溶栓作用,其本身对血管内微血栓具有清除功能,抑制氧化应激反应,缓解神经的缺氧、缺血的目的,从而促进损伤神经恢复。神经电生理学检查为评估DPN的金指标[10]。本研究结果显示,观察组总有效率高于对照组,观察组正中神经和腓总神经的SNCV和MNCV高于对照组,证实了前列地尔促进损伤神经恢复、提高神经传导功能的作用。近年来,有研究显示[11],TCSS 评分成为2型糖尿病周围神经病变简便、有效的筛查工具,即使无神经电生理检查条件,仍可单独作为治疗方案疗效评价的参考依据,本研究结果显示,观察组TCSS评分低于对照组,再次说明应用前列地尔可有效改善患者神经相关症状、神经反射功能及感觉功能。TESS评分两组差异无统计学意义,提示前列地尔具有可靠的安全性。
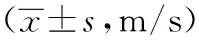
表2 两组神经电生理指标对比

表4 两组血清Hcy及抗氧化能力对比
为进一步研究其可能的作用机制,以Hcy、SOD、T-AOC为切入点,Hcy为维持体内氨基酸水平平衡的重要指标,为提示动脉粥样硬化的独立危险因子[12],胰岛素可影响氨基酸水平代谢,其抵抗可导致Hcy代谢障碍,从而导致糖尿病患者高Hcy血症,Hcy本身具有细胞毒作用,可刺激氧化应激反应,损伤血管内皮,损伤神经纤维,因此DPN患者体内Hcy水平高于无并发症的糖尿病患者,这已被临床研究证实。治疗后,两组Hcy水平均降低,观察组Hcy低于对照组,提示前列地尔可通过抑制Hcy水平发挥神经纤维保护作用。有学者研究显示[13-14],氧化与抗氧化能力之间的失衡是DPN发病机制之一,即前述提到的氧化应激反应环节,氧化应激能够影响线粒体内能量调节,而神经元缺少能量,最终导致神经元受损。SOD是自由基损伤和组织清除自由基作用的敏感指标,T-AOC是近年研究发现的用于衡量机体抗氧化系统功能状况的综合性指标,可反映机体自由基代谢的状态及机体防御体系的抗氧化能力的强弱。治疗后,两组SOD和T-AOC水平升高,观察组高于对照组,提示前列地尔具有抑制氧化应激反应作用,提高机体抗氧化能力,从而发挥促进神经功能恢复的作用。
综上所述,前列地尔联合常规可有效改善2型糖尿病患者周围神经病变程度,改善运动和感觉神经传导速度,提高TCSS 评分,可能与降低患者Hcy和提高机体抗氧化能力有关。

