超声造影在糖尿病肾病评估中的应用价值▲
吴 鹏 肖海燕* 张 璇 吴光秀 龙 艳 周 丽 罗润兰 文凤梅
(重庆市涪陵中心医院,1 超声科,2 内分泌科,3 科教科,重庆市 408010)
糖尿病是临床上一种较常见的内分泌疾病,因机体长期处于糖代谢紊乱状态,可造成肾小球肥大、肾脏微血管损伤,严重时可引发肾间质纤维化,进而导致糖尿病肾病(diabetic nephropathy,DN)的发生。由于DN起病隐匿,常不易被察觉,常规超声检查也无特异性表现,出现临床症状如持续蛋白尿、高血压等时,病情已发展到不可逆阶段[1]。近年来,超声造影(contrast-enhanced ultrasound,CEUS)技术发展迅速,因其可以实时显示脏器的微血管灌注情况,越来越多地被应用于肾脏疾病微循环改变的定量分析中。本研究利用CEUS技术对DN治疗过程中的肾皮质微血流灌注情况进行定量分析,探讨其临床应用价值。现将结果报告如下。
1 资料与方法
1.1 一般资料 选择2014年6月至2017年7月我院收治的2型糖尿病住院患者56例为观察对象,年龄32~60(53.4±3.8)岁。按照糖尿病肾病Mogensen分期法[2],其中26例为早期DN组(临床Ⅰ期、Ⅱ期),男19例,女7例,尿微量白蛋白排泄率<30 mg/24 h;30例为临床DN组(临床Ⅲ期、Ⅳ期),男18例,女12例,尿微量白蛋白排泄率30~300 mg/24 h。另选取我院年龄、性别相匹配的健康体检者30例为对照组。病例纳入标准:确切的糖尿病史,年龄18~60岁,符合世界卫生组织的糖尿病诊断标准。对照组纳入标准:既往体健,无糖尿病、肾脏疾病、高血压等病史。排除标准:合并严重的心、肝及造血系统疾病。
1.2 方法
1.2.1 治疗方法 早期DN组、临床DN组患者均给予前列地尔10 μg,加入100 mL生理盐水中静脉滴注,1次/d,14 d为1个疗程。用药期间避免同时使用抗凝药物、血管紧张素转换酶抑制剂类药物,以及抗血小板类药物等。
1.2.2 血生化及超声检查 (1)血生化检查:常规做血尿素氮(blood urea nitrogen,BUN)、血肌酐(serum creatinine,Cr)、白蛋白排泄率(UAE)等生化检查。(2)超声检查:采用东芝Aplio 500型彩色多普勒超声仪,随机配备编码谐波造影及时间-强度曲线(time intensity curve,TIC)分析软件,造影剂为Bracco公司的声诺维(Sono Vue)。取左侧卧位,二维超声观察右肾形态结构及实质回声表现,并排除肾脏发育异常、弥漫性肾实质病变及肾盂积水病变。然后采用彩色多普勒超声检查了解肾实质血供情况并测量肾段动脉、肾叶间动脉收缩期流速(peak systolic velocity,PSV)、舒张期流速(end-diastolic velocity,EDV)、阻力指数(resistance index,RI)等指标,排除副肾动脉伴行。(3)CEUS检查:在谐波造影模式下,取右肾最大冠状切面后保持探头固定,嘱受检者较长时间屏气,尽量减小呼吸运动导致的肾脏位移影响造影结果。注射造影剂前切换至CHI成像模式,机械指数设定为0.06,声诺维(Sono Vue)25 mg干粉溶解于5 mL生理盐水内,充分震荡后,经肘部浅静脉快速注入2.0 mL,随后推注5 mL生理盐水。注射造影剂后连续观察右肾3 min并存储RAW格式视频。第一次造影结束后,用前列地尔10 μg,加入100 mL生理盐水中静脉滴注1 h后,重复造影一次,造影剂剂量同前次。回放视频观察造影的全过程,设置取样部位于肾中段外侧皮质较厚部分,获取TIC曲线。根据TIC获取达峰时间(time to peak,TTP)、平均渡越时间(mean transit time,MTT)、峰值强度(derived peak intensity,DPI)、曲线下面积(area under the curve,AUC)。
1.3 观察指标 记录对照组及早期DN组、临床DN组治疗前后的以下指标:PSV、EDV、RI、AUC、DPI、TTP、MTT。
1.4 统计学分析 采用SPSS 17.0统计学软件进行数据分析,计量资料以均数±标准差(x±s)表示,多组数据间的比较采用方差分析,两组间比较采用独立样本t检验,同组间治疗前后采用配对t检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 血流动力学指标比较 治疗前,三组肾段动脉、叶间动脉的PSV、EDV及RI比较,差异均有统计意义(均P<0.05)。用药后,早期DN组、临床DN组肾段动脉、叶间动脉的PSV、EDV均明显增高,RI均明显降低,两组间比较,差异均有统计学意义(均P<0.05)。见表1。
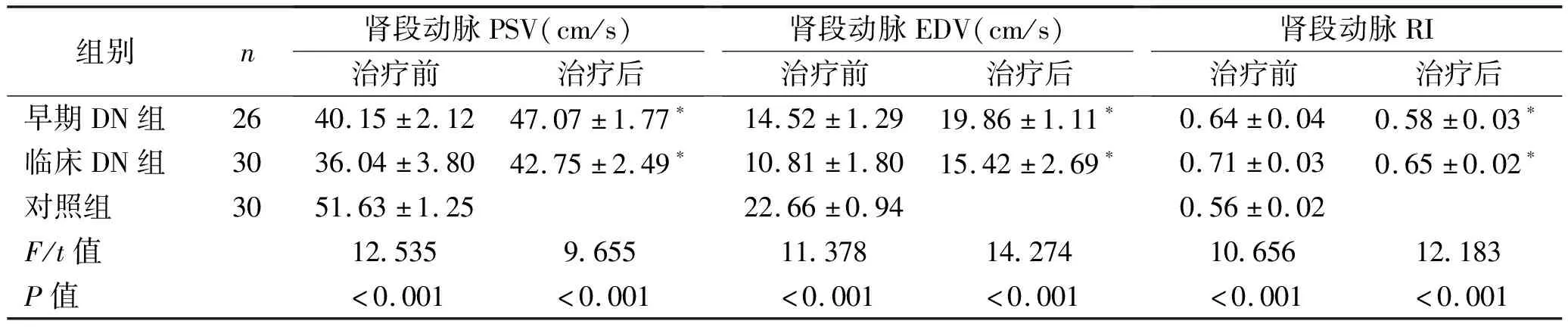
表1 各组患者动脉血流动力学指标比较 (x±s)
续表1
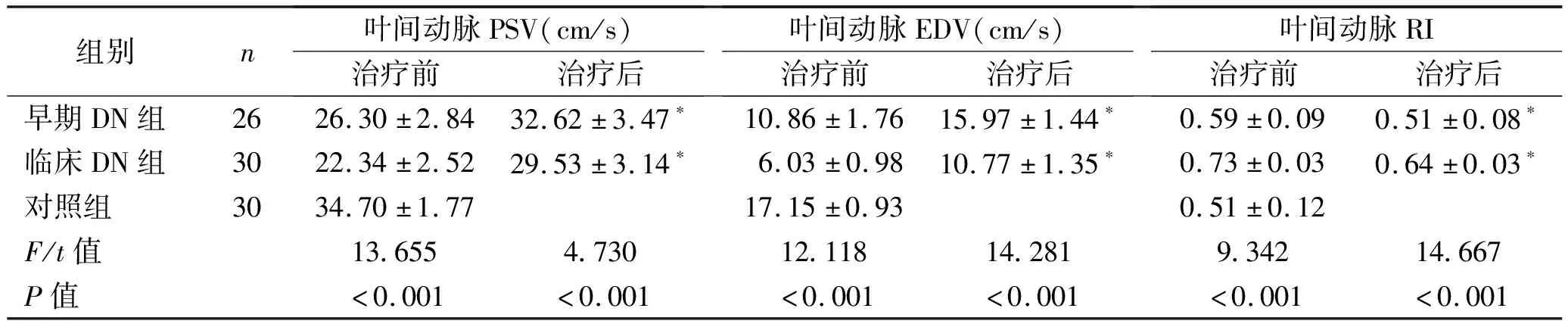
组别n叶间动脉PSV(cm/s)治疗前治疗后叶间动脉EDV(cm/s)治疗前治疗后叶间动脉RI治疗前治疗后早期DN组2626.30±2.8432.62±3.47∗10.86±1.7615.97±1.44∗0.59±0.090.51±0.08∗临床DN组3022.34±2.5229.53±3.14∗6.03±0.9810.77±1.35∗0.73±0.030.64±0.03∗对照组3034.70±1.7717.15±0.930.51±0.12F/t值13.6554.73012.11814.2819.34214.667P值<0.001<0.001<0.001<0.001<0.001<0.001
注:与同组治疗前比较,*P<0.05。
2.2 肾血流造影灌注参数比较 注入造影剂后,右肾肾动脉、肾皮质髓质依次显影,直至与肾皮质强度达到一致。对照组肾皮质TIC曲线为非对称性的单峰曲线,流入相上升支陡直,快速到达峰值强度,峰顶较圆钝,流出相迅速下降直至基础水平(图1)。治疗前早期DN组(图2)及临床DN组(图3)TIC曲线流入相上升支较对照组更加陡直,快速到达峰值强度,峰顶尖锐,流出相迅速下降,但廓清到基线水平较缓慢。治疗前,早期DN组、临床DN组及对照组三组间比较,DPI、TTP、MTT、AUC值差异均有统计学意义(均P<0.05)。治疗后,早期DN组(图4)及临床DN组(图5)DPI升高,TTP、MTT、AUC均降低,两组间比较,差异有统计学意义(均P<0.05)。见表2。

图1 对照组
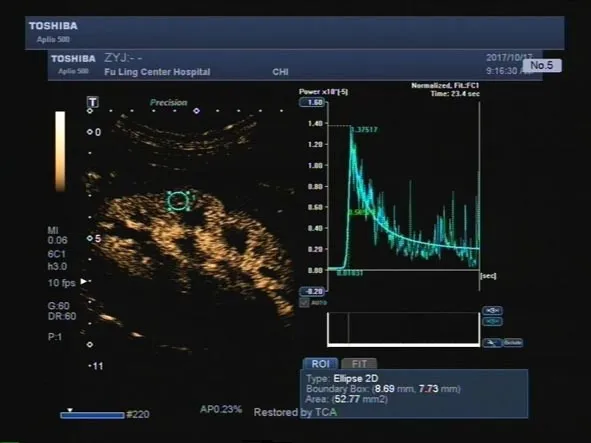
图2 早期DN组前列地尔治疗前
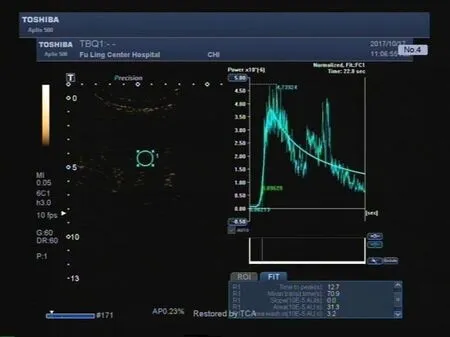
图3 临床DN组前列地尔治疗前

图4 早期DN组前列地尔治疗后
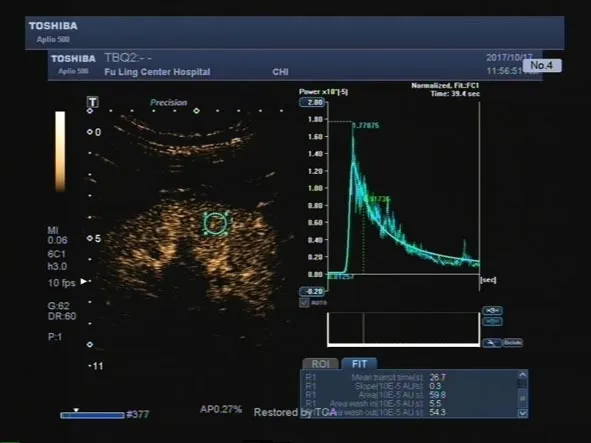
图5 临床DN组前列地尔治疗后

表2 各组患者超声造影不同指标比较 (x±s)
续表2

组别nMTT(s)治疗前治疗后AUC治疗前治疗后 早期DN组2636.87±3.5828.26±3.63∗2232.04±98.791988.16±64.35∗ 临床DN组3046.74±4.8432.59±5.02∗2597.02±64.312262.44±53.41∗ 对照组3026.3±4.021894.67±62.38 F/t值10.3513.54423.13417.219 P值<0.001<0.001<0.001<0.001
注:与同组治疗前比较,*P<0.05。
3 讨 论
近年来糖尿病患病率不断上升,DN的发病人数也逐年递增,占糖尿病患者的20%~40%,其中伴有终末期肾病的糖尿病患者5年生存率低于20%。糖尿病患者机体内长期处于高血糖状态导致肾毛细血管持续性扩张。早期改变为肾血流灌注量增加,肾小球滤过率显著增高,以及球内静水压增高。这种长期高滤过、高灌注、高内压状态进一步发展引起肾毛细血管通透性改变,肾小球毛细血管基底膜增厚和系膜扩张,毛细血管管腔逐渐狭窄,肾小球微血管硬化等病理改变,肾微细血管血流动力学参数也发生相应变化。超声造影剂声诺维(Sono Vue)为脂质包裹的六氟化硫(SF6)气体,其平均直径仅为2.5 μm,作为一种血流示踪剂可以随血液循环分布到全身脏器,由肾动脉进入肾实质毛细血管床后经肾静脉排出,不经肾小球-肾小管通路排泄到肾盏内[2]。研究证实CEUS信号强度与造影剂微气泡浓度有相关性,而组织内造影剂微气泡的浓度能够反应组织血流灌注的水平[3]。因此近几年逐渐有学者开展对慢性肾病的肾脏造影研究。本研究中,早期DN组肾脏肾段动脉、肾叶间动脉的PSV和EDV均低于对照组,而反映肾血管弹性及灌注阻力的RI增高则提示肾小球内压增高,肾内血管床阻力升高,肾内微循环受损,肾脏出现了损伤性改变[4-6],CEUS表现为对照组肾皮质TIC曲线呈非对称性的单峰曲线,流入相上升支陡直,快速到达峰值强度,峰顶较圆钝,流出相缓慢下降(图1)。而早期DN组TIC曲线流入相上升支较对照组更加陡直,快速到达峰值强度,峰顶尖锐,流出相迅速下降(图2)。造影参数中早期DN组DPI增加,而TTP、MTT及AUC逐渐降低,说明肾病早期虽然肾小球滤过膜屏障还未受损,但肾内小血管阻力已有所增高,导致造影剂微泡灌注时间延长,灌注速率及清除速率下降,肾脏毛细血管内造影剂微泡与血液淤积,说明超声造影参数能够反映早期肾功能的改变。而临床DN的主要病理特征是肾纤维化、肾脏高灌注状态恶化、肾脏供血显著减少、肾小球毛细血管基底膜不断增厚、肾小球硬化、肾动脉及分支动脉血管发生粥样硬化,继发血栓形成,导致动脉管腔狭窄或完全阻塞[7]。临床DN组肾段动脉、肾叶间动脉PSV及EDV则进一步降低,而RI进一步升高。CEUS后TIC曲线表现出流入相上升支较早期DN组更加陡直,DPI较早期DN组进一步降低,而TTP、MTT及AUC继续增加,流入相造影剂廓清阶段不能迅速降至基础水平(图3),二者有较显著差异。这与董怡等[8]研究结果相似,说明随着肾小球动脉的硬化狭窄,进入肾脏微循环造影剂微泡量减少,造影剂灌注速率明显减慢,相应单位时间内肾实质局部血流量也同步下降。
由于目前临床治疗中尚无特效的方法防止DN的发生与恶化[9],因此强调DN需要早期防治。有研究[10]表明早期多疗程应用前列地尔可有效减少DN早期和临床肾功能代偿期患者尿蛋白的排泄率,从而改善肾功能,降低肾脏病变进展速度。前列地尔注射液的有效成分为前列腺素E1,其为脂微球包裹药物,具有靶向作用,能把药物输送到受损血管,从而在病灶部位发挥扩张血管、抑制血小板聚集的作用,增加肾血流量,降低肾血管阻力,调节肾小球入球和出球小动脉,降低肾小球毛细血管压力[11-13],改善残存肾单位的高灌注和高滤过状态。本研究在使用前列地尔短期治疗早期DN与临床期DN组患者后,再次分析其造影后TIC曲线参数的改变,结合肾段动脉、肾叶间动脉血流速、RI值等指标了解不同肾病阶段的肾血管灌注对于药物治疗的改善差异性。治疗后,早期DN组与临床DN组的肾段动脉、叶间动脉PSV及EDV均明显升高,且肾段动脉PSV及EDV上升幅度最大,而RI降低更明显(均P<0.05)。CEUS后TIC曲线,早期DN 组(图4)与临床DN组(图5)DPI均有升高,早期DN组升高较明显。TTP、MTT及AUC的数值均有不同程度降低,且早期DN组下降幅度大于临床DN组(均P<0.05)。早期DN组流出相造影剂廓清阶段下降更接近基础水平,更接近于对照组,说明前列腺素E1能够降低患者肾小球毛细血管压力以及肾血管阻力,增加肾小球血流量,除了能有效降低尿素氮、肌酐以及尿白蛋白排泄率,改善肾功能,还可改善其血流动力学[14]。造影结果显示肾脏作为前列腺素E1的靶器官之一,早期DN组的治疗效果优于临床DN组,与二者在肾小球微循环损伤的差异程度密切相关。
综上所述,CEUS技术作为一种成熟的血流灌注显像技术,不仅可以较灵敏地反映DN患者肾脏微血管损伤所造成的局部血流动力学改变,而且结合造影曲线多参数分析,可以评估前列地尔对不同阶段肾病的治疗效果,具有操作方便、无副作用、敏感度高、可重复检查等优点,临床推广应用价值高。

