椎体切除术联合同种异体骨环治疗骨质疏松性压缩骨折伴后凸畸形
王颖博,刘 鹏,赵建华,胡 波
随着进入老龄化社会,骨质疏松症的发病率逐年增高[1],骨质疏松性椎体压缩性骨折(osteoporotic vertebral compression fracture,OVCF)是骨质疏松症的严重阶段[2-3],可引起多种并发症。多数患者经过严格的非手术治疗或给予椎体强化手术包括椎体成形术(PVP)和椎体后凸成形术(PKP)等[5-6],可明显降低骨折带来的疼痛。但部分患者早期未严格卧床及治疗,导致椎体压缩进行性加重并出现明显的后凸畸形,造成脊柱矢状位失平衡或局部不稳定,除引起明显的腰背部疼痛外还会出现脊髓受压等损伤,导致患者生活质量明显下降[4]。严重的压缩骨折往往呈亚急性,椎体体积严重丧失,难以行椎体成形术恢复椎体高度及纠正后凸畸形。OVCF患者大多高龄,骨质疏松症使得骨的质量明显下降,内固定手术失败的风险明显增加,这类患者的手术治疗较为困难。回顾性分析笔者科室实施的29例经后路椎体切除、同种异体骨环支撑、植骨融合内固定手术,取得较好的临床效果。
临床资料
1 一般资料
2013年6月—2017年6月笔者科室收治29例骨质疏松性压缩骨折伴后凸畸形患者,其中男性3例,女性26例;年龄56~70岁,平均62.1岁。术后患者均给予钙剂、维生素D及双磷酸盐抗骨质疏松治疗。所有患者均存在低能量损伤(3例男性患者为滑倒摔伤,26例女性中有16例为滑倒摔伤,6例为负重后出现疼痛,2例为弯腰后出现疼痛,2例为打喷嚏后出现疼痛),创伤时间≥4周,椎体压缩>80%,9例患者合并后方韧带复合体损伤。入院后所有患者行脊柱正侧位X线、64排CT、全脊柱去脂像MRI检查及双能X线骨密度检查。
纳入标准:(1)骨密度T值<-2.5SD;(2)均有低能量损伤的病史;(3)全脊柱去脂像MRI检查提示骨折为亚急性骨折;(4)CT检查提示椎体明显压缩≥80%,压缩椎体骨密度增高,可见明显后凸畸形。排除标准:(1)极重度骨质疏松;(2)年龄>70岁;(3)合并严重基础疾病,包括心肌梗死、脑出血急性期、严重肝肾功能障碍、未控制的糖尿病等。
2 手术方法
手术均由同一组手术经验丰富的医师操作完成。患者全身麻醉后取俯卧位,胸腹部垫软垫防止胸腹部受压,术前C臂机透视确定骨折节段,以骨折椎体为中心行背部正中纵切口,范围包括骨折的上、下各1~2个椎体节段,固定节段根据患者年龄,骨质情况、病椎节段有所区别。骨膜下剥离两侧肌肉,显露脊柱两侧椎板及关节突关节,在骨折椎体上下各1~2个椎体植入椎弓根螺钉,骨质过于疏松者给与骨水泥强化椎弓根螺钉。切除骨折椎体的棘突、椎板及关节突。一侧安装临时固定棒,双极电凝进行椎管内静脉丛止血,切除上位椎体的下关节突和下位椎体的上关节突,咬除伤椎的横突和椎弓根,注意保护脊髓及神经根。将骨折椎的上下椎间盘切除,刮除终板上的软骨,保留骨性终板,应用髓核钳清除脊髓腹侧的骨块,使用超声骨刀及髓核钳对骨折椎体行次全切除,选择合适的同种异体骨环[本组病例均选择同种异体腓骨环,均由北京大清生物技术有限公司提供,产品注册证号:国食药器械(准)字2011第3460627号],以切除的自体骨松质骨碎屑充填后,将骨环放置椎体前中柱,透视证实骨折椎体部位脊柱高度恢复,骨环位置满意后,适当进行椎体间加压,使骨环被牢固镶嵌于上下椎体之间,将连接棒锁紧,安装横连杆;然后行骨环外侧及椎体间植骨,放置引流管,逐层缝合伤口。术后处理:每日记录切口引流量,引流管拔除标准为连续2d 24h引流量<50mL,下肢功能允许者术后3~5d佩戴硬质支具下地,支具佩戴3个月,下肢功能较差者可同期佩戴支具练习床上坐起。
3 观察指标
观察手术时间、出血量、Cobb角、腰椎前凸角的变化及手术前后疼痛VAS评分。术前、术后1周、术后3个月、1年行脊柱X线片同种异体骨环植入的并发症、骨环塌陷情况、植骨融合情况及内植物稳定情况进行随访。
4 统计学分析
结 果
手术时间180~320min,平均155.3min;失血量330~1 100mL,平均660.7mL。其中5例患者因骨质过于疏松,给予骨水泥强化椎弓根螺钉。1例术后切口延迟愈合,1例出现L4神经根牵拉症状导致股四头肌肌力下降,其余病例术后未出现切口感染、医源性脊髓及神经根损伤。术后随访12~36个月,未见内固定松动及断裂,未见同种异体骨环塌陷,末次随访后凸角度平均(11.1±5.8)°,腰椎前凸角平均(23.5±9.6)°(表1)。术前腰痛VAS 评分平均(7.2±1.1)分,术后腰痛VAS 评分平均(2.4±1.6)分,相比术前明显改善,差异有统计学意义(P<0.05)。典型病例见图1。
表1 患者术前、末次随访时后凸角、腰椎前凸角及VAS 评分改善情况
与术前相比:*P<0.05
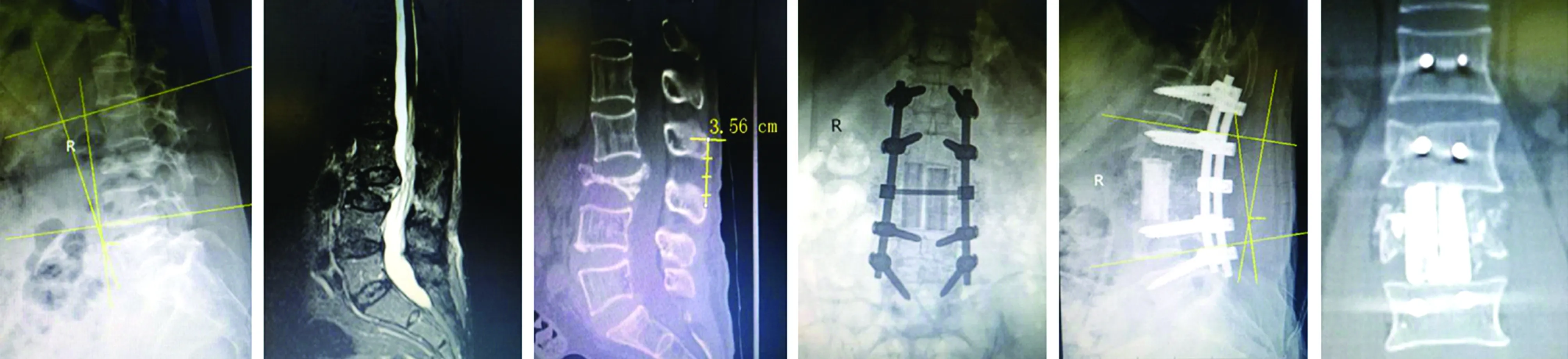
a b c d e f
讨 论
1 骨质疏松压缩骨折的手术方式选择
脊柱是骨质疏松性骨折中最为常见的部位,胸腰椎最为多见。与暴力外伤导致的脊柱压缩骨折相比,OVCF具有以下特点[7-8]:(1)患者卧床制动后,将发生快速骨丢失,会加重骨质疏松症;(2)椎体持续压缩加重,导致后凸畸形及脊柱失衡;(3)骨折愈合过程缓慢,易发生骨折延迟愈合甚至不愈合;(4)内固定治疗稳定性差,内固定物及植入物易松动、脱出,植骨易被吸收;(5)多见于老年患者,全身状况欠佳,卧床可导致多种并发症。因此,笔者认为除了症状和体征较轻,影像学检查显示为轻度椎体压缩骨折,或存在绝对手术禁忌者,在正规抗骨质疏松的基础上应积极手术治疗,促使患者尽早下床,预防卧床相关并发症的发生。PVP和PKP是目前最常用的微创手术治疗方法[6-9],在改善新鲜椎体骨折引起的疼痛和预防后凸畸形方面有很好的临床疗效。应用PKP技术在椎体骨折不愈合或椎体内部囊性变、椎体坏死裂隙内填充PMMA以实现稳定椎体的目的,一定程度上缓解了此类脊柱不稳的腰背痛[10]。但对于本组病例,患者骨折时间>4周,为亚急性骨折,骨折椎体骨密度明显增高,椎体压缩超过80%,骨水泥无法良好弥散,PKP手术无法恢复前方椎体高度及矫正畸形,难以解决后凸引起的邻近节段不稳定,也难以恢复脊柱序列重建矢状位平衡。因此对于此类严重椎体压缩合并脊柱后凸畸形及不稳的OVCF应采取椎体切除或截骨矫形及内固定手术治疗,纠正后凸畸形,恢复脊柱生理序列,同时前方给予良好的支撑。
2 后凸矫形方式的选择及注意事项
脊柱后凸矫形手术有很多不同的术式,可经前路或后路行各种截骨矫形手术,随着脊柱后路手术技术的发展及椎弓根螺钉在脊柱外科的广泛应用,经后路行矫形手术逐渐为脊柱外科医生所接受。Suk等[11]采用后路截骨矫形术治疗15例OVCF患者,获得了较好的疗效。OVCF多发生于老年人,其继发形成后凸畸形的程度与椎体压缩的程度相关。本组病例骨折压缩程度较重,均超过80%,难以通过椎间隙或椎弓根进行楔形截骨,需切除压缩椎体获得后凸矫形。所有患者均采用VCR术式治疗,该术式便于将压缩椎体完整切除,在撑开力作用下放入同种异体骨环或钛网重建前柱,增加前柱高度,获得较好的矫形效果。OVCF患者由于合并严重的骨质疏松,存在较高的内固定失败风险,因此置钉过程应尽量保证一次性成功,避免反复置钉破坏椎体内松质骨而降低螺钉把持力。为了降低椎体疏松骨质对内固定物的影响,部分学者采用骨水泥注入椎体增加螺钉把持力。Heini[12]总结了21例OVCF 合并后凸畸形的病例,应用PMMA与内固定螺钉相结合增加螺钉的把持力,降低因椎体骨质疏松带来的拔钉风险。本组患者中有5例患者因骨质过于疏松,给予骨水泥强化椎弓根螺钉。术中预弯钛棒一定要符合整体脊柱的生理曲度,不可过度依靠撑开及加压来维持后凸矫形效果,应结合手术床体位复位,以免出现椎弓根螺钉对疏松骨质的切割。
3 同种异体骨环的特点
钛网作为一种较为成熟的前路支撑材料已广泛应用于胸腰椎爆裂性骨折或肿瘤的手术治疗[13-14],钛网的优点包括取材方便、灵活适应椎体切除后所需的植骨支撑长度、其上下齿状设计增加其把持力及抗剪切力作用。但钛网仍存在相应的缺点,其上下齿状设计虽然增加其把持力,但由于单位面积压强较大,常出现下沉及塌陷的情况。在OVCF中尤为明显。自体骨难以寻找大段的骨支撑来源,且增加额外的创伤。同种异体骨环作为一种新的修复材料,目前正逐渐应用于脊柱创伤及畸形的修复中[15]。同种异体骨环是由骨内蛋白多且脂肪含量低的皮质骨制成,经过后期冰冻等处理后既保证了其无菌性,又降低了植入组织的抗原性。在植入后与自体组织的融合过程中骨痂会逐渐对骨环形成包裹,进而减少了排斥反应的发生。且皮质骨的生物力学强度高,能够满足支撑和传导力的功能,达到了金属支架的支撑效果,同种异体骨环的环形压强分布均匀,后期塌陷率低。
综上所述,椎体切除术联合同种异体骨环支撑,可恢复脊柱生理序列,获得前方良好的支撑,能在内固定下获得满意的稳定性,获得更好的生物相容性,值得在临床中推广及应用。
- 创伤外科杂志的其它文章
- 保留旋前方肌多轴锁定钢板治疗C1、C2型桡骨远端骨折Treatment of C1-type and C2-type fractures of the distal radius by open reduction and numelock II polyaxial system fixation with pronator quadratus reserved
- 解剖型锁定钢板对粉碎性Pilon骨折疗效的影响Effect of anatomic locking plate on the curative effect of comminuted Pilon fracture
- 胸腔镜辅助镍钛记忆合金肋骨接骨板内固定术治疗多发肋骨骨折临床疗效研究
- 股骨头骨折合并同侧髋臼骨折的手术疗效分析
- 玉米剥皮机致手部复杂损伤的临床治疗分析
- 内外侧联合入路合并早期支具固定治疗复杂肘关节脱位的临床疗效

