美国猪伪狂犬病监测程序手册(1.3版)—样本运送、提交程序及附件
文│美国农业部动植物卫生检验局兽医处
译校│张淼洁 付雯 翟新验(中国动物疫病预防控制中心)
一、样本的运送
关于动物卫生官员收集的样本,应采用以下程序将样本提交至NAHLN或USDA实验室。
1.包装。将贴有标签的样本管/容器放入透明的带有吸收剂的生物学危害品袋(STP—741)中,并密封;将该生物学危害品放入生物学危害品袋(STP—740)中,并密封;将白色袋子放入运送箱中;在袋子上放置冷冻冰块;将填写好的美国农业部农场现场猪监测提交表(若有)放置在泡沫箱盖子上;密封箱子;将运送地址标签贴在箱子上,送至对该收集样本进行PRV(猪伪狂犬病病毒)检测的指定实验室;将其他需要的运送标签贴在箱子上,满足当前的IATA运送要求(比如,UN 3373标签等);由合同承运服务商隔夜送达;若在周五运送,确保在箱子上贴上周六送达的标志。确保实验室可在周六接收并冷冻运送到的物品。(注:运送监测样本至实验室的个人需要满足生物物质运送的要求。上述个人至少应熟悉IATA包装须知。)
2.运送至指定的NAHLN实验室。只能通过承包的隔夜送达服务将样本送至NAHLN实验室。附件A包括指定的PRV NAHLN实验室的名单。
二、提交样本至NAHLN实验室
VS人员可联系VS地区办公室获得一次性的血液采集用品。在可能的情况下,血液样本应用离心机分离出血清。然后将血清存放在离心管中,同提交表格一起送至NAHLN实验室或USDA实验室。提交至NAHLN实验室的所有血液/血清管都必须拥有独立的条形码。可联系NVSL的运送部门获取条形码。
血液收集和血清提交推荐的物品/设备:冷却器;冰袋;血液收集时可选择的针;10~15毫升的注射器(顶部带有卢尔锁);10毫升的真空容器;猪监测样本条形码标签,WS—联系布兰顿·斯密特获取条形码 ,VS—联系NVSL获取条形码;装血清的离心管或冷冻管;离心管运送容器;封口冷冻袋,用作主要和次要的运送容器;纸巾,用作主次运送容器之间的吸收性材料;用离心机分离血清;GPS装置用于记录样本收集的位置;猪保定装置;提交表格(见附件D)。
在可能的情况下,每个进行PRV检测的动物至少提供2毫升的清澈、非溶血血清。
三、诊断专家的酌情判断
执业兽医提交至NAHLN实验室进行PRV血清或抗原检测(监测流程2和3)的样本必须满足最低的信息要求。没有监测所需的最低信息的样本不适合进行USDA国家PRV监测计划下的PRV检测,且不得使用USDA支持的资金进行PRV分析。此外,诊断专家需要遵守本文件中列出的采样标准。
关于样本可追踪性的最低信息要求为:提交样本的执业兽医的信息,包含姓名 、城市 、州 、邮政编码;动物识别号;样本提交日期;生产地信息应明确为进行采样而取样的猪的实际位置;经营场所的ID或经营场所的名称,必须包括街道、城市、州、邮政编码。
检测的样本应能够在空间和时间上代表所有提交的样本。每次提交样本中最多检测五个样本。在执业兽医提交至实验室的每份合格样本上粘贴NVSL提供的独立条形码。
诊断专家若有关于样本检测和所需信息的问题,应联系USDA VS NAHLN的协调员。
附件A:指定的NAHLN PRV检测实验室的地址和联系信息(略)
附件B:州、机构及屠宰场进行的PRV监测活动
在屠宰场收集母猪—公猪市场屠宰样本(监测流程6)。屠宰样本的检测将在KS和KY的两个联邦PRV实验室进行。各州应提交所有必要的监测或检测样本至USDA堪萨斯和肯塔基地区检测实验室,以满足最低常规监测要求(5%)。
收集用于监测或回溯调查的血清样本(除屠宰以外)的监管官员应将贴有正确的标签和条形码的样本送至PRV NAHLN实验室。各州应在提交样本前联系NAHLN实验室,确定其能在不超过指定样本检测配额的情况下处理样本,或各州可联系其地区传染病学家决定将样本送至何处(即哪个NAHLN实验室)。
为监测流程3“提交至诊断实验室的猪病例的血清检测”而选择的样本应在时间和空间上能够代表提交至NAHLN实验室的所有样本。每批提交的样本中最多检测5个样本。实验室将在每个样本上使用USDA提供的独立条形码。
各州列出的预期检测的样本目标(略)。
1.野生动物处的野猪PRV监测。WS国家野生动物疾病计划将在VS官员的帮助下确定PRV采样的地区。WS负责确定样本量并根据已知的各州野猪分布情况分配样本量。通过WS和VS的联合决定,WS生物学家为PRV监测而收集的样本将按照WS指导提交至NAHLN实验室。只有WS提交的样本适合使用本计划中的USDA资金。
2.PRV高风险猪群的监测。AVIC和州兽医应根据高风险猪群的血清检测流程(监测流程4)列出的标准确定高风险猪群。AVIC/州兽医应同其地区的传染病学家合作,从高风险中获取样本,确定采集样本的数量确定最实用的方法。为了帮助各州确定高风险农场的所在地,国家监测为上述高风险的州提供指南。本表(略)列出有文件记录的野猪的县,这些县也报告了饲养了超过1000个猪群及其种猪的密度,可在同地区传染病学家的咨询下用作各州的抽样指南。该表不是绝对的,各州参考或者不参考该表,确定高风险猪所在地区名单。此外,各州可将其他地区和猪群视为“高风险”。监测的目标是快速确定商业猪群中的PRV感染。重点在于检测接触野猪的高风险的商业猪群。此类猪群可能在NSU提供的地区内。由当地VS和地区官员确定高风险猪群。只有被定义为“高风险”的猪群才能够使用联邦资金支持的高风险猪群检测流程(监测流程4)。
表1

表2
表3
附件C:AVIC和州兽医办公室名录
可通过查阅以下网站找到目前的AVIC办公室和详细的AVIC信息:州动物卫生办公室可通过查阅以下网站找到目前的州动物卫生办公室和官员的名单:http://www.nasda.org/cms/7195/8617.aspx
附件D:美国农业部伪狂犬病监测数据表
数据表1,表2是USDA APHIS WS人员使用的例子。只有被授权的人员才能填写该表格,填写需符合WS国家野生动物疾病计划要求。以下并非完整的表格,删除了一部分说明。
执行监测或传染病追踪活动的USDA VS或州人员使用的数据表必须包括在样本内,并送至合适的PRV NAHLN实验室获得检测资格。
提交的所有样本都必须有独立的条形码。表3、4、5并非完整表格,有部分说明被删除。
附件E:NAHLN实验室PRV血液/血清检测程序
提示,屠宰监测和移动资格,包括展览(出口/跨州移动)的样本不适用于此检测程序。
在对样本进行PRV检测之前,选择猪血液/血清用于PRV检测的NAHLN实验室需要确保:已提供所需的流行病学回溯信息;有足够的血清量;以及血清质量好,无细菌污染或过多的溶血。
若样本有必要的回溯信息,则应分析样本以确保其符合定量和定性要求。由于样本由执业兽医提交至实验室进行其他检测,因此只有在有足够的血清能进行所有必要的检测时才进行检测。若样本有足够的血清进行多项检测(包括PRV),请考虑,如果PRV抗体为疑似/阳性的情况下,必须将样本转发至NVSL进行确认检测。因此,每份样本应至少含有2毫升的优质血清。
实验室若为了除USDA监测计划以外的目的而对样本进行检测,则应按照CFR的要求,遵照生产商推荐的测试/复检程序,并将所有阳性样本送至NVSL进行确认。
为USDA监测目的而进行血清筛查的实验室需要按照以下要求处理所有PRV监测血液/血清样本。
1.查看文件和信息以获取正确的回溯信息,至少应包括猪所在实际位置(非公司所在地)的邮政编码或经营场所标识。
2.观察样本是否具备足够的血清量和质量。
3.若样本适合进行检测,则在样本上粘贴USDA提供的条形码。检测样本:筛查检测PRV gB ELISA,或者自动乳胶凝集试验(ALA)(实验室可选择以上方法之一进行初次样本筛查,但应保持一种检测方法)。
若筛查检测结果为疑似【在PRV监测中,疑似定义在初次检测中及按照生产商建议的程序进行复测后既非阳性也非阴性(重新测试)的样本】或阳性,则应在1个工作日内使用PRV g1 ELISA方法重新检测样本。
若g1结果为疑似或阳性,将已有检测结果的所有相关信息连同样品一起提交至NVSL进行确认检测。如果使用的是gB筛选检测,由于临界值会随着方法而变化,则提交的信息中应包括使用的是哪种检测方法。样本应隔夜运送到NVSL。
运送样本之前需打电话通报NVSL代表。在处理样本后,实验室将在PRV实验室数据表上记录所有信息。
样本保存标准:若样本在初次筛查中为阴性,可根据实验室规程废弃该样本;若样本在初次筛查中为阳性,在二次筛查中为阴性,根据实验室规程废弃该样本;若样本在初次和二次筛查中均为阳性,应将样本送至NVSL进行再次检测,并应将样本及同批所有其他样本至少保留十五天。

表4

表5
USDA监测计划中的PRV血液/血清检测程序见图1。
注:从USDA WS提交至实验室的USDA PRV野猪监测样本只能进行筛查检测(PRV gB ELISA或自动乳胶凝集)。所有筛查检测结果,包括疑似、阳性和阴性结果,应报告至USDA WS,国家野生动物疫病计划。测试野猪血清不需要g1 ELISA。此外,野猪的阳性样本无须提交至NVSL进行确认检测,除非因其他监管目的需要进行检测。
附件F:血清检测的95/10采样程序
该采样程序将用于所有进行PRV检测的猪群,包括因回溯而检测的猪群。95/10采样程序有95%的概率从流行率至少为10%的猪群中发现一个阳性动物。 每个独立的猪群(不同地点,同一所有者)应作为单独的猪群进行检测。以下为满足95/10程序需要进行检测的动物数量:数量低于100头的猪群检测25头;数量在100~200头的猪群检测27头;数量在201~999头的猪群检测28头;数量在1000头以上的猪群检测29头。
附件G:PRV通报和响应行动
本附件规定了出现阳性或疑似PRV的实验室结果而产生的通报和响应行动。本文件并不取代任何兽医处备忘录或通报。NAHLN实验室或NVSL公司报告的疑似或阳性结果将启动通报和响应行动。NVSL确认的PRV阳性结果预示着全面响应。
1.响应行动。PRV监测计划中检测的样本将由经过培训的人员在指定的NAHLN实验室进行初步筛查。上述人员必须按照指定的程序筛选血清、肌红蛋白和组织以进行PRV监测。若筛查结果为疑似或阳性,则将由爱荷华州艾姆斯市的NVSL进行确认检测。
若野猪血清在NAHLN实验室检测为阳性或不确定性,应将结果报告至WS。WS将通过涉及其野生动物疾病生物学家的认证沟通程序向VS发布实验室结果。上述样本无须递送至NVSL,除非因其他监管或研究目的需要。野猪样本出现PRV阳性不会启动下述行动,根据当地监管机构和特定州的野猪群体状况,州机构和WS可能对野猪的PRV调查结果采取不同的对策。
提交至NAHLN检测实验室的血清(包括肌红蛋白样本)或组织的疑似或阳性结果,不包括常规的野猪样本,若NAHLN实验室认定疑似或阳性结果,则将采取以下行动。
A NAHLN实验室的行动。第一,立即通过电话或传真将结果汇报至爱荷华州艾姆斯市的NVSL,按照附件E提交所有样本至爱荷华州艾姆斯市的NVSL进行确认检测。不得分离样本。样本包括所有必要的文件和此前检测的结果;第二,在数据表或电子数据表中输入结果和所需数据。
B NVSL的行动。第一,从NAHLN实验室接收的样本进行确认检测;第二,若结果为阴性,将检测结果告知提交样本的实验室;第三,若结果为阳性,将检测结果告知提交样本的实验室、实验室所在州的AVIC、动物来源州的AVIC以及地区传染病学家和猪卫生计划员工。
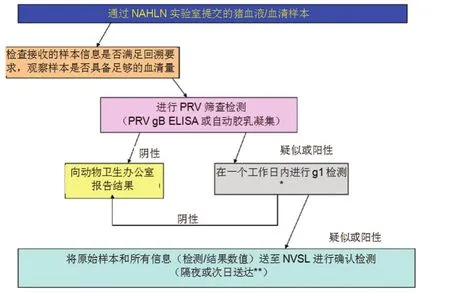
◎图1 PRV血液/血清检测程序
C NAHLN实验室所在州、样本采集州以及猪来源州VS、SAHO的行动,仅在NVSL确定样本为阳性时进行此类行动。第一,确保提交样本相关的所有文件和任何鉴定材料安全。第二,确定提交样本的来源。第三,确定涉及动物的最后一处已知的居住场所。第四,若样本采集自屠宰场,则收集最初的回溯信息。第五,同地区办公室的人员沟通调查结果。第六,遵照“伪狂犬病根除的州—联邦—产业计划标准”中的规定。
D 当确定样本为阳性时猪群卫生项目员工采取的行动。第一,告知NCAHEM员工;第二,若有必要,协助地区官员获取所需的信息;第三,检查从地区接收的信息。
E 通报。外部到VS:AVIC确保告知州兽医;在合适的情况下,员工或地区官员将通报立法和公共事务部(LPA)去告知产业和公众。
注意:如果本节的部分内容不适用或需要修改,则将进行适用的修订。应通过电子邮件同猪卫生计划相关部门沟通。
2.NAHLN检测的疑似或阳性结果在NVSL检测为阴性。若NAHLN实验室报告并提交了疑似或阳性结果,NVSL的检测显示为阴性,则需要将阴性结果通报到以前得到NAHLN疑似或阳性结果通报的各方。无需要开展进一步的调查行动。
3.NVSL阳性结果的确认。若NVSL确认阳性结果,将执行本部分C到E中概述的程序。控制和清除感染猪群的PRV的相应行动将尽快开始。需立即通报到NAHLN实验所在州和动物所在州的州动物卫生官员。此外,动物卫生官员应开始执行所有必要的措施,如确定疾病的来源,收集所有追溯信息,并启动检疫以防止疾病蔓延。动物卫生官员将遵循“伪狂犬病根除州—联邦—产业计划标准”中概述的疾病控制和清除方法。
响应和沟通行动的流程见图2。
附件H:国家伪狂犬病监测计划
可在网上查阅国家伪狂犬病监测计划。网址为:h t t p://www.aphis.usda.gov/vs/nahss/swine/prv/prv_surveillance_plan_final_draft_04_16_08.pdf

◎图2 响应和沟通行动流程图

