经导管二尖瓣置换术的研究进展及展望*
李 昕 综述 宋 兵 审校
(兰州大学第一临床医学院,兰州 730000)
在发达国家,二尖瓣关闭不全(mitral valve regurgitation, MR)是最常见的心脏瓣膜病。在75岁以上老人中,二尖瓣关闭不全发生率超过10%[1]。尽管瓣膜置换术被认为是治疗MR的金标准,但是至少一半的高龄重度MR患者无法耐受手术治疗[2],这些病人5年生存率约为50%[3]。因此,对于有症状且无法耐受手术治疗的严重MR病人,经导管治疗成为拥有巨大潜力的新方法。基于经导管主动脉瓣置换术(transcatheter aortic valve implantation, TAVI)的巨大成功,2012年6月丹麦哥本哈根Rigshospitalalet大学附属医院完成世界首例人体经导管二尖瓣置换术(transcatheter mitral valve replacement, TMVR)后[4],TMVR正以前所未有的速度发展。几个经导管二尖瓣置换装置已经在欧洲上市,并且在降低二尖瓣返流和减轻症状方面取得优异成绩。然而,这些装置并不是适用于全部病人,在技术上还有很大的挑战和发展空间。
1 当前研究人群
当前,TMVR仍然处于临床试验阶段,并未获得临床准入,主要治疗无法耐受手术的晚期高龄二尖瓣病变患者,部分文献定义为[5,6]:①中、重度瓣膜关闭不全及不适合行球囊成形术的严重狭窄和瓣膜钙化患者;②心脏手术风险评分高,不适宜行TMVR以外手术的高手术风险患者(EUROScore≥20%);③解剖上适合TMVR的患者(主要指二尖瓣瓣环内径和外周血管内径在器械所能达到的合适范围内)。
2 入路途径
基于TAVI的经验总结和二尖瓣的特殊解剖结构,当前入路途径主要为经心尖途径[7]和经股动静脉途径[4]。其中经心尖途径TMVR具体操作与经心尖途径TAVI基本类似,具有定位准确、操作简便等优点。相比之下,经股动脉途径TMVR较为复杂,行股动静脉穿刺后,经股静脉置入的导丝经房间隔穿刺后,经过二尖瓣瓣环和左心室,到达降主动脉与股动脉所置导丝抓捕器汇合,从而建立动静脉环,并经此动静脉环行瓣膜植入,最终需要用房间隔封堵器封堵人为房间隔缺损。
尽管心尖途径优势更大,并且在当前的TMVR中占主要地位。Glower等[8]研究显示,经股动静脉途径安全性更高、创伤更小、术后恢复快,从而增加手术的安全性。因此,结合TAVI的发展经验,随着设备尺寸缩小,经股动静脉途径或许将在未来有着更大的舞台。
3 器械
自2012年在人体上首次植入Edwards研发的CardiAQ经皮二尖瓣瓣膜后[4],TMVR装置的研究进入快车道,各类瓣膜均在锚定、覆盖和部署机制上有独特的见解和设计。现在已经报道的用于人体的TMVR装置至少有8种: CardiAQ(Edwards Lifesciences),Tiara(Neovasc, Richmond, BC, Canada)[9],FORTIS (Edwards Lifesciences)[10],Tendyne (Abbott Vascular, Roseville, MN, USA)[11],Intrepid (Medtronic, Minneapolis, MN, USA)[12],Navi(NaviGate Cardiac Structures, Inc., Lake Forest, CA, USA),MValve (MValve Technologies Ltd, Herzliya, Tel Aviv, Israel),HighLife (HighLife Medical, Irvine, CA, USA)[13]。主要TMVR瓣膜形状见图1,主要瓣膜临床试验数据[14]见表1。另外,国产的2款TMVR瓣膜AccuFit(天津赛诺医疗科学技术有限公司)和Mithos(上海纽脉医疗科技有限公司)均已经完成动物实验,效果良好,即将进行临床实验[15]。
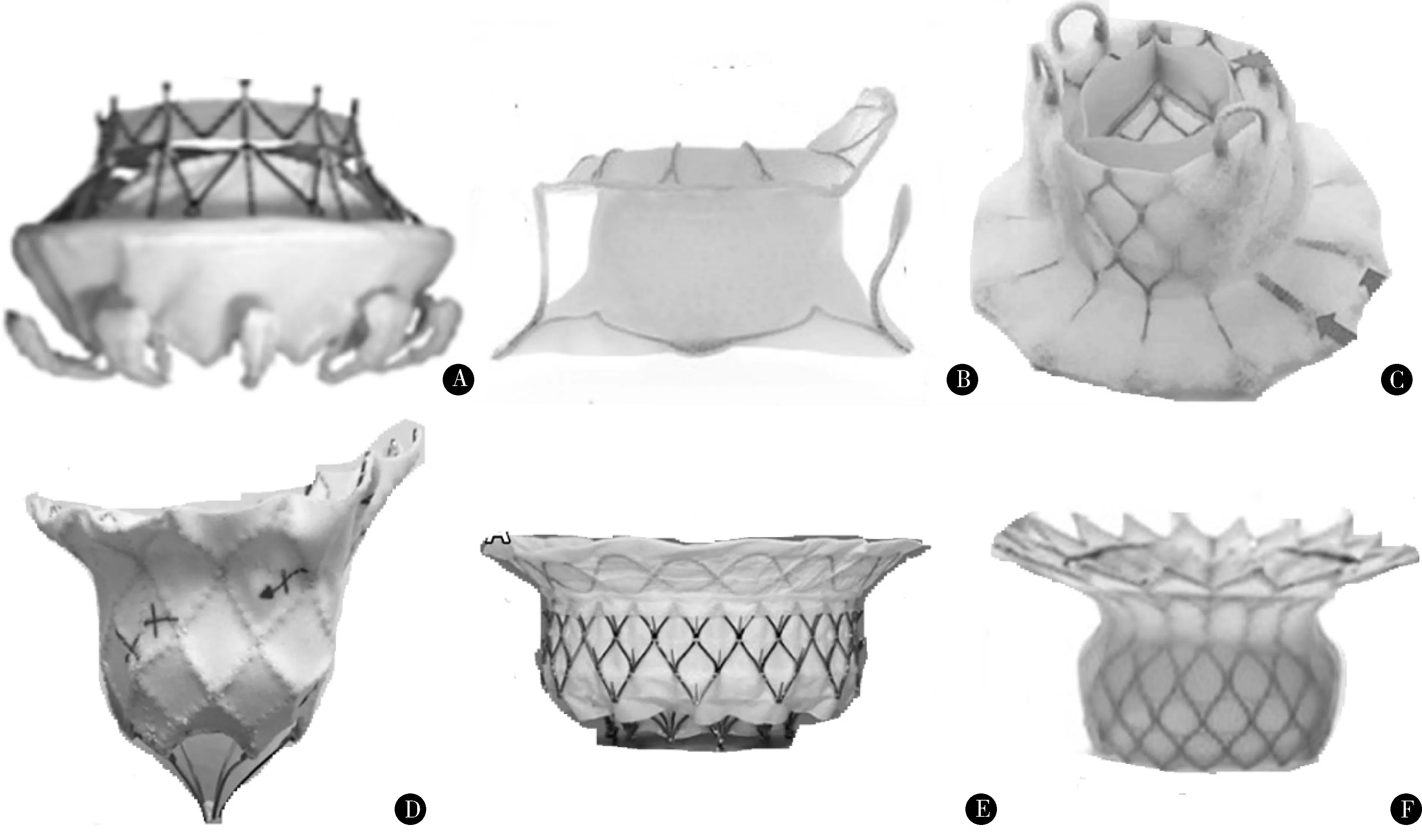
图1 主要TMVR瓣膜 A.CardiAQ瓣膜;B.Tiara瓣膜;C.FORTIS瓣膜;D.Tendyne瓣膜;E.Intrepid瓣膜;F.HighLife瓣膜
虽然越来越多的TMVR瓣膜涌现,但是回望2016年美国经导管心血管治疗学术会议公布的数据,CardiAQ瓣膜植入术后30 d死亡率50%,FORTIS瓣膜植入术后30 d死亡率38%。这样的数据也曾使这2种瓣膜充满争议。但是Tendyne瓣膜的临床表现或许能为TMVR继续发展带来曙光,死亡率只有4%,手术失败率也仅有7%。此外,其余各类瓣膜也正在临床前期实验中。
同时,Tendyne瓣膜当前也被认为是当前临床实验中,最有希望获批临床应用的瓣膜系统。TMVR装置相关的解剖学要求包括[16]:瓣膜系统必须被输送、固定以及覆盖在一个大的、非圆形、鞍状、搏动幅度较大并有钙化的环状区域,同时,瓣膜系统必须适应复杂、个体化差异较大的瓣下结构,还要注意左室流出道、冠状静脉窦以及左旋支这些解剖结构不受影响。相较于其他瓣膜系统,Tendyne瓣膜的设计很好的回应上述解剖特点:①心尖细绳瓣膜固定系统结合马鞍形设计,避免瓣膜移位及左室流出道梗阻;②具有重复收回定位功能,定位准确;③设计心房缘,降低瓣周漏;④心尖垫片设计既协助固定瓣膜,又可以封堵入路切口。
总的来说,解剖上的困难就足以看出TMVR装置的发展可谓困难重重。现行各类主要的TMVR瓣膜,包括Tendyne瓣膜,虽然已经较大程度上解决特殊解剖位置带来的结构设计问题,但是在封口技术、瓣膜及输送系统体积、瓣膜工作机制上还有很大的研究空间[17]。
4 并发症
TMVR早期临床结果使项目发展经常陷入停滞,这些急性和亚急性的并发症包括[18]:瓣膜错位、瓣周漏、左室流出道梗阻、血栓形成与栓塞、溶血、主动脉瓣损伤、射血分数降低与低心排综合征、卒中(部分并发症情况[14]见表1),且因上述并发症致患者30 d死亡率一度高达54%。

表1 主要TMVR瓣膜临床试验数据[14]
NA:原文未见相关数据
*30 d检查发现二尖瓣再次出现中度以上反流;**全因死亡指所有死亡因素引起的死亡
同时,瓣周漏和左室流出道梗阻等非致命围术期并发症的中远期临床影响亦对TMVR的发展提出挑战,这些研究对于我们设计临床实验来比较TMVR的实际效果至关重要。在近期出版的《欧洲介入医学杂志》上,Duncan等[19]报道伦敦一所医院5例接受新式Tendyne TMVR瓣膜置入后的中期(2年)临床效果,结果令人欣喜。在这个报告中,所有的病人病愈出院,但是典型的TMVR并发症也均有发生:1例左室流出道梗阻(接受左心室支架治疗)、1例瓣周漏、1例轻度溶血。为防止装置血栓,所有病人均口服抗凝药物。1例发生疑似短暂性脑缺血,1例发生卒中出院后12个月死亡(这2例均患有房颤,且其中1例没有规律服用抗凝药物)。另外,1例因行房颤消融术而停服抗凝药物,心脏超声发现装置血栓形成后,我们让病人继续口服抗凝药物,暂未发现异常。2年后随访4例存活,心功能得到提升,且没有新发装置相关并发症。
TMVR领域的进步不应只关注围手术期并发症,还需关注这些并发症对远期临床效果的影响。其中设备血栓形成成为当前远期并发症的关注焦点。早期研究者将TAVI系统实验性用于二尖瓣位置后发生一系列设备血栓形成[20]。当前一些新研究的TMVR系统的动物实验也提示设备血栓形成不容忽视[21,22]。目前,使用充足的口服抗凝药物是这些文献中提出的主要解决方案之一[19~22],但是抗凝药物(合并抗血小板药物)的剂量和使用时间仍有待进一步研究。此外,4D多层螺旋CT对于术后器械血栓形成的预测价值较高,应在TMVR术后被常规应用[23]。Ruel等[24]提出我们普遍认为二尖瓣腱索组织是心室收缩功能的一部分,因此,目前施行二尖瓣置换手术也倾向于采用保留腱索组织等瓣下结构的术式。但是TMVR必然损伤二尖瓣腱索组织,从而导致心室功能受损,甚至心力衰竭[25]。因此,TMVR的远期临床效果仍需关注。
5 展望
当前,TMVR研究仍停留在器械和早期临床效果研究,还未出现真正能够推动TMVR迈向实际临床应用的有力研究。虽然当前的TMVR瓣膜已经能满足基本要求,例如适应复杂解剖位置、瓣膜功能良好、瓣周漏情况改善、短期并发症逐步减少,但是在瓣膜血栓、瓣膜耐久性、心功能损害等长期并发症方面,仍有较多空白和挑战。回顾TAVI技术从质疑到普及的过程,我们有理由相信,随着生物工程与导管技术的发展,更优的TMVR瓣膜结构设计和临床结果势必会出现,并最终服务于广大患者。

