氩气刀定位法在胸腔镜肺楔形切除手术中的应用
许德新 代祖建 林铿强
(福建省福州肺科医院胸外科,福州 350004)
随着体检意识的加强及胸部CT薄层扫描的普及,大量肺部小结节被检出。部分手术切除的肺小结节为早期肺癌、癌前病变,故亚肺叶切除术在肺癌手术中所占的比例越来越大。术中快速找到肺结节是手术成功的关键。我们既往采用CT引导下经皮肺穿刺置入定位钩、注射亚甲蓝及医用胶等方法进行定位,体会并发症较多,近年来采用氩气刀定位法,获得了较好的效果。2015年1月~2018年1月,我们应用氩气刀术中定位法对63例肺内小结节实施单操作孔胸腔镜肺楔形切除术,现将操作方法及体会总结如下。
1 临床资料与方法
1.1 一般资料
本组63例,男29例,女34例。年龄29~75岁,(46.6±13.4)岁,其中8例>70岁。咳嗽9例,胸背痛3例,余51例均为体检行CT检查发现。均行胸部增强CT检查(三维重建),病灶均为单发,结节最大径0.8~2 cm,(1.22±0.34)cm。纯磨玻璃影35例,混杂密度磨玻璃影28例。结节位于左上叶18例,左下叶9例,右上叶25例,右中叶4例,右下叶7例。病灶均位于肺边缘,CT测量病灶距离脏层胸膜0.5~3 cm,(1.67±0.54)cm。术前常规检查包括腹部彩超、头颅CT或MRI、心电图、肺功能,3例有胸背痛症状者加行全身骨ECT扫描,9例65岁以上者行心脏彩超及24 h动态心电图检查,除外远处转移及其他手术禁忌证。3例合并纵隔淋巴结肿大者行PET-CT检查,提示肿大淋巴结为阴性。术前均诊断为“肺结节待查:肺癌?”
病例选择标准:单发肺部小结节,最大径≤2 cm,密度为纯磨玻璃影或混杂密度磨玻璃影,CT下测量病灶距离脏层胸膜≤3 cm。
1.2 方法
双腔气管插管单肺通气。侧卧位、折刀位。胸腔镜观察孔取腋中线平剑突水平,长约1 cm,操作孔位于腋前线第4肋间,长约3 cm。术中通过氩气刀定位法确定病变部位,均先行肺小结节楔形切除术。氩气刀定位法具体操作:先仔细阅读分析胸部CT三维重建,明确结节所在的肺叶及肺段。CT上先判断病灶位于第几肋间层面(图1),再结合钟表盘定位法[1,2],确定病灶位于几点钟方向(图2),然后在胸腔镜下将病灶虚拟投影在壁层胸膜表面。将氩气刀对准壁层胸膜投影处,喷射定位留下烧灼记号。固定氩气刀,嘱麻醉师膨肺,让肺充分膨胀直至紧贴胸壁,再次喷射氩气,使肺表面亦留下烧灼点,形成病灶在肺脏层胸膜表面的投影定位点(图3)。以肺表面定位点为中心,向外周扩展3 cm做环形标记,卵圆钳夹起标记区域,在环形标记内用指尖触碰病灶。若能触摸到病灶,则距病灶边缘超过2 cm做楔形切除(图4);若无法精确触摸到病灶,则直接予Endo-GIA切除标记区域的肺组织。取出病灶送检术中冰冻(病灶及切缘),根据冰冻病理结果决定下一步手术方案。术中冰冻报告病灶为良性则手术结束;为原位癌或微浸润癌、切缘阴性且切缘距离足够(≥2 cm,或≥结节大小[3~5]),则加行淋巴结采样;若为浸润性肺癌,原则上行肺叶切除加系统性淋巴结清扫。
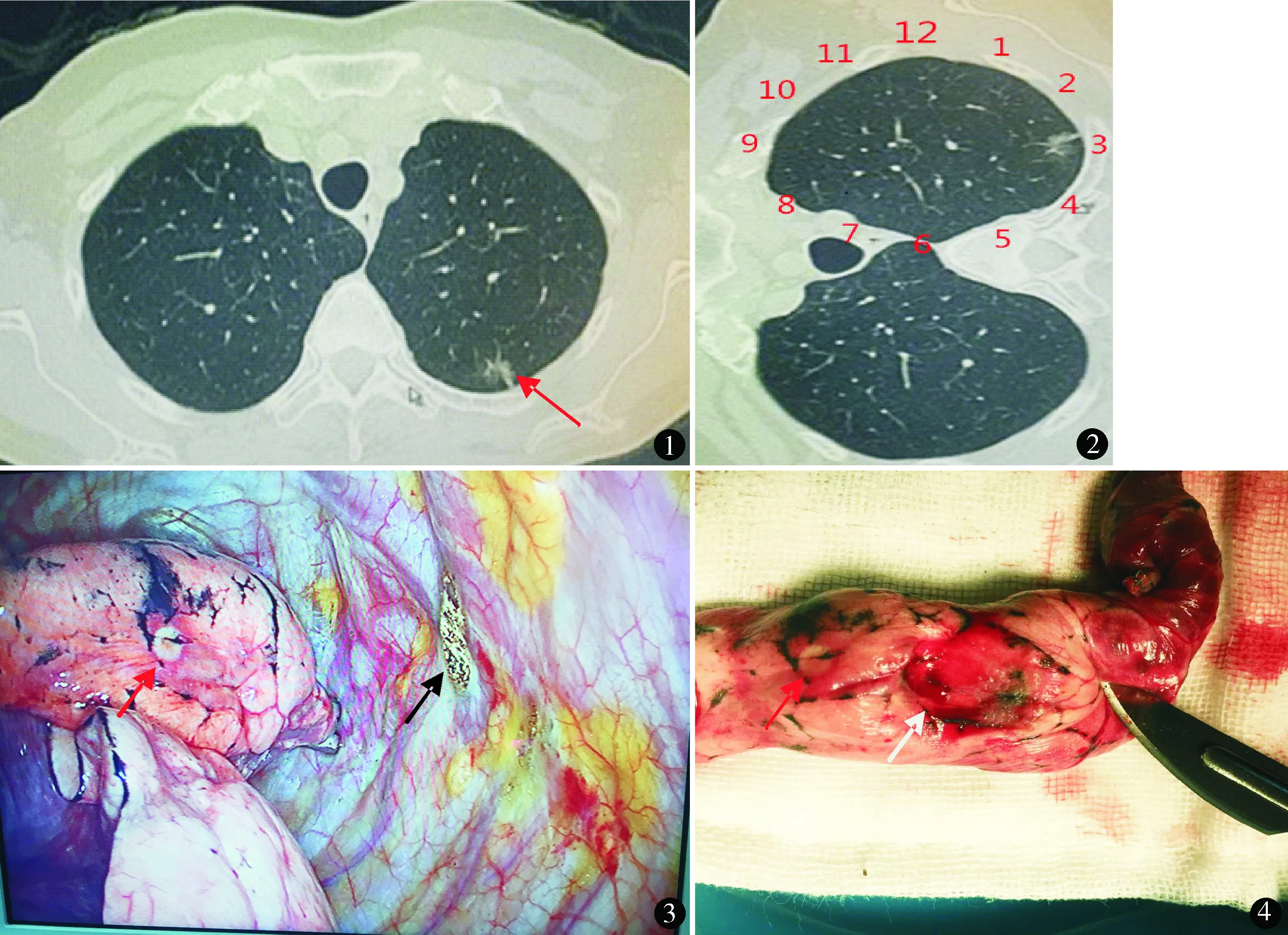
图1 CT上判断病灶对应第4肋骨层面 图2 钟表盘定位法得出病灶位于3点钟方向 图3 氩气刀在壁层(黑箭头)、脏层(红箭头)胸膜上留下定位点 图4 指尖触摸到病灶后予楔形切除病灶,取出后切开见病灶(白箭头),氩气刀定位成功
2 结果
63例均先实施单操作孔胸腔镜肺楔形切除术,2例切下标本未找到病灶,继续行肺段切除术,在残余肺段中找到病灶,冰冻报告为微浸润性腺癌。61例在楔形切除标本中找到病灶,其中12例冰冻报告浸润性腺癌,8例继续行肺叶切除+系统性肺门纵隔淋巴结清扫术,4例因肺功能低未行扩大切除;44例冰冻报告原位癌或微浸润癌,均行淋巴结采样,其中2例因切缘距离不够行扩大楔形切除;5例冰冻报告良性病变,仅行楔形切除。术后病理结果与术中冰冻基本吻合。
采用氩气刀定位法,63例实施肺楔形切除后找到病灶61例,定位成功率96.8%,此61例标本取出胸腔后,大体标本测量病灶距离切缘的距离为(2.3±0.6) cm。
术后病理诊断:良性病变5例,包括不典型腺瘤样增生3例,尘结节2例;肺癌58例,包括原位癌19例,微浸润性腺癌27例,浸润性腺癌12例,所有采样的淋巴结均未见癌转移,分期均为Ⅰa期肺腺癌。
术后早期并发症:肺部感染6例,术后持续肺漏气超过1周5例,术后心律失常8例。均行加强抗感染、改善胸腔引流、抗心律失常等保守对症治疗治愈。无术中、术后死亡。
3 讨论
肺结节的精准定位是微创手术成功的关键,包括术前定位与术中定位。术前定位主要是借助CT引导下经皮肺穿刺实现,均为有创性操作,常用的定位材料包括金属材料(Hook-wire、Spiral-wire、微弹簧圈[6]),染料,医用胶[7],核素等。Hook-wire已广泛用于术前CT引导下定位,但并发症多,病灶较浅表时易出现脱钩,穿刺后出血、气胸、胸膜反应等风险亦不可避免[8],甚至气体栓塞[9]。Spiral-wire尖端呈螺旋状,可牢固地锚定在肺内,不易脱出,对比Hook-wire并发症相对较少[10],但肺穿刺的共同并发症仍存在。CT三维重建定位法[11]能精确显示病灶在肺内的空间位置、与周围血管和支气管的毗邻关系,但是术中肺萎陷后,会因病灶出现向心旋转性收缩而产生定位误差,尤其是位于肺外周带的结节,移位更为明显。电磁导航支气管镜引导定位因费用昂贵我院目前难以推广。术中定位法有肉眼观察、卵圆钳胸膜表面滑动定位、手指触诊定位、胸腔镜B超探头定位、CT定位等。病灶贴近脏层胸膜或侵犯脏层胸膜者,在肺完全萎陷状态下通常肉眼观察就能轻易发现。手指触诊是凭借指尖触碰到病灶时细微的感觉找到病灶,对术者的技术要求较高。术中超声定位是简易、无创的定位方法,安全性佳[12],但是需要术者熟练掌握超声技术,且超声受气体干扰,要求在肺组织完全萎陷时进行,不适用于肺气肿患者及术中麻醉气管插管对位不良导致肺无法完全萎陷者。术中CT定位要求手术室有放射防护,一般基层医院难以开展。
我院最初采用手指或卵圆钳触诊法,失败率较高。若病灶距离主操作孔较远、病灶较靠近肺门,则指尖难以触及;或病灶为纯磨玻璃影,质地与正常肺组织接近,难以通过手指触诊定位。后来大量采用钟表盘定位法,常出现定位偏差较大的情况,分析原因主要为肺萎陷后发生向心旋转性收缩造成定位误差。再后来采用CT引导下经皮肺穿刺置入定位钩、注射亚甲蓝或医用胶等方法定位,出现较多并发症,如气胸、出血、定位钩脱落、亚甲蓝迅速弥散开、医用胶引起剧烈咳嗽等。近年我们采用氩气刀定位法,获得较好的效果。与目前主流的术前CT引导下经皮肺穿刺定位方法相比,氩气刀定位法优势在于:①应用范围更广,后者难以到达的部位如肺尖、肩胛骨后、叶间裂、大血管旁等,均可使用氩气刀定位。②更安全,只要操作得当,刀头不直接顶着血管或神经喷射,没有出血、气胸、胸膜反应、空气栓塞等并发症的风险,也不存在Hook-wire的定位钩移位或脱落问题。③更经济,因为我们术中已广泛应用氩气刀进行止血操作,故氩气刀定位不产生额外的耗材费用。与钟表盘定位法相比,因是在肺充分膨胀的状态下用氩气刀在脏层胸膜上做标记,消除了肺萎陷后发生旋转收缩所造成的误差。不足之处在于,与术前定位法相比,增加术中操作步骤,且在定位的精准度上还是逊色于直观的经皮肺穿刺方法。另外,氩气刀定位法适用于肺外周带病灶。
使用氩气刀定位的同时,也可同时利用一些解剖标志协助精准定位,如奇静脉、主动脉弓、肺裂、肺下静脉、支气管间嵴等。有些患者肺内存在副裂,结合CT上所见的病灶与副裂的解剖关系,可以把副裂作为定位的参照点。
采用氩气刀定位法应注意,肺充分膨胀时氩气刀头是在肺脏层胸膜面“盲喷”留下标记,此时膨胀的肺有可能会顶开氩气刀头造成移位。故需要先用氩气刀在壁层胸膜上做标记点,这样当肺萎陷后就可以观察到氩气刀头有无移位。选择氩气刀在壁层胸膜上做标记的优点在于,不易损伤肋间血管及神经,若使用电刀或电凝钩做标记,当麻醉师膨肺使肺充分紧贴胸壁的时候,因无法直视刀头,有可能误伤肋间血管及神经。我们利用手指在胸腔内触诊病灶的体会是,先用氩气刀定位法确定病灶的大致区域,再用卵圆钳夹取目标区域肺组织,指尖轻轻触摸卵圆钳上方的肺组织寻找病灶。如只是把肺组织向操作孔方向牵拉,此时触摸病灶时指尖下方无硬物支撑,难有触感,且肺组织经牵拉绷紧后,病灶周边的肺组织质地变硬,难与病灶相区分。楔形切除的肺组织取出后,需耐心寻找病灶,切不可在未确切找到病灶的情况下盲目送检造成术中冰冻误判。有时因病灶过小,或病变呈纯磨玻璃影样密度较低难以找到,可在肺表面涂磨少量石蜡油,在触摸到病灶时指尖可能会有跳跃感。有时病灶太靠近闭合钉切缘,因邻近肺组织被闭合钉收紧质地变硬造成干扰,此时可细心剪开闭合钉,再寻找病灶。
本组2例楔形切除的肺组织未找到病灶,出现定位失败,分析主要原因为:CT扫描时的体位为双手举高抱头平卧位,且患者为深吸气后屏气状态,而术中为侧卧位折刀体位,通过麻醉师膨肺至肺完全复张再行氩气刀定位。体位变化及肺充气状态不同导致肺内病灶在壁层胸膜面的投影出现移位偏差。我们认为术前CT检查时采用术中的体位,可有效减少术中氩气刀定位时体位变化造成的误差。
总之,我们认为胸腔镜下氩气刀定位法作为一种简便、经济且相对无创的方法,更易被医患接受,其对于肺内小结节的术中定位是实用、可靠的,值得临床推广。

