富镍系层状正极材料的研究进展*
郭 慧
(厦门海洋职业技术学院 厦门 361102)
随着不可再生化石能源的减少和环境问题,开发利用新清洁能源得到越来越多的关注。化学电源作为重要的化学能和电能相互转化的装置,在新能源的利用中起着重要的推动作用。锂离子电池以其优良的性能,广泛应用于便携式电子工具、交通工具、储能等多个领域。提高能量密度和降低材料成本是锂离子电池发展的主要方向,正极材料作为锂离子电池的重要组成部分,对低成本和高比能量密度的追求,促使了一系列材料的研究,如橄榄石结构的LiMPO4(M=Fe、Mn、Co、Ni等)和尖晶石结构的LiM2O4(M=Ni、Co和Mn),但这些结构的材料的容量较低。层状富锂材料[1]虽然具有超过250mAh/g的容量,但其首次不可逆容量大,较差的循环和倍率性能,限制了其在实际上的应用。
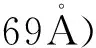
1 富镍系层状正极材料的结构
作为富镍系层状材料LiNi1-xMxO2(M=Co、Mn、Al等0≤x≤0.3)的基本结构,LiNiO2具有α-NaFeO2型六方层状结构,R-3m空间群,如图1所示。Li+和Ni3+分别位于(3a)和(3b)位置,O2-位于6c位置,层状结构为Li+的迁移提供二维通道。其理论容量与 LiCoO2相当,为275mAh/g。由于Ni3+在eg轨道上电子不均等占有,存在John-Teller效应,容易转变成Ni2+,而Ni2+离子半径与Li+半径相近,Ni2+迁移到Li+(3a)位置,形成微小的局部立方岩盐相结构,该结构的电化学性能不活泼降低了材料的电化学活性;此外,Ni2+占据Li+层,会阻碍Li+在锂单层中的二维固相扩散,导致LiNiO2过充性能变差,热稳定性差,循环性能劣化(见图1)。
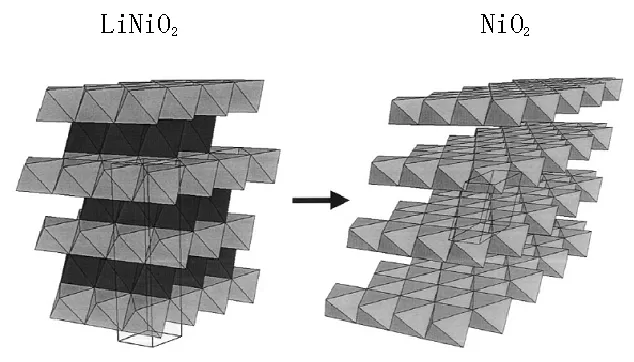
图1 LiNiO2结构示意图
LiNiO2脱嵌Li过程包含多次相变,降低了电极的循环稳定性,导致电极容量的衰减和寿命的缩短。Noh对LiNixCoyMn1-x-yO2进行研究[2],发现对于x=1/3 的材料首次循环的氧化/还原峰分别为3.76V和3.72V,但当Ni含量增加时,在3.64V增加一个新的氧化峰;当x=0.8时,出现4对明显的氧化还原峰,氧化峰分别为3.62V、3.78V、4.04V和4.23V,相应的还原峰分别为3.58V,3.72V,3.98V和4.18V。在循环过程中,x=1/3的材料氧化还原峰非常稳定,而随着Ni含量的增加,氧化还原峰极化增大,对于x=0.8的材料循环100次时3.62V峰已经移向3.76V。由六方相H2向六方相H3的结构转变所导致的体积收缩是造成容量衰减的主要原因。另外,LiNiO2在高脱锂状态下热稳定性差,也带来了严重的安全问题。
2 富镍系层状结构材料的问题与挑战
2.1富镍系层状结构材料的阳离子混排
通常层状结构材料具有R-3m结构,其表现为沿着菱方的[111]方向,具有O-Li-O-TM-O-Li-O-TM-O的重复O3构型。因此,一般情况下,R-3m结构中,Li和过渡金属是完全被隔离的,分别占据3a和3b位置。但根据晶体场理论, Ni3+离子在eg轨道上电子不均等占有,存在Jahn-Teller效应,因此,在FCC八面体间隙中的Ni倾向于形成Ni2+(见图2)。
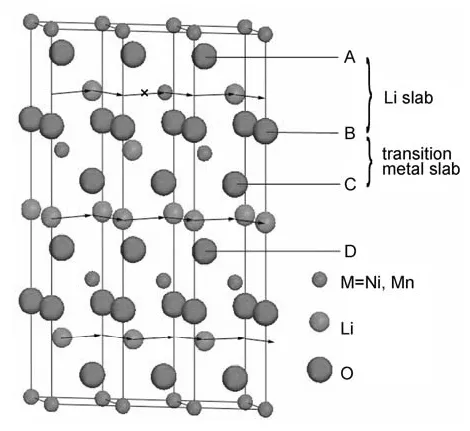
图2 层状LiNi0.5Mn0.5O2 材料晶体结构中Li/Ni 混排示意图[3]

表1 Li、Ni、Co、Mn 的离子半径
2.2富镍系层状结构材料的表面化学反应
为减少锂镍混排,富镍系材料的制备过程中一般会加入过量的,而这部分在材料表面残留的Li极容易和空气中的CO2和水发生反应,形成Li2CO3和LiOH。这也使富镍材料的pH值较高,容易在调浆时与NMP反应形成凝胶;LiOH与电解液中的LiPF6反应产生HF,加剧对材料的腐蚀,高温存储时Li2CO3的分解导致严重的气胀。其次,放电后的高脱锂态形成了高反应活性的Ni4+容易造成电解液的分解、缺失,并形成较厚的SEI膜阻碍了锂离子的扩散,影响了材料的电化学性能。此外,由于动力学影响,粒子表面Li的脱出与基体内部不一致,这种不一致导致了材料结构的不稳定,为改善这部分不稳定,过渡金属离子会通过失去氧还原,维持材料电中性,在材料表面形成了新相和孔隙[4]。因此,表面化学和副反应对富镍系材料的性能有着重大影响。
3 富镍系层状结构材料的制备方法
制备富镍系层状结构材料的常用方法包括高温固相合成,共沉淀法、溶胶凝胶法等等。
3.1固相合成法
高温固相合成通常以Li2CO3、LiOH、LiAc、LiNO3为锂源,与Ni源、Co 源、Mn 源如相应的过渡金属氧化物、氢氧化物、碳酸盐、羧酸盐、硝酸盐等混合均匀后,按一定的热处理程序,在高温下(一般在600℃-900℃)煅烧制成层状材料。T.Ohzuku等[5]将LiOH·H2O、Li2CO3或LiNO3与Ni、NiCO3、Ni(OH)2、NiOOH 或 Ni(NO3)2进行不同组合,在空气或氧气气氛中于750-900℃下焙烧24h。其中以LiNO3与NiCO3或Ni(OH)2为原料,氧气气氛中合成的LiNiO2正极材料,在2.5-4.2 V电压范围内具有最高的放电比容量。
固相合成工艺简单,设备成熟,便于规模化生产,但产品性能一般不理想,各批次产品性能一致性差。其主要原因是Li 源与过渡金属源难以混合均匀,固相反应时各离子传输路径过长,而且难以形成均相的固溶体,得到化学计量比的产物。
3.2溶胶凝胶法
溶胶凝胶法制备富镍系层状材料的一般过程是:使金属盐溶液在一定条件下形成溶胶,然后通过陈化、溶剂蒸发,逐步除去溶剂形成凝胶,再经研磨干燥焙烧得到产物。溶胶凝胶法前驱体中各离子混合十分均匀,因而后续煅烧反应中可以降低反应温度,缩短反应时间。CJ Han等[6]以锂、镍、钴的醋酸盐和硝酸锂为原料,丙稀酸为络合剂, 80℃真空蒸发4h,140℃干燥4h形成凝胶, 500℃预处理6h,然后置于氧气流中,800℃焙烧24h获得LiNi0.8Co0.2-xAlxO2(x=0、0.01、0.03、0.05)。溶胶凝胶法制备产物成分均匀,化学计量比易于控制,电化学性能较好,但产业化难度较大。
3.3共沉淀法
共沉淀法制备LiNi1-xMxO2是将相应的金属盐以水溶液状态混合,用适当的沉淀剂结合络合剂,使溶液中各组分按化学计量共同沉淀出来。液相反应制得的前驱体再经高温煅烧即可得到高性能电极材料。共沉淀法可以使原料达到原子尺度的均匀混合, 同时可精确控制各组分含量,且通过控制反应温度、反应时间、搅拌速度、反应原料液浓度和反应体系pH 值等参数,可以得到不同粒径分布的球形产品。ZX Yang 等[7]将 Ni(NO3)2·6H2O 和 Co(NO3)2·6H2O 配制成混合溶液,以NH4HCO3作沉淀剂,合成了(Ni0.8Co0.2)2(OH)2CO3前驱体,然后将前驱体与LiOH·H2O混合球磨0.5 h,在空气中置于750℃下倍烧15 h,制得亚微米级LiNi0.8Co0.2O2,该材料首次放电比容量194.8 mAh/g, 循环20次容量保持率为91.9%。共沉淀法各组分混合均匀、批次质量稳定、设备简单,易于工业化规模化生产。因此共沉淀法在科研和生产上得到广泛应用。此外喷雾干燥法熔融盐法、自蔓延高温合成法等也可制备LiNi1-xMxO2材料,但相对应用较少。
4 富镍系层状结构材料的改性研究
4.1体相掺杂
通过在材料主体结构中引入新的元素,来改善富镍系层状材料的结构不稳定性,根据掺杂效果大致可分为3个方面:①采用稳定的元素来取代不稳定的Li和Ni;②抑制Li+/Ni2+阳离子混排;③强化金属-氧键,提高结构稳定性,减少氧释放。
Rougier[8-9]等发现随着掺Co量增加,LiNi1-xCoxO2材料的阳离子无序度降低,晶胞体积收缩,材料结构稳定性提高,当x>0.3时,可以形成结晶完好的二维层状LiNi1-xCoxO2,利于Li+的快速扩散。在富镍层状结构材料采用Co离子取代Ni离子的报道出现后,Mn和Co取代Ni离子的研究得到了广泛的关注[9],形成了LiNiO2-LiCoO2-LiMO2的体系研究。这些体系的研究表明,更高的镍含量带来更高的容量,但循环和热稳定性变差。
Al的掺杂i[10]能够稳定LiNiO2的结构,提高材料的热稳定性,且稳定的二维结构有利于Li+的扩散,从而改善锂镍氧化物大倍率性能。因为Al的掺杂带来材料放电容量的降低,之前研究人员大多将Al限定在5%以下,在不大降低材料放点容量的同时达到更大的结构稳定效果[11-12]。但随着富镍系材料在电动车上的应用,热稳定性和高温循环成为了瓶颈,研究人员也开始逐渐提高材料中Al的掺杂量。
Ti元素的掺杂也能提高材料的循环稳定性和热稳定性,一方面,Ti4+[13]掺杂离子在材料充放电过程中价态并不发生变化,起到支撑材料结构的作用;另一方面,Ti4+还可以抑制Ni2+向Li层的迁移,减少阳离子混排。Mg的掺杂可改善材料的结构稳定性,虽然Mg2+在材料中的占位情况,仍然存在争议[14-15],但都通过实验证明Mg2+的掺入提高了材料的循环性和热稳定性。F阴离子由于具有比氧更高的电负性,可改善材料的结构稳定性,并降低锂镍的混排,提高材料的循环性能[16]。
4.2表面改性
为抑制富镍系材料表面的副反应,研究人员通过在材料表面包覆一层电化学惰性的保护层,如金属氧化物(ZrO2[17],Al2O3[18],MgO[19]等),磷酸盐(AlPO4[20],FePO4[21]等)氟化物(AlF3[22]等),这些金属保护层通常为电化学非活性,能有效隔绝材料与酸性电解液接触,减少材料的表面副反应,从而提高材料的循环性能,但这部分材料也因为其电化学非活性和不导电性,增加了材料的阻抗。因此研究人员也通过在材料表面包覆电子导电或离子导电的材料,如Yoon等[23]通过高能球磨在LiNi0.8Co0.15Al0.05O2表面包覆石墨烯,当电流从10C提高到20C,包覆石墨烯的LiNi0.8Co0.15Al0.05O2放电容量为152 mAh/g和112mAh/g,是未包覆样品的2倍。应皆荣等[24]用Li2O-2B2O3玻璃层包覆在LiNi0.8Co0.2O2表面,这种包覆层可以避免电极材料与电解液的直接接触,同时具有较好的离子导电性。包覆后材料的可逆比容量由161mAh/g提高到195mAh/g,循环性能明显改善,自放电速率也有所减慢。
近年来,采用一种锂离子电池正极材料或嵌锂化合物对另一种锂离子电池正极材料或嵌锂化合物进行表相改性,以形成包覆型、核-壳型或梯度型材料也受到了广泛的关注[25]。
5 结论
与层状富锂材料相比,富镍系层状结构正极材料LiNi1-xMxO2(M=Co、Mn、Al等,0≤x≤0.3)具有较少的首次不可逆容量,较好的倍率和循环性能,极有可能应用在对能量密度要求高的混合动力汽车或电动车上。市场上,采用LiNi0.815Co0.15Al0.035O2(NCA)正极材料的锂离子电池已经应用在了Tesla电动汽车上,显示出了富镍系层状材料的广阔的应用前景。富镍系正极材料这几年得到了广泛的发展,但Li+/Ni2+阳离子混排导致的结构不稳定和锂扩散受阻,表面副反应引起的容量损失,过度脱锂带来安全性能下降,依然是富镍系层状材料所面临的挑战,但相信随着技术的进步,富镍系层状正极材料必然得到更为广泛的应用。

