抗结核骨组织工程复合体局部治疗兔脊柱结核的对比研究
王腾飞,麦麦提艾力·阿不力克木,杨勇,陈江涛,王翀,陶颖,宋兴华
(新疆医科大学第一附属医院骨科中心,新疆 乌鲁木齐 830054)
结核病是感染性疾病中的头号杀手,且在全球范围内呈逐年上升趋势,我国结核病疫情尤为严重[1]。尤其是感染艾滋病病毒的患者越来越多,增加了此类患者患有结核病的可能。脊柱结核是常见的肺外结核,约占结核患者的9%~12%[2-3]。对于脊柱结核的治疗,化疗是首选[4]。但骨结核血液供应差,口服药很难到达病灶,且8%~12%的患者具有一线抗结核药物耐药性。骨结核最常用的治疗方法是外科手术清除病灶。而结核病灶清除后,需要在椎体缺损区域进行植骨填补以支撑脊柱,否则会造成椎体塌陷,植骨能一定程度上维持脊柱的力学稳定性。虽然自体骨移植是骨修复技术的“金标准”[5]。但自体骨来源有限,易出现取骨区感染、疼痛等症状。而且同种异体骨有免疫排斥、愈合缓慢、感染等特点。因此研发新型骨缺埙修复材料迫在眉睫。随着组织工程的快速发展,人工骨作为一种良好的骨替代材料,越来越被大家所认可[4]。羟基磷灰石与/β-磷酸三钙(hydroxyapatite and/β-tricalcium phosphate,HA/β-TCP)构成的复合材料是目前广泛应用于临床的人工复合材料。HA/β-TCA与脂肪干细胞的复合可以更好地诱导骨细胞生长,促进骨组织的生成,而且具有良好的孔隙率,有利于种子细胞与材料复合,是骨组织工程中比较理想的生物复合材料[6]。结核术后患者仍然需要长周期服用抗结核药物,由于副作用较大,患者依从性差,使得全身用药的临床疗效受到限制。因此,提高脊柱结核局部病变血药浓度,增强灭菌能力,而且能在病灶局部形成有效的药物浓度,寻找一种新的替代给药途径就显得尤为重要[7]。缓控释制剂可以长期缓释药物,控制药物剂量,减少给药次数,提高患者顺应性,受到广大医务工作者及患者的青睐。本实验采用利福喷丁微球作为包封药物,采用降解可控的高分子生物材料HA/β-TC作为载体,与脂肪干细胞构成抗结核性骨组织工程复合体,我们希望将缓控释微球的优点和新型植骨材料的特点结合起来,研发一种既能满足局部长效释药,又能提供一定力学强度、促进骨融合的新型辅助抗结核治疗的植骨材料。
1 实验材料
1.1 实验动物及场所 成年健康新西兰大白兔72只,雌雄不限,体重(3.0±0.3)kg,由新疆疾病防控中心提供。实验场地为新疆自治区动物试验中心,饲养温度及湿度适中。动物实验伦理审批号:IACUC-20130217048。
1.2 实验仪器 超净工作台(赛默飞世尔科技公司)、CO2培养箱(力新HF240)、水浴箱(上海精密设备)、UV2550紫外可见分光光度计(日本岛津)、酶标仪(Thermo)、流式细胞仪(Beckman),倒置显微镜、共聚焦荧光显微镜(Leica)、电镜(上海菁华科技仪器有限公司)、兽医用X线摄影(天地智慧ELITE 2000 Plus型)。Ingenia1.5T全数字磁共振成像仪(荷兰Philips公司)。
1.3 实验试剂 低糖DMEM培养基、胎牛血清、磷酸盐缓冲液PBS(HyClone)、Ⅰ型胶原酶(Worthington)、胰蛋白酶R溶液、青一链霉素(Gibco)、地塞米松、抗坏血酸、维生素C、β-甘油磷酸钠、茜红素染液、ALP检测试剂盒、ALP染液(Sigma)、人工骨粒复合体(HA/β-TCP,Bi-Ostetic)(复合体是有60%的羟基磷灰石和40%的β-磷酸三钙组成)。利福喷丁微球(已申请国家专利),聚乳酸由山东医疗器械公司提供(试剂级,分子量3万),二氯甲烷、甲醇等试剂,细胞凋亡试剂盒(BD)均购自市售,结核杆菌由新疆畜牧科学院提供。
2 实验方法
2.1 兔脂肪干细胞的提取、培养及体外成骨诱导分化 选取新西兰大白兔2只,耳缘静脉采用3%戊巴比妥钠(1~2 mg/kg)麻醉,在无菌手术台下取腹股沟区脂肪组织,分离大体可见的筋膜、血管,用眼科剪剪碎,放入含有20 mL PBS管离心、震荡消化,终止消化后加入低糖DMEM完全生长液,隔天更换培养基,细胞达90%融合时进行传代。将细胞扩增至第3代、细胞贴壁生长达90%融合时加入成骨诱导培养液诱导培养,每3天更换1次培养液,4周后进行茜素红染色。
2.2 抗结核性骨组织工程复合体的构建
2.2.1 制备同种异体部分脱钙骨支架 取处死的新西兰大白兔双侧髂骨,剔除表面脂层、肌层、筋膜、骨膜等,经蒸馏水、1︰1的氯仿/甲醇、0.5%盐酸充分冲洗。经脱脂、脱钙、脱蛋白后,修剪成约5 mm×5 mm×2 mm大小。于-20℃冷藏1 d后经60Co-γ射线辐照灭菌,一次性封口包装收集。
2.2.2 兔脂肪干细胞-利福喷丁微球-骨支架的复合 经前期实验取得利福喷丁微球,精密称取3 mg利福喷丁微球与400 μL的细胞悬液(细胞浓度为3×106/ mL)混匀后,缓慢均匀滴加至HA/β-TCP、同种异体骨支架空隙上,置于37℃培养箱中复合培养4 h后,待脂肪干细胞大部分贴壁后,缓慢沿皿壁加入DMEM完全生长液,计算细胞数贴壁率并定期培养行电镜扫描观察,了解三维复合后利福喷丁微球与兔脂肪干细胞在支架上的黏附、生长情况。
2.3 兔脊柱结核模型构建及治疗
2.3.1 兔脊柱结核模型的构建 3%戊巴比妥钠耳缘静脉注射麻醉,术区备皮,常规消毒。铺双层无菌洞巾,沿L3横突向下至髂嵴做一长约3 cm纵行切口,逐层分开皮下、脂层,肌层,充分显露L4~5椎体及左侧椎旁,开路锥沿椎间盘边缘钻骨孔,深度约为0.6 cm,止血后,缓慢浸注结核菌悬液0.1 mL,表面用明胶海绵填塞,逐层关闭切口。术中严格遵守无菌操作及安全防护术后动物隔离分笼饲养。保持房间通气良好,定时定点补食水,严格遵守动物伦理等原则,术后2个月通过影像学(DR、MRI)分析,可见椎体破坏、椎间隙变窄、椎旁脓肿者即为造模成功。
2.3.2 兔脊柱结核疗效的研究 取36只造模成功、感染程度相似的家兔行病灶清除术,并将其随机分为3组,A组于骨缺损处植入rADSCs/利福喷丁微球/HA/β-TCA抗结核骨组织工程复合体,B组于骨缺损处植入rADSCs/利福喷丁微球/同种异体骨抗结核骨组织工程复合体,C组清创后未做任何处理。逐层严密缝合脂层、皮下、表皮,术区切口涂抹红霉素,预防感染,分笼常规条件饲养,定时通风换气。
2.4 观察指标
2.4.1 大体观察 术后观察兔饮食、活动及伤口愈合情况。处死的家兔将植骨处骨质连同周围骨质一并取出,取材后观察骨缺损修复、骨痂形成情况。
2.4.2 影像学检查 造模2个月后行脊柱正侧位DR照射及MRI检查,了解造模情况;病灶刮除植入抗结核性骨组织工程复合体术后4、8、12周行脊柱正侧位DR照射,参照Lane-sandhu X线评分法对骨缺损修复准进行评分。
2.4.3 组织病理学检查 将取出的标本用4%甲醛固定,常规脱钙,标本流水冲洗过夜,脱水,透明石蜡包埋,切片(厚度5 μm),行HE染色,电子显微镜下观察支架材料边缘愈合情况,类骨质、骨质生成情况,有无炎性细胞浸润以及利福喷丁微球降解情况。

3 结 果
3.1 兔脂肪干细胞的镜下特点 镜下可见原代rADSCs培养3~4 h贴壁,梭形,接种24 h后细胞基本完全贴壁,贴壁初期细胞形态不一,培养5~7 d后融合率高达80%~90%,传代后rADSCs增殖速度明显(见图1)。
3.2 抗结核性骨组织工程复合体的鉴定 将利福喷丁微球与脂肪干细胞二维复合后与骨组织支架培养14 d后,期间定期更换培养液,电镜扫描观察到利福喷丁微球-rADSCs/HA/β-TCA及利福喷丁微球-rADSCs/同种异体骨两种抗结核骨组织工程复合体表面呈不规则颗粒状,微球紧紧黏附于细胞及支架上,微球保持圆形轮廓(见图2~3)。
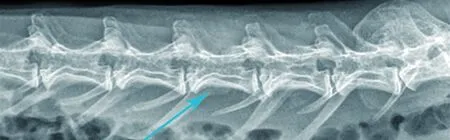
3.3 新西兰大白兔脊柱结核模型的构建 兔脊柱结核模型术后2个月椎旁脓肿形成(见图4)、L4~5椎间隙变窄(见图5),脊柱MRI提示椎旁脓肿形成(见图6)。
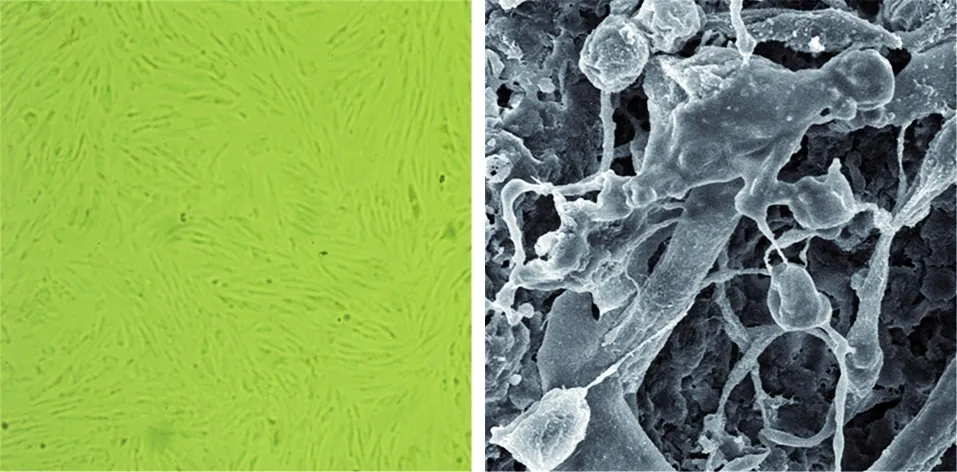
图1 第3代兔脂肪干细胞(×10)图2 利福喷丁微球-rADSCs/同种异体骨复合体(SEM,×1 000)
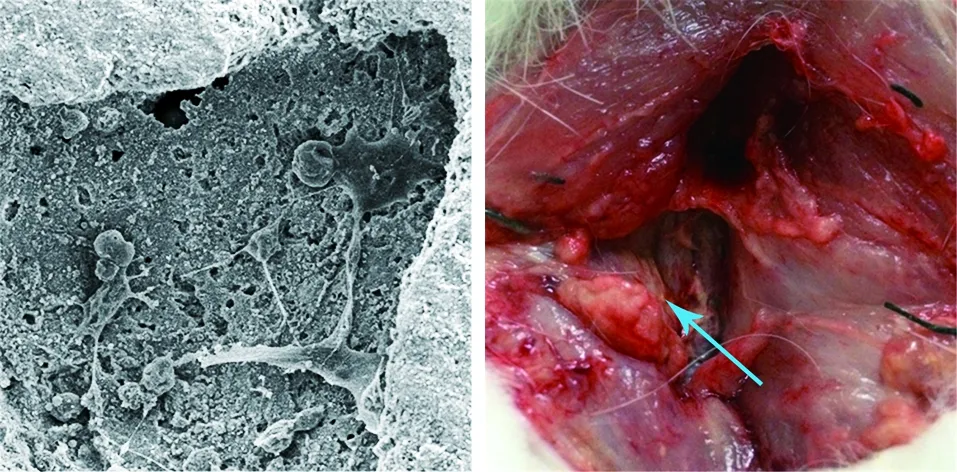
图3 利福喷丁微球-rADSCs/HA/β-TCA复合体(SEM,×400) 图4 脓肿形成
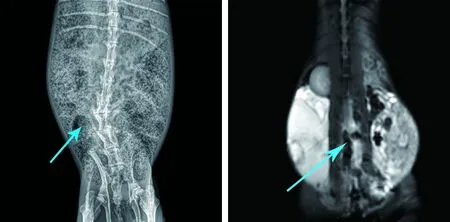
图5 术后2个月X线片示椎间隙变窄,椎体侧弯 图6 MRI提示椎旁脓肿
3.4 术后实验动物基本情况及标本大体观察 术后第1天A组1只兔子因术中牵拉伤及神经,术后截瘫;C组1只兔子因术中伤及神经、血管,术后第2天出血过多死亡;术后第6天、7天空白组兔子因食欲不振、切口感染等原因死亡3只;术后4周实验对照组1只兔子行DR检查后第2天死亡,解剖未见明显异常,考虑行DR检查时,运输途中过热致死。其他动物均存活良好,及时补充各组实验动物数量,术后12周取材时,所有实验动物精神、饮食可,切口无感染、化脓,局部无明显畸形。经空气栓塞处死后,取出L5及相邻椎体骨标本,可见A组及B组骨缺损处基本修复,表面欠光滑,B组可见少量支架材料残存,空白对照组缺损处可见有大量的纤维肉芽形成,骨缺损明显,相邻椎体畸形愈合(见图7)。

a A组 b B组 c C组
3.5 影像学检查 术后4周:A组骨缺损区少量骨痂形成,支架材料包埋于椎体缺损区,周边可见散在高密度影(见图8a)。B组缺损区材料填充明显,材料与周围骨组织界线尚清,周边可见少许骨痂形成(见图8b),复合体材料与周围组织界限模糊。C组椎体畸形,骨缺损区界线清晰,片状低密度影,未见骨痂形成(见图8c)。
a A组

b B组

c C组
术后8周:A组部分材料吸收,骨缺损区可见片状密度增高影,边界模糊(见图9a)。B组骨缺损区可见絮状高密度影,复合体与周围骨组织界限模糊,可见较多骨痂形成(见图9b)。C组脊柱侧弯明显,骨缺损未见明显变化,缺损周边可见点状钙化影(见图9C)。

a A组
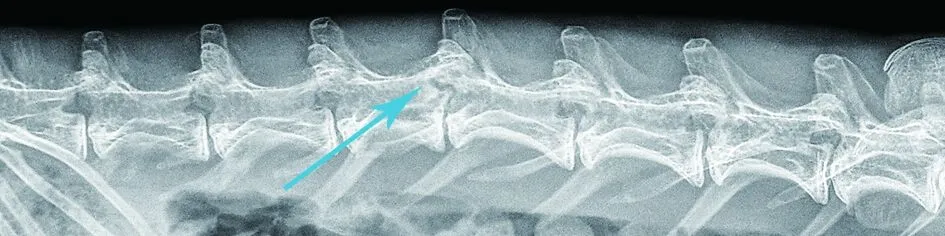
b B组
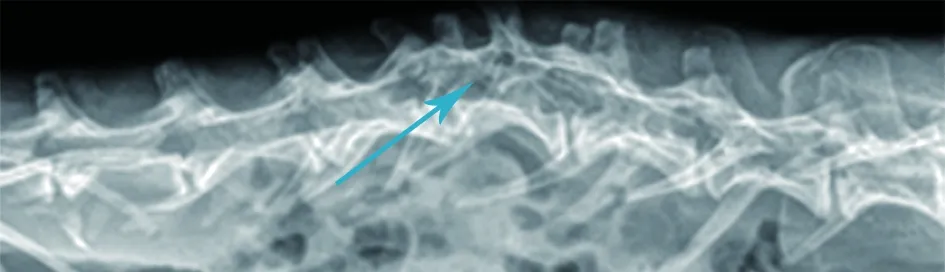
c C组
术后12周:A组骨缺损区复合体材料基本吸收,复合体与骨有骨性连接,两椎体间基本融合(见图10a)。B组骨缺损区大部分修复,部分骨痂形成,椎间隙融合,融合周边可见高密度影,部分边界模糊(见图10b)。C组骨缺损区边界尚清,缺损周边可见片状钙化影,脊柱侧弯明显(见图10c)。

a A组
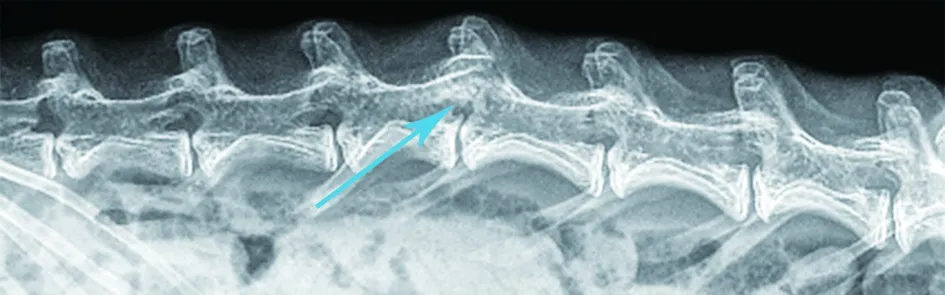
b B组

c C组
根据X线片结果,按照Lane-SandhuX线评分标准进行骨缺损修复的放射学评分(见表2)。
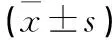
表2 各组放射学评分
3.6 组织病理学检查 术后12周:A组材料吸收明显,可见成熟骨组织出现,结构不规则的骨小梁形成,少量成纤维细胞,新生骨组织排列规则(见图11a);B组部分材料残留,可见新生骨细胞生成,纤维骨痂组织生成骨组织及少许类骨样组织形成(见图11b);C组可见大量纤维结缔组织,少许骨痂形成(见图11c)。

a A组(×10) b B组(×10) c C组(×10)
4 讨 论
脊柱结核是骨与关节结核中最常见的形式,在临床上,因其具有较高的致残率,而且面临耐药、复发、窦道形成等问题,给家庭及社会带来了极大的负担[8]。
全身联合化疗已经是治疗结核的首选方案,抗结核治疗方案分为两个阶段:强化阶段(初始阶段)和持续阶段,治疗时间长达9个月[9]。而且在结核病治疗过程中因患者抵抗力差,结核杆菌致病力强,骨结核口服药很难保证局部血药浓度。耐多药结核病更是一种严峻的挑战,在我国耐多药结核病例和相关的耐多药结核后遗症的数量有所增加,其多见于应用异烟肼和利福平两种抗结核药物后。2016年,全球约有24万人因耐多药结核或耐药结核病死亡。耐多药结核病的治疗成本更高,毒性更大,并且比治疗药物易感性结核的时间更长,为我们行结核病防治带来更大的挑战[10-11]。
虽然化疗是抗结核治疗的基本方法,有数据显示单纯保守治疗的平均脊柱塌陷为15%~20%,而及时的外科干预可以有效地降低椎体塌陷致截瘫等并发症。目前脊柱结核的外科治疗多采用病灶清除术,必要时行植骨融合内固定术,由病灶清除术后骨缺损所造成的脊柱稳定性下降一直是外科治疗所面临的难题[12-13]。自体骨移植是骨缺损修复的“金标准”[14],但由于自体骨来源有限,易出现取骨区感染、疼痛等症状,内固定技术在解决因骨缺损导致的脊柱稳定性下降方面具有一定的优势,但因术中病灶清除不彻底、术后因患者营养差、未进一步正规化疗等因素导致局部复发,给患者带来严重的负担。
在骨结核治疗中,局部植入能够有效保持抗结核药物浓度并促进骨缺损修复的生物工程复合体成为近来研究的热点。结核性骨缺损的修复不仅需要促进缺损愈合,更重要的是彻底的清除、消灭结核杆菌,降低复发率,减少耐药菌的发生。自体移植技术中提供最佳的骨诱导性、骨传导性和成骨特性。由于自体移植增加额外伤口,供区疼痛和骨供应不足等缺点[15-17],因此研发新型骨缺埙修复材料迫在眉睫。
天然高分子复合材料利用组织工程学的原理和方法,通过对缺损骨组织修复并重建,它不仅满足自体骨的优点,同时避免二次创伤等缺点[18-19]。理想的骨组织工程支架材料不仅需要具备适合细胞生长的环境及细胞亲和性,而且需要维持较好的生物相容性、骨传导性、高孔隙率和生物力学相容性等优势。种子细胞、支架材料、细胞生长和分化因子作为骨组织工程的三个基本要素[20]。理想的种子细胞应取材方便,来源丰富,对机体损伤小,具备定向分化为成骨的能力。rADSCs是多能干细胞,具有分化成不同谱系的能力并分泌启动组织再生过程的旁分泌因子,且脂肪组织的供应充足,易于分离,体外广泛的增殖能力以及分泌促血管生成生长因子的能力使其成为治疗非愈合性伤口的理想细胞类型[21-22]。HA/β-TCA构成的复合材料是目前广泛应用于临床的人工复合材料。Tang等[23]将兔自体脂肪干细胞接种于纳米羟基磷灰石复合支架上,研究脊柱融合,发现复合体的融合率及新骨生成量明显高于单纯支架组,李海建等[24]将分化诱导后的rADSCs与HA/β-TCA复合材料体外培养,发现rADSCs较均匀的黏附在复合体上,并填充于支架材料微孔中,细胞在复合体上生长良好,增殖明显。龙志成等[25]在脊柱骨缺损修复的体内实验发现,将rADSCs/HA/β-TCA复合材料与rADSCs/同种异体骨进行对比,rADSCs/HA/β-TCA具有较好的生物黏附性及促进新骨形成的能力。
脊柱结核治疗过程中,如何提高局部结核药物的血药浓度,降低耐药的发生风险,减少化疗副反应是研究的重点,微球靶向等技术的发展为脊柱结核局部给药提供了新的思路。因抗结核药物的时间长、副作用大等缺点,如能通过改变现有抗结核药物剂型,达到局部控制药物浓度,有效降低药物毒副作用具有重要意义,利福喷丁具有很好的脂溶性,且有效抗结核杆菌作用强,本课题组制备的利福喷丁微球具有较好的载药率及包封率。吴林波等[26]将利福喷丁微球与脂肪干细胞二维复合,发现其利福喷丁微球对兔脂肪干细胞生长、增殖的影响较小。梁求真等[27-28]在体外以同种异体骨为支架材料构建的抗结核性骨组织工程复合体的实验研究,发现该复合体具有持续缓慢释放药物的性质,且该释药浓度不影响rADSCs的成骨活性。本实验将分化诱导后的rADSCs与利福喷丁微球二维复合后构建的HA/β-TCA复合材料、同种异体骨构建的两种抗结核性骨组织工程复合体,在脊柱结核造成的骨缺损的对比研究中发现以HA/β-TCA为支架构建的抗结核性骨组织工程复合体,利于骨缺损的修复,而且具有较好的生物相容性。该方案为结核性骨缺损修复材料进行初步研究和探索,为构建抗结核性骨组织工程复合体的局部治疗提供一种新的思路,为临床治疗提供一种方法。但因脂肪干细胞与利福喷丁微球相关方面研究较少,且构建的抗结核骨组织工程复合体在实验动物脊柱结核模型中的动物数量较少,且观察时间短,对该复合材料体内药物特征及成骨修复方面需进一步研究。
综上所述,以HA/β-TCA为支架材料构建的利福喷丁微球抗结核性骨组织工程复合体具有良好的生物相容性及成骨性,可以通过增加局部药物浓度抑制结核杆菌生长,减少椎体骨质破坏,在动物实验基础研究中,对脊柱结核具有一定的治疗作用。

